常規超聲聯合超聲造影術前評估乳腺癌患者腋窩淋巴結的診斷價值
杜麗雯,鞏海燕,鄧 晶,王 慧,易春蓓,栗翠英
南京醫科大學第一附屬醫院超聲診斷科,江蘇 南京 210029
乳腺癌是中國女性最常見的惡性腫瘤[1]。腋窩淋巴結是乳腺癌最先及最常見的轉移部位,腋窩淋巴結狀態不僅決定了患者的治療方案而且是重要的預后因素之一[2]。對于乳腺癌腋窩淋巴結臨床陰性患者,將行前哨淋巴結活檢術(sentinel lymph node biopsy,SLNB)。對乳腺癌腋窩淋巴結臨床陽性患者和前哨淋巴結活檢陽性患者予以腋窩淋巴結清掃術(axillary lymph node dissection,ALND)[3-4]。然而,乳腺癌患者ALND術后可能會出現感染、感覺異常、上肢及肩關節活動度減低、上肢淋巴水腫等并發癥,上肢淋巴水腫是ALND最嚴重的并發癥,發生率為6%~30%[5]。此外,一些研究表明SLNB術后也可出現上肢淋巴水腫,發生率為2%~7%[4-7]。乳腺癌患者腋窩淋巴結體格檢查靈敏度低,僅為33%~68%[8-9]。而超聲檢查具有較高的靈敏度及特異度,其良好的診斷價值已被臨床認可,已普遍用于乳腺癌患者術前檢查。
國內外已有研究表明常規超聲(灰階超聲、彩色多普勒超聲)及超聲造影(contrast-enhanced ultrasound,CEUS)對乳腺癌患者腋窩淋巴結診斷具有較好的診斷價值[10]。術前超聲評估乳腺癌腋窩淋巴結狀態得到了廣泛的臨床認可,但有關其診斷的標準仍有爭議。本研究總結了常規超聲和CEUS評估中各種測量參數,比較其診斷價值,以尋找腋窩淋巴結術前檢查最優方法。
1 資料和方法
1.1 臨床資料
回顧并分析2014年11月—2019年5月于南京醫科大學第一附屬醫院就診的乳腺癌患者的腋窩淋巴結超聲聲像圖。患者均行常規超聲及CEUS檢查,排除超聲聲像圖信息不完全或無病理學檢查結果的患者,最終納入234例患者。根據術前乳腺鉬靶X線檢查、乳腺磁共振成像和超聲檢查,患者計劃進行SLNB或ALND。
1.2 方法
采用意大利Esaote公司的MyLab Twice超聲診斷儀。彩色多普勒超聲和灰階超聲采用頻率為4~15 MHz的線性陣列探頭L523,機械指數0.7,增益100~120 dB。CEUS采用頻率為4~9 MHz的低頻超聲探頭L522。造影劑使用意大利Bracco公司的聲諾維(SonoVue),用5 mL 0.9%的NaCl溶液稀釋,每次檢查經肘靜脈推注1.2 mL造影劑。患者均簽署知情同意書。
根據胸小肌的相對位置將腋窩淋巴結分為3個水平。Ⅰ區:胸小肌外側,包括乳腺外側組、中央組、肩胛下組及腋靜脈淋巴結;胸大小肌之間,Rotter淋巴結。Ⅱ區:胸小肌深面的腋靜脈淋巴結。Ⅲ區:胸小肌內側靜脈淋巴結,即鎖骨下淋巴結。乳腺癌引流淋巴結轉移常以順序形式由較低水平至較高水平有序發生,偶有跳躍式轉移[11]。超聲檢查重點關注腋窩Ⅰ區淋巴結。灰階超聲腋窩淋巴結測量參數包括淋巴結長徑(L)、淋巴結短徑(S)、最大皮質厚度、開始增強時間和阻力指數(resistance index,RI)。當淋巴門結構消失時,只測量L、S、開始增強時間和RI[12-13]。檢查后計算L/S。所有數據均需在淋巴結長軸上測量。根據皮質形態學特征,將淋巴結分為4型:Ⅰ型,薄而均勻的低回聲皮質,最大皮質厚度<1.6 mm或皮質幾乎不顯示。Ⅱ型,均勻的低回聲皮質,1.6 mm≤最大皮質厚度<3 mm。Ⅲ型,局灶性皮質增厚或不均勻增厚,最大皮質厚度≥3.0 mm。Ⅳ型,完全低回聲結節,無高回聲淋巴門結構[14-15]。
彩色多普勒超聲檢查需在低壁濾波和低速度模式下進行。彩色增益需要動態調整,彩色增益最大化且無紅、藍彩色雜波。根據相關文獻血流模式[12,15-16],將腋窩淋巴結分為4類:淋巴門型血流、中央型血流、周圍型血流和混合型血流。淋巴門型血流定義為淋巴結髓質中央或偏心血流信號,呈點狀、條狀或樹枝狀。中央型血流定義為散在點狀或條狀血流信號、皮質或髓質中長軸徑向的、變形的徑向或異常的多焦點聚集血流信號。周圍型血流定義為沿淋巴結邊緣走行的環形條狀血流信號[16-17]。混合型血流定義為具有多種血流模式的淋巴結。無淋巴門型淋巴結中,血流被描述為中央型、周圍型或混合型血流。淋巴門型血流多見于非轉移性淋巴結。中央型、周圍型及混合型血流多出現于轉移性淋巴結中。
根據腋窩淋巴結造影臨床經驗及先前文獻研究,造影增強模式分為均勻性增強和非均勻性增強[18-19]。均勻性增強模式定義為淋巴結整體增強強度一致。非均勻性增強模式被定義為淋巴結的不均勻增強,包括部分高增強、低增強和灌注缺損。多指標聯合診斷乳腺癌腋窩淋巴結,當淋巴結具有一個可疑參數時,被認為屬于可疑淋巴結。
1.3 統計學處理
所有統計學分析均使用SPSS 20.0及MedCalc 15.6。參數分析采用t檢驗和χ2檢驗。繪制受試者工作特征(receiver operating characteristic,ROC)曲線并計算各檢查參數界值。分析并記錄每個檢查參數的靈敏度、特異度、陽性預測值(positive predictive value,PPV)、陰性預測值(negative predictive value,NPV)、Youden指數、曲線下面積(area under curve,AUC)及多元回歸模型。
2 結 果
234例患者均為原發性乳腺癌,年齡24~84歲,平均(49.4±11.0)歲。腫瘤大小5~115 mm,平均大小(26.4±15.7)mm。病理學檢查證實轉移性淋巴結有130例(55.56%)。
在灰階超聲聲像圖中,轉移性及非轉移性淋巴結最大皮質厚度、S、L/S的差異有統計學意義(P<0.001,表1)。S≥7.1 mm、L/S≤2.0、最大皮質厚度≥3.0 mm更多地出現在轉移性淋巴結中,且最大皮質厚度是轉移性淋巴結最準確的診斷標準(P<0.001,AUC=0.808)。在234例腋窩淋巴結灰階皮質分型中,135例(57.69%)淋巴結被分為Ⅱ~Ⅳ型。轉移性淋巴結所占各型比例為24.04%、38.46%、26.92%,顯著高于非轉移性淋巴結所占比例13.85%、16.15%、2.30%。11例轉移性淋巴結被分為Ⅰ型,假陰性率(false negative rate,FNR)為10.58%。42例非轉移性淋巴結被分為Ⅱ~Ⅳ型,假陽性率(false positive rate,FPR)為33.31%。灰階皮質淋巴結分型診斷轉移性淋巴結的靈敏度、特異度、PPV、NPV和AUC分別為89.4%、67.7%、68.9%、88.9和0.786(圖1,表2)。
彩色多普勒超聲檢查發現,非轉移性淋巴結多表現為淋巴門型血流(94.62%)。中央型、周圍型和混合型血流在轉移性淋巴結組百分比為7.69%、2.88%、49.04%,明顯高于非轉移性淋巴結組0.77%、0.77%及3.85%(P<0.01)。74.04%轉移性淋巴結血流豐富,而非轉移性淋巴結僅17.69%血流豐富,兩組之間差異有統計學意義(P<0.001)。使用血流豐富程度診斷腋窩淋巴結靈敏度、特異度、AUC分別為74.0%、82.3%、0.782。RI≥0.7時特異度最高(98.4%),但靈敏度低(26.0%),AUC為0.622。開始增強時間診斷轉移性淋巴結差異無統計學意義(P>0.05)。CEUS檢查中,轉移性淋巴結多表現為非均勻性增強(P<0.001,圖2~3)。
多因素logistic回歸分析結果顯示最大皮質厚度≥3 mm,淋巴結灰階分型,血流分型和CEUS增強模式診斷轉移性淋巴結差異有統計學意義(P<0.05,表3)。常規超聲聯合CEUS并不能提高常規超聲檢查的診斷價值,兩種方法比較差異無統計學意義(P>0.05,表4,圖4)。
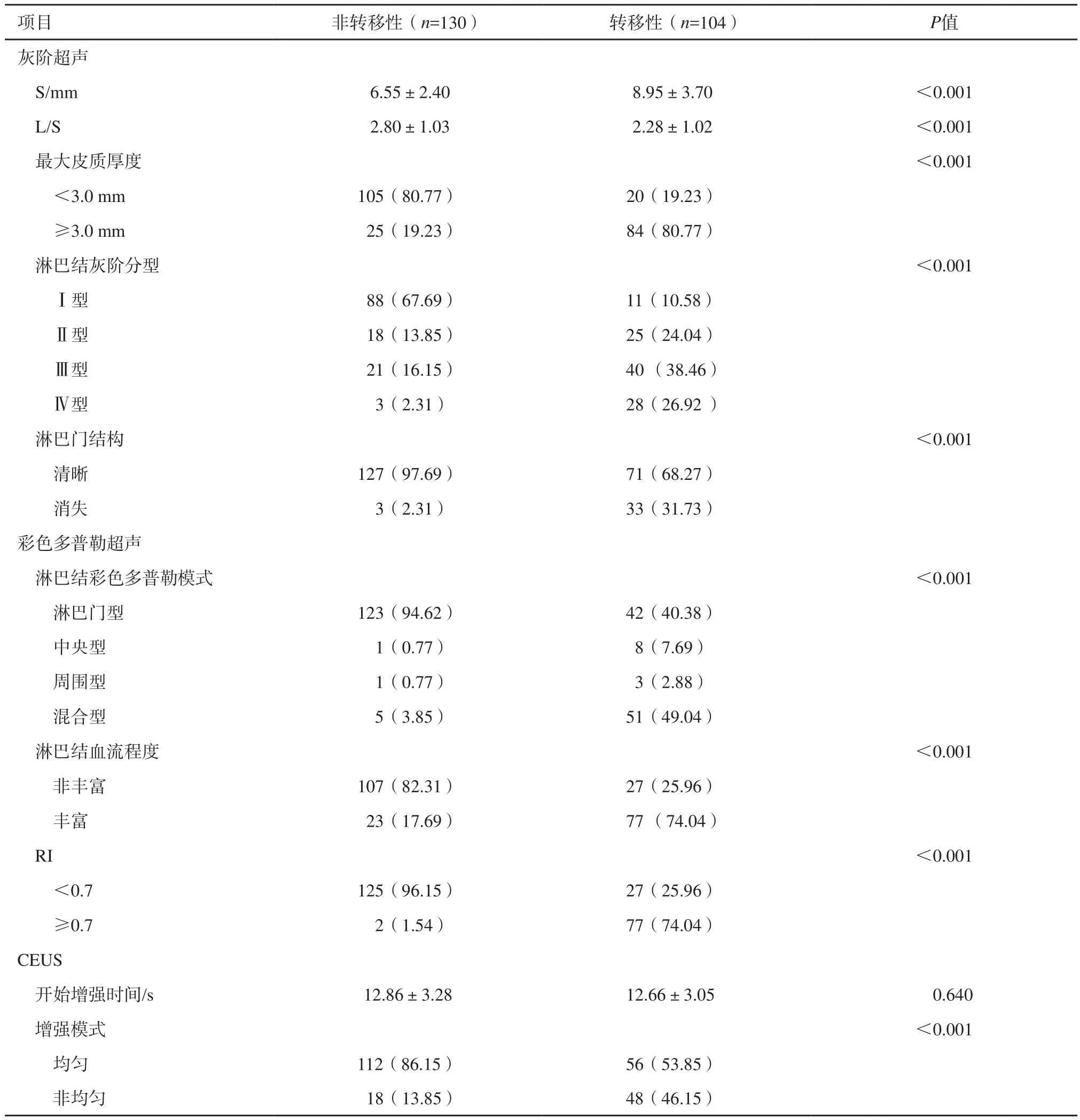
表 1 234例腋窩淋巴結常規超聲和CEUS特征[n(%)]
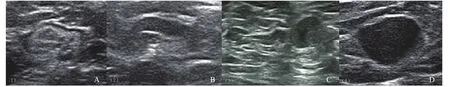
圖 1 淋巴結灰階超聲Ⅰ~Ⅳ型
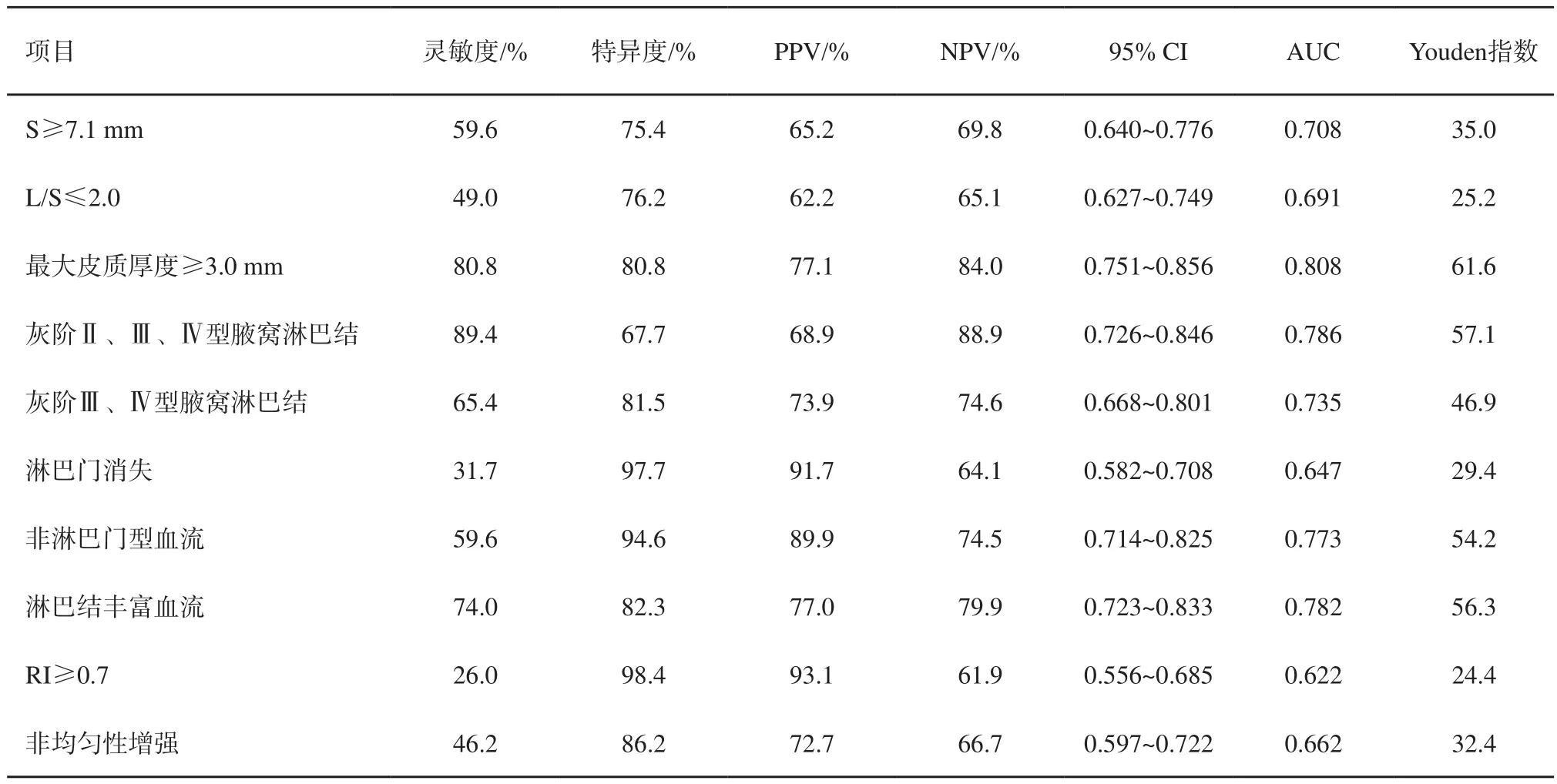
表 2 常規超聲和超聲造影中轉移性腋窩淋巴結特征
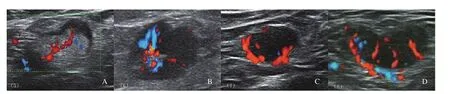
圖 2 彩色多普勒血流分型
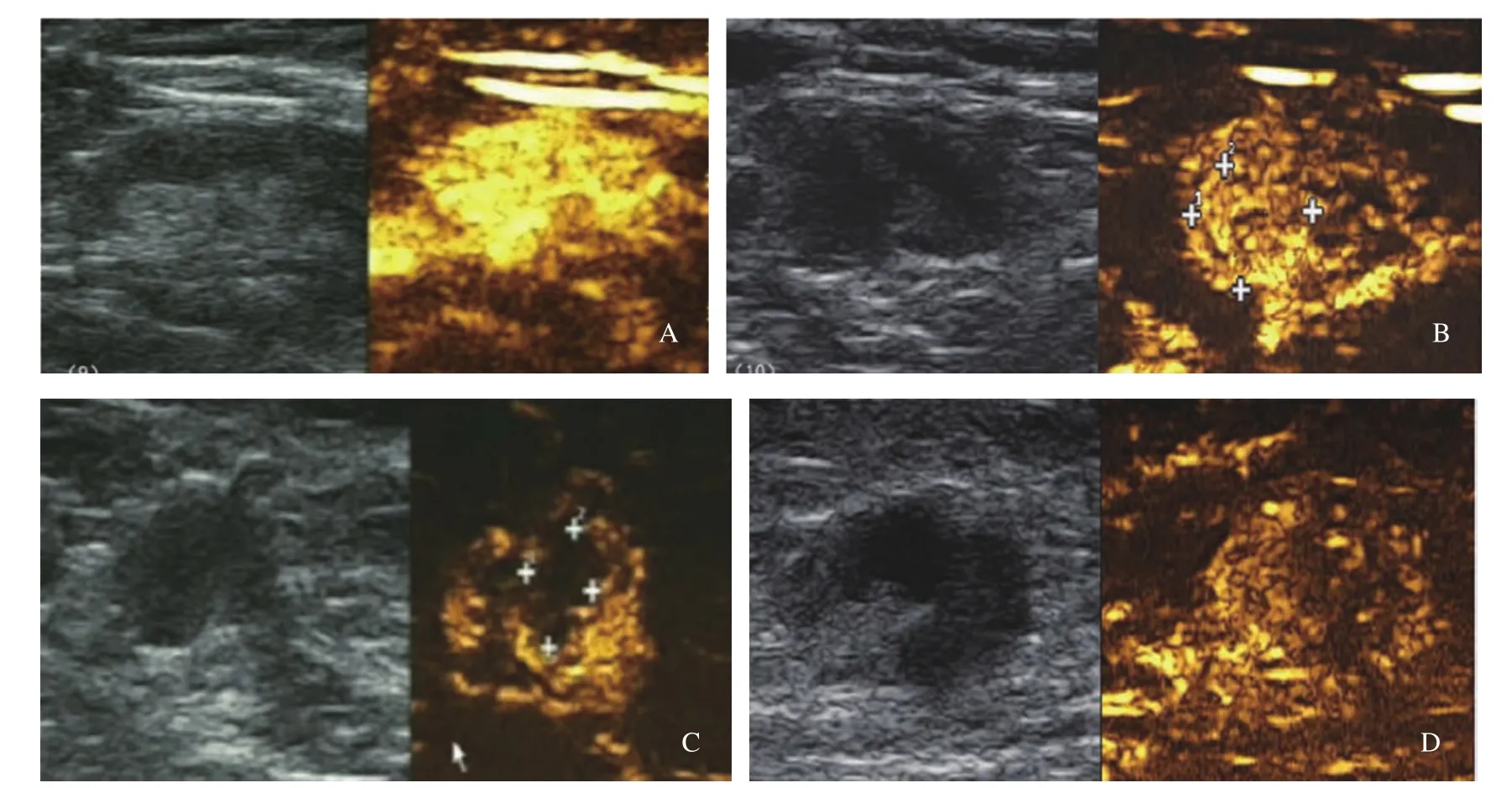
圖 3 腋窩淋巴結超聲增強模式

表 3 常規超聲和超聲造影多變量logistic回歸分析結果
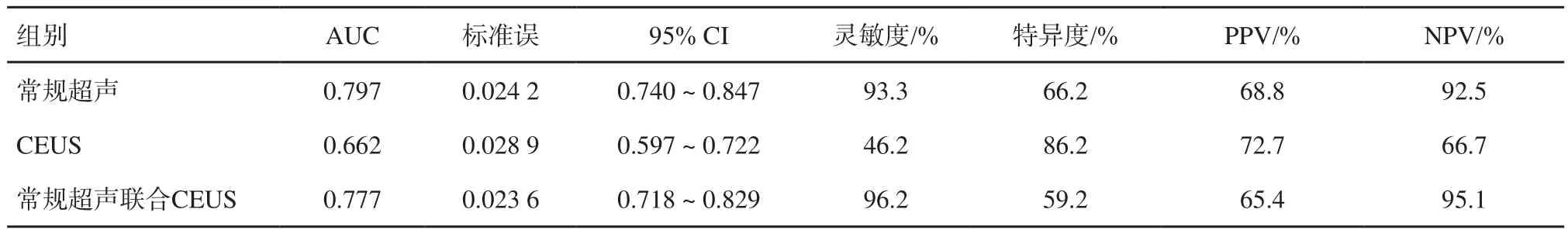
表 4 常規超聲、CEUS及聯合診斷ROC結果
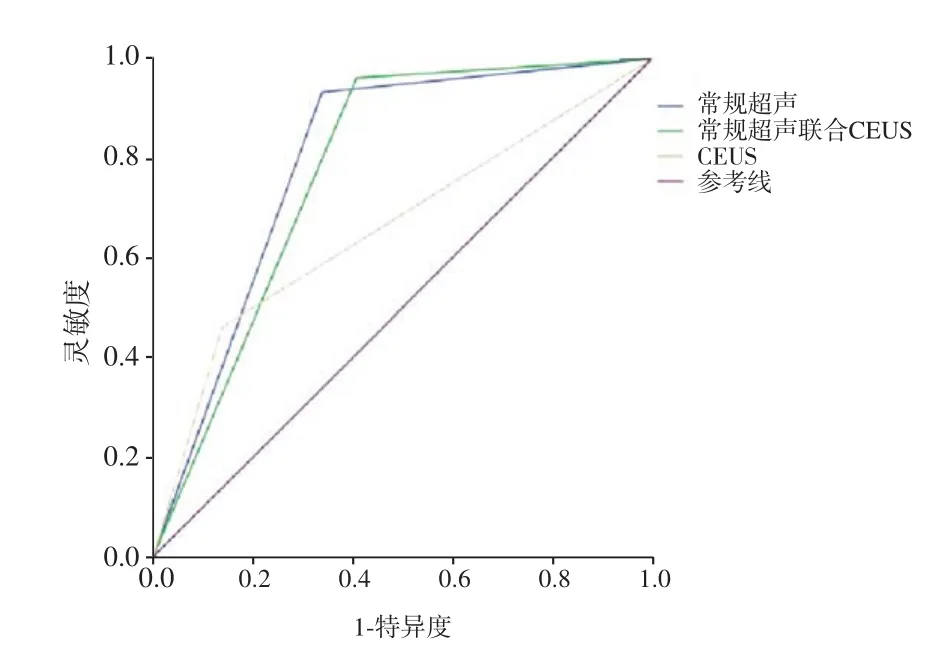
圖 4 常規超聲、CEUS及聯合ROC曲線
3 討 論
術前超聲檢查評估乳腺癌患者腋窩淋巴結狀態,其較好的靈敏度及特異度經國內外學者研究證實,并作為乳腺癌患者術前常規檢查方法[9]。當超聲檢查無可疑淋巴結時,患者可行SLNB,減少不必要的腋窩淋巴結清掃,減少并發癥發生。此外,當患者有可疑腋窩淋巴結時可以行超聲引導下腋窩淋巴結細針穿刺或空心針活檢,避免不必要的SLNB并減少前哨FNR[20]。研究發現CEUS對于鑒別乳腺腫塊良惡性有重要的診斷價值,其對乳腺癌患者腋窩淋巴結的診斷效能也有相關報道[21-22]。但對乳腺癌患者腋窩淋巴結行超聲多種方法聯合診斷的研究較少[23]。
灰階超聲聲像圖中低回聲皮質代表邊緣竇,淋巴濾泡和副皮質。由于血管、脂肪及中央竇的多重反射界面,淋巴門表現為高回聲。輸入淋巴管和輸出淋巴管在灰階超聲聲像圖中不能被顯示[14]。非轉移性腋窩淋巴結常規超聲聲像圖表現為薄且均勻的低回聲皮質、最大皮質厚度<3 mm、淋巴門結構存在、淋巴門型血流,CEUS表現為均勻性增強[24]。超聲診斷腋窩淋巴結良惡性時,關注淋巴結的形態及整體回聲(有無淋巴結門結構)。由于癌細胞轉移至淋巴結首先通過輸入淋巴管到達邊緣竇,沉積在淋巴結的外圍,所以淋巴結皮質形態變化最為重要。隨后癌細胞侵犯小梁竇和髓竇,導致皮質彌漫性或偏心增厚,并逐漸侵犯整個淋巴結至淋巴門消失[25]。轉移性淋巴結常規超聲表現為淋巴結皮質彌漫性或局限性增厚、L/S減小、淋巴門結構偏心或消失、非淋巴門型血流,而CEUS表現為非均勻性增強[15,20]。
根據淋巴結皮質形態變化,目前有多種分型方法。Bedi等[14]將淋巴結分為Ⅰ~Ⅵ型。Ⅰ型:幾乎無淋巴結皮質;Ⅱ型:皮質薄而均勻的低回聲區;Ⅲ型:均勻低回聲皮質厚度>3 mm和輕微分葉狀;Ⅳ型:增厚的皮質分葉為淋巴門回聲的延續。Ⅰ~Ⅳ型為非轉移性淋巴結。Ⅴ型(局灶性增厚低回聲皮質)和Ⅵ型(淋巴門結構消失)淋巴結為轉移性淋巴結,其診斷的靈敏度、特異度和準確率分別為77.0%、80.0%和80.0%。反應性淋巴結與轉移性淋巴結在超聲聲像圖中相似,通常當機體有炎性反應時,淋巴結反應性增大,皮質均勻性增厚,血流增多,但以往文獻中沒有關于均勻性增厚淋巴結皮質厚度界值。本研究中,我們將1.6 mm定義為Ⅰ型與Ⅱ型最大皮質厚度臨界值,區分部分反應性淋巴結和轉移性淋巴結,其結果,靈敏度為89.9%、特異度為37.5%。Abe等[26]報道,淋巴門結構消失診斷轉移性淋巴結具有較好PPV(93.0%),但靈敏度較低(33.0%)。Vijayaraghavan等[4]研究發現,以最大皮質厚度和淋巴門消失診斷轉移性淋巴結,AUC、準確率和95.0% CI分別為0.830、81.7%和76.2%~89.7%。所以當高回聲淋巴門消失時,應該高度懷疑轉移性淋巴結。本研究中淋巴門消失仍有3例為非轉移性淋巴結,FNR為3.65%,回顧并分析圖像,可能原因為超聲檢查受操作者主觀因素影響較大,淋巴結較小(<10 mm)或增益較低時,高回聲淋巴門顯示不清。
淋巴結的最大皮質厚度是轉移性淋巴結的獨立預測因素。在Abe等[26]的研究中,最大皮質厚度界值為3 mm,該界值用于診斷轉移性淋巴結的靈敏度和特異度分別為95.0%和6.0%。當以4 mm為界值時,靈敏度為88.0%,特異度為42.0%。隨著最大皮質厚度界值增加,靈敏度逐漸下降,而PPV和特異度逐漸增加。因此,我們采用S≥7.1 mm、L/S≤2.0等其他參數,雖然之前研究顯示L/S和S是較好診斷指標,但其可能受到皮質厚度因素的影響。在多元logistics回歸分析中,這些參數不是獨立的預測因素,差異無統計學意義。
彩色多普勒超聲診斷乳腺癌患者的淋巴結狀態具有重要價值。Na等[16]將淋巴門血流分為淋巴門型、中央型和周圍型,并將這3種血流模式進一步細分。Yang等[12]的研究中將淋巴結血流分為周圍型血流、中央型血流、中央門型血流、混合型血流。本研究中,因部分中央型血流患者被計入混合型血流,所以轉移組中央型血流患者例數較少。轉移性癌細胞導致正常淋巴門血流中斷,周圍腫瘤滋養血供增多導致血流增多。RI和搏動指數增高與血管狹窄有關。由于血管生成素促進轉移性淋巴結新生血管形成,新生血管結構缺乏肌層,易出現血管狹窄、血管閉塞,不規則血管分支和動靜脈瘺[27]。這些血流特征導致不同類型的血流動力學變化。不同研究選擇不同RI界值,范圍為0.6~0.9。本研究中,我們選用界值RI≥0.7,靈敏度為26.0%,特異度為98.4%、AUC為0.622,診斷效能較低。反應性淋巴結也可表現為周圍型血流、豐富血流信號、RI增高。如雙側腋窩淋巴結皮質均勻性增厚,應考慮反應性淋巴結可能。
隨著儀器性能的改進和新型聲學造影劑的出現,CEUS已成為超聲診斷的主要進展之一。CEUS可以顯示直徑為0.1~0.3 mm的血管,以彌補彩色多普勒超聲檢查的局限性[28]。CEUS在乳腺疾病診斷中的主要應用包括良惡性腫塊鑒別診斷、腋窩轉移性淋巴結診斷、經皮CEUS前哨淋巴結定位等[29-31]。在本研究中,開始增強時間診斷轉移性淋巴結差異無統計學意義。非均勻性增強模式包括整體或部分淋巴結皮質早期增強、早退、高增強、低增強和灌注缺損[30-31]。CEUS診斷轉移性淋巴結時,應觀察淋巴結皮質區域,當淋巴門脂肪含量較高時,脂肪組織區域會顯示出低增強,不應診斷為非均勻性增強。病理學檢查顯示轉移性淋巴結被腫瘤細胞浸潤,造影劑不能進入淋巴結或在其他區域積聚,導致不均勻性增強[32]。2004年,Rubaltelli等[33]研究首次提出了灌注缺損,定義為與正常淋巴組織增強相比病灶血流減少,增強強度減低或未增強。Dellaportas等[18]研究發現,非轉移性淋巴結表現為均勻高增強,慢進和慢退。而轉移性淋巴結表現為不均勻性增強,早進和早退。
多因素logistic回歸分析顯示淋巴結灰階分型、最大皮質厚度、血流模式和增強模式是診斷轉移性淋巴結的獨立預測因素(P<0.05)。非均勻性增強AUC、靈敏度、特異度分別為0.662、46.2%、86.2%。CEUS作為輔助檢查方法需要在常規超聲的基礎上,當常規超聲發現可疑惡性淋巴結時,宜通過CEUS對可疑惡性淋巴結進行進一步成像。CEUS聯合常規超聲檢查并不會提高診斷效能,AUC 0.777(95%CI:0.718~0.829),但其具有較高的靈敏度(96.2%),盡管兩種檢查方法之間差異無統計學意義(P>0.05)。
相關研究結果顯示,超聲檢查的眾多診斷參數具有低靈敏度和高特異度的特征[33-35]。超聲診斷轉移性腋窩淋巴結FNR為16.7%~22.9%[28,33]。超聲檢查靈敏度和FNR均低的原因可能與轉移性淋巴結的大小、位置和數量有關。一方面,較少的腫瘤細胞進入淋巴結,如微轉移,不會引起形態學改變。另一方面,超聲檢查依賴于操作者,主觀因素較強,腋窩超聲檢查范圍較小時,轉移性淋巴結可能被漏診。高頻超聲可評估直徑>5.0 mm淋巴結[35-36]。超聲檢查分辨率直接影響腋窩淋巴結評估的準確性。
本研究存在一些局限性。首先,術前腋窩淋巴結超聲檢查和術后病理學檢查結果均代表整個腋窩淋巴結狀態,超聲評估的腋窩淋巴結與術后病理學檢查結果未完全匹配。其次,超聲檢查具有一定的主觀性。CEUS檢查中,本研究僅使用了經肘靜脈推注造影劑,而沒有進行多種方法的對比,今后需要進一步研究。
最大皮質厚度是惡性腋窩淋巴結最準確的指標。常規超聲對乳腺癌患者腋窩淋巴結的診斷具有一定的意義。CEUS的增強模式可用于診斷腋窩淋巴結轉移。CEUS作為輔助手段不能提高超聲的準確率。

