溫度誘導鱖三倍體的比較研究
魏 晉,宋 文,王守榮,陳元元,曾可為
(1.武漢市農業科學院,武漢 430065;2.江漢大學,武漢 430056)
鱖(Sinipercachuatsi)隸屬于鱸形目(Perciformes)鱸亞目(Percoidei)真鱸科(Percichthyidae)鱖屬(Siniperca),在中國、俄羅斯、日本、韓國、朝鮮以及越南等國均有分布,在我國的中東部平原區分布最為廣泛。鱖與其他魚類相似,在性腺發育階段及產卵季節會消耗更多的能量,存在生長減緩、抗逆能力下降及肉質變差等現象。采用現代生物學手段,開發鱖的三倍體誘導技術,可以有效提升鱖的生長速度和抗逆能力,降低其餌料系數,對縮短鱖的養殖周期,提升產量和肉質,提高養殖經濟效益,具有重要意義和實際價值[1]。
人工誘導三倍體魚形成已先后在40多種海水和淡水魚類中成功,其中三倍體興國紅鯉、湘云鯽、湘云鯉、異育銀鯽和三倍體虹鱒等品種已進入規模化生產階段,帶來了巨大的經濟效益[2,3]。本研究參考了泥鰍(Misgurnusanguillicaudatus)[4]、黃顙魚(Pelteobagrusfulvidraco)[5,6]、團頭魴(Megalobramaamblycephala)[7]、烏鱧(Channaargus)[8]、細鱗鮭(Brachymystaxlenok)[9]及鱖(S.chuatsi)[10]等淡水魚類的三倍體誘導方法,采用冷休克和熱休克法進行了鱖三倍體的誘導研究,篩選到了最佳的誘導條件,對冷、熱休克法誘導的效果進行了綜合比較,并對三倍體和二倍體鱖魚苗的生長性狀及存活率進行了研究,以期為進一步開展鱖三倍體苗種的規模化生產提供理論基礎和實踐依據。
1 材料與方法
1.1 親本來源及受精卵的獲取
本試驗所采用的鱖親本采集自武漢市佳恒水產有限公司養殖基地。在鱖的繁殖季節,挑選表型正常、無傷病、身體健壯并且已達性成熟的2齡雌魚和雄魚各30尾進行人工繁殖,雌魚體重750~950 g,雄魚體重650~800 g。
采用人工催產的方法獲得鱖受精卵,產前培育、藥物催產及孵化管理等具體步驟參照李志成等[11]和劉希良等[12]的方法。
1.2 溫度休克處理最佳誘導條件的篩選
本研究中,在魚苗發育不同階段,統計各處理組和對照組的受精率、存活率、畸形率和三倍化率。受精率(FR):胚胎發育原腸胚期,存活胚胎數目占總卵數目的比例。存活率:孵化后5 d,存活個體數目占受精卵數目的比例;相對存活率(SR)=處理組存活率/對照組存活率×100%。畸形率:孵化后5 d,畸形個體數目占存活個體數目的比例;相對畸形率(MR)=處理組畸形率/對照組畸形率×100%。三倍化率(TR):孵化后8 d從各處理組隨機挑選50尾魚苗檢測其倍性,其中三倍體魚苗所占比例。數據處理軟件為SPSS 13.0和Microsoft Office Excel 2003。
1.2.1 冷休克處理最佳誘導條件的篩選
冷休克試驗過程參照宋立民等[5]的方法,采用單因子試驗獲得最適的冷休克誘導條件。三個單因素分別為:處理起始時間(BT)、處理溫度(Temp)和處理持續時間(DT)。試驗設置如表1,各組經冷休克處理后,受精卵轉移至26 ℃水體中繼續培養。設置對照組:受精卵始終置于26 ℃水溫條件下培養。每個處理組和對照組均設置3個重復,每個重復的受精卵數量約2 000粒。
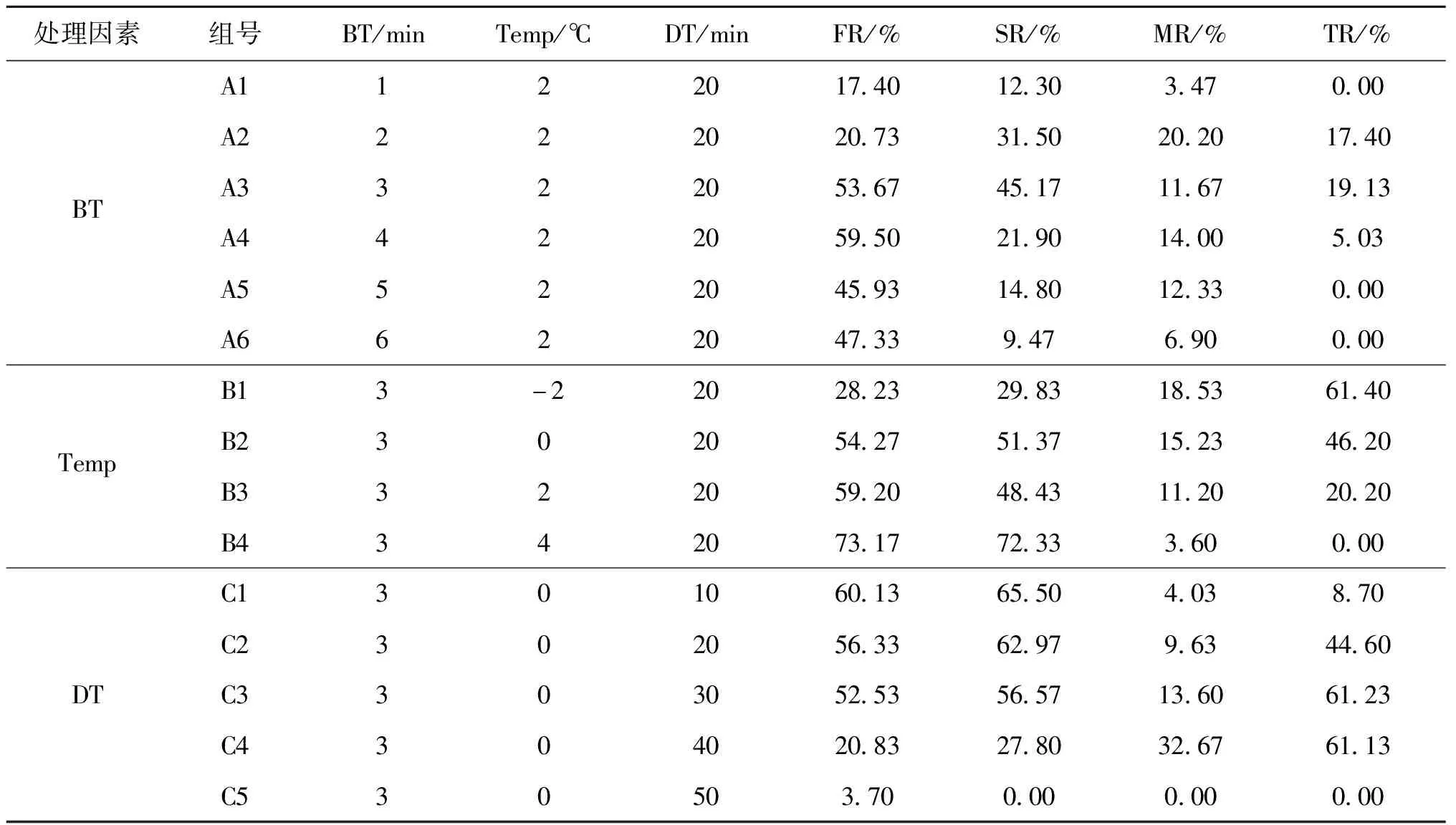
表1 冷休克單因素處理試驗設置
1.2.2 熱休克處理最佳誘導條件的篩選
魚類三倍體的熱休克誘導試驗一般于亞致死溫度附近實施,參考Xu等[10]的研究結果進行預實驗,發現當水溫高于40 ℃后,魚苗存活率為0%,因此,本研究將熱休克處理溫度范圍設置為32~38 ℃。其他單因素試驗條件設置如表2,各組經熱休克處理后,受精卵轉移至26 ℃水體中繼續培養。設置對照組:受精卵始終置于26 ℃水溫條件下培養。每個處理組和對照組均設置3個重復,每個重復的受精卵數量約為2 000粒。
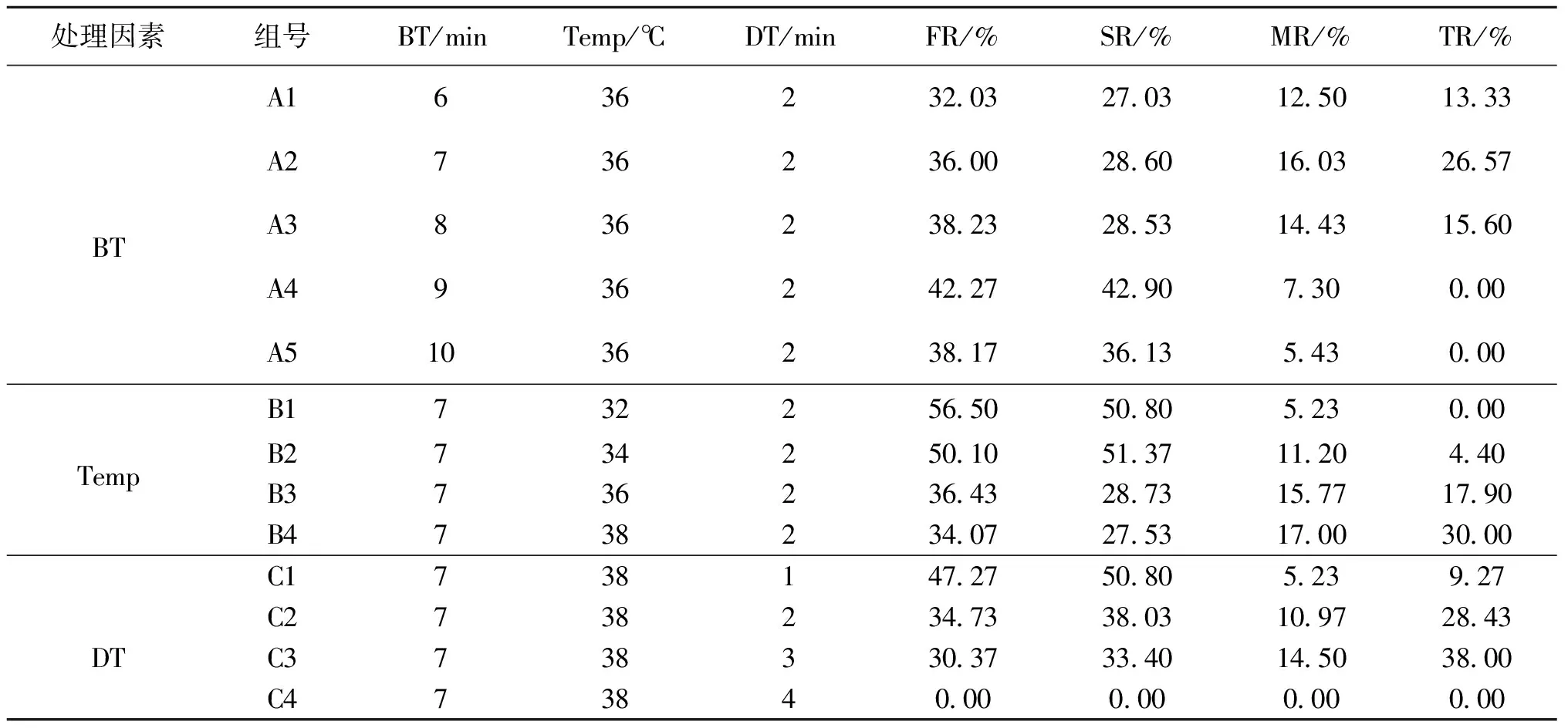
表2 熱休克單因素處理試驗設置
1.3 倍性檢測
孵化后8 d的鱖魚苗體型較小,無法進行尾柄采血,因此從每組中隨機挑選50尾魚苗,制備單細胞懸液進行倍性檢測。將每尾待檢鱖魚苗放入2 mL EP管中,蒸餾水清洗2次后,加入0.4 mL PBS(pH 7.4)溶液,利用組織破碎儀將魚苗碾碎,經300目篩絹過濾后加入PBS(pH 7.4)溶液制備成細胞濃度約為103個/mL的單細胞懸液。1月齡以后的幼魚,通過尾部靜脈取血,利用PBS(pH 7.4)溶液制備成濃度約為103個/mL的血細胞懸液進行倍性檢測。
制備好的細胞懸液采用4′,6-二脒基-2-苯基吲哚(4′,6-diamidino-2-phenylindole,DAPI)染色 1 min,用流式細胞儀(Beckman Coulter,CytoFlex,USA)進行 DNA 含量分析。采用正常二倍體鱖魚苗作為對照。本研究中二倍體鱖細胞DNA相對含量為(204.2±4.3),三倍體鱖細胞的DNA相對含量為(301.1±6.1),約為二倍體的1.47倍(圖1),可判斷誘導出的鱖魚苗為三倍體。
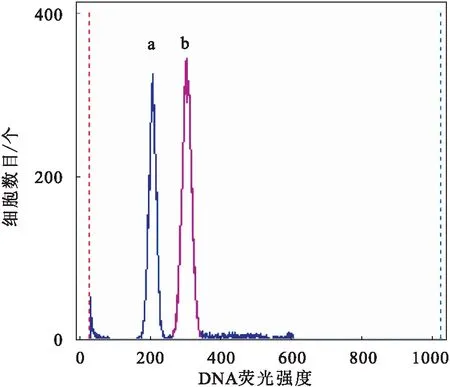
圖1 二倍體(a)和三倍體鱖(b)細胞 DNA 相對含量直方圖
1.4 冷、熱休克誘導效果比較及鱖三倍體魚苗生長性能檢測
為排除親本遺傳差異對試驗結果的影響,在確定冷、熱休克法的最優誘導條件后,利用3對鱖親本分別構建3個全同胞家系,對兩種方法的誘導效果進行比較。每個家系隨機選取約2 000顆受精卵,采用優化后的冷、熱休克誘導條件分別各處理1 000顆以獲得三倍體魚苗;剩余受精卵在正常條件下培育,以獲得二倍體魚苗作為對照組。
所有魚苗均在同等適宜條件下培育,充足投飼,分別在孵化后10、20、40、60、100和150 d,從溫度休克處理組和正常對照組中隨機抽取50尾幼魚進行倍性鑒定,并測量其體長和體重。剩余魚苗繼續培養至180 d(幼魚期),統計三個家系中,采用冷、熱休克法所產生后代的存活率及TR。三倍體和二倍體鱖在不同發育階段生長差異分析采用t檢驗,統計分析及作圖均利用SPSS 13.0軟件完成。統計值采用平均值±標準差(Mean±SD)表示,P<0.05表示具有顯著差異,P<0.01表示具有極顯著差異。
2 結果與分析
2.1 冷休克最佳誘導條件的確定
在設定條件(Temp=2 ℃,DT=20 min)下進行冷休克處理最佳起始時間的篩選,結果表明受精卵在受精后2、3和4 min進行冷休克處理都能誘導產生三倍體鱖魚苗,其中受精后3 min進行冷休克處理的SR和TR均達到峰值(表1,圖2A),因此采用冷休克法誘導鱖三倍體的最佳起始時間為受精后3 min。在設定條件(BT=3 min,DT=20 min)下進行冷休克處理最適溫度的篩選,結果表明在-2、0和2 ℃下,均可以誘導產生三倍體鱖魚苗,其中在-2 ℃下處理獲得后代的TR雖然最高,但FR和SR相對較低;而在0 ℃條件下處理獲得的后代,其FR、SR和TR均相對較高(表1,圖2B),因此綜合考慮,采用冷休克法誘導鱖三倍體的最適處理溫度為0 ℃。在設定條件(BT=3 min,Temp=0 ℃)下進行冷休克處理持續時間的篩選,結果表明冷休克處理10、20、30和40 min都能誘導產生三倍體鱖魚苗,其中處理30 min和40 min時TR相對更高,分別可達到61.2 %和61.1 %,但是冷休克處理40 min的FR和SR急劇下降,而MR則達到峰值(表1,圖2C),因此綜合考慮,采用冷休克法誘導鱖三倍體的最適處理持續時間為30 min。
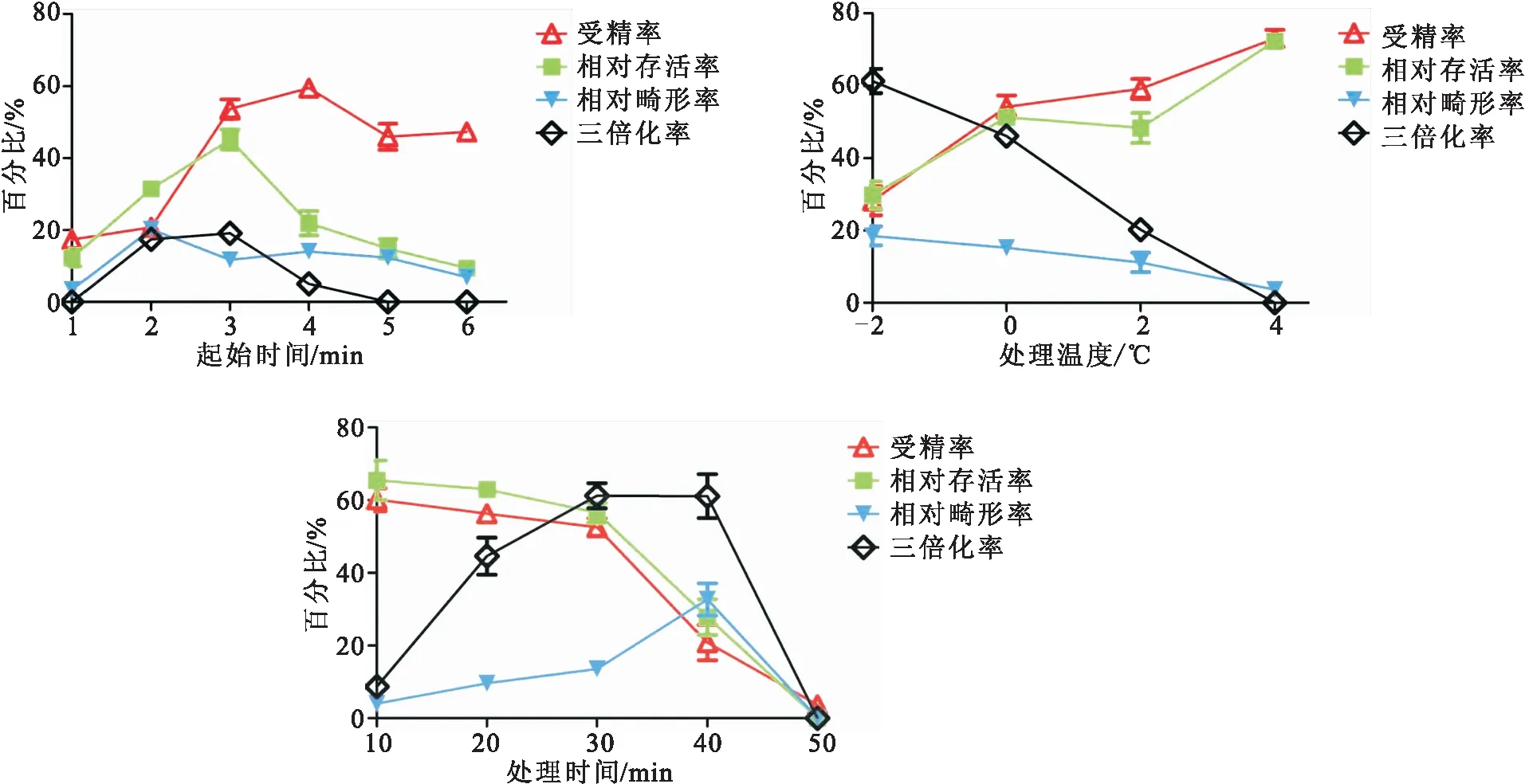
圖2 不同冷休克誘導條件下FR、SR、MR及TR的變化
2.2 熱休克最佳誘導條件的確定
在設定條件(Temp=36 ℃,DT=2 min)下進行熱休克處理最佳起始時間的篩選,結果表明受精卵在受精后6、7和8 min進行誘導可產生三倍體鱖魚苗,并且FR、SR和MR無顯著差異(P>0.05),其中受精后7 min進行熱休克處理的TR達到峰值,平均可達到26.6%(表2,圖3A),因此采用熱休克法誘導鱖三倍體的最佳起始時間為受精后7 min。在設定條件(BT=7 min,DT=2 min)下進行熱休克處理最適溫度的篩選,結果表明在34、36和38 ℃下誘導均能產生三倍體鱖魚苗,并且FR、SR和MR無顯著性差異,其中38 ℃下誘導的TR達到峰值,平均可達到30.0%(表2,圖3B),因此綜合考慮,采用熱休克法誘導鱖三倍體的最適處理溫度為38 ℃。在設定條件(BT=7 min,Temp=38 ℃)下進行熱休克處理持續時間的篩選,結果表明熱休克處理1 min、2 min和3 min均能誘導產生三倍體,其中處理3 min后TR達到峰值,盡管FR和SR略低于2 min時,但并無顯著性差異(表2,圖3C),因此綜合考慮,采用熱休克法誘導鱖三倍體的最適處理持續時間為3 min。
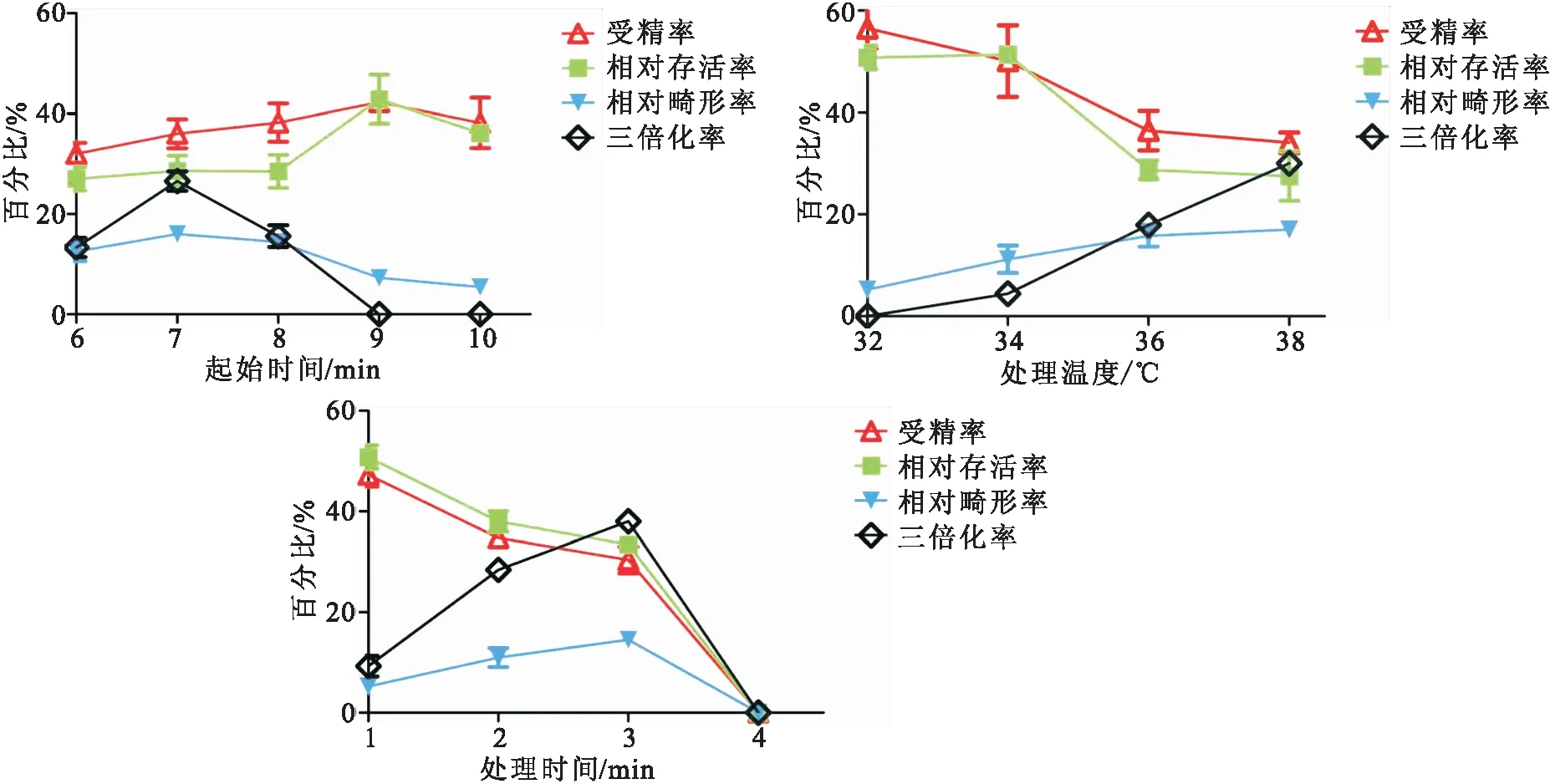
圖3 不同熱休克誘導條件下FR、SR、MR及TR的變化
2.3 優化條件下冷、熱休克方法的比較
由于親本的遺傳差異也會對溫度休克的效果造成影響[10],因此本研究在獲得兩種方法的優化條件后,又構建了三個全同胞家系來比較冷、熱休克法誘導三倍體鱖的實際效果。結果表明,采用冷休克法誘導(BT=3 min,Temp=0 ℃,DT=20 min),幼魚期(180 dph)平均存活率約為40.9%,其中平均TR約為55.40%;采用熱休克法誘導(BT=7 min,Temp=38 ℃,DT=3 min),三個家系均在孵化后25~30 d開始出現大量發育畸形的情況,最終1號和2號家系的TR盡管分別可達到26.97% 和22.81%,但幼魚期存活率均未超過10%,而3號家系幼魚期存活率僅為1.6%,其中無三倍體幼魚(表3)。該結果表明冷休克誘導更適用于鱖三倍體魚苗的規模化生產。
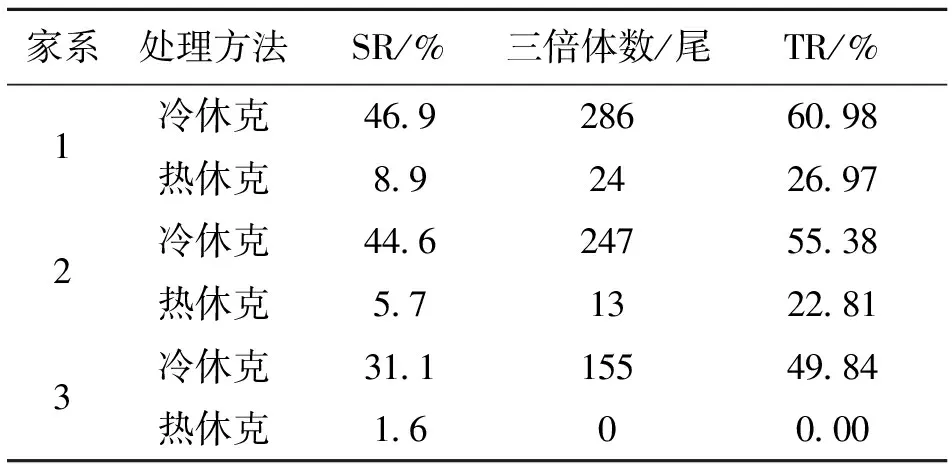
表3 冷、熱休克方法誘導效果比較
2.5 二倍體和三倍體鱖魚苗的生長性能比較
飼養過程中觀察到,二倍體和三倍體魚苗在卵黃囊吸收完全后均出現死亡高峰,而三倍體群體在體長約為20 mm時又出現一個明顯的死亡高峰,其中多數死亡個體為畸形,在飼養過程中未出現明顯的發病現象。對不同發育階段的二倍體和三倍體鱖的體長和體重進行t檢驗,結果表明孵化后10、20和40 d的二倍體與三倍體鱖魚苗的體長和體重均無顯著差異,60、100和150 d的三倍體鱖魚苗體長顯著高于二倍體,體重極顯著高于二倍體。生長速率方面,在孵化后40 d內,二倍體和三倍體鱖的體長和體重平均增長率均無顯著差異;孵化后40~150 d,二倍體的體長和體重平均增長率分別為0.102 cm/d和3.414 g/d,三倍體的體長和體重平均增長率分別為0.159 cm/d和5.037 g/d,均顯著高于二倍體;其中在孵化后40~60 d階段,二倍體和三倍體的生長速率均達到最高(表4,圖4)。綜上所述,鱖三倍體魚苗的生長性能優于二倍體,但也存在畸形率較高的問題。
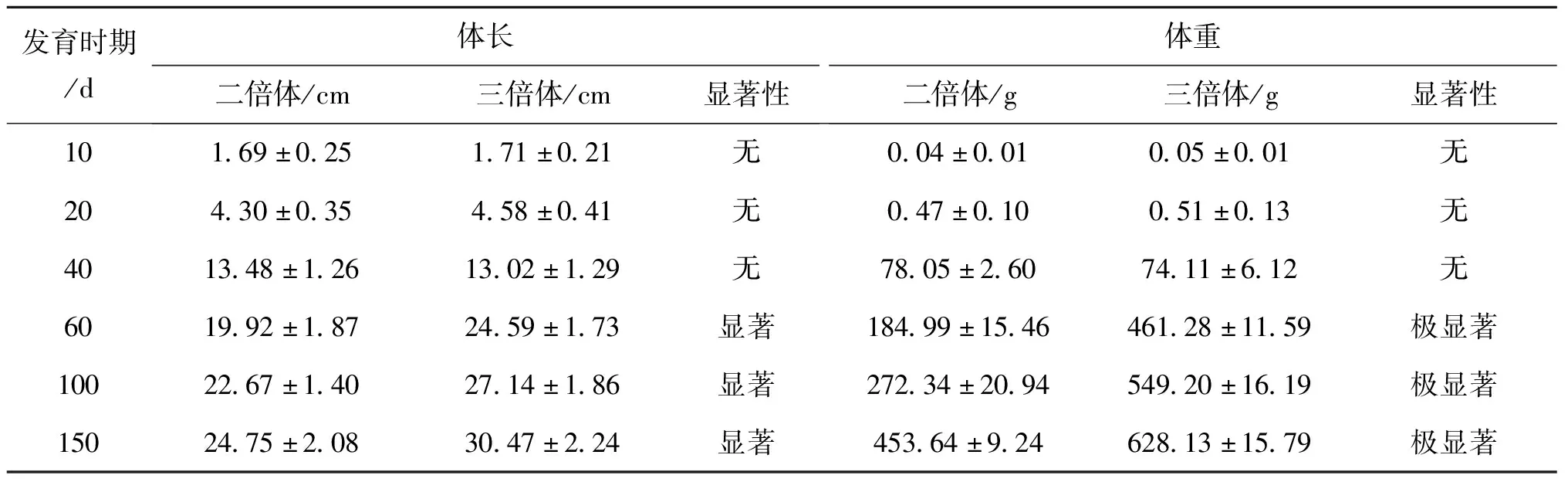
表4 二倍體和三倍體鱖在不同發育階段體長和體重比較
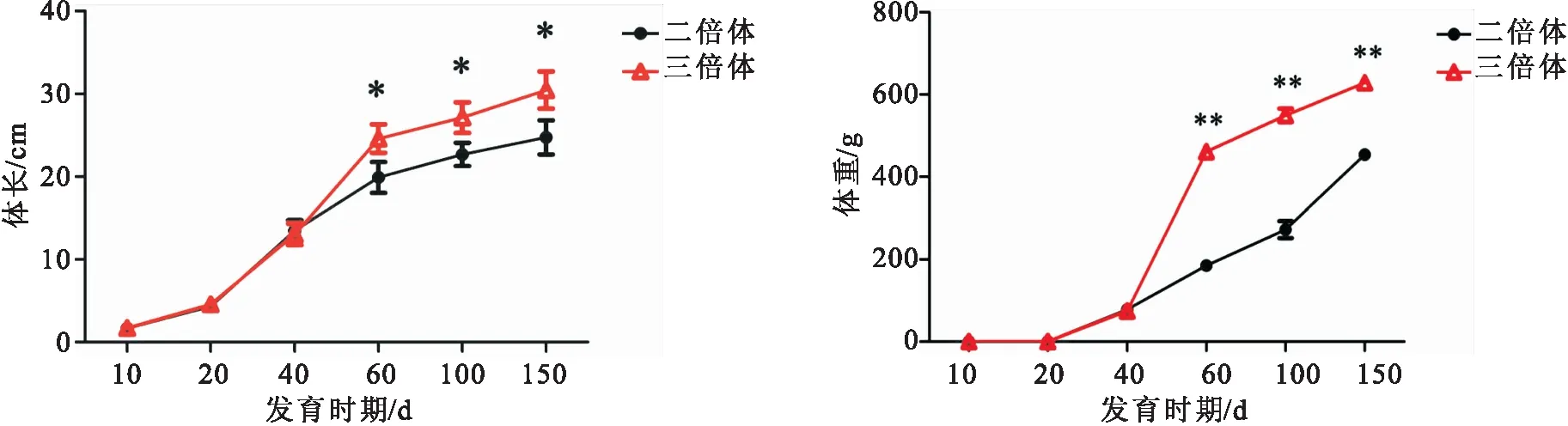
圖4 二倍體和三倍體鱖生長性能比較
3 討論
3.1 冷、熱休克誘導效果的比較
人工誘導魚類三倍體的主要方法包括冷休克法[13]、熱休克法[14]以及靜水壓法[15]。由于不同魚類的遺傳背景、生物學特性以及對溫度或壓力的敏感性有差異,因此這些方法不一定適用于所有的魚類,并且不同方法的誘導效率通常也有區別。靜水壓法的誘導率通常高于溫度休克法。例如在人工誘導大黃魚(Pseudosciaenacrocea)三倍體時發現,靜水壓法的誘導率要明顯優于冷休克法[16]。不過由于靜水壓休克設備要求較高,限制了批量化生產的效率,因此目前的研究更多采用溫度休克法誘導魚類三倍體。選擇冷休克法還是熱休克法需要根據不同物種自然生活環境的水溫來判斷,并通過反復試驗確定[17]。因為不同魚類受精卵對溫度的敏感性不同,從而造成了耐受溫度的差異,通常溫水性魚類采用冷休克法誘導,而冷水性魚類常采用熱休克法誘導,冷、熱刺激的溫度均不能超過該物種的自然致死溫度[18]。
Xu等[10]采用熱休克法誘導鱖三倍體時發現,在受精后8 min將受精卵置于41 ℃下熱休克處理2 min,可獲得40%的三倍體檢出率。本研究的結果與之有所區別,當孵化水溫高于40 ℃后,發現鱖受精卵及魚苗幾乎無法存活,這一結果與何利君[19]的結論較為一致。而在優化后的熱休克處理條件下,盡管仔魚期(孵化后8 d)的三倍體檢出率可達到38.0%,但在孵化后25~30 d開始出現大量發育畸形的情況,最終三倍體幼魚的存活率不足3%,推測可能是鱖的胚胎發育對高溫較為敏感導致的[19]。此外,在優化后的冷休克處理條件下,仔魚期(孵化后8 d)和幼魚期的三倍體檢出率分別為61.2% 和56.0%,表明相比于熱休克誘導,冷休克誘導更適用于鱖三倍體的規模化生產。不過本研究在飼養冷休克誘導的三倍體鱖時也發現,魚苗在體長約為20 mm時出現了一個明顯的死亡高峰,其中多數死亡個體為畸形,這可能是由于冷休克處理的時間較長,對胚胎造成了一定損害所導致的[18]。宋立民等在采用冷、熱休克兩種方法誘導黃顙魚三倍體時也發現了類似的現象[5]。
3.2 影響溫度休克誘導效果的因素
結合國內外學者對多種魚類進行溫度休克誘導的研究結果,適宜的休克起始時間、休克溫度和持續時間是保證三倍體誘導成功的關鍵因素和重要前提。而在不同魚類中或者在同一物種中利用不同的溫度休克方法時,這三個關鍵因素的重要性主次順序也有所不同。尤鋒[20]在采用冷、熱休克法對黑鯛(Sparusmicrocephalus)進行三倍體人工誘導時發現,兩種方法的三倍體率受三個因素影響程度的順序均依次為:持續時間>起始時間>處理溫度。而利用冷休克法誘導紅鰭東方鲀(Takifugurubripe)三倍體[21]和利用熱休克法誘導虹鱒(Oncorhynchusmykiss)三倍體[22]時,溫度休克持續時間也是影響三倍體率的最重要因素。宋立民等[5]利用冷休克法對黃顙魚進行三倍體人工誘導時發現,休克起始時間是TR和孵化率的重要影響因子,處理溫度則是畸形率的重要影響因子;而利用熱休克法誘導三倍體時,處理溫度是三倍體率、畸形率和SR的重要影響因子,次之為起始時間和持續時間。產生這種差異的原因目前尚不明確,而除了上述三個重要因子外,不同物種當中影響多倍體誘導效果的其他因素也不盡相同,親本的遺傳差異,受精卵的質量和生物性狀,以及休克處理時的具體環境條件等都是值得考慮的因素[5,9]。目前在關于鱖魚三倍體誘導的研究中,尚無對多因素影響的討論[10],未來將對此進行更為深入的研究。
3.3 二倍體和三倍體鱖魚苗的生長性能比較
人工誘導魚類三倍體的主要目的,是希望通過阻礙其性腺發育,提高生長速度和抗逆性能,提升肉質和產量,此外由于三倍體的不育性,也能有效防止其對原始生態系統的破壞[1]。然而關于三倍體魚類生長性能的研究,不同品種的魚類其結果也有差異。例如,楊興棋和陳敏容利用二倍體白鯽(Carassiusauratus)與四倍體白鯽交配獲得了異源三倍體白鯽,相比正常二倍體,其體型更大,生長更快[23]。而在歐洲黑鱸(Dicentrarchuslabrax)[24]和烏鱧(C.argus)[8]中發現,三倍體與二倍體的生長速度無顯著差異。大菱鲆(Scophthalmusmaximus)三倍體在性成熟前,與二倍體的生長無顯著差異,但達到初次性成熟后,三倍體生長顯著快于二倍體[25]。本研究發現,孵化后10~40 d的三倍體與二倍體鱖的生長速度無顯著差異,孵化后60~150 d的三倍體生長速度顯著快于二倍體,隨著二倍體鱖性腺的發育,兩者的生長性能變化仍需進一步研究。
4 結論
綜上所述,受精后3 min將受精卵置于0 ℃下冷休克處理20 min,然后轉移至26 ℃水體中繼續培養,此方法獲得魚苗的受精率為52.5%,相對存活率為56.6%,相對畸形率為13.6%,三倍化率為61.2%;最優的熱休克誘導條件為:受精后7 min將受精卵置于38 ℃下熱休克處理3 min,然后轉移至26 ℃水體中繼續培養,此方法獲得魚苗的受精率為30.4%,相對存活率為33.4%,相對畸形率為14.5%,三倍化率為38.0%。通過比較冷、熱休克法誘導的魚苗在幼魚期的存活率和三倍化率,證明了冷休克誘導更適用于鱖三倍體魚苗的規模化生產。通過比較二倍體和三倍體鱖在不同生長階段的生長速率,證明了三倍體鱖魚苗具有更為優良的生長性能。后續需要對冷休克法誘導鱖三倍體的條件進一步優化,提高誘導率,降低畸形率,以期達到滿足規模化生產的要求。

