介孔TiO2晶須-γ-Al2O3復合載體催化劑的制備及對二苯并噻吩的加氫脫硫性能
岳 凡,李 蒙,楊祝紅,花澤林,李 龍,李力成
(1.南京工業大學 化工學院,江蘇 南京 210009;2.南京林業大學 化學工程學院,江蘇 南京 210037)
近年來,環境問題逐漸受到大眾的廣泛關注,中國出臺的相關法規對污染排放控制也隨之愈發嚴格,其中GB 19147—2016《車用柴油》標準要求燃料油中的硫質量分數低于10 μg/g,這對目前工業上廣泛使用的油品加氫脫硫技術(HDS)提出了更高的要求,而催化劑性能的優劣是決定該技術的核心。
在眾多催化劑調控技術中,開發新型載體材料是提升加氫脫硫催化劑性能較為簡略的有效途徑之一。目前最為廣泛應用的加氫脫硫催化劑載體是γ-Al2O3,其具有高比表面積、高熱穩定性和良好的孔結構等特點[1-2]。但是γ-Al2O3與活性組分間有強相互作用,容易形成尖晶石結構的穩定物質,這類物質不利于硫化形成催化活性中心[3],導致所制得的催化劑脫硫性能下降,因此,僅以γ-Al2O3為載體的催化劑將難以應對更加嚴峻的挑戰。為了進一步提高催化劑的加氫脫硫性能,大量技術人員研究了其他類型的催化劑載體材料,如Zhang等[4]通過水熱法制備出鈦硅沸石納米棒(TS-1),負載鈷、鉬制備了CoMo/TS-1催化劑,經研究發現,TS-1骨架中的Ti物種可以增強Mo與TS-1間的相互作用,有助于暴露更多有利于加氫的活性位點,進而提高催化劑的加氫脫硫性能。Cortes-Jacome等[5]采用水熱法制備出高比表面積的氧化鈦納米管,并以此為載體制備出高分散的CoMoS催化劑,可表現出良好的脫硫性能。另外,Huang等[6]以四正丁基鈦酸為鈦源,采用溶膠-凝膠法制備TiO2-Al2O3復合載體,負載鎳、鉬制備出具有高活性的加氫脫硫催化劑。
由上可見,Ti的引入能夠有效避免純γ-Al2O3載體催化劑上存在的問題,通過將TiO2與γ-Al2O3載體進行復合,可以有效地發揮TiO2與γ-Al2O3各自的優勢,進而制備出優異的加氫脫硫催化劑。然而,常規TiO2作為載體存在比表面積小、機械強度差等缺點,雖然用溶膠-凝膠等[7-8]方法能夠制備出高比表面積的TiO2,但是制備成本高、工業化困難等缺點限制了其在工業方面的應用,將其進一步與γ-Al2O3進行復合,會對所制得的復合載體的孔結構、兩者間相互復合強度以及機械性能等因素產生負面影響。筆者所在課題組前期[9]從二鈦酸鉀(K2Ti2O5)晶須出發,成功制得比表面積大于 139 m2/g 的介孔TiO2晶須材料,所制得的TiO2成型載體抗破碎強度大于12 N/mm。劉金龍等[10]、朱銀華等[11]、Li等[12]以TiO2為載體制備HDS催化劑,均顯示出優異的催化活性。在此基礎上,溫廣明等[13]開展介孔TiO2晶須與γ-Al2O3的復合制備研究,可以有效克服常規TiO2與γ-Al2O3復合所存在的不足,并發現介孔TiO2晶須在復合載體中的最佳質量分數為5%,初步負載活性組分后,所得催化劑可表現出優異的加氫脫硫性能。
然而,已有文獻[14-15]對不同載體進行活性組分負載過程對比考察的結果表明,催化劑性能受到載體的表面性質、孔結構、晶相等多方面因素影響,所得到的實驗結果難以直接借鑒到其他類型的催化劑載體,故針對新型載體材料需要重新開展活性組分負載研究。因此,筆者對新型的介孔TiO2晶須-γ-Al2O3復合載體開展活性組分負載量的系統性研究,通過一系列技術手段對所制備的催化劑進行結構表征,并以DBT作為模型反應物對催化劑的性能進行評價。
1 實驗部分
1.1 試劑和原料
鉬酸銨((NH4)6Mo7O24·4H2O)、二硫化碳(CS2)、十氫萘(C10H18),均為分析純,國藥集團化學試劑有限公司產品;二苯并噻吩(C12H8S,質量分數99%),麥克林試劑有限公司產品;硝酸(HNO3,質量分數69%),國藥集團化學試劑有限公司產品。介孔TiO2晶須,自制,制備方法參考文獻[7];擬薄水鋁石,工業級,淄博萬霖化工科技有限公司產品;TiO2(比表面積11.9 m2/g),分析純,國藥集團化學試劑有限公司產品。
1.2 載體和催化劑的制備
采用常規的溶膠-凝膠法制備介孔TiO2晶須-γ-Al2O3復合載體,具體步驟如下:稱取10 g擬薄水鋁石放入裝有200 mL去離子水的三角燒瓶中,攪拌混勻;將三口燒瓶置于油浴鍋中加熱至70 ℃并保持恒溫,緩慢滴加稀硝酸,將混合物體系pH值調至1左右,加入0.5 g介孔TiO2晶須;繼續攪拌6 h,期間每隔0.5 h補充適量的稀硝酸維持體系pH=1;結束后,緩慢滴加適量氨水,將體系pH值調至9左右,形成復合膠狀物,陳化3 h后取出,用去離子水將其洗至pH=7,經抽濾、烘干、550 ℃ 焙燒2 h后得到介孔TiO2晶須-γ-Al2O3復合載體,記為TiO2-Al2O3。以常規TiO2為鈦源,采用同樣的方法制備TiO2質量分數為5%的復合載體,記為c-TiO2-Al2O3。
以(NH4)6Mo7O24·4H2O作為鉬源配制前驅體溶液,通過等體積浸漬法負載活性組分。將一定量前驅體溶液加入到載體中,經攪拌、陳化、干燥和500 ℃焙燒2 h后得到不同MoO3含量的介孔TiO2晶須-γ-Al2O3復合載體催化劑,記為x-MoO3/TiO2-Al2O3,其中x為MoO3的質量分數。另外,采用同樣的方法制備純γ-Al2O3為載體及c-TiO2-Al2O3為載體MoO3質量分數為20%的催化劑作為參比樣,分別記為20%MoO3/γ-Al2O3和20%MoO3/c-TiO2-Al2O3。
1.3 催化劑表征
采用美國Micromeritics公司TristarII 3020M型比表面孔隙吸附儀分析各個催化劑的孔結構,測試前,樣品在150 ℃下脫氣處理6 h,以N2作為吸附質在液氮(-196 ℃)下進行測定。樣品的微觀形貌結構分析以及EDX測試采用日立公司生產的Hitachi S-4800場發射掃描電鏡(FESEM)進行,操作電壓為5 kV。硫化后催化劑的形貌分析在JEOL JEM-2100透射電子顯微鏡上進行,通過TEM顯微照片確定的顆粒尺寸來統計評估MoS2顆粒的尺寸信息。樣品的晶體結構分析采用德國Bruke公司的D8 Adavance型X射線衍射儀,CuKα輻射源,管電流為100 mA,管電壓為40 kV,掃描范圍2θ=5°~80°,掃描步長為0.02°,掃描速率為20 s/step。樣品的拉曼光譜分析在配備CCD相機探測器的Horiba HR 800光譜儀上進行,采用波長為 514 nm Ar/Kr離子激光器作為激發光源,物鏡放大倍數為50倍,樣品激光功率不超過5 mV。氫氣程序升溫還原(H2-TPR)實驗在天津先權工貿發展有限公司的TP-5000型多用吸附儀上進行。硫化狀態催化劑的X-射線光電子能譜分析在ESCALAB 250光譜儀(美國Thermo Fisher Scientific公司產品)上進行,AlKαX射線激發源,功率300 W。
1.4 催化劑活性評價
催化劑的加氫脫硫性能在固定床微反應裝置上進行評價。將0.33 g催化劑放置在反應器的恒溫段,反應前將催化劑置于3%(質量分數)CS2/十氫萘溶液中,在溫度300 ℃、H2壓力2 MPa、H2流量20 mL/min、硫化液流量0.033 mL/min條件下預硫化處理6 h。預硫化結束后,將硫化液切換成1%(質量分數)DBT/十氫萘反應液,在溫度300 ℃、H2壓力2 MPa、氫/油體積比600、體積空速6 h-1的條件下進行反應。預反應5 h穩定后開始采集第一個產物,之后每隔1 h采集一次反應產物。反應產物采用山東魯南瑞虹化工儀器有限公司SP-6890 型氣相色譜儀進行檢測。DBT轉化率通過公式(1)計算。
(1)
DBT的加氫脫硫途徑主要有兩種[12]:直接脫硫(DDS)產物為聯苯(BP),氫化脫硫(HYD)產物為環己基苯(CHB)。DDS選擇性根據公式(2)計算。
(2)
式(1)和(2)中,win和wout分別為原料和產物中DBT的質量分數,%;w為產物中聯苯的質量分數,%。
2 結果與討論
2.1 催化劑的物性表征結果
2.1.1 XRD分析
圖1是TiO2-Al2O3復合載體和不同MoO3含量MoO3/TiO2-Al2O3催化劑以及20%MoO3/c-TiO2-Al2O3催化劑的XRD譜圖。由圖1可見,TiO2-Al2O3復合載體樣品在2θ為46.0°和67.0°處的衍射峰對應于γ-Al2O3相[16]的特征峰,而在2θ為25.3°和48.0°兩處微弱的衍射峰對應于銳鈦礦相TiO2[17]的特征峰。此外,當MoO3負載質量分數為25%和30%時,在2θ為23.5°處出現明顯的MoO3衍射峰[11],這主要是由于MoO3負載量過高,在載體表面發生了團聚所引起。當MoO3負載質量分數低于20%時,在MoO3/TiO2-Al2O3催化劑的XRD曲線上沒有出現MoO3衍射峰,表明在該范圍內活性金屬在載體表面具有良好的分散性,這有利于催化劑還原和提高反應活性。而20%MoO3/c-TiO2-Al2O3催化劑在2θ為25.3°、37.7°、48.0°、53.8°和55.1°處均出現明顯的銳鈦礦型TiO2的衍射峰[17],并且在2θ為23.5°處出現明顯的MoO3衍射峰。此結果表明20%MoO3/c-TiO2-Al2O3催化劑中的活性金屬發生團聚,生成了晶態MoO3,而MoO3負載質量分數為20%時,20%MoO3/TiO2-Al2O3催化劑中并沒有出現晶態MoO3的衍射峰。

圖1 TiO2-Al2O3復合載體以及負載不同含量MoO3的催化劑XRD圖譜
2.1.2 比表面積和孔結構分析
圖2為TiO2-Al2O3復合載體以及負載不同含量MoO3的催化劑的N2吸附-脫附等溫線。由圖2(a)可見,所有樣品的N2吸附-脫附等溫線均呈IV型,這表明所有材料均具有介孔結構[18]。圖2(b)的孔徑分布圖顯示,各催化劑以及復合載體的最可幾孔徑主要集中在5 nm左右,進一步證明復合載體催化劑具有介孔結構。
表1為復合載體及其不同MoO3含量催化劑的比表面積、平均孔徑及孔體積數據。由表1可知,TiO2-Al2O3復合載體的比表面積為308.7 m2/g,孔體積為0.56 cm3/g,平均孔徑為6.1 nm,具有豐富的孔結構。而常規TiO2為Ti源的c-TiO2-Al2O3復合載體的比表面積僅為203.4 m2/g,孔體積為0.32 cm3/g,平均孔徑為4.5 nm。負載活性組分MoO3后,所制得的催化劑比表面積和孔體積均有所降低,當MoO3負載質量分數為30%時,MoO3/TiO2-Al2O3催化劑的比表面積和孔體積最低;而20%MoO3/c-TiO2-Al2O3催化劑的比表面積遠小于20%MoO3/TiO2-Al2O3的。負載MoO3后催化劑的比表面積和孔結構數據減小是由于金屬負載于載體表面和孔道之中,導致載體部分表面以及小孔孔道被覆蓋或堵塞[19]。

圖2 TiO2-Al2O3復合載體與不同MoO3含量催化劑的N2吸附-脫附曲線和孔徑分布圖
2.1.3 Raman分析
圖3給出了不同MoO3負載量的MoO3/TiO2-Al2O3復合載體催化劑的Raman光譜圖。由圖3可知:所有催化劑在640 cm-1處出現的Raman信號峰對應于銳鈦礦型TiO2的特征峰[20];在865 cm-1處出現的Raman信號峰與低聚體MoOx中橋接Mo—O—Mo的對稱和反對稱伸縮振動有關[21],并且隨著催化劑中Mo含量增加,拉曼振動峰強度先增加后減少;在930~970 cm-1范圍內的寬信號峰可能與氧化鉬中的Mo=O的伸縮振動有關[22-23],當MoO3負載量較低時,930~970 cm-1幾乎沒有拉曼峰出現,隨著MoO3負載量增加,930~970 cm-1的拉曼信號峰強度明顯增加,表明在催化劑表面形成了更多 Mo=O 的Mo物種,有報道指出這種Mo物種有利于提高催化劑活性[24]。
2.1.4 SEM和TEM分析
圖4是5%MoO3/TiO2-Al2O3、20%MoO3/TiO2-Al2O3和30%MoO3/TiO2-Al2O3催化劑的SEM照片。由圖4可以看出,金屬負載量的增加并沒有對載體的形貌產生大的影響。為了證明氧化狀態的Mo在載體表面的分散度差異,采用SEM-EDX對 20%MoO3/TiO2-Al2O3和30%MoO3/TiO2-Al2O32個催化劑進行EDX測試,在每個催化劑中隨機取2點進行測試,結果如圖5所示。由圖5可知,MoO3

圖3 不同MoO3負載量的MoO3/TiO2-Al2O3復合載體催化劑Raman光譜圖
負載質量分數為20%時,催化劑表面所測得的Mo金屬元素的質量分數分別為13.17%和13.04%,Mo含量基本一致,表明MoO3質量分數為20%時在載體表面分散均勻;MoO3負載質量分數為30%時,催化劑表面所測得的Mo元素的質量分數分別為18.12%和19.51%,差別較大,此結果表明,MoO3質量分數為30%時,活性金屬在載體表面的團簇使局部Mo金屬含量偏高。圖6是新鮮硫化的20%MoO3/TiO2-Al2O3和30%MoO3/TiO2-Al2O3催化劑的TEM照片。TEM結果表明各催化劑表面的MoS2均呈現層狀結構。通過統計(對150個MoS2進行尺寸統計)和計算[25]得到20%MoO3/TiO2-Al2O3和30%MoO3/TiO2-Al2O3的MoS2片晶的平均長度分別為2.5 nm和2.7 nm,堆疊層數分別為1.9和2.0。
2.1.5 H2-TPR分析
圖7是不同MoO3含量MoO3/TiO2-Al2O3催化劑的H2-TPR圖譜。由圖7看到,所有催化劑的TPR曲線均在350~500 ℃范圍內出現1個明顯的還原峰,這對應于八面體配位的聚合Mo物種從Mo6+到Mo4+的還原過程。Zhou等認為,該類型的Mo物種與載體之間的相互作用弱,易于還原成具有優異加氫脫硫性能的活性物種[26]。MoO3負載質量分數低于20%時,催化劑還原峰峰值為475 ℃,當MoO3負載質量分數高于20%時,催化劑的還原溫度略有升高,還原峰的峰值由475 ℃升高至494 ℃,并且在500~600 ℃范圍內出現1個小的還

圖4 不同MoO3含量MoO3/TiO2-Al2O3催化劑的SEM照片

圖5 不同MoO3含量MoO3/TiO2-Al2O3催化劑的SEM-EDX譜

圖6 不同MoO3含量MoO3/TiO2-Al2O3催化劑的TEM圖
原峰。據報道,晶態MoO3在480、575和665 ℃處出現還原峰[27],而圖1的XRD結果顯示,MoO3負載質量分數超過20%時催化劑上會出現晶態MoO3,由此判斷該還原峰為晶態MoO3的還原峰。圖7中還看到,20%MoO3/γ-Al2O3催化劑的還原峰峰值在506 ℃,而MoO3/TiO2-Al2O3催化劑的還原峰峰值明顯低于506 ℃,表明TiO2的引入能夠有效減弱Mo與Al2O3之間的相互作用,從而促進形成更多的活性相。
2.1.6 XPS分析
圖8是硫化態的20%MoO3/TiO2-Al2O3催化劑的Mo 3d的XPS圖譜。由圖8可知,硫化后的催化劑主要存在2種價態的Mo物種,特征峰的結合能位置分別為232.5和238.6 eV,可歸屬于Mo6+物種[28](Mo VI: (232.5±0.1) eV 3d5/2, (238.6±0.1) eV 3d3/2),特征峰的結合能位置分別為229 eV和232.1 eV的可歸因于Mo4+物種(Mo IV:(229.0±0.1) eV 3d5/2, (232.2±0.1) eV 3d3/2)[28]。van Haandel等[29]對比研究了硫化前后的Mo物種結合能變化情況,發現硫化前催化劑中的Mo物種只在高結合能位置(232.5 eV和238.6 eV)出現特征峰,經硫化后,Mo物種在高結合能位置和低結合能(229.0 eV和232.3 eV)位置均出現特征峰,認為這是催化劑中高價態的Mo物種被還原成低價態Mo物種所致。同理,圖8中在低結合能處出現的Mo4+物種信號表明催化劑中Mo物種在硫化過程中發生還原。通過分峰計算可知20%MoO3/TiO2-Al2O3催化劑的硫化度為32.2%(硫化度計算公式:F=AMo4+/(AMo4++AMo6+)×100%,其中F為硫化度,AMo4+和AMo6+分別代表XPS中Mo4+和Mo6+的特征峰面積),Zhang等[30]在相同硫化條件下發現MoO3/Al2O3系列催化劑中Mo的硫化度為22%~31%,顯然,本實驗中MoO3/TiO2-Al2O3催化劑的硫化度更高,這可歸因于MoO3/TiO2-Al2O3催化劑中的TiO2促進了MoO3發生硫化。

圖7 不同MoO3負載量的MoO3/TiO2-Al2O3復合載體催化劑和20%MoO3/γ-Al2O3的H2-TPR譜圖
2.2 不同催化劑樣品的DBT加氫脫硫反應性能評價
不同催化劑的DBT加氫脫硫反應結果如表2所示。表2表明:MoO3/TiO2-Al2O3催化劑的DBT轉化率隨MoO3負載量增加呈先增加后降低的趨勢,當MoO3負載質量分數為20%時,MoO3/TiO2-Al2O3催化劑在當前的反應條件下表現出最佳的加氫脫硫性能,其DBT轉化率達到56%;20%MoO3/γ-Al2O3和20%MoO3/c-TiO2-Al2O3的DBT轉化率分別為49%和41%,由此可見介孔TiO2晶須-Al2O3復合載體作為脫硫催化劑載體可以表現出比純γ-Al2O3和常規TiO2為Ti源的復合載體更為優異的深度加氫脫硫性能。Ferdous等[31]報道,Ti的引入可以有效促進Mo在Al2O3催化劑表面形成更多活性多鉬氧化物。因此可以解釋介孔TiO2晶須-Al2O3復合載體催化劑的脫硫性能優于γ-Al2O3催化劑。常規TiO2為Ti源的c-TiO2-Al2O3載體催化劑的加氫脫硫活性低于介孔TiO2晶須-Al2O3復合載體催化劑和γ-Al2O3催化劑,可能是由于載體比表面積低,使得Mo金屬在載體表面團聚形成不利于催化活性的晶態MoO3。而另一方面,由2.1節表征結果可知,當MoO3負載量較低時,MoO3能夠在載體表面良好地分散,在該條件下,催化劑的活性位點數量隨負載量增加也得到了進一步的提升;然而,當負載質量分數高于分散閾值(20%)時,MoO3在載體的分散度有所下降,活性金屬團聚形成了難以還原的晶態MoO3,進而使得催化劑的DBT轉化率下降。
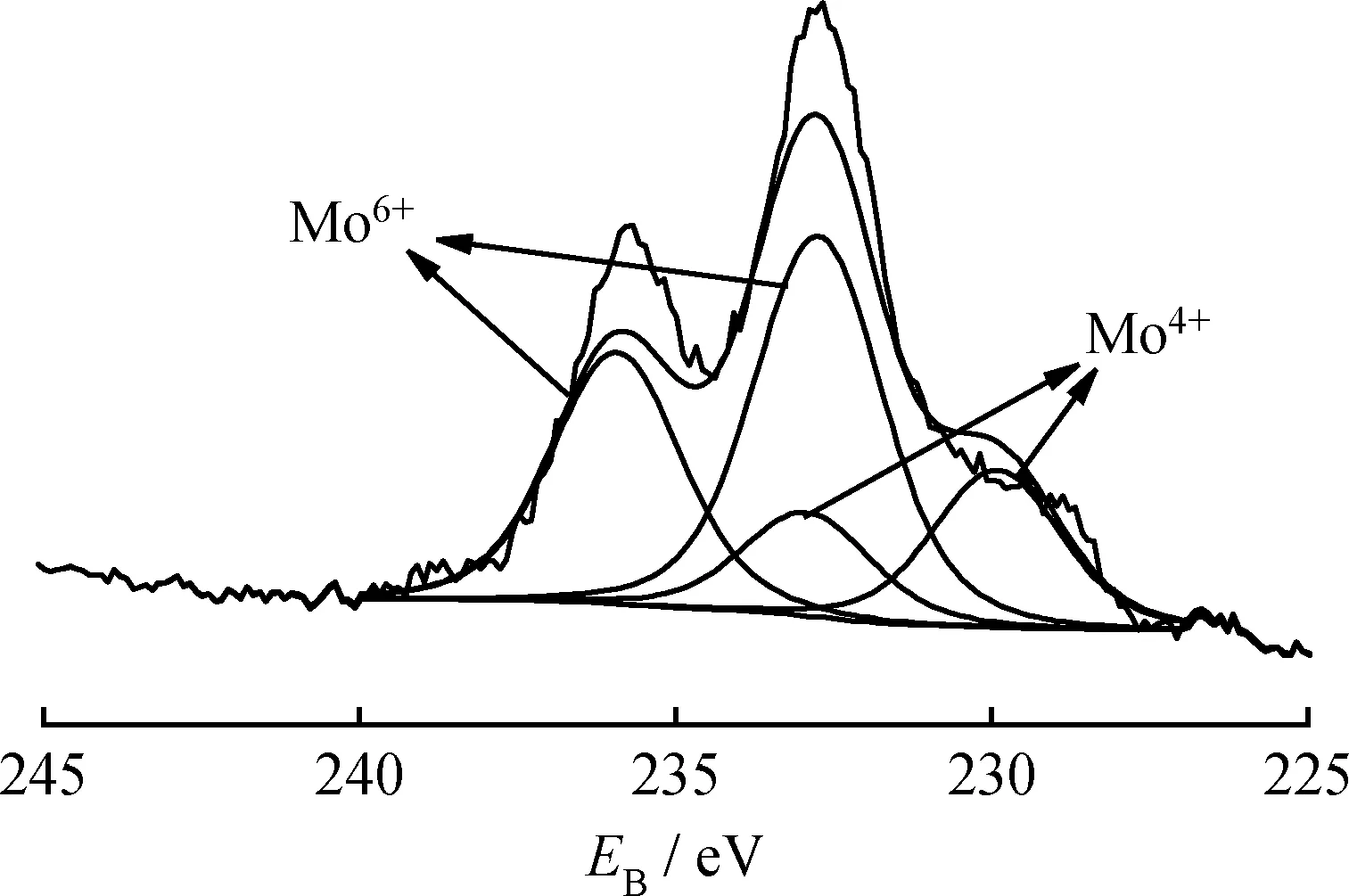
圖8 硫化后20%MoO3/TiO2-Al2O3催化劑的XPS譜圖
由表2可知,不同MoO3負載量的 MoO3/TiO2-Al2O3催化劑的DDS選擇性均在70%左右,表明MoO3負載量的變化沒有對催化劑的DDS選擇性產生明顯的影響。20%MoO3/c-TiO2-Al2O3催化劑的DDS選擇性在57%左右,而20%MoO3/γ-Al2O3催化劑的DDS選擇性僅為46%,明顯低于復合載體催化劑,表明Ti引入使得催化劑更加傾向于DDS路徑。Vazquez-Garrido等[32]和Guevara等[33]的研究結果同樣表明,TiO2能夠有效減弱活性金屬與Al2O3間相互作用,從而增加催化劑的DDS選擇性。

表2 不同催化劑加氫脫硫反應的DBT轉化率和DDS選擇性
3 結 論
制備了介孔TiO2晶須與γ-Al2O3復合載體(TiO2-Al2O3)及不同MoO3負載量的MoO3/TiO2-Al2O3催化劑,并進行了物性表征和對二苯并噻吩的加氫脫硫反應性能評價,發現當MoO3負載質量分數為20%時,MoO3在復合載體上分散良好,所制得的20%MoO3/TiO2-Al2O催化劑具有高的比表面積和豐富的介孔結構,活性組分易于還原,能夠展示出最佳的加氫脫硫性能,DBT轉化率達到56%,優于相同條件下純γ-Al2O3為載體的催化劑(49%)。

