血清戊糖素水平與骨質疏松性椎體壓縮性骨折相關性研究
肖軍 黃振峰 馬中希
武漢市第四醫院古田院區骨科,湖北 武漢 430032
骨質疏松癥是一種骨骼疾病,其特征是骨強度受損,導致骨脆性增加、骨折風險增加。研究表明,骨強度由骨密度和骨質量決定[1]。I型膠原蛋白是骨骼的組成成分,因此,骨強度可能受到骨中膠原纖維性質的影響。一些研究[2-3]表明,膠原蛋白的性質包括其成分和交聯,可以影響骨強度。為了評估膠原蛋白和骨骼特性之間的關系,有必要了解骨骼中膠原蛋白形成的過程。最初通過在相鄰膠原分子之間形成共價交聯來實現新形成的膠原纖維的穩定性。膠原蛋白交聯可分為以下兩種類型:賴氨酸羥化酶和賴氨酰氧化酶控制的交聯(酶交聯)及糖化或氧化誘導的晚期糖基化終點(AGE)產品交聯(非酶促交聯)[4]。酶促交聯可以改善骨強度[5],然而,研究結果[4,6]普遍認為非酶促交聯會破壞骨骼的生物學和機械功能。戊糖素(pentosidine)是一種眾所周知的AGE,被認為是骨中AGE的有用替代指標[4,6]。血清戊糖素濃度與骨強度呈負相關[7-8]。然而,尚不清楚血清戊糖素水平是否可能成為中國人骨質疏松性椎體壓縮性骨折(osteoporosis vertebral compression fracture,OVCF)的潛在標志物。因此,本研究旨在評估使用血清戊糖素水平作為OVCF潛在標志物的可行性。
1 材料與方法
1.1 一般臨床資料
選取2016年1月至2018年12月在武漢市第四醫院由于骨質疏松壓縮性骨折進行手術的110例患者作為研究對象,其中48名高能量創傷患者、車禍等交通事故受傷患者及高于1.8米的高空墜落患者被排除在研究之外。另外,28名未被確診為骨質疏松癥及患有慢性腎功能疾病、類固醇類疾病、多發性惡性腫瘤疾病的患者也被排除在本研究之外。此外,為了識別與骨質疏松癥相關的骨折,使用了50歲的臨界值[9]。年齡<50歲的患者也被排除在外。最后共篩選出33例50歲或以上低能量創傷導致脊椎骨折的受試者(8名男性、25名女性)作為椎體骨折組。同時,選取2016年1月至2018年12月在武漢市第四醫院接受健康檢查符合條件的58名50歲或以上的受試者。排除標準:糖尿病患者血清戊糖素水平升高或腎功能下降;服用過任何可能影響骨代謝藥物的患者,包括糖皮質激素、性激素、華法林和雙膦酸鹽等。所有受試者均簽署知情同意書。
1.2 方法
1.2.1骨密度檢測:使用雙能X線吸收測定法(DXA;GE Lunar,Medison,WI,USA)進行腰椎(L1~4)的骨密度(bone mineral density, BMD檢測。在骨折的情況下,使用另一側。腰椎和近端股骨的最低T評分用于確定骨質疏松癥。根據世界衛生組織(WHO)標準,T分數高于-1被定義為正常;低于-1至高于-2.5被定義為骨質減少;-2.5或更低被定義為骨質疏松癥。當T值低于-2.5合并骨質疏松性骨折時,該病例被歸類為嚴重的骨質疏松癥[10]。椎體骨折通過放射學平片檢查和磁共振成像診斷。OVCF患者中篩選出的33例患者為椎體骨折組,87例非椎體骨折的患者納入非骨折組。椎體骨折組受試者的平均年齡為76.5歲且所有患者均被診斷為骨質疏松癥。非骨折組受試者的平均年齡為68.4歲,在87名患者中,有38名被診斷患有骨質疏松癥。兩組的性別、年齡或BMD比較差異無統計學意義。見表1。
1.2.2生化標志物檢測:禁食一夜后于第二天早晨通過靜脈獲得受試者血液樣本,測量其空腹血糖、糖化血紅蛋白(HbA1c)、血尿素氮(BUN)、血清肌酐、血清堿性磷酸酶和骨鈣素水平,比較兩組間的生化測量結果。使用定量夾心酶聯免疫吸附測定(ELISA)試劑盒(Human Pentosidine ELISA Kit; My BioSource Inc.,San Diego,CA,USA)測量受試者血清戊糖素水平。
1.2.3骨折風險評估:所有受試者均回答問卷,使用亞洲版骨折風險評估(FRAX)工具計算其未來10年的骨折概率,以確定OVCF的重要危險因素。此外,還分析了FRAX與戊糖素水平之間的相關性。
1.3 統計學分析
使用SPSS 22.0 統計軟件對數據進行統計分析。使用卡方檢驗比較患者的性別、年齡和骨質疏松癥狀況。使用Mann WhitneyU檢驗分析臨床結果。分析FRAX與血清戊糖素水平之間的相關性以確定它們之間關系的顯著性。進行邏輯回歸分析以檢查每個因子對OVCF的貢獻。P<0.05被認為具有統計學意義。
2 結果
所有受試者的一般情況如表1所示,比較差異沒有統計學意義(P均>0.05)。椎體骨折組平均血清戊糖素水平為110.8 ng/mL,非骨折組為64.3 ng/mL。椎體骨折組與非骨折組之間的平均血清戊糖素水平比較差異具有統計學意義(P=0.04)。Logistic回歸分析顯示皮質類固醇的使用(OR=19.97,P=0.03)、吸煙(OR=14.82,P=0.01)、血清戊糖素(OR=1.03,P=0.01)、體重(OR=0.94,P=0.01)、HbA1c(OR=0.91,P=0.01)和BMD(OR=0.58,P=0.01)與OVCF顯著相關(表2)。然而,兩組受試者的空腹血糖(P=0.70)、HbA1c(P=0.70)、血肌酐(P=0.24)、BUN(P=0.33)、血液堿性磷酸酶(P=0.17)和血清骨鈣素(P=0.55)水平比較差異不具有統計學意義(表3)。
骨折組腰椎平均T值為-3.9,非骨折組腰椎T值為-2.4,比較差異不具有統計學意義(P=0.23),見表1。使用FRAX預測10年椎體骨折概率在椎骨骨折組中為19.1%,在非骨折組中為10.8%。椎體骨折組的10年骨折概率顯著高于非骨折組(P=0.02)。此外,血清戊糖素水平與FRAX結果之間存在明顯的正相關(r=0.35,P=0.02)。見圖1。

表1 受試者一般臨床資料Table 1 Subject’s general clinical data

表2 骨質疏松性椎體骨折的多變量回歸分析
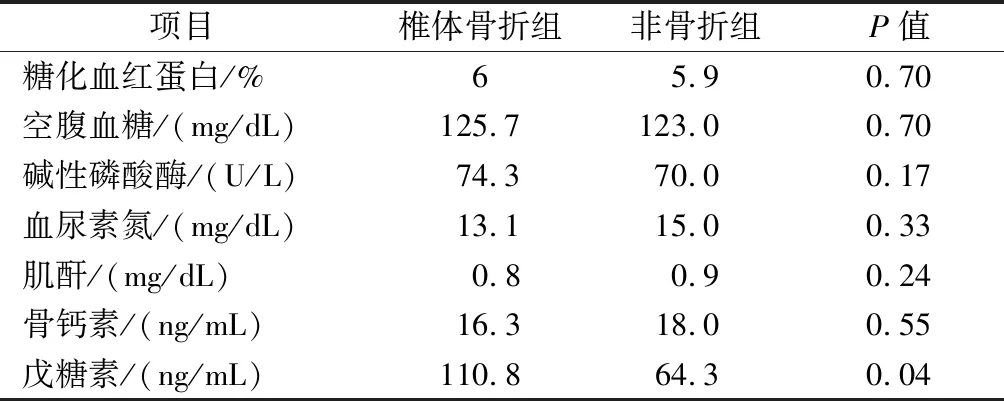
表3 椎體骨折組和非骨折組之間生化結果比較
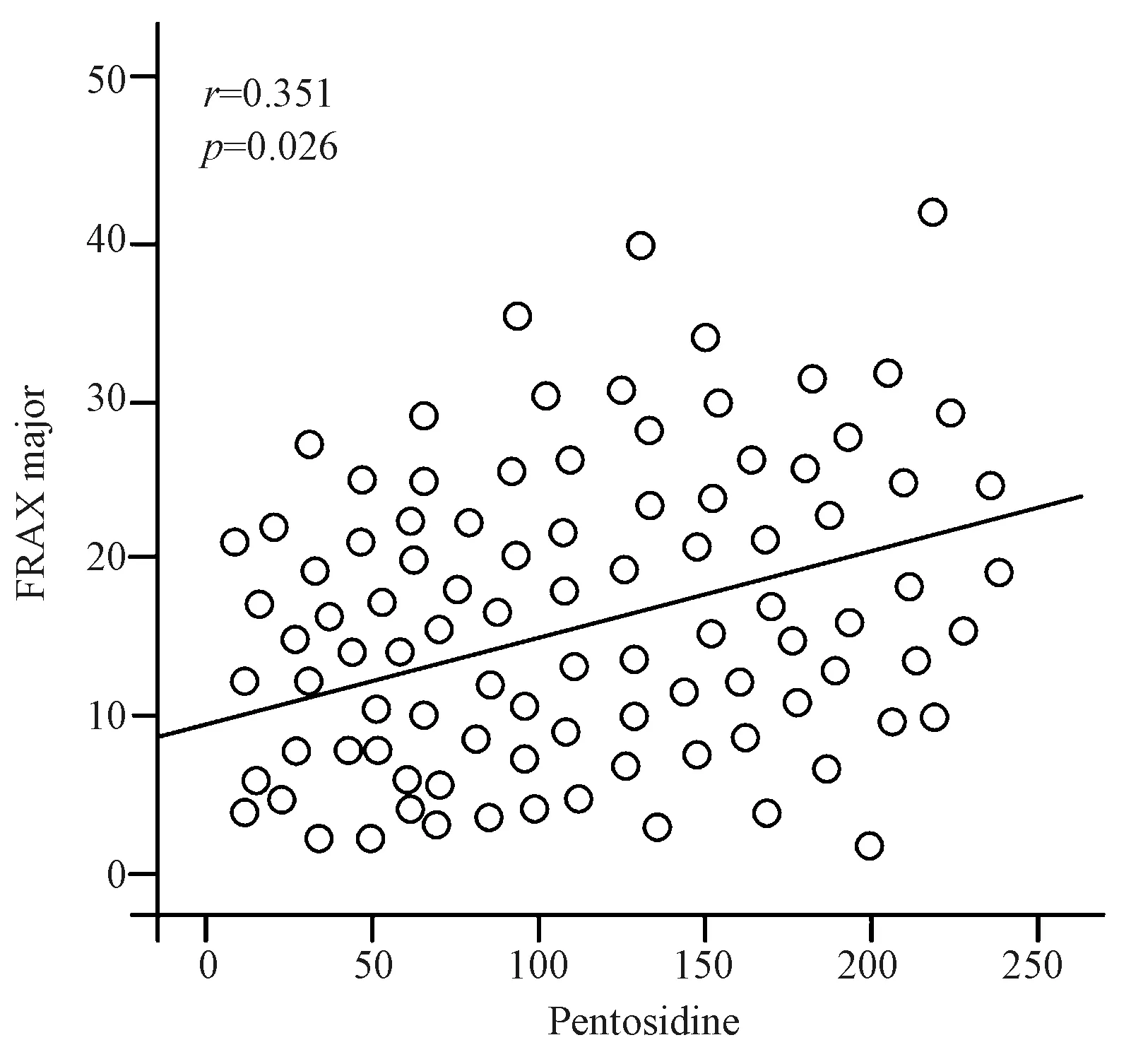
圖1 血清戊糖素水平與FRAX之間的關系Fig.1 Relationship between the serum pentosidine levels and FRAX
3 討論
戊糖素是一種在老年人細胞外基質發現的AGE[11]。戊糖素蓄積于低骨轉換率骨病患者體內,如糖尿病或雙膦酸鹽抑制骨吸收或人體衰老過程中的機體內[12]。為了消除可能影響血清戊糖素水平的因素,本研究排除了糖尿病患者和雙膦酸鹽類藥物使用者。此外,有可能影響骨代謝藥物史的人也被排除在外。
一些研究[13]表明,椎體皮質或骨小梁中的戊糖素含量與機械性能呈負相關。另據報道[14],血清戊糖素水平與皮質骨中的戊糖素具有顯著的線性相關性,進一步研究[15]發現戊糖素還具有降低成骨細胞的功能。它的積累使膠原纖維變脆并且會影響彎曲后的性能和韌性[16]。本次研究結果表明,血清戊糖素水平升高還可能是OVCF的潛在危險因素。
FRAX工具主要用于評估髖部和主要骨質疏松性骨折的個體化10年概率[17]。該工具基于個體患者模型,整合了與臨床危險因素和股骨頸BMD相關的風險[18]。FRAX評分反映了未來骨質疏松性骨折的可能性。在本研究中,使用FRAX計算的主要骨質疏松性骨折的10年概率在椎體骨折組中明顯高于非骨折組。此外,血清戊糖素水平與FRAX結果呈正相關(r=0.35,P=0.02)。
當然本研究也存在一定的自身局限性。首先,樣本量很小,統計功效較弱;其次,椎體骨折組和非骨折組之間存在非均勻的人口統計學數據;第三,沒有研究OVCF患者戊糖素水平性別差異。
綜上,本次研究結果表明血清戊糖素水平升高可能是OVCF的潛在危險因素。然而,為了獲得更高的可靠性,需要進行前瞻性的大型隊列研究,進一步探討OVCF高血清戊糖素水平潛在風險的真實影響。

