金匱腎氣丸調控β-catenin 通路治療去卵巢小鼠骨質疏松
陳一洲 葉勇健 李之斌 陳丹琦
絕經后骨質疏松癥(postmenopausal osteoporosis,PMOP)是一類以骨量流失,骨微結構異常導致骨骼脆性增加的代謝性疾病。中醫認為,PMOP 屬于“骨萎”范疇,其根本病機為“腎虛”。金匱腎氣丸作為溫補腎陽的經典代表方[1],廣泛應用于PMOP 患者的治療,取得一定的臨床療效。經典Wnt/β-catenin 信號通路在骨穩態平衡中發揮重要作用,其缺失或過度活化會導致骨量的驟降或激增[2-3],是治療PMOP 重要的分子靶點[4]。本實驗通過金匱腎氣丸干預去勢骨質疏松小鼠模型,驗證金匱腎氣丸防治PMOP 的療效,進一步探討其對β-catenin 信號通路的影響。
1 材料與方法
1.1 動 物 雌性10 周齡C57BL/6 小鼠24 只,體質量(20±2)g,由浙江中醫藥大學動物實驗中心提供[生產許可證號:SCXK(浙)2019-0008;使用許可證號:SYXK(浙)2019-0015]。小鼠飼養在濕度(40±5)%、溫度(23±2)℃,晝夜12h 更替的環境下,可自由飲水和進食。本研究經浙江省寧波市鄞州區第二醫院倫理委員會審核[審批號:(2019)倫審(31)號]。
1.2 藥物及試劑 戊巴比妥粉(中生瑞泰科技有限公司,批號921019),青霉素(規格:80 萬單位,山東魯抗醫藥股份有限公司,批號10121909073),4%多聚甲醛(Solarbio 公司,批號P1110),Alcian blue/hematoxylon(ABH)染液(Sigma 公司,美國,批號17372-87-1),Orange G 染液(Sigma 公司,美國,批號1936-15-8),核酸檢測試劑盒(Takara 公司,日本,批號9534),金匱腎氣丸(規格:72g/瓶,北京同仁堂,批號Z11020147)。
1.3 主要儀器 蔡司顯微鏡(Zeiss 公司,德國),Micro-CT(Skyscan 1170,Bruker 公司,比利時),骨形態計量儀(Osteometrics 公司,美國),熒光定量PCR儀(Termor 公司,美國)。
1.4 小鼠造模及分組 按照隨機數字表法,將小鼠分成假手術組、模型組和金匱腎氣丸組,每組8 只。造模方法:腹腔注射0.3%戊巴比妥(0.1mL/10g)麻醉后,常規皮膚剃毛消毒,于背部正中線作長約1.5cm的切口,沿背部肋弓緣、腰椎旁逐層進入腹腔,暴露兩側卵巢及輸卵管。其中模型組和金匱腎氣丸組摘除雙側卵巢及結扎輸卵管;假手術組8 只,摘除雙側卵巢周圍等量脂肪組織。檢查無活動性出血,逐層縫合傷口。術后連續3 天腹腔注射青霉素(每次6 萬,每天1 次)預防感染。
1.5 藥物干預 術后觀察3 天,所有小鼠均未出現切口感染或死亡,第4 天起開始藥物干預。根據實驗小鼠與成人的體表面積比例進行劑量換算[5],每只小鼠(體質量按20g 計算)灌胃劑量為0.2mL/天。金匱腎氣丸組小鼠予金匱腎氣丸溶液(72g 腎氣丸加熱溶于100mL 蒸餾水中,繼續加熱濃縮至含生藥1g/mL)0.2mL/天連續灌胃8 周。模型組小鼠給予等體積0.9%生理鹽水灌胃,假手術組小鼠不作處理。
表1 小鼠Micro-CT 骨微結構參數比較()

表1 小鼠Micro-CT 骨微結構參數比較()
注:假手術組予切除等量脂肪組織;模型組予切除雙側卵巢;金匱腎氣丸組予切除雙側卵巢+金匱腎氣丸灌胃;與假手術組比較,aP<0.05;與模型組比較,bP<0.05
1.6 Micro-CT 掃描分析 造模8 周后,摘取小鼠左側股骨,剔除周圍軟組織,置于Micro-CT 進行掃描檢測。掃描參數為:分辨率4000×2672,鋁板0.2μm,掃描層厚為10μm。骨微結構重點分析股骨干骺端松質骨的區域,具體檢測參數為:骨密度、骨體積分數、骨小梁數目、骨小梁間距和骨小梁厚度。
1.7 樣本制作 Micro-CT 掃描完成后,將股骨組織置于4%多聚甲醛中固定48h,隨后進行脫鈣、脫水及石蠟包埋處理,制作成3μm 厚度的石蠟切片。
1.8 特殊染色及定量分析 完成脫蠟復水后,將切片置于ABH 染液染色1h。0.3%鹽酸酒精分化、1%氨水返藍后,置于Orange G 染液浸洗1min。純水清洗,酒精梯度脫水,二甲苯透明,透明樹脂封片。使用骨形態計量儀對染色后的切片進行組織形態定量分析,包括骨小梁面積分數(%)、脂肪空泡面積比(%)和脂肪空泡直徑(μm)。
1.9 聚合酶鏈式反應(qRT-PCR) 摘取小鼠右側股骨,剔除周圍軟組織,PBS 清洗3 遍后,按照核酸檢測試劑盒進行熒光定量PCR 檢測β-catenin、鋅指結構轉錄因子(Osterix),堿性磷酸酶(ALP)mRNA 表達情況。
2 結果
2.1 金匱腎氣丸延緩PMOP 小鼠骨量流失 Micro-CT 檢測分析顯示,與假手術組比較,去卵巢后模型組小鼠股骨骨密度下降,骨結構破壞,骨小梁數量減少,間距增大(P 均<0.05),提示去卵巢PMOP 小鼠模型建立成功;與模型組比較,金匱腎氣丸組小鼠骨密度、骨體積分數、骨小梁數目和骨小梁間距均顯著改善(P 均<0.05)。見表1。
2.2 金匱腎氣丸改善PMOP 小鼠股骨遠端骨髓腔結構 小鼠骨組織經ABH 染色后,骨小梁呈橘色,骨髓細胞呈紫色和脂肪空泡呈白色圓形。ABH 染色及骨組織形態計量分析結果顯示,與假手術組比較,模型組小鼠骨小梁結構稀疏,髓腔內骨髓細胞排列紊亂,出現大量脂肪空泡。骨面積分數減少,脂肪空泡面積比和直徑變大(P 均<0.05);金匱腎氣丸治療后,小鼠股骨骨小梁明顯增粗,髓腔內骨髓細胞數量增多且排列有序。骨面積分數增加,脂肪空泡面積及直徑顯著減小(P 均<0.05)。見圖1,表2。

圖1 小鼠股骨病理(ABH 染色×100 倍)
表2 小鼠骨組織形態定量分析()
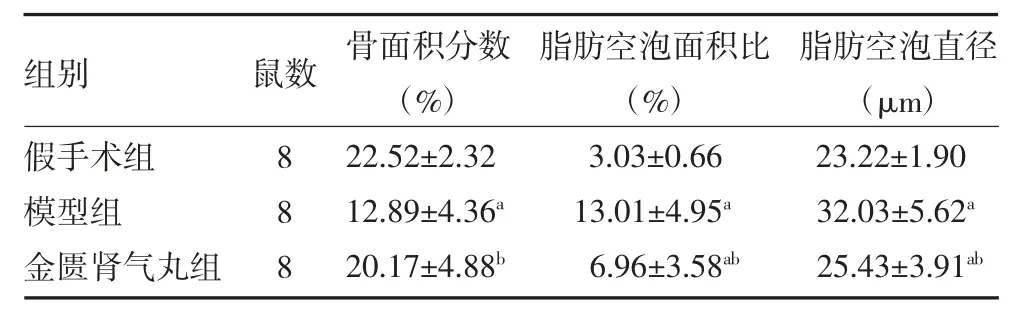
表2 小鼠骨組織形態定量分析()
注:假手術組予切除等量脂肪組織;模型組予切除雙側卵巢;金匱腎氣丸組予切除雙側卵巢+金匱腎氣丸灌胃;與假手術組比較,aP<0.05;與模型組比較,bP<0.05
2.3 金匱腎氣丸促進β-catenin 及其下游成骨基因表達 mRNA 定量檢測分析結果顯示,與假手術組比較,模型組β-catenin 及下游的成骨基因Osterix和ALP 表達顯著下降(P 均<0.05);與模型組比較,金匱腎氣丸干預8 周后,β-catenin、Osterix 和ALP的mRNA 表達明顯改善(P 均<0.05),見表3。
表3 β-catenin、Osterix 及ALP mRNA 定量分析(IOD/Area,)
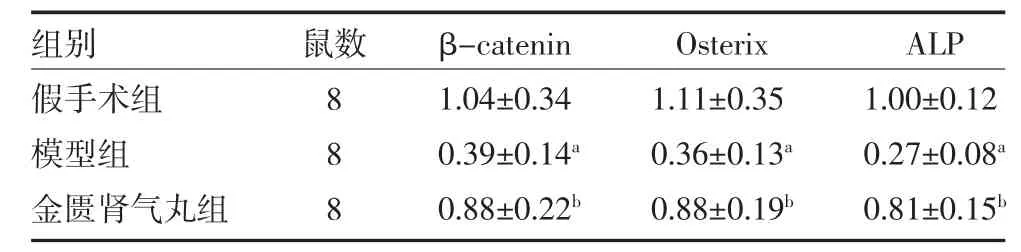
表3 β-catenin、Osterix 及ALP mRNA 定量分析(IOD/Area,)
注:假手術組予切除等量脂肪組織;模型組予切除雙側卵巢;金匱腎氣丸組予切除雙側卵巢+金匱腎氣丸灌胃;β-catenin 為β 連環蛋白;Osterix 為結構轉錄因子;ALP 為堿性磷酸酶;與假手術組比較,aP<0.05;與模型組比較,bP<0.05
3 討論
PMOP 是一類與干細胞分化異常相關的骨代謝性疾病[6-7]。干細胞具有自我更新及持續成骨分化的能力,在機體骨穩態維持中起關鍵作用。干細胞表面表達有雌激素受體,與雌激素特異性結合后,能促進干細胞向成骨細胞分化,抑制其成脂肪分化[8]。女性絕經后,雌激素水平下降,導致干細胞成骨-成脂分化異常,是PMOP 重要的細胞學發病機制。
根據中醫“腎藏精主骨”理論,中醫治療PMOP重在“補腎”。《醫經精義》指出,“腎藏精,精生髓,髓養骨,故骨者,腎之合也”。現代研究發現,“腎藏精主骨”的科學內涵主要體現在通過補腎來調控干細胞的增殖分化狀態,進而影響骨量和骨微結構[9-10]。金匱腎氣丸是“補腎”的經典方劑,其干預PMOP 可能是通過調控干細胞的分化實現的。
β-catenin 作為一個肌肉骨骼分子調控開關,能夠決定干細胞分化方向。經典Wnt 信號通路中,Wnt配體與細胞膜表面受體Frizzled 和LRP5/6 相結合,募集Disheveled 和Axin,破壞了穩定的四聚體結構,導致胞漿內β-catenin 堆積,經跨核膜轉激活下游成骨靶基因表達[11]。轉基因動物研究表明,β-catenin基因缺失會導致骨形成及骨礦化能力下降,出現嚴重的骨質疏松表型[12]。由此提示,β-catenin 是治療骨質疏松癥潛在的分子靶點。
本研究結果顯示,模型組小鼠骨量較假手術組顯著下降,骨微結構破壞明顯,提示PMOP 小鼠模型成功建立。金匱腎氣丸干預8 周后,PMOP 小鼠骨量丟失減少,證明金匱腎氣丸能夠有效防治去勢小鼠PMOP 的發生。病理上,造模組小鼠骨小梁稀疏,髓腔內脂肪空泡堆積;金匱腎氣丸治療后,脂肪空泡數量顯著減少,并且代替以正常的骨髓細胞及骨小梁,提示去勢造模后,小鼠骨內存在干細胞成骨-成脂分化異常,而金匱腎氣丸能夠調控干細胞向成骨細胞分化,從而改善小鼠骨量丟失。Osterix 和ALP 是經典Wnt/β-catenin 信號通路下游的成骨靶基因。Osterix是MSCs 成骨分化的特異性轉錄調節因子,ALP 具有促進羥磷灰石沉積,能夠反映成骨形成能力。qRTPCR 結果顯示,去勢造模后,小鼠股骨β-catenin 及下游Osterix 和ALP 的mRNA 表達明顯減少,可能導致干細胞成骨分化減弱。金匱腎氣丸能夠激活βcatenin 信號通路,促進下游的Osterix 和ALP 靶基因的表達,影響MSCs 成骨-成脂分化,延緩去勢小鼠骨量流失和骨微結構破壞。
綜上所述,金匱腎氣丸可能通過激活β-catenin信號通路及下游Osterix、ALP 成骨基因表達,進而調控干細胞成骨分化,防治去勢小鼠骨質疏松。

