Polymyxin NP實驗篩查腸桿菌科多黏菌素耐藥菌株臨床評價
唐 瑜, 沈平華, 史保慶, 蔣曉飛
(1. 上海交通大學附屬胸科醫院檢驗科,上海 200030;2. 上海市第一婦嬰保健院檢驗科,上海 200040;3. 棗莊市市中區礦務局醫院檢驗科,山東 棗莊 277100);4. 復旦大學附屬華山醫院檢驗科,上海 200040;
碳青霉烯類耐藥腸桿菌科細菌(carbapenemresistantEnterobacteriaceae,CRE)引起的臨床感染在全球范圍內均有報道,由于可選的抗菌藥物十分有限,CRE已成為臨床抗感染治療面臨的重大挑戰[1]。多黏菌素被認為是治療CRE感染的最后一道防線,但其耐藥率也呈逐漸上升趨勢。目前實驗室的常規檢測方法(紙片擴散法、E試驗和儀器法等)無法有效、準確地檢出多黏菌素耐藥菌株[2-5],微量肉湯稀釋法操作繁瑣,且費時費力[2]。NORDMANN等[6]建立的Polymyxin NP實驗操作簡便,可以在2~4 h內快速檢出對多黏菌素耐藥的腸桿菌科細菌。本研究擬對臨床分離的461株腸桿菌科細菌進行Polymyxin NP實驗初篩,并采用微量肉湯稀釋法進行驗證,采用實時定量聚合酶鏈反應(realtime quantitative polymerase chain reaction,qRT-PCR)、聚合酶鏈反應(polymerase chain reaction,PCR)及測序法分析各菌株多黏菌素耐藥機制,探討Polymyxin NP實驗在多黏菌素耐藥菌株檢測中的臨床價值。
1 材料和方法
1.1 菌株來源及分類
收集2016年2—6月復旦大學附屬華山醫院腸桿菌科非重復臨床分離株,采用VITEK-2 compact微生物鑒定系統(法國生物梅里埃公司)對所有菌株進行鑒定。461株腸桿菌科細菌中,肺炎克雷伯菌292株(63.34%)、大腸埃希菌160株(34.71%)、陰溝腸桿菌7株(1.52%)、產酸克雷伯菌2株(0.43%)。分離自痰液樣本201株(43.60%)、尿液樣本177株(38.39%)、血液樣本24株(5.21%)、引流液樣本21株(4.56%)、膽汁樣本8株(1.74%)、其他樣本30株(6.51%)。
1.2 體外藥物敏感性試驗
采用紙片擴散法檢測461株腸桿菌科細菌對臨床常用抗菌藥物的敏感性,替加環素耐藥折點參考歐洲抗菌藥物敏感性試驗委員會(European Committee on Antimicrobial Susceptibility Testing,EUCAST)的判讀標準[7],其他藥物敏感性結果評判以美國臨床實驗室標準化委員會(Clinical and Laboratory Standards Institute,CLSI)抗菌藥物敏感性試驗2014版要求為標準[8]。采用微量肉湯稀釋法測定菌株對多黏菌素的最小抑菌濃度(minimum inhibitory concentration,MIC),并以該結果為標準,與Polymyxin NP實驗結果進行比對。質控菌株大腸埃希菌(ATCC 25922)購自上海臨床檢驗中心。
1.3 Polymyxin NP實驗
參考文獻[6]的方法預先配制Polymyxin NP實驗所需溶液。(1)A液:準確稱量M-H肉湯粉末25 g、酚紅指示劑0.05 g,溶解于800 mL去離子水中,然后用鹽酸溶液調節pH值為6.7,加水補足至900 mL。標準大氣壓下,121 ℃高壓滅菌15 min,待恢復至室溫(22~24℃)后,加入100 mL無菌的10%葡萄糖溶液,混勻后備用。(2)B液:在A液中加入多黏菌素(美國Sigma-Aldrich公司)至終濃度為5 μg/mL。挑取新鮮培養的待測菌株、陰性對照菌株[大腸埃希菌(ATCC 25922)]和陽性對照菌株(奇異變形桿菌),用0.9%氯化鈉溶液調成3.0~3.5麥氏濃度的菌懸液,用于后續實驗。在無菌96孔培養板的A1~A6孔中加入150 μL A液,作為每組的生長對照,在B1~B6孔中加入150 μL B液(含5 μg/mL多黏菌素);在A1和B1孔中分別加入50 μL 0.9%氯化鈉溶液作空白對照,A2和B2孔中分別加入50 μL已配制好的大腸埃希菌(ATCC 25922)菌液作陰性對照,A3和B3孔中分別加入50 μL奇異變形桿菌菌液作陽性對照,其余每組的A和B孔中分別加入50 μL待測菌株菌液,B孔中多黏菌素終濃度為3.75 μg/mL,在36 ℃條件下孵育4 h,觀察并記錄顏色變化。結果判讀:當空白對照2孔均為橙色,其余各組生長對照(A孔)均為黃色,則實驗結果有效;若B孔溶液由橙色變為黃色,表示Polymyxin NP實驗結果為陽性,提示該菌對多黏菌素耐藥。
1.4 PCR擴增
采用高溫煮沸法裂解細菌,提取總DNA為模板,采用PCR擴增質粒介導的多黏菌素耐藥基因mcr,擴增引物見表1,擴增產物經測序進一步驗證;采用PCR擴增肺炎克雷伯菌染色體上的pmrA、pmrB、phoP、phoQ和mgrB基因,引物設計參考文獻[9],PCR擴增產物測序后與NCBI數據庫(www.ncbi.nlm.nih.gov)中的信息進行比對,分析序列變異性。

表1 擴增多黏菌素耐藥基因mcr引物序列
1.5 qRT-PCR
采用qRT-PCR檢測phoP、phoQ、pmrD、pmrC、pmrA、pmrB和pmrK基因的轉錄水平。首先將菌株培養至對數期[600 nm處吸光度(A)值為0.8~0.9],取1 mL培養物,按RNA抽提試劑盒(德國Qiagen公司)說明書要求提取總RNA。采用SYBR PrimeScript RT-PCR試劑盒(日本Takara公司)進行逆轉錄和基因轉錄的定量檢測,引物設計參考文獻[9],以多黏菌素敏感的肺炎克雷伯菌標準株(ATCC 13883)(購自上海臨床檢驗中心)為參考,分析耐藥菌株中雙組分調控系統相關基因的表達水平。
1.6 統計學方法
采用Excel 2016及GraphPad Prism 6軟件進行統計分析。計數資料采用率表示,組間比較采用χ2檢驗。以P<0.05為差異有統計學意義。
2 結果
2.1 Polymyxin NP實驗結果及多黏菌素耐藥腸桿菌科細菌檢出情況
461株腸桿菌科細菌中,Polymyxin NP實驗篩查顯示13株為陽性,耐藥率為2.81%。其中肺炎克雷伯菌10株,陰溝腸桿菌2株,大腸埃希菌1株,Polymyxin NP實驗陽性菌株MIC見表2,部分Polymyxin NP實驗結果見圖1。微量肉湯稀釋法藥物敏感試驗結果顯示,Polymyxin NP實驗陽性的菌株對多黏菌素的MIC值均達到耐藥水平,符合率為100%。未發現2種方法結果不一致的情況。
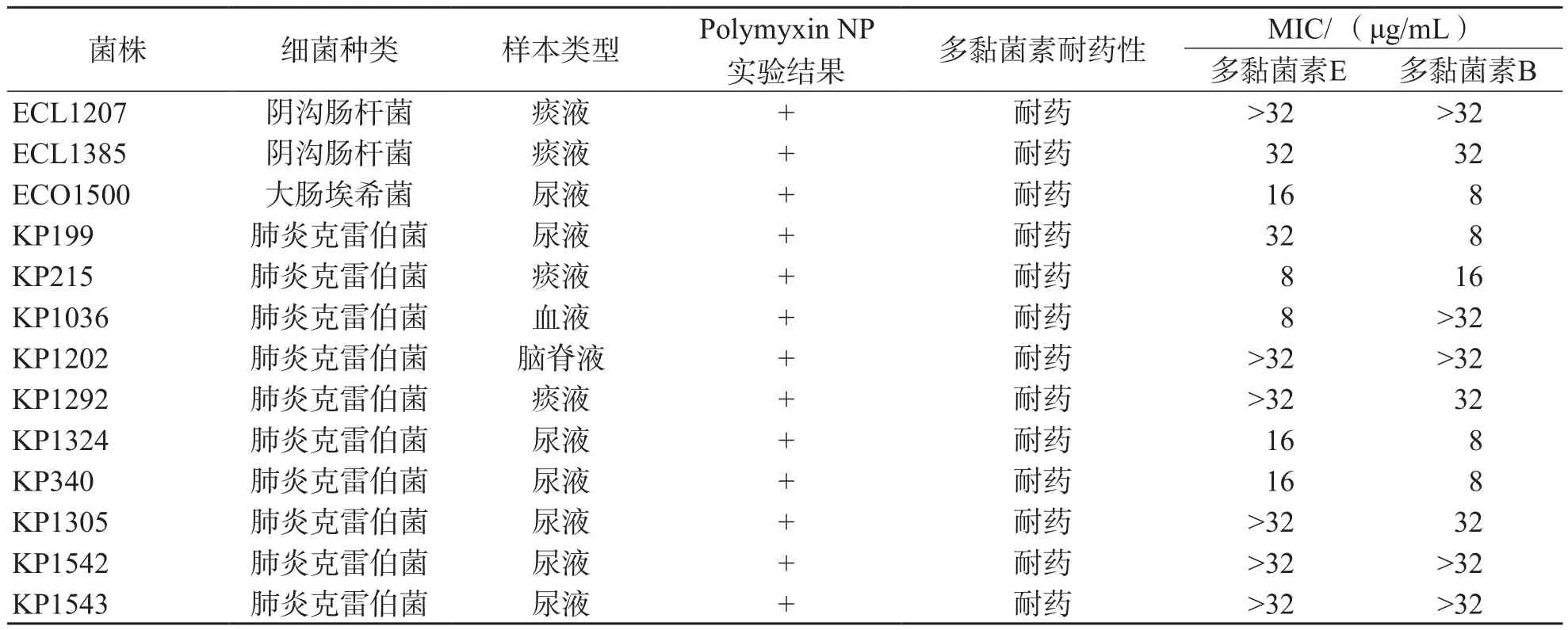
表2 Polymyxin NP實驗陽性菌株信息和多黏菌素MIC結果
2.2 體外藥物敏感性試驗結果
461株腸桿菌科細菌對多種頭孢菌素(頭孢唑啉、頭孢呋辛、頭孢噻肟和頭孢吡肟)、環丙沙星、哌拉西林的耐藥率>75%,對替加環素的耐藥率為7.16%。多黏菌素耐藥菌株和敏感菌株對多種常用抗菌藥物(慶大霉素、頭孢唑啉、頭孢呋辛、頭孢噻肟、頭孢美唑、頭孢他啶、亞胺培南、美羅培南和替加環素)的耐藥率差異無統計學意義(P>0.05)。見表3。

圖1 部分Polymyxin NP實驗結果
2.3 多黏菌素耐藥菌株的耐藥機制分析
13株多黏菌素耐藥腸桿菌科細菌中,mcr基因擴增后,經1%瓊脂糖凝膠電泳分析及測序確認,大腸埃希菌ECO1500攜帶質粒介導的多黏菌素耐藥基因mcr-1(圖2)。對多黏菌素耐藥菌株進行雙組分調控系統相關基因PCR篩查發現,10株肺炎克雷伯菌均含有pmrA/pmrB和PhoP/PhoQ雙組分調控系統,2株陰溝腸桿菌和1株大腸埃希菌為陰性。對10株雙組分調控系統陽性的肺炎克雷伯菌進行pmrA、pmrB、phoP、phoQ和mgrB基因測序及qRT-PCR,結果顯示有3株(KP1305、KP1542和KP1543)mgrB基因有ISKpn14插入突變,KP340的pmrB位點出現了R256G突變;其余6株pmrK基因表達水平均有不同程度的上調,最低為9.6倍,最高為31倍,KP1202和KP199的pmrA、pmrD、phoP和phoQ基因也明顯上調。各基因的相對表達水平見表4。
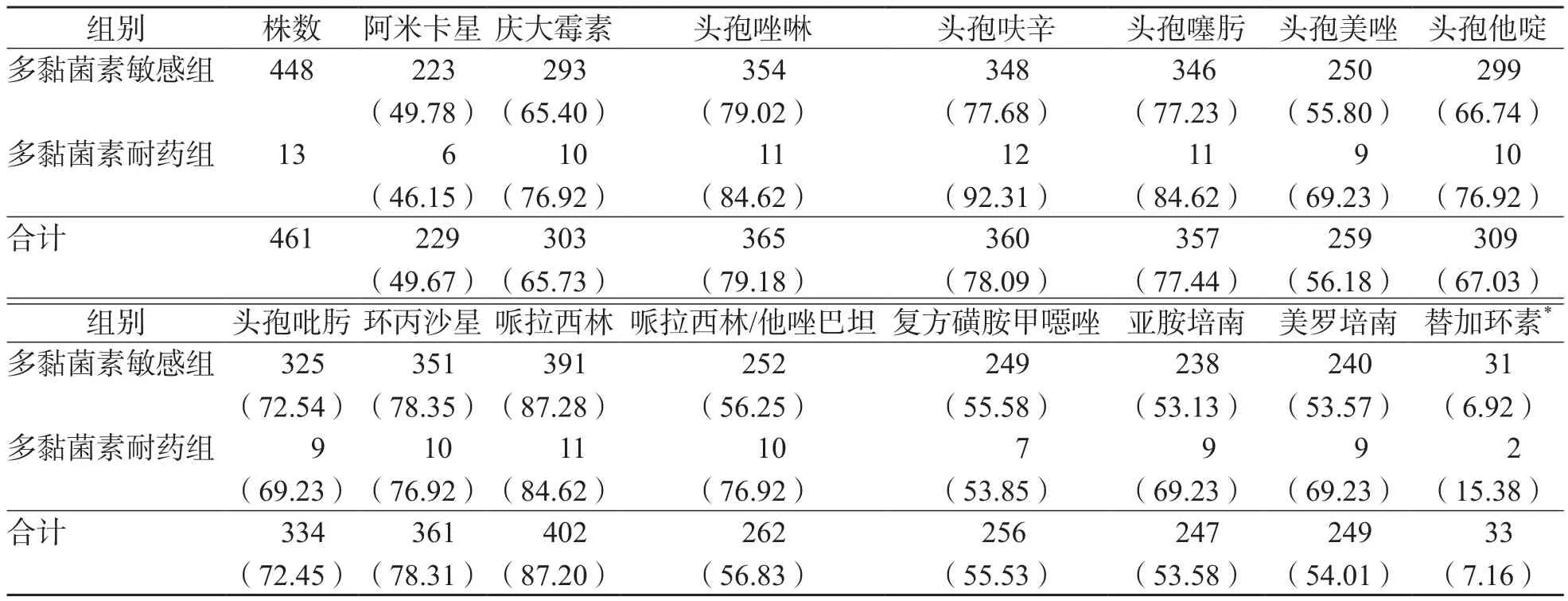
表3 腸桿菌科細菌對臨床常用抗菌藥物的耐藥情況
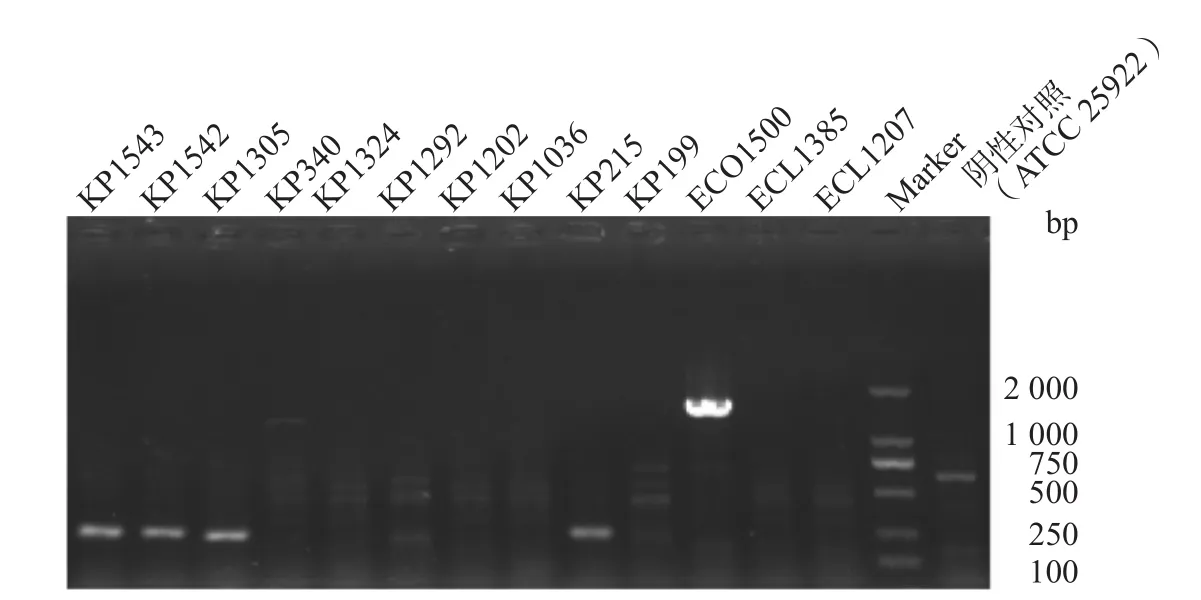
圖2 mcr基因檢測結果電泳圖
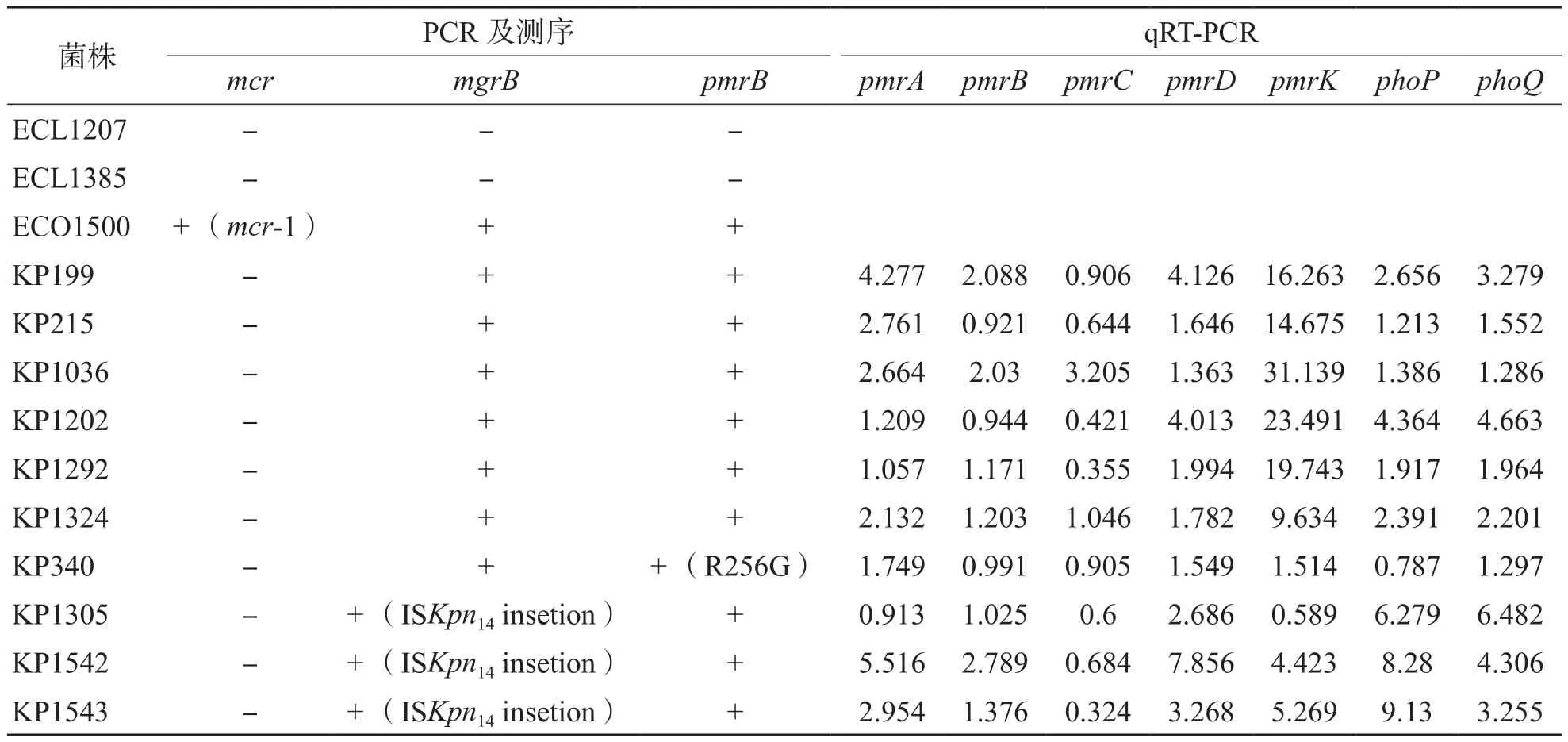
表4 13株多黏菌素耐藥菌株的耐藥機制分析
3 討論
腸桿菌科細菌是臨床主要的條件致病菌,可引起嚴重的非社區性感染,如肺炎、血流感染、腹腔感染和中樞神經系統感染等[10]。多重耐藥腸桿菌科細菌在全球范圍內的廣泛流行已成為臨床抗感染治療的一大難題[11]。多黏菌素(E和B)被認為是治療多重耐藥腸桿菌科細菌感染的最后一道防線[12-13]。近年來,多黏菌素耐藥腸桿菌科細菌在全球的報道逐漸增多,尤其是質粒介導的多黏菌素耐藥基因mcr在社區和醫院環境的出現和快速播散,使得腸桿菌科細菌的耐藥形勢更為嚴峻,尤其是在CRE流行的國家和地區,因此有必要在臨床工作中進行多黏菌素藥物敏感性監測[5,14]。
目前臨床實驗室的常規檢測方法,如紙片擴散法、E試驗或儀器法等均無法有效檢出多黏菌素耐藥菌株。微量肉湯稀釋法操作繁瑣、耗時長,難以在實驗室日常工作中進行。此外,由于染色體介導的多黏菌素耐藥機制復雜多樣,分子檢測方法同樣不適用于多黏菌素耐藥菌株的檢測[2,5]。
Polymyxin NP實驗可以在2~4 h內快速檢出對多黏菌素耐藥的腸桿菌科細菌,該方法利用腸桿菌科細菌生長過程中的糖類代謝特征,即腸桿菌科細菌發酵葡萄糖產酸,pH值改變使酸堿指示劑酚紅由橙色轉變為黃色,從而達到檢測的目的[12]。Polymyxin NP實驗結果與CLSI和EUCAST推薦的微量肉湯稀釋法結果一樣可靠,但更加簡單、快速,且不需要苛刻的實驗條件,一般的臨床微生物實驗室均可開展,是非常理想的多黏菌素耐藥菌株監測方法。本研究納入的461株腸桿菌科細菌中,13株多黏菌素耐藥株在2 h內均表現為Polymyxin NP實驗陽性,所有多黏菌素敏感菌株均表現為陰性結果。13株多黏菌素耐藥株中,肺炎克雷伯菌主要由染色體上的mgrB基因發生插入突變和雙組分調控系統pmrA/pmrB、PhoP/PhoQ突變或表達上調介導,大腸埃希菌則由質粒攜帶的mcr-1基因介導,而以上多黏菌素耐藥相關基因在陰溝腸桿菌中均未被檢出,提示陰溝腸桿菌對多黏菌素的耐藥性由其他機制介導。上述結果表明,Polymyxin NP實驗對不同機制的介導的多黏菌素耐藥腸桿菌科細菌均具有良好的檢出率和準確性,可以用于多黏菌素耐藥腸桿菌科細菌的臨床篩查。
相較于歐美國家,我國的多黏菌素耐藥率較低[15-16]。多黏菌素耐藥一般由染色體上的基因突變pmrA/pmrB和PhoP/PhoQ表達上調引起,常出現在肺炎克雷伯菌中,但近年來隨著質粒介導的mcr基因的出現和播散,多黏菌素耐藥性可通過質粒介導的基因水平轉移在種屬內和不同種屬之間傳播,mcr基因主要流行于大腸埃希菌和肺炎克雷伯菌中[5,9,16-17]。此外,鮑曼不動桿菌、銅綠假單胞菌等革蘭陰性菌對多黏菌素耐藥的報道和研究也日益增多,但不動桿菌屬、假單胞菌屬等非發酵菌無法酵解葡萄糖產酸,因而無法通過Polymyxin NP實驗進行臨床篩查和監測[6,12,18]。
綜上所述,Polymyxin NP實驗是一種快速、有效的多黏菌素耐藥腸桿菌科細菌篩查方法,盡管目前我國腸桿菌科細菌對多黏菌素的耐藥率顯著低于歐美國家,但耐藥菌株的日益增多,尤其是質粒介導的mcr基因的播散使耐藥性難以控制,應當引起足夠的重視。多黏菌素耐藥腸桿菌科細菌嚴重影響著臨床抗感染治療,有必要進行多黏菌素耐藥性監測,對該類耐藥細菌的防控至關重要。

