轉錄組學分析外源H2S調控黃瓜響應鹽脅迫的機理
蔣景龍,李 麗
(1. 陜西理工大學 生物科學與工程學院,陜西 漢中 723001;2. 陜西理工大學 化學與環境科學學院,陜西 漢中 723001)
土壤鹽漬化是嚴重影響農業生產的一個全球性的問題,直接影響農作物的產量和質量[1-2]。黃瓜(CucumissativusL.)作為主要的設施蔬菜之一,其對鹽脅迫抗性較弱,發芽期和幼苗期對鹽脅迫尤其敏感,鹽會導致其產生滲透脅迫和離子毒害,引起養分虧缺、氧化脅迫、光合作用抑制及關鍵酶活性和基因表達變化、生物膜的正常結構和功能變化等一系列次生脅迫[3-5],最終抑制其種子萌發及植株生長。研究黃瓜耐鹽機制對提高農作物的耐鹽性具有重要的參考價值。
硫化氫(H2S)是一種植物內源性氣體信號分子,其與植物激素及信號分子相互作用,在植物生長發育的調控及非生物脅迫的響應中發揮著重要作用[6]。信號分子H2S對植物鹽脅迫的傷害具有緩解作用,在抵御植物鹽害中發揮著重要作用[7-9]。外源H2S能有效緩解加工番茄種子萌發過程中鹽脅迫的抑制作用,促進種子的萌發[10]。外源H2S能夠通過提高鹽脅迫下茶樹和水稻的抗氧化水平來降低活性氧(Reactive oxygen species, ROS)的積累,減輕膜脂過氧化程度,從而緩解鹽脅迫引起的氧化損傷[11-12]。外源H2S可能與一氧化氮(Nitric oxide,NO)相互作用減少氧化損傷來增強苜蓿種子萌發過程中抵御鹽脅迫的能力[13]。外源H2S和過氧化氫(Hydrogen peroxide,H2O2)協同作用可以誘導增強NaCl脅迫下加工番茄幼苗植株滲透調節能力、提高清除ROS的酶促系統的防御能力,從而減弱加工番茄細胞內ROS自由基對質膜的傷害,進而提高加工番茄幼苗對鹽脅迫的適應[14]。在前期研究中發現外源H2S能夠通過提高黃瓜光合作用和蒸騰作用,有效改善光系統Ⅱ參數和氣孔參數;增強抗氧化系統,降低活性氧的積累和膜質過氧化作用,調節細胞內Na+和K+的平衡穩定狀態,從而有效緩解鹽脅迫對黃瓜幼苗造成的生長抑制[15];然后利用蛋白質組學技術研究了外源H2S對高鹽脅迫下黃瓜葉片蛋白質表達的影響,發現差異表達蛋白的分子功能主要以蛋白質結合和水解酶活性為主,生物學過程主要以應激反應、有機物代謝、脅迫響應和細胞分化過程等為主[16]。根系是澆灌脅迫作物最先感受逆境脅迫的器官,當根區受到脅迫時,根系首先感受到并發出信號。因此,本研究以春夏秋王黃瓜根系為試材,用NaCl、NaCl+H2S處理,采用高通量測序技術對其根系進行轉錄組學測序分析,以期探討外源H2S調控黃瓜幼苗響應鹽脅迫的機理,為H2S調控植物代謝,緩解高鹽逆境障礙提供理論依據。
1 材料和方法
1.1 試驗材料和處理
試驗材料選用春夏秋王黃瓜種子(山東省寧陽縣魯明種子有限公司),處理方法參考蔣景龍等[17],待所有幼苗第1片真葉完全展開時,選取長勢一致的幼苗分成3組,每組8個平行對照,分別用Hoagland營養液(CK)、200 mmol/L NaCl(T)和200 mmol/L NaCl+15 μmol/L NaHS(S)澆灌處理7 d。選取根系用液氮速凍,轉移到-80 ℃冰箱內保存。
1.2 黃瓜根系總RNA提取及文庫構建
黃瓜根系總RNA提取方法參照TRIzol Reagent方法進行。采用RNA專用瓊脂糖電泳檢測RNA的濃度和純度。通過Oligo(dT)磁珠富集總RNA中帶有polyA結構的mRNA,采用離子打斷將RNA打斷到200~300 bp。文庫構建完成后,采用PCR擴增進行文庫片段富集,文庫大小在300~400 bp。通過Agilent 2100 Bioanalyzer檢測文庫大小,熒光定量檢測文庫總濃度。
1.3 轉錄組測序及分析
由上海派森諾公司完成測序,測序平臺為Illumina HiSeq。樣品上機測序獲得的原始數據經進一步過濾,去除一些帶接頭、低質量的序列從而獲得高質量序列。比對參考基因、基因表達差異分析、GO富集分析和KEGG富集分析參考文獻[18]。
2 結果與分析
2.1 原始數據整理
如表1 所示,9個樣本cDNA測序共獲得原始序列365.35 Mb,原始序列經質控過濾后得到高質量序列 360.63 Mb,高質量序列堿基數共53.05 Gb,比對上參考基因組的序列總數為315.74 Mb,比例為86.27%~88.64%。Q30在87.65%以上,表明測序結果可靠,可用于后續的分析。
2.2 基因表達差異分析
通過DESeq對3組的差異表達基因分析結果用火山圖(圖1)展示。圖中越靠近左邊或右邊的點表達差異越顯著。結果顯示,CK-T比較組共2 244個差異表達基因,其中上調表達基因有1 168個,下調表達基因有1 076個;T-S比較組共653個差異表達基因,其中上調表達基因有435個,下調表達基因有218個;CK-S比較組共1 696個差異表達基因,其中上調表達基因有757個,下調表達基因有939個。
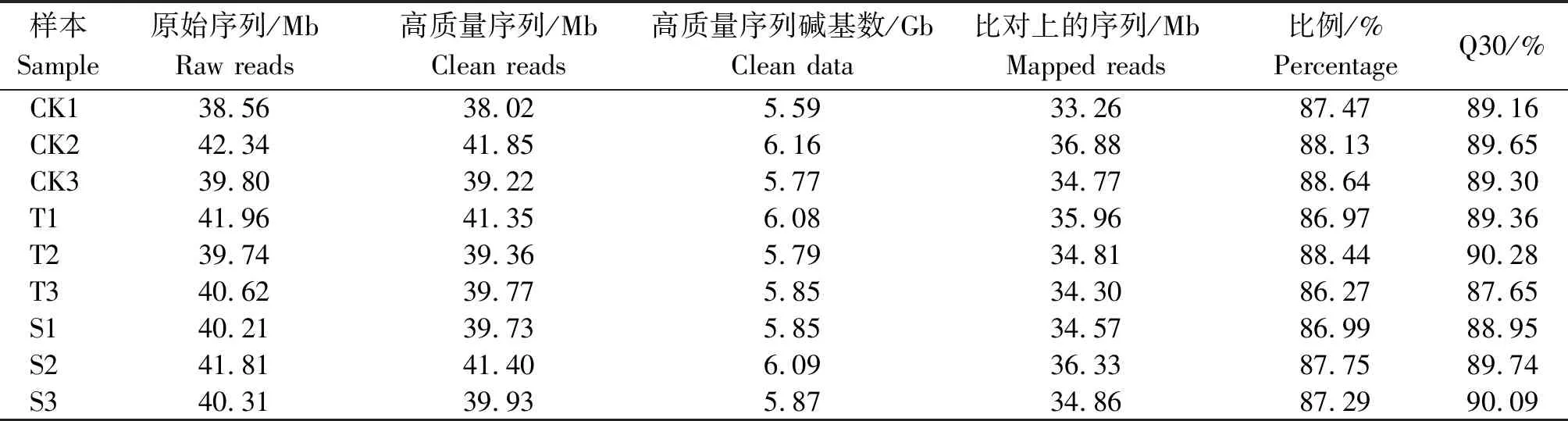
表1 數據過濾和RNA-Seq Map統計Tab.1 Data filtering and statistics of RNA-Seq Map
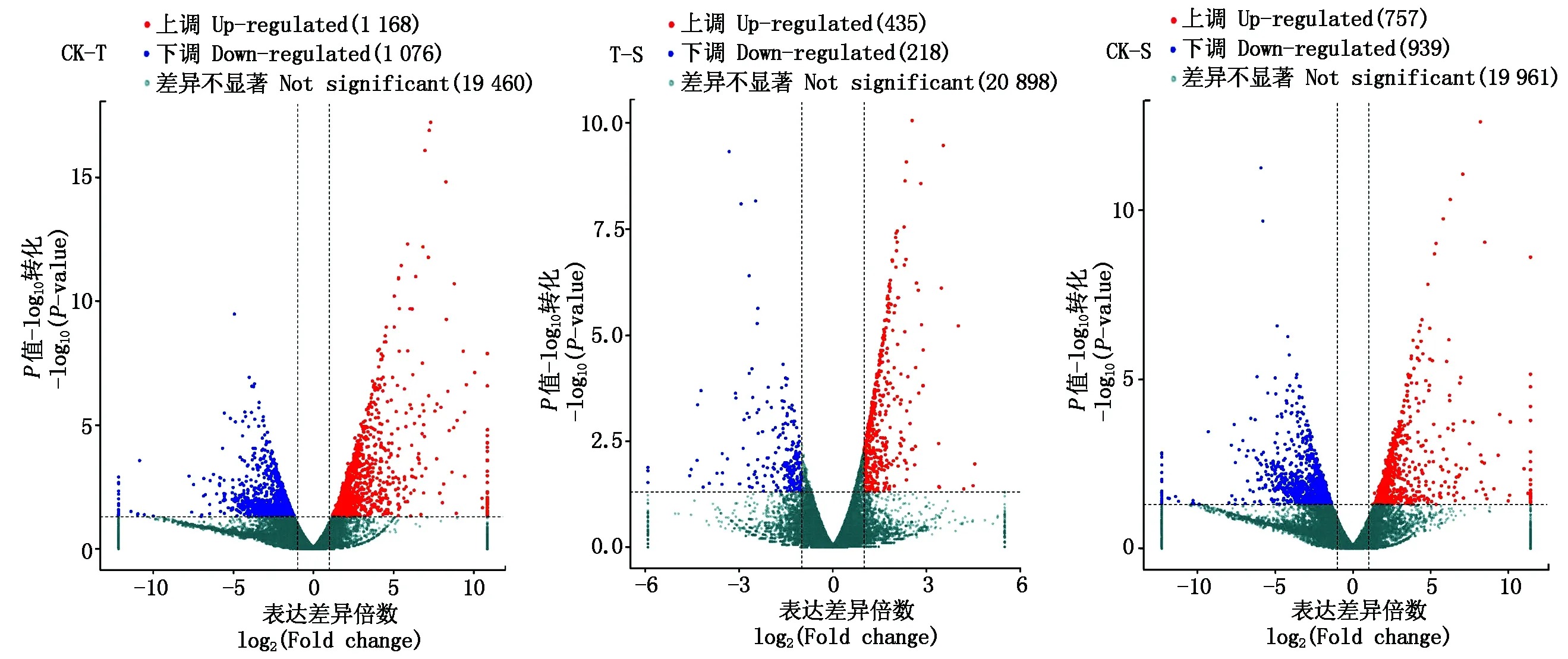
圖1 黃瓜根系差異表達基因的火山圖分析Fig.1 Volcano gram analysis of differentially expressed genes in cucumber roots
將3個組差異表達基因繪制維恩圖,尋找特有的和共有的差異表達基因。如圖2所示,3個比較組一共有3 073個差異表達基因,其中CK-T、T-S和CK-S比較組特有的差異表達基因數分別為836,415,331個,共有的差異表達基因有29個,CK-T和T-S組共有的差異表達基因有155個。CK-T、T-S組共有的差異表達基因極有可能與H2S調控黃瓜響應鹽脅迫的分子機制有關。篩選CK-T和T-S比較組共有差異表達基因中差異最顯著的10個基因,由表2可見,在CK-T比較組中除了Csa_1G303700上調,其他均為下調,而在T-S比較組中均為上調。
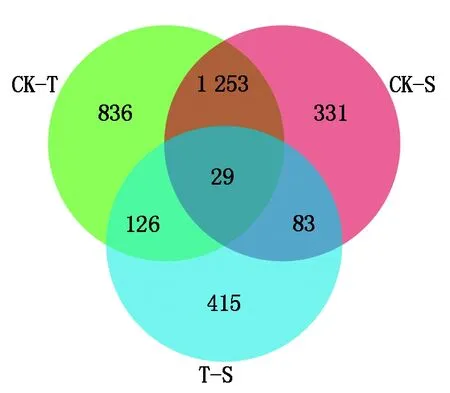
圖2 黃瓜根系差異表達基因的維恩圖Fig.2 Venn diagram of differentially expressed genes in cucumber roots
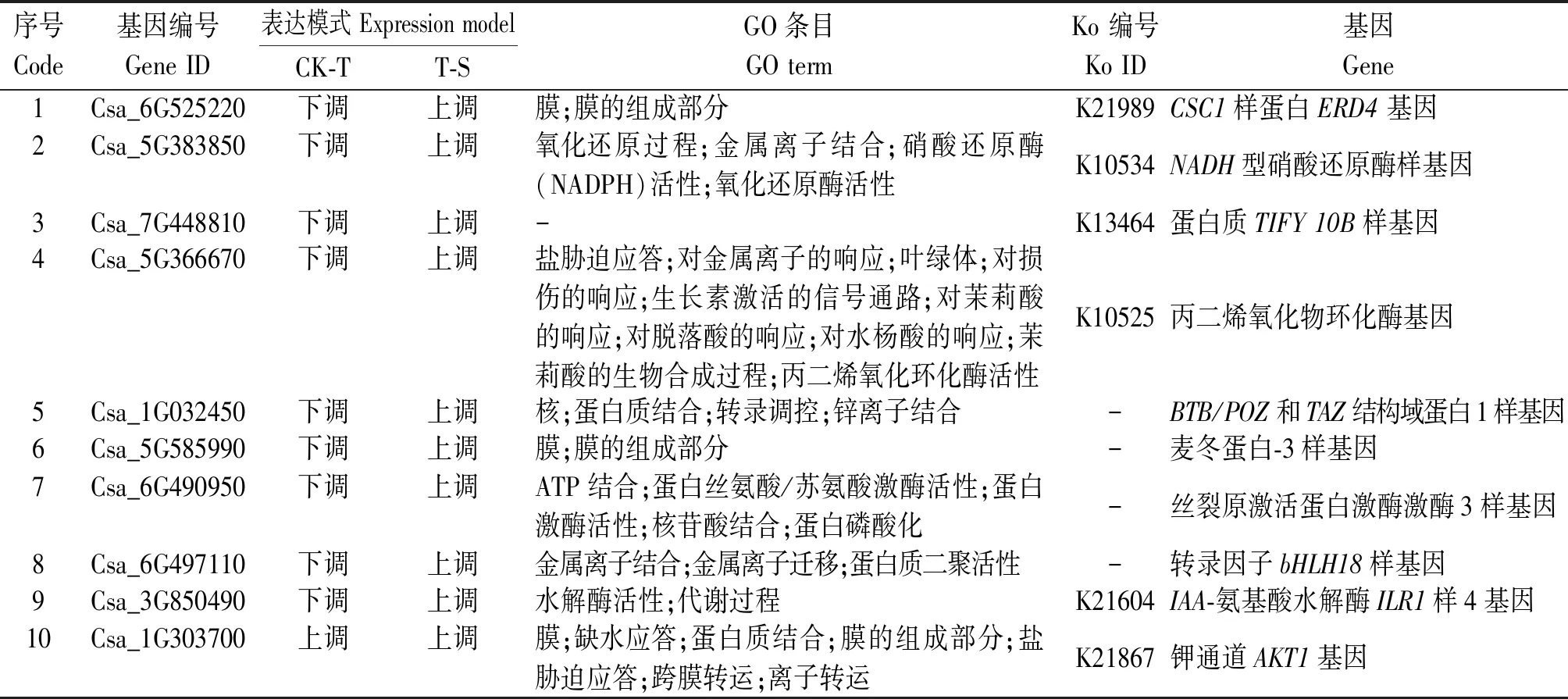
表2 CK-T和T-S組共有差異表達基因中Top10基因Tab.2 CK-T and T-S groups share the 10 most significant differentially expressed genes
2.3 差異表達基因GO富集分析
對篩選到的差異表達基因進行GO富集分析,可分為生物過程、細胞組分和分子功能3個一級分類,每一類又分別進一步劃分為1 117,155和409個二級分類。圖3展示了3個比較組差異表達基因GO富集程度最高的前20個分類。差異表達基因在3個一級分類中均有分布,主要富集在分子功能類中的結合(Binding)和催化活性(Catalytic activity)類,生物過程類中的代謝過程(Metabolic process)、細胞過程(Cellular process)和單一生物過程(Single-organism process)類及細胞組分類中的膜(Membrane)和膜組分(Membrane part)類中。表2統計了CK-T和T-S比較組共有差異表達基因中差異最顯著的10個基因富集的功能類;Csa_6G525220、Csa_5G585990、Csa_1G303700都富集在細胞組分類中的膜(Membrane)和膜的組成部分(Integral component of membrane)類。
2.4 差異表達基因KEGG富集分析
對差異表達基因進行KEGG通路富集分析(表3)。差異表達基因共歸為4大類,CK-T比較組的2 244個差異表達基因歸為20個亞類、139個代謝通路,T-S比較組的653個差異表達基因歸為16個亞類、75個代謝通路,CK-S比較組的1 696個差異表達基因歸為20個亞類、127個代謝通路。
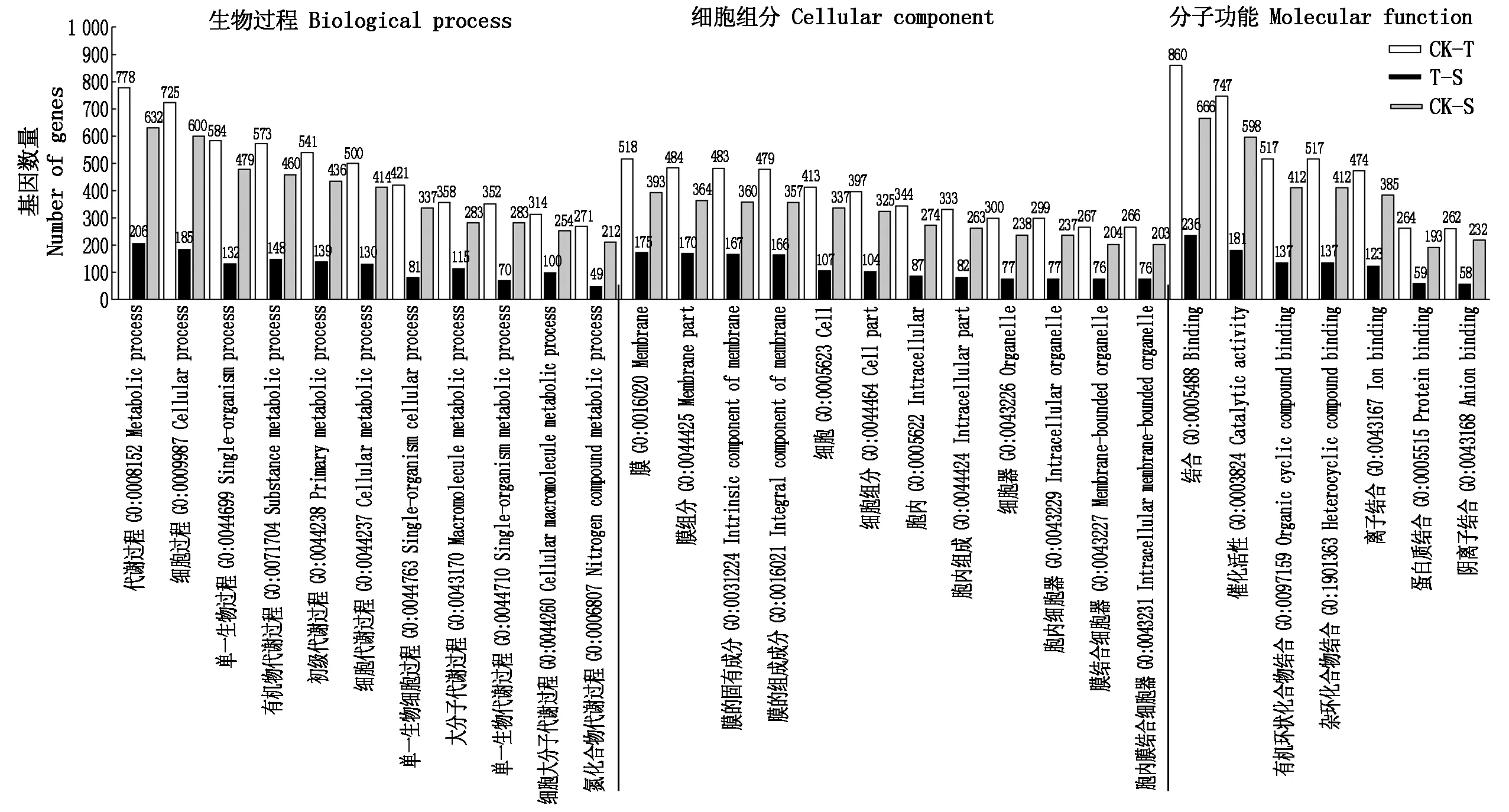
圖3 黃瓜根系差異表達基因GO富集分析柱狀圖Fig.3 Histogram of GO enrichment analysis of differentially expressed genes in cucumber roots
對KEGG富集分析中排名前20的代謝通路做散點圖。由圖4-5可見,CK-T比較組的差異表達基因主要富集在植物激素信號轉導(Plant hormone signal transduction)、碳代謝(Carbon metabolism)、淀粉和蔗糖代謝(Starch and sucrose metabolism)、苯丙烷生物合成(Phenylpropanoid biosynthesis)、氨基酸的生物合成(Biosynthesis of amino acids)、細胞周期(Cell cycle)、氨基糖和核苷酸糖代謝(Amino sugar and nucleotide sugar metabolism)通路中;T-S比較組的差異表達基因主要集中在植物激素信號轉導(Plant hormone signal transduction)、內質網中的蛋白質加工(Protein processing in endoplasmic reticulum)和光合作用(Photosynthesis)通路中。經基因的相似性比對和同源性分析,從不同處理的黃瓜根轉錄組數據中發掘出與NaCl和H2S處理相關的基因,如表2所示,CK-T和T-S比較組差異表達基因主要富集在植物激素信號轉導、鈣滲透應力門控陽離子通道、氮代謝、α-亞麻酸代謝、茉莉單酰-L-氨基酸水解酶和鉀通道代謝通路。
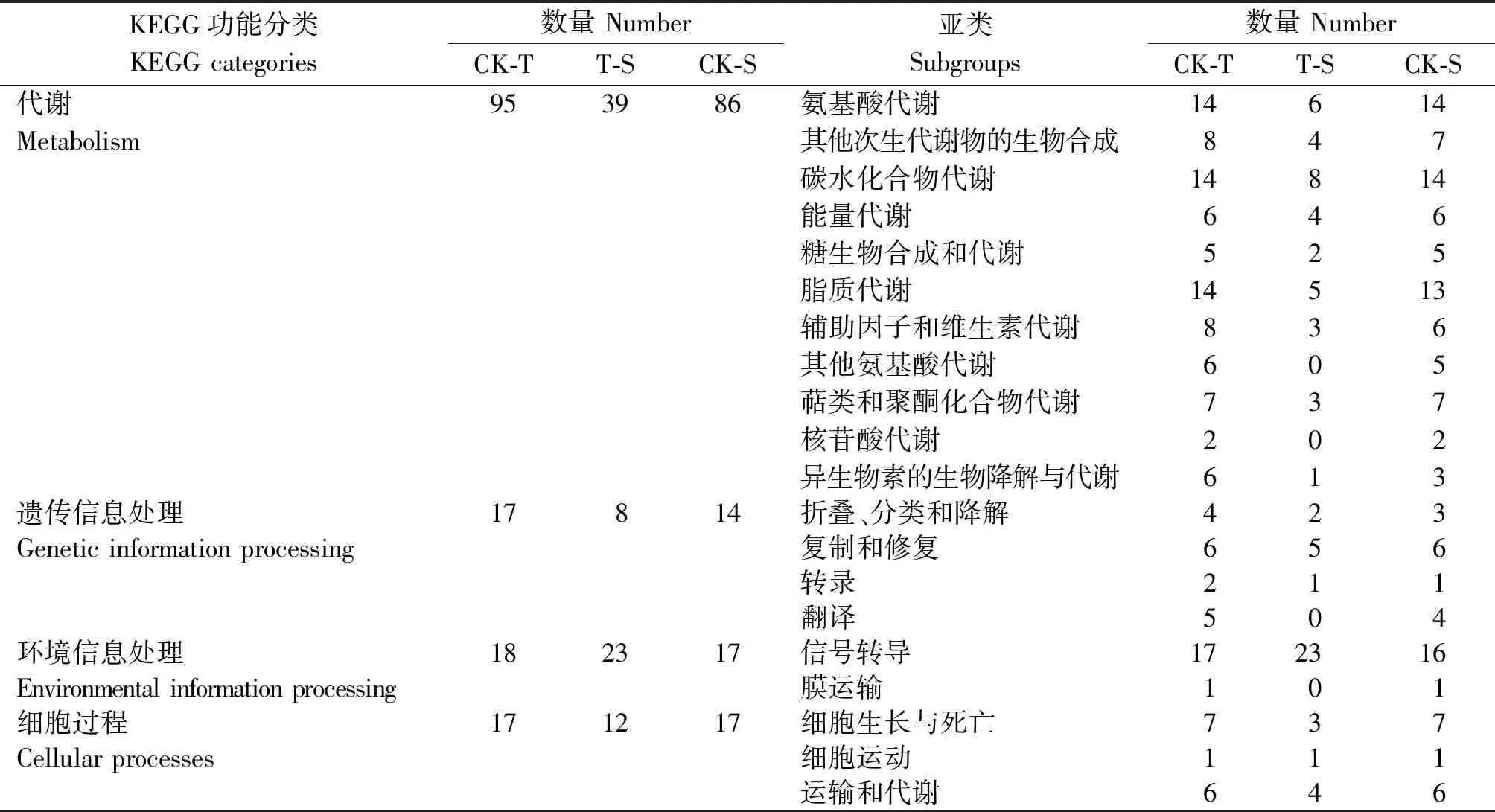
表3 差異表達基因KEGG富集分析Tab.3 KEGG enrichment analysis of differentially expressed genes
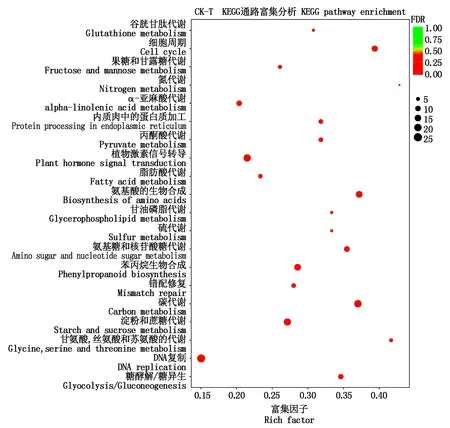
顏色表示顯著性P值的大小,P值越小顏色越接近紅色;每個通路下包含的差異基因的多少用點的大小來表示。圖5同。 The size of P-value is represented by the color of dots, the smaller the P-value, the closer the color is to red; The number of differential genes contained in each pathway is represented by the size of dots. The same as Fig.5.
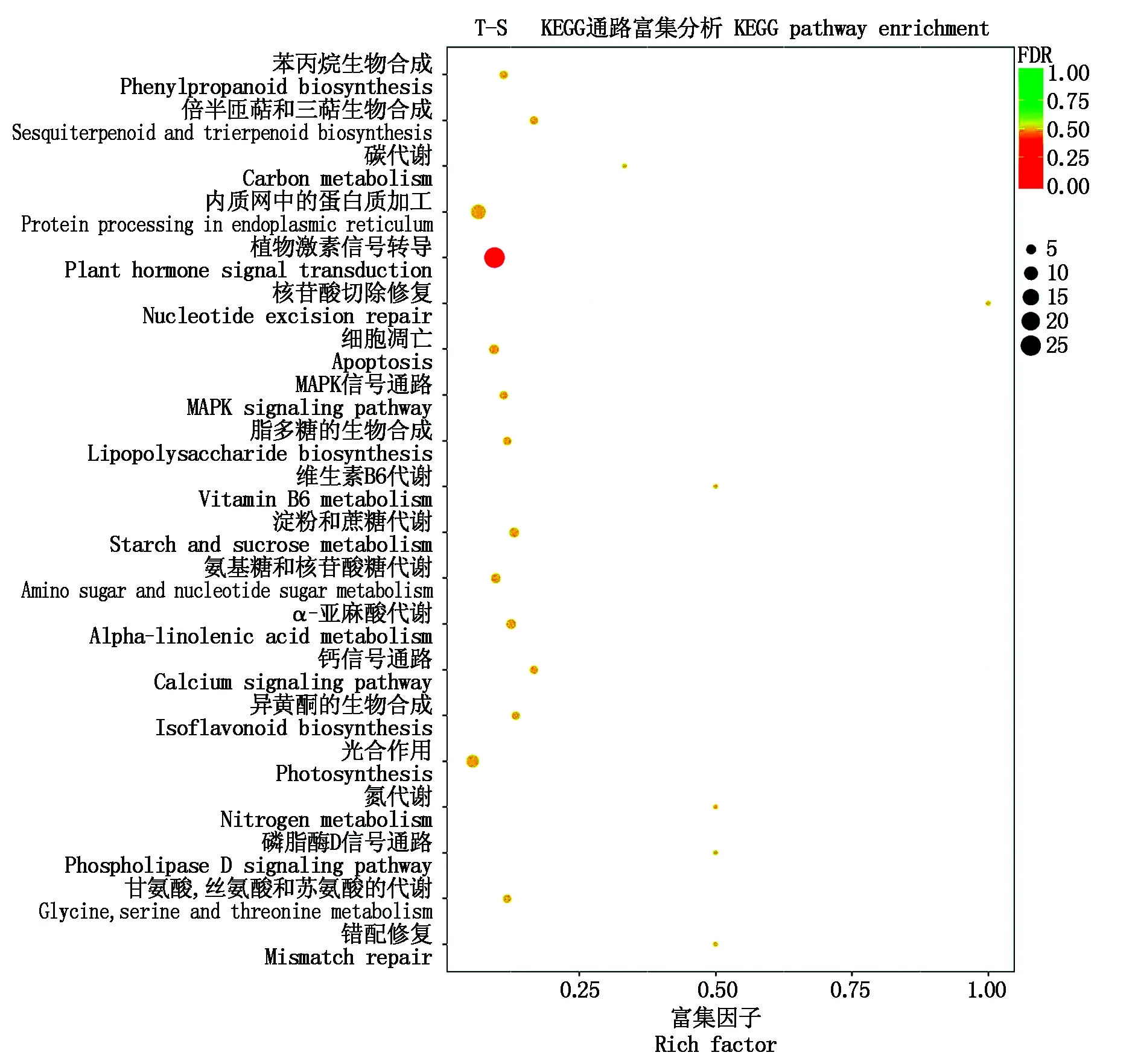
圖5 T-S組差異表達基因KEGG富集分析散點圖Fig.5 KEGG pathways enrichment analysis of differentially expressed genes of group T-S
3 討論
鹽度是一種多組分非生物脅迫,鹽度過高通常會導致植物發生細胞脫水和膜系統損傷等破壞[19],通過滲透脅迫、離子毒害和氧化脅迫等對植物造成巨大傷害[20]。本研究結果中GO富集分析表明,CK-T比較組和T-S比較組共有差異表達基因富集較多的分類為膜和膜的組成部分等。已有報道H2S通過上調楊樹根系胞質膜Na+/H+逆向轉運體系,促進Na+和H+逆向跨膜轉運,而且H+泵通過抑制去極化激活的離子通道來限制鹽誘導的K+外流,從而調節鹽脅迫下楊樹根系K+/Na+的平衡[21]。這說明H2S能夠通過調節鹽脅迫下植物組織細胞離子平衡及氧化還原過程,減輕膜損傷,調節相關基因和蛋白從而緩解鹽脅迫引起的損傷。
遭遇滲透脅迫時,植物會通過一系列信號轉導途徑來減少蒸騰失水,從而維持體內水分代謝的相對平衡[22]。目前,鹽超敏感信號轉導途徑(Salt overly sensitive,SOS)、鈣依賴型蛋白激酶(Calcium-dependent protein kinase,CDPK)信號轉導級聯反應途徑、脫落酸(Abscisic acid,ABA)信號轉導途徑和絲裂原活化蛋白激酶(Mitogen-activated protein kinase,MAPK)級聯反應途徑等是植物應答鹽脅迫相關的主要信號轉導途徑[23]。植物體內的H2S主要是通過L-/D-半胱氨酸脫氫酶(L-/D-cysteine desulfhydrase,L-/D-CDes)途徑合成,H2S位于SOS上游,參與鹽脅迫、茉莉酸(Jasmonic acid,JA)、ABA等誘導的氣孔關閉過程[24-26]。本研究結果中KEGG富集分析表明,CK-T和T-S比較組差異表達基因主要富集在植物激素信號轉導、鈣滲透應力門控陽離子通道、氮代謝、α-亞麻酸代謝、茉莉單酰-L-氨基酸水解酶和鉀通道代謝通路。和CK組相比,NaCl處理組CSC1樣蛋白ERD4基因、NADH型硝酸還原酶樣基因、蛋白質TIFY10B樣基因、丙二烯氧化物環化酶基因(Allene oxide cyclase,AOC)、BTB/POZ和TAZ結構域蛋白1樣基因、麥冬蛋白-3樣基因、絲裂原激活蛋白激酶激酶3樣基因、轉錄因子bHLH18樣基因和IAA-氨基酸水解酶ILR1樣4基因下調,而H2S處理后上述基因上調,鉀通道AKT1基因在NaCl脅迫和H2S處理后均上調表達。研究表明AOC基因參與對鹽脅迫、金屬離子、損傷、JA、ABA及水楊酸(Salicylic acid,SA)的響應等,是JA生物合成途徑中一個關鍵酶,在植物抗逆境反應中發揮著重要作用[27]。SA信號途徑和JA信號途徑被認為是相互拮抗的2條信號轉導途徑[28];CSC1樣蛋白ERD4基因參與膜和膜的組成,具有ERD4的轉基因擬南芥植物生長旺盛,產量高,并且對鹽和滲透脅迫具有耐受性[29];NADH型硝酸還原酶基因的表達與高濃度鹽脅迫下,鹽敏感蕎麥品種葉片NADH型硝酸還原酶活性顯著降低研究一致[30];TIFY蛋白質構成植物特有的超家族,它們參與調節許多植物過程,例如發育、防御和脅迫反應[31];MAPK在植物的應激反應和發育中起著重要作用[32];AKT表達與植物的Na+選擇性密切相關[33]。植物耐鹽性是由植物體內一系列因素共同作用的結果,同時受外界環境因子的影響和制約。鹽脅迫后,黃瓜在一系列代謝的信號轉導相關基因的調控下,維持機體代謝相對平衡,并適應鹽脅迫環境。研究鹽脅迫相關基因及其功能分析為下一步篩選耐鹽關鍵基因提供了信息。

