黃芪甲苷通過抑制細胞凋亡減輕氧糖剝奪/復氧復糖PC12細胞損傷的研究
杜澍金,趙艷萌,周曉紅,高維娟
(河北中醫學院 河北省中醫藥防治心腦血管病基礎研究重點實驗室,河北 石家莊 050091)
腦血管疾病發病率高、致死/致殘率高,是我國居民致死的首位病因[1-2],尤其是40歲以上人群每年新發腦卒中約300萬例,死亡110萬例,其中急性缺血性腦卒中約占80%,造成的經濟負擔高達400億元/年[3]。缺血性腦卒中一般預后較差,治療的關鍵在于盡早恢復缺血區腦組織的血液再灌注,而恢復血液再灌注的過程有時反而引起更加嚴重的二次腦損傷,即腦缺血再灌注損傷(Cerebral ischemia reperfusion injury,CIRI)。在CIRI的發生發展過程中炎癥、氧自由基、鈣超載、毒性氨基酸、能量代謝等均可通過引起細胞凋亡、壞死導致腦組織病理損傷的發生,最終導致神經功能缺損癥狀的出現。因此,防治細胞凋亡是抑制CIRI的重要環節。前期研究證實,臨床常用于中風治療的中藥黃芪[4]的主要活性成分黃芪甲苷對CIRI有保護作用[5]。本實驗以PC12細胞為研究對象,通過建立氧糖剝奪/復氧復糖細胞模型模擬CIRI對神經細胞的損傷過程,研究黃芪甲苷對腦缺血再灌注所致神經元損傷的保護作用及機制。
1 材料與方法
1.1 細胞
PC12細胞(經NGF 誘導高分化),由河北醫科大學第一醫院中心實驗室主任許順江教授惠贈。
1.2 主要試劑
黃芪甲苷(HY-N0099,MCE);胎牛血清,購自浙江天杭生物科技股份有限公司;DMEM basic(1×)、胰蛋白酶、1×PBS緩沖液,均購于美國Gibco公司;Earle's平衡鹽溶液(1×EBSS,無鈣鎂糖)購自北京雷根生物科技有限公司;青鏈霉素混合液購自BIOND公司; Triton X-100、多聚賴氨酸均購自北京索萊寶科技有限公司;Bcl-2單克隆抗體、Caspase-3多克隆抗體購自Abcam公司;Bax多克隆抗體,HRP標記的山羊抗兔IgG、RIPA裂解液、PVDF膜、β-actin、蛋白maker、ECL發光液等購自塞維爾生物科技有限公司;BCA蛋白定量試劑盒購自北京中杉金橋科技有限公;MTS試劑盒,購自Promega公司。
1.3 主要儀器
3111型CO2培養箱,3131型三氣培養箱,Varioskan LUX型多功能微孔板讀數儀(Thermo公司,超凈工作臺SW-CJ-ID型(蘇州凈化公司),DMI3000B 型倒置顯微鏡,5417R型低溫離心機,酶聯免疫檢測儀,勻漿器,JA1203電子天平,Bio-rad電泳儀PowerPacTM HC及半干轉膜儀Trans- Blot SD Cell,UVP凝膠成像系統。
1.4 PC12細胞培養
PC12細胞于37 ℃水浴中迅速復蘇后接種于含10%胎牛血清和1%青鏈霉素混合液的DMEM高糖培養基中,在37 ℃、5% CO2飽和濕度的CO2培養箱中常規培養,經 1~2次傳代細胞處于對數生長期且生長狀態良好時,建立氧糖剝奪/復氧復糖模型。
1.5 氧糖剝奪/復氧復糖模型的建立及分組
對數期生長細胞,隨機分為3組:Control組、Model組和AST-IV組。除Control組外,其他各組均氧糖剝奪2 h后復氧復糖24 h:棄去正常細胞培養液,用復溫的1×PBS緩沖液輕柔清洗細胞2遍后,更換為無糖的Earle's平衡鹽溶液以模擬細胞缺血狀態,然后將細胞置于94%N2+5%CO2+1%O2的37 ℃三氣培養箱中模擬缺氧狀態,培養(氧糖剝奪)2 h后,將Earle's平衡鹽溶液更換為正常細胞培養液,置37 ℃、5%CO2培養箱中繼續培養(復氧復糖)。同時,Control組細胞給予換液處理;AST-IV組于復氧復糖的同時給予含黃芪甲苷(終濃度為100 mmol/L)的培養液,Model組細胞給予正常培養液,培養24 h。倒置顯微鏡觀察各組細胞形態,并收集各組細胞進行相應指標的檢測。
1.6 倒置顯微鏡觀察細胞形態
將PC12細胞傳代于6孔板中,正常培養24 h后,Control組繼續正常培養,Model組和AST-IV組先進行氧糖剝奪2 h 處理。之后Control組細胞換液,Model組更換為正常培養液,AST-IV組更換為含黃芪甲苷(終濃度為100 mmol/L)的培養液,繼續培養24 h。隨后用倒置顯微鏡觀察細胞形態及生長狀態(400×),每組細胞取5個視野,拍照保存。
1.7 MTS法檢測細胞存活率
將對數生長期細胞傳代于96孔板中,常規培養24 h使細胞貼壁,按造模方法處理各組細胞后,于96孔板中每孔(100 mL)加入20 mL MTS溶液,于37 ℃、5%CO2培養箱中孵育1 h后,在多功能微孔板讀數儀中測定450 nm處OD值,檢測細胞存活率。細胞存活率=(實驗組OD 值-空白組OD 值)/(對照組OD值-空白組OD值)×100%。
1.8 Western blot檢測Bax、Bcl-2和Caspase-3的表達
造模結束后,用1×PBS緩沖液清洗細胞2遍;以一次性細胞刮刮取細胞于1.5 mL離心管中;4 ℃下,10 000 rpm離心5 min,棄去上清后再次離心2 min;再棄去上清,加入適量細胞裂解液,冰上裂解細胞30 min;提取總蛋白,BCA法測定蛋白含量。調整上樣量后,按比例加入上樣緩沖液,混勻,100 ℃煮沸10 min使蛋白變性。SDS-PAGE電泳分離蛋白,半干電轉移法將蛋白轉移到PVDF膜上,以5 %脫脂奶粉封閉2 h后,相應一抗4 ℃孵育過夜。TBST洗膜液洗膜3次后,相應HRP二抗室溫下孵育1 h。TBST洗滌后以ECL化學發光法顯色。用UVP軟件采圖,分析蛋白條帶灰度值,以β-actin為內參照。
1.9 統計學處理
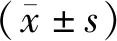
2 實驗結果
2.1 倒置顯微鏡觀察氧糖剝奪/復氧復糖PC12細胞生長狀態
Control組細胞貼壁生長,生長狀態良好,細胞折光性較強,呈多角形,突觸明顯,并交織成網。與Control組相比,Model組細胞貼壁較差,折光性減弱,細胞多呈圓形且聚集成團,突觸減少甚至消失,部分細胞脫落、漂浮于培養液中。與Model組相比,AST-IV組細胞損傷減輕,折光性增強,突觸增多,趨向于正常生長。見圖1。
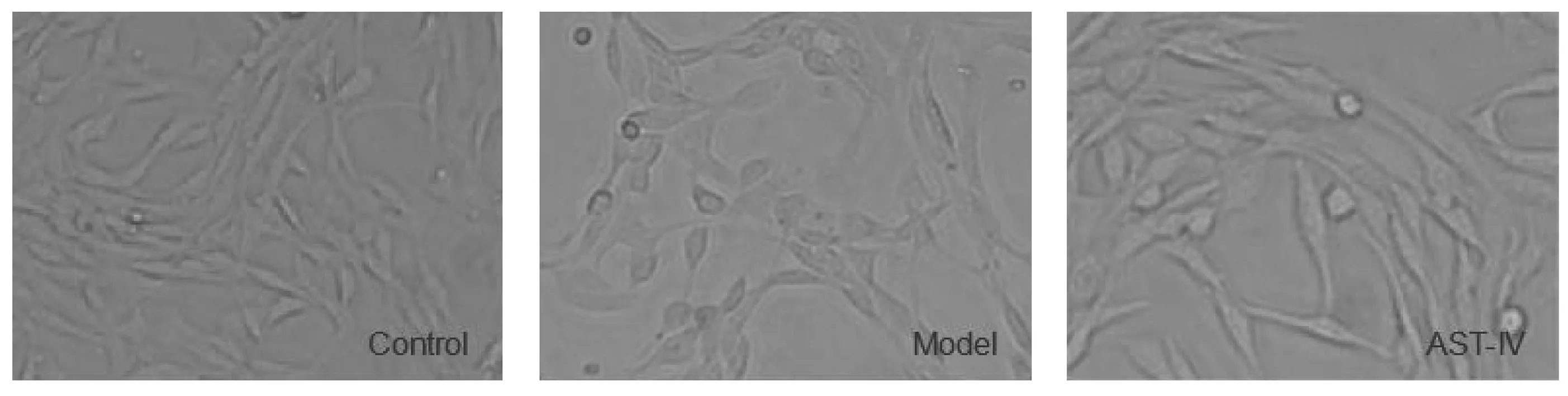
圖1 黃芪甲苷對氧糖剝奪/復氧復糖PC12細胞形態學變化
2.2 MTS法檢測PC12細胞存活率
與Control組相比,Model組細胞存活率明顯下降(P<0.05);與Model組相比,AST-IV組細胞細胞存活率明顯升高(P<0.05),差異有統計學意義。見表1。
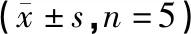
表1 黃芪甲苷對各組PC12細胞存活率的影響
2.3 黃芪甲苷對不同組別PC12 細胞Bax、Bcl-2和Caspase-3的Western blot檢測結果比較
與Control組相比,Model組PC12細胞Bax,Caspase-3的表達增多,Bcl-2表達減少(P<0.05),差異有統計學意義;與Model組相比,AST-IV組PC12細胞Bax、Caspase-3的表達減少,Bcl-2表達增多(P<0.05),差異有統計學意義(見表2)。
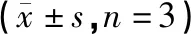
表2 黃芪甲苷對各組PC12細胞Bax、Bcl-2和Caspase 3相對蛋白含量的影響
3 討論
PC12細胞是大鼠腎上腺嗜鉻細胞瘤分化細胞株,經誘導分化后具有交感神經元特性,常用于神經系統疾病的體外研究。氧糖剝奪/復氧復糖細胞模型是較理想的模擬腦缺血再灌注致神經元損傷的細胞模型[6]。本實驗以高分化PC12細胞氧糖剝奪/復氧復糖模型模擬臨床腦卒中患者經溶栓或其他血管內治療恢復血流灌注后的臨床病理過程中的神經元損傷情況,即腦缺血再灌注所致的神經元損傷,研究黃芪甲苷對CIRI的保護作用及機制。實驗結果提示,再灌注的同時給予黃芪甲苷處理可以減輕氧糖剝奪/復氧復糖對PC12細胞的損傷,其保護作用體現在:改善細胞生長狀態和形態,提高損傷后細胞存活率,通過促進抗凋亡蛋白Bcl-2表達,降低抗凋亡蛋白Bax表達,抑制細胞凋亡過程中最主要的終末剪切酶Caspase-3蛋白表達,抑制PC12細胞凋亡。
Bcl-2具有抑制凋亡的作用,而Bax可促進凋亡,兩者是在功能上相互對立的蛋白,其比值大小決定著損傷細胞是否趨于凋亡[7]。在生理狀態下,Bcl-2與Bax形成異源二聚體,穩定線粒體膜的完整性,抑制Caspase-3的活化所介導的凋亡過程[8];在病理狀態下,如細胞受到缺血、缺氧等有害刺激時Bcl-2表達降低,Bax表達增多,且向線粒體膜聚集,形成同源二聚體,導致線粒體通透性增高,致使線粒體內凋亡因子如細胞色素C(Cyt C)和凋亡誘導因子(AIF)釋放入胞質,進而啟動Caspase級聯反應及其他凋亡通路。因此Bax/Bcl-2增高,可促進細胞趨于凋亡,反之則抑制細胞凋亡,且其促進凋亡的機制與增大線粒體膜通透性,導致促凋亡物質的釋放有關。有研究發現,腦缺血引起的遲發性神經元死亡即是神經元的凋亡,且神經元的凋亡與缺血缺氧引起的起腦組織Bcl-2蛋白的一過性表達增加及Bax蛋白的持續表達增多有關[9]。而本研究發現黃芪甲苷可促進氧糖剝奪/復氧復糖后PC12細胞Bcl-2蛋白表達,抑制Bax蛋白表達的增多,導致Bax/Bcl-2減小,這可能是黃芪甲苷抑制CIRI所致神經元凋亡的重要因素之一。本實驗發現經氧糖剝奪/復氧復糖處理后,PC12細胞Bcl-2水平降低、Bax水平升高,表明細胞凋亡增多,而在復氧復糖的同時給予黃芪甲苷處理后,Bcl-2水平的升高和Bax的降低表明黃芪甲苷增強了細胞對抗凋亡的能力。
Caspase-3在細胞凋亡過程中起著不可替代的作用,是細胞凋亡過程中最主要的終末剪切酶。有研究證實黃芪甲苷與三七有效成分配伍可降低Caspase-3 蛋白的表達量,抑制CIRI小鼠海馬 CA1 區神經細胞凋亡,發揮神經保護作用[10]。本實驗也證實黃芪甲苷可降低氧糖剝奪/復氧復糖所致PC12細胞Caspase-3 蛋白的表達增多,從而抑制細胞凋亡,提升細胞存活率。
腦缺血再灌注損傷繼發于腦卒中恢復血液灌注之后,其發生機制復雜,病理過程涉及多個環節,包括能量代謝障礙、興奮性氨基酸釋放、胞內鈣超載、氧自由基增多、炎性因子釋放等,這些因素相互作用、互為因果,最終導致神經細胞的凋亡和壞死,進而出現嚴重的臨床癥狀及不良預后[11]。目前,對于CIRI的治療包括抗炎、抗氧化、抗凋亡、抑制細胞內鈣超載及中醫藥類神經保護措施。近年來中醫藥治療以其多靶點、多功效性,在CIRI中的研究逐漸增多。中醫理論認為,氣虛、血瘀為腦中風發作的病因病機,治療上宜采用益氣活血、祛瘀通絡類方藥,其中補陽還五湯是中醫用于治療缺血性腦卒中的經典方劑,其使用歷史悠久,已逾數千年。黃芪甲苷作為補陽還五湯君藥黃芪的主要活性成分之一[12],具有清除氧自由基、抑制細胞凋亡、抗炎、調節免疫等生物活性[13-15]。多項實驗證實,黃芪甲苷對CIRI具有保護作用[5,16]:黃芪甲苷可以改善實驗性腦缺血再灌注動物模型的神經功能學評分、縮小其腦梗死體積;同時,在模擬腦缺血再灌注損傷的體外模型中發現,黃芪甲苷可以提升氧糖剝奪/復氧復糖導致的PC12和HT22細胞的存活率,抑制細胞凋亡率,改善細胞生長狀態,但其具體機制仍有待進一步研究。
本研究證實黃芪甲苷可通過抑制細胞凋亡發揮對氧糖剝奪/復氧復糖PC12細胞的保護作用,機制與促進抗凋亡蛋白Bcl-2表達,抑制促凋亡蛋白Bax和細胞凋亡過程中最主要的終末剪切酶Caspase-3表達有關。本課題將在動物水平和細胞水平進一步探究黃芪甲苷對CIRI的保護作用及機制。

