術(shù)中持續(xù)生理鹽水沖洗對(duì)腰椎后路術(shù)后患者切口疼痛的影響
楊家祥,董連峰,高欣,劉鐵龍,肖建如*
1安徽省六安市中醫(yī)院骨科,安徽六安 237006;2海軍軍醫(yī)大學(xué)附屬長(zhǎng)征醫(yī)院骨腫瘤科,上海 200003
高頻電刀是一種取代機(jī)械手術(shù)刀進(jìn)行組織切割的電子外科器械,在與機(jī)體接觸時(shí)通過(guò)電極尖端產(chǎn)生的高頻高壓電流對(duì)組織進(jìn)行加熱,實(shí)現(xiàn)對(duì)機(jī)體組織的分離和凝固,從而達(dá)到切割及止血的目的。高頻電刀在切割區(qū)域及周圍組織中可產(chǎn)生400~600 ℃的瞬時(shí)高溫,造成周圍組織的急性熱損傷,并可能加劇患者術(shù)后傷口的疼痛[1-3]。在手術(shù)過(guò)程中通過(guò)生理鹽水沖洗降溫可能有助于減輕肌肉組織的損傷,從而間接減輕術(shù)后傷口的疼痛。本研究探討腰椎后路手術(shù)采用高頻電刀暴露腰椎椎板過(guò)程中持續(xù)生理鹽水沖洗降溫對(duì)患者術(shù)后傷口疼痛的影響,以期為臨床提供借鑒。
1 資料與方法
1.1 研究對(duì)象 納入2017年8月-2018年7月在海軍軍醫(yī)大學(xué)附屬長(zhǎng)征醫(yī)院接受后路腰椎管內(nèi)腫瘤切除重建內(nèi)固定術(shù)的成年患者進(jìn)行前瞻性研究。納入標(biāo)準(zhǔn):①手術(shù)范圍為單節(jié)段的腰椎管內(nèi)腫瘤;②腫瘤位于髓外硬膜下或硬膜外;③術(shù)后病理提示為良性腫瘤;④初次進(jìn)行手術(shù)的患者;⑤45歲≤年齡≤70歲,性別不限;⑥主要臟器功能正常,無(wú)精神、神經(jīng)癥狀,意識(shí)清楚,有一定的閱讀能力。排除標(biāo)準(zhǔn):①術(shù)前對(duì)疼痛過(guò)于敏感或不敏感;②腫瘤侵犯大部分椎體或附件;③患有其他系統(tǒng)疾病; ④術(shù)后出現(xiàn)嚴(yán)重的中樞系統(tǒng)疾病。本研究經(jīng)海軍軍醫(yī)大學(xué)附屬長(zhǎng)征醫(yī)院倫理委員會(huì)審核批準(zhǔn),所有患者及家屬均知情并簽署知情同意書(shū)。
1.2 方法 所有患者均在全麻下行后路腰椎管內(nèi)腫瘤切除重建內(nèi)固定術(shù)。通過(guò)隨機(jī)數(shù)字表法將納入的34例患者均分為兩組,隨機(jī)數(shù)為奇數(shù)的患者納入觀察組(接受持續(xù)生理鹽水沖洗),為偶數(shù)的納入對(duì)照組(未接受持續(xù)生理鹽水沖洗)。觀察組:患者取俯臥位,術(shù)中常規(guī)消毒、鋪單,高頻電刀及電凝功率均設(shè)置為35 W,用皮刀切皮,電刀切開(kāi)皮膚,雙極電凝止血,在電刀切割過(guò)程中,對(duì)周圍肌肉及軟組織給予持續(xù)生理鹽水沖洗降溫,用吸引器及時(shí)吸出沖洗的生理鹽水以保證電刀順利工作,并記錄暴露出兩側(cè)椎板的時(shí)間。以微波測(cè)溫針測(cè)量肌肉切面的局部溫度,反復(fù)測(cè)量多次并取平均值。用組織剪取電刀切割部位大小約1 cm×1 cm×1 cm的肌肉組織,置于肌肉固定液中,用于HE染色及臺(tái)盼藍(lán)染色。對(duì)照組除術(shù)中不采用持續(xù)生理鹽水沖洗降溫外,其余操作步驟同觀察組。所有患者均由同一副主任醫(yī)師作為術(shù)者,同一主治醫(yī)師作為第一助手共同完成手術(shù)。
1.3 觀察指標(biāo)及評(píng)定標(biāo)準(zhǔn)
1.3.1 觀察指標(biāo) 主要指標(biāo):術(shù)后第1、2、3天的疼痛視覺(jué)模擬量表(visual analogue scale,VAS)評(píng)分及止痛藥用量。次要指標(biāo):術(shù)中暴露出雙側(cè)椎板所需的時(shí)間、電刀周圍組織的溫度、肌肉組織熱損傷程度及術(shù)后C反應(yīng)蛋白水平。
1.3.2 評(píng)定標(biāo)準(zhǔn) ①術(shù)后疼痛VAS評(píng)分:0分為無(wú)痛,1~3分為輕微疼痛,4~6分為疼痛影響休息,7~10分疼痛難以忍受,10分為想象中最劇烈的疼痛,讓患者詳細(xì)了解評(píng)分量表的評(píng)判標(biāo)準(zhǔn)及意義,由患者自行評(píng)分。②止痛藥用量:告知患者若傷口疼痛較劇烈影響睡眠時(shí),可酌情增加止痛藥的用量,術(shù)后3 d每天記錄患者非甾體抗炎藥(nonsteroidal antiinflammatory drugs,NSAID)的用量。③術(shù)中暴露出雙側(cè)椎板所需的時(shí)間:從切皮開(kāi)始至完全暴露出雙側(cè)椎板及關(guān)節(jié)突所需的時(shí)間。 ④電刀周圍組織的溫度:對(duì)照組在高頻電刀分離椎板周圍肌肉組織的過(guò)程中將測(cè)溫針頭置于肌肉表面,記錄溫度數(shù)值;觀察組在分離肌肉的過(guò)程中立刻用生理鹽水沖洗,局部測(cè)溫針測(cè)出肌肉表面的溫度(沖洗后立刻測(cè)溫),記錄溫度數(shù)值。⑤肌肉組織熱損傷程度:術(shù)中取出的肌肉組織經(jīng)常規(guī)脫水、石蠟包埋、切片后進(jìn)行HE染色及臺(tái)盼藍(lán)染色,光鏡下觀察熱損傷的程度。在光鏡下通過(guò)HE染色可以觀察到肌肉組織變性、壞死及缺損。根據(jù)正常細(xì)胞與變性、壞死、缺損細(xì)胞的交界判定熱損傷的深度,每張切片均以其最深處記為該切片的熱損傷深度。臺(tái)盼藍(lán)染色切片中活細(xì)胞不著色,而死亡細(xì)胞被染成淡藍(lán)色,光鏡下觀察細(xì)胞的死亡數(shù)量。⑥術(shù)后C反應(yīng)蛋白水平:為兩組患者手術(shù)當(dāng)天外周靜脈血中的C反應(yīng)蛋白水平。
1.4 統(tǒng)計(jì)學(xué)處理 采用SPSS 22.0軟件進(jìn)行統(tǒng)計(jì)分析。計(jì)量資料以±s表示,兩組間比較采用獨(dú)立樣本t檢驗(yàn),多組間比較采用重復(fù)測(cè)量方差分析,進(jìn)一步兩兩比較采用LSD-t檢驗(yàn);計(jì)數(shù)資料以例(%)表示,組間比較采用χ2檢驗(yàn)。P<0.05為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié) 果
2.1 一般情況 本研究共納入患者34例,其中男19例,女15例,年齡46~68(57.0±11.0)歲,術(shù)后病理提示神經(jīng)鞘瘤20例、脊膜瘤14例。觀察組與對(duì)照組的年齡、性別、體重指數(shù)、術(shù)前合并癥、術(shù)前VAS評(píng)分、腫瘤類型等基線資料比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),具有可比性(表1)。
2.2 兩組患者術(shù)中暴露出雙側(cè)椎板所需的時(shí)間、電刀周圍組織溫度、肌肉組織熱損傷程度及術(shù)后C反應(yīng)蛋白水平比較 觀察組術(shù)中暴露出雙側(cè)椎板所需時(shí)間明顯長(zhǎng)于對(duì)照組,電刀周圍組織溫度明顯低于對(duì)照組,差異均有統(tǒng)計(jì)學(xué)意義(P<0.01,表2)。HE染色可見(jiàn)對(duì)照組肌肉組織的染色熱損傷深度大于觀察組;臺(tái)盼藍(lán)染色可見(jiàn)對(duì)照組肌肉中的藍(lán)染細(xì)胞多于觀察組(圖1)。兩組術(shù)后C反應(yīng)蛋白水平比較差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05,表2)。
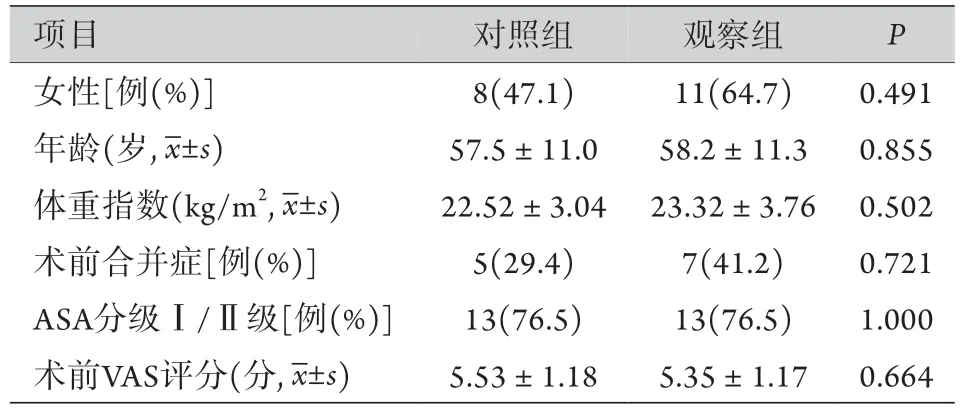
表1 兩組腰椎后路手術(shù)患者基線資料比較(n=17)Tab. 1 Comparison of general information and baseline data of patients undergoing posterior lumbar surgery of two groups (n=17)
2.3 兩組術(shù)后VAS評(píng)分及止痛藥用量比較 兩組術(shù)后第1、2、3天的VAS評(píng)分均明顯低于術(shù)前,且術(shù)后第1天觀察組的VAS評(píng)分明顯低于對(duì)照組,差異均有統(tǒng)計(jì)學(xué)意義(P<0.05),而術(shù)后第2天和第3天兩組的VAS評(píng)分比較差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05)。術(shù)后第1天觀察組的止痛藥用量明顯低于對(duì)照組(P<0.05),術(shù)后第2天和第3天兩組止痛藥用量比較差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05,表2)。
表2 兩組腰椎后路手術(shù)患者術(shù)中及術(shù)后各項(xiàng)指標(biāo)比較(±s,n=17)Tab. 2 Comparison of intra- and post-operative indexes between the patients undergoing posterior lumbar surgery of two groups (±s, n=17)
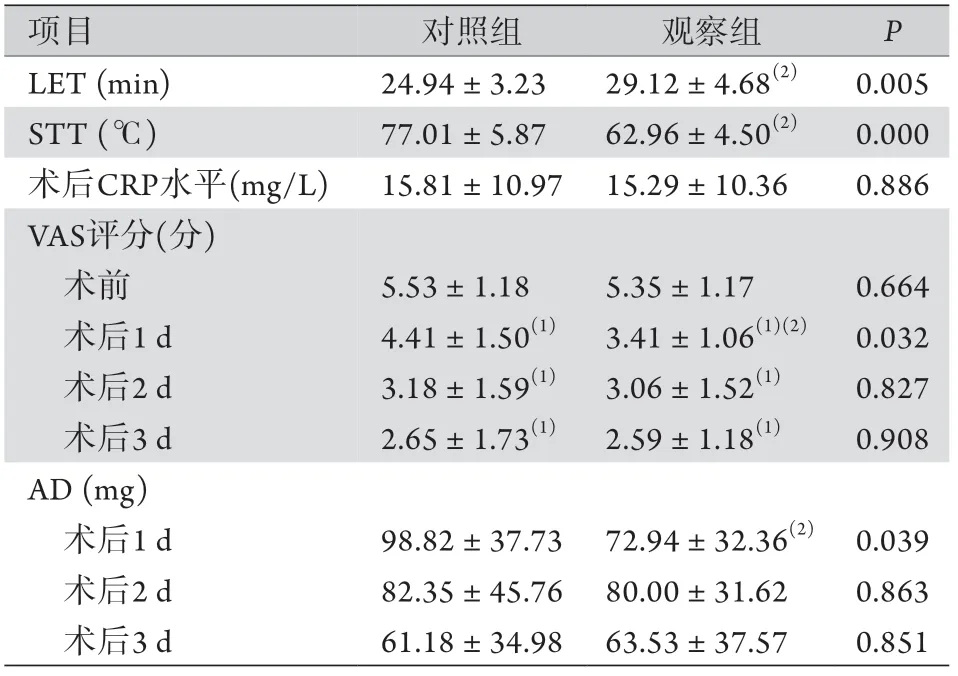
表2 兩組腰椎后路手術(shù)患者術(shù)中及術(shù)后各項(xiàng)指標(biāo)比較(±s,n=17)Tab. 2 Comparison of intra- and post-operative indexes between the patients undergoing posterior lumbar surgery of two groups (±s, n=17)
LET. 暴露雙側(cè)椎板所需時(shí)間;STT. 電刀周圍組織溫度;CRP. C反應(yīng)蛋白;VAS. 疼痛視覺(jué)模擬量表;AD. 止痛藥用量;對(duì)照組未接受持續(xù)生理鹽水沖洗,觀察組接受持續(xù)生理鹽水沖洗;與術(shù)前比較,(1)P<0.05;與對(duì)照組比較,(2)P<0.05。
項(xiàng)目對(duì)照組觀察組P LET (min)24.94±3.2329.12±4.68(2)0.005 STT (℃)77.01±5.8762.96±4.50(2)0.000術(shù)后CRP水平(mg/L)15.81±10.97 15.29±10.360.886 VAS評(píng)分(分)術(shù)前5.53±1.185.35±1.170.664術(shù)后1 d4.41±1.50(1) 3.41±1.06(1)(2) 0.032術(shù)后2 d3.18±1.59(1) 3.06±1.52(1)0.827術(shù)后3 d2.65±1.73(1) 2.59±1.18(1)0.908 AD (mg)術(shù)后1 d98.82±37.73 72.94±32.36(2) 0.039術(shù)后2 d82.35±45.76 80.00±31.620.863術(shù)后3 d61.18±34.98 63.53±37.570.851
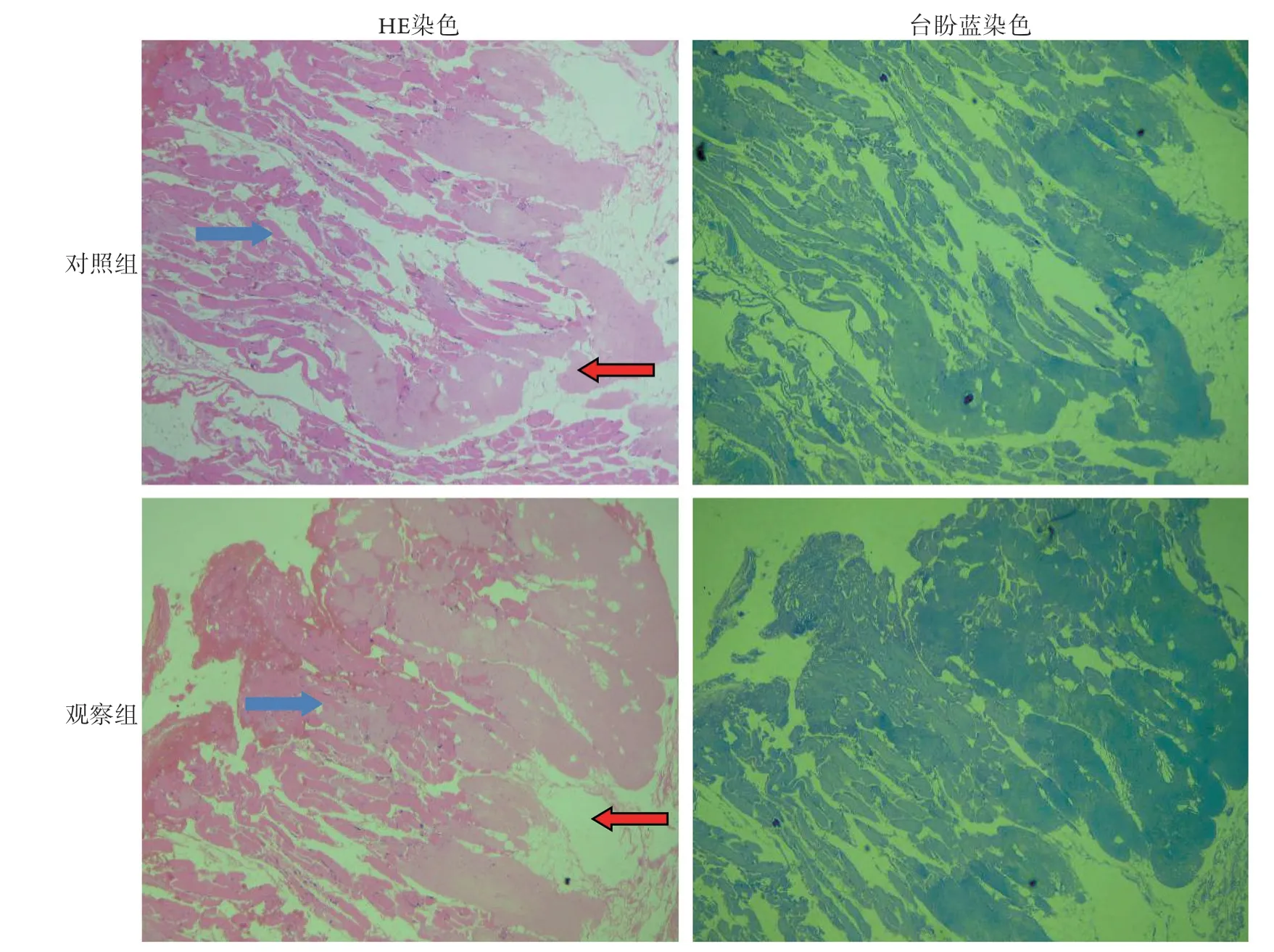
圖1 兩組腰椎后路術(shù)后患者肌肉組織熱損傷情況(×40)Fig.1 Thermal injury of muscle tissues in patients undergoing posterior lumbar surgery of two groups (×40)
3 討 論
脊柱術(shù)后有效鎮(zhèn)痛是患者早期下床活動(dòng)、進(jìn)行功能鍛煉以及減少臥床相關(guān)并發(fā)癥的關(guān)鍵[4-6]。雖然過(guò)去幾十年來(lái)脊柱術(shù)后鎮(zhèn)痛取得了一定進(jìn)步,但臨床上術(shù)后疼痛控制不足仍然較為普遍[7-8]。2003年美國(guó)的一項(xiàng)全國(guó)性調(diào)查顯示,約80%的患者在手術(shù)后出現(xiàn)急性疼痛,其中86%的患者經(jīng)歷了中度及以上程度的術(shù)后疼痛[9]。使用阿片類藥物一直是術(shù)后疼痛管理的主要方法,但由于存在發(fā)生相關(guān)不良事件的風(fēng)險(xiǎn),必須加以限制[10-11]。近期的研究主要集中于多模式鎮(zhèn)痛方案及止痛藥物新的給藥途徑等方面[12-18],但如何在脊柱開(kāi)放手術(shù)中通過(guò)減少組織損傷這一更直接的方法減輕術(shù)后疼痛卻鮮見(jiàn)報(bào)道。
電刀自1917年由法國(guó)醫(yī)師Doyen發(fā)明以來(lái),逐漸被優(yōu)化并廣泛應(yīng)用于臨床各類手術(shù)中[19]。高頻電刀具有可減少術(shù)中失血及快速切割的優(yōu)點(diǎn),因此在脊柱外科手術(shù)中常將其用于分離骨表面的肌肉及軟組織,但電切模式輸出連續(xù)的高頻電流,可產(chǎn)生大量的熱量和極高的溫度(400~600 ℃)[20],導(dǎo)致肌肉組織發(fā)生熱損傷,出現(xiàn)肌肉細(xì)胞核濃縮、核碎裂、核溶解甚至細(xì)胞崩解等一系列病理改變。椎旁肌肉組織血運(yùn)豐富,在高頻電刀切割過(guò)程中還可能損傷肌肉組織內(nèi)的血管。此外,若術(shù)中頻繁使用電刀的電凝模式止血,可進(jìn)一步導(dǎo)致術(shù)后傷口疼痛。
脊柱術(shù)后傷口疼痛程度除了受患者年齡、個(gè)體痛閾影響外,主要與肌肉損傷、神經(jīng)末梢刺激及局部炎癥反應(yīng)有關(guān)。C反應(yīng)蛋白是一種急性期蛋白,在感染和局部組織損傷時(shí)血清濃度急劇升高,可激活補(bǔ)體并增強(qiáng)吞噬細(xì)胞的吞噬作用,從而清除入侵機(jī)體的病原微生物及損傷、壞死、凋亡的組織細(xì)胞,在機(jī)體的天然免疫過(guò)程中發(fā)揮重要的保護(hù)作用[21]。 研究顯示,血清中C反應(yīng)蛋白水平可與肌肉損傷程度呈正相關(guān)[22-25]。
本研究發(fā)現(xiàn),術(shù)中采用生理鹽水持續(xù)沖洗可明顯減輕肌肉組織的熱損傷,HE染色及臺(tái)盼藍(lán)染色均發(fā)現(xiàn)觀察組的肌肉變性、壞死、缺損程度及死亡細(xì)胞數(shù)量明顯低于對(duì)照組,考慮是由于術(shù)中生理鹽水持續(xù)沖洗可降低使用高頻電刀暴露腰椎椎板操作時(shí)周圍局部肌肉組織的瞬時(shí)溫度,減輕組織損傷。但是本研究手術(shù)過(guò)程中發(fā)現(xiàn),術(shù)中生理鹽水持續(xù)沖洗會(huì)導(dǎo)致電刀無(wú)法流暢工作,因?yàn)楦鶕?jù)醫(yī)用物理學(xué)的原理,當(dāng)高頻電流通過(guò)人體組織時(shí),由于每次振蕩的電脈沖時(shí)間極短,離子很難發(fā)生遷移,僅在富有黏滯性的體液中振蕩,因摩擦而生熱,而生理鹽水沒(méi)有黏滯性,導(dǎo)致術(shù)中電刀無(wú)法正常工作,故本研究只能通過(guò)邊電切邊沖洗的方式減輕肌肉組織損傷。這也導(dǎo)致觀察組術(shù)中暴露出椎板的時(shí)間長(zhǎng)于對(duì)照組,這也是術(shù)中沖洗的不足之處。
本研究結(jié)果顯示,術(shù)中采用生理鹽水持續(xù)沖洗可緩解術(shù)后傷口疼痛,減輕肌肉組織損傷。但該措施僅對(duì)于術(shù)后第1天的疼痛緩解作用較明顯,術(shù)后第2、3天患者的疼痛程度與對(duì)照組比較無(wú)明顯差異,考慮可能與術(shù)后傷口疼痛隨著時(shí)間延長(zhǎng)而減輕,以及術(shù)后止痛藥物的應(yīng)用有關(guān)。
綜上所述,本研究結(jié)果表明,雖然術(shù)中持續(xù)生理鹽水沖洗會(huì)延長(zhǎng)手術(shù)時(shí)間,但可以有效減輕肌肉組織的熱損傷及術(shù)后第1天的傷口疼痛,有利于患者術(shù)后疼痛的控制,可考慮臨床推廣應(yīng)用。

