高壓氧治療冠心病不穩定型心絞痛的療效分析
尤琪,關旭,黃杰,晏沐陽
1990年以來,我國心血管病死亡率、發病率及患病率呈上升趨勢,冠心病是動脈粥樣硬化為主要病理基礎的急性缺血性心臟病,急性冠脈綜合征是大多數冠心病患者就診的原因[1],包括:ST段抬高型心肌梗死、非ST段抬高型心肌梗死、不穩定型心絞痛(unstable angina,UA)。UA的治療包括內科藥物治療,冠脈介入(percutaneous coronary intervention,PCI)治療及外科治療,而后者費用高且屬有創治療。有研究證明高壓氧能改善組織缺氧、減輕炎癥反應、減輕缺血再灌注損傷提高組織氧分壓的重要作用,其聯合藥物治療能改善患者靜息心率、心肌缺血、血管內皮及血脂代謝的狀況,讓冠心病患者獲益[2-3]。本課題研究高壓氧聯合藥物治療冠心病的療效及對相關化驗指標的改善。
1 資料與方法
1.1 一般資料 收集2018年1月~2018年12月在我科住院治療的冠心病不穩定型心絞痛患者的所有信息進行回顧性分析,納入標準符合《不穩定型心絞痛診斷和治療建議》[4]。排除標準:高壓氧治療療程不足10次或藥物治療不足14d;缺少血清學檢驗指標;4周內發生急性冠脈綜合征;2周內有心臟介入史或心臟搭橋手術史;急性心肌炎;不能控制的高血壓或收縮壓>160mmHg;嚴重的肺大泡或重癥肺部感染;活動性內出血或出血性疾病;二度以上房室間傳導阻滯。將接受0.13Mpa高壓氧治療的48例冠心病患者分為觀察組,隨機選擇未進行高壓氧治療的48例冠心病患者為對照組,2組患者一般資料比較差異無統計學意義,見表1。

表1 2組患者一般資料比較
1.2 方法 2組患者均給予冠心病藥物對癥支持治療,阿斯匹林(100mg 1次/d)聯合氯吡格雷(75mg 1次/d)或替格瑞洛(90mg 2次/d)雙聯抗血小板聚集,阿托伐他汀(20mg 1/晚)穩定斑塊、低分子肝素抗凝(黃達肝葵鈉 0.5ml 皮下注射 1次/d或依諾肝素 0.4ml 皮下注射 1次/12h)、硝酸酯類藥物(單硝酸異山梨酯緩釋片40mg 1次/d或硝酸異山梨酯片 5mg 3次/d)擴張冠脈、β受體阻滯劑(琥珀酸美托洛爾緩釋片23.75~95mg 1次/d或卡維地洛 12.5mg 2次/d或酒石酸美托洛爾 12.5~25mg 2次/d)控制心室率,合并高血壓者給予鹽酸貝尼地平(4~8mg 1次/d)或奧美沙坦(20mg 1次/d)降壓,合并糖尿病者給予降糖治療,常規輸液治療:前列地爾注射液10ug入壺靜滴1次/d,馬來酸桂哌齊特注射液320mg靜滴1次/d,丹參酮IIA磺酸鈉注射液80mg靜滴1次/d。觀察組再進行高壓氧治療:采用醫用高壓氧艙(YC03800J-X,煙臺冰輪高壓氧艙有限公司),氧艙內10min 加壓至0.13MPa,面罩吸入100% 氧氣40min,10min內減壓至常壓,共60 min。對照組使用上述藥物治療(14.72±3.23)d,高壓氧組使用藥物治療(14.36±3.02)d聯合高壓氧治療(9.87±2.67)次。
1.3 評定標準 觀察指標包括心絞痛發作次數、持續時間及心電圖顯示缺血性ST段。入院第二天及出院前一天對患者進行胸痛HEART評分,通過心電圖,胸痛持續時間及發作頻率評估患者胸痛改善情況。2組分別于入院第二天清晨及出院當天清晨空腹抽血化驗指標腦利鈉肽前體(pro brain natriuretic peptide,pro-BNP)、C反應蛋白(C-reactive protein,CRP)、D-二聚體(D-Dimer),對比2組治療前后pro-BNP、CRP及D-Dimer的值評估高壓氧療效。心絞痛療效評估依據《心血管藥物臨床試驗評價方法的建議》[5]:①顯效:心絞痛發作次數和持續時間較治療前下降80%以上、缺血性ST段回升0.1mV或恢復正常;②有效:心絞痛發作次數和持續時間下降50%~80% 且缺血性ST段下降回升0.05~0.1mV 或主導聯T波變淺大于50%;③無效:心絞痛發作次數和持續時間下降均小于50% ,心電圖無明顯改善甚至病情加重。
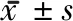
2 結果
2.1 2組患者心絞痛發作次數、持續時間及血清學指標比較 治療前,2組患者心絞痛發作次數、持續時間及血清學指標比較差異均無統計學意義。治療后,2組患者心絞痛發作次數和持續時間較治療前均明顯減少(均P<0.05),且觀察組均更少于對照組(均P<0.05);2組患者pro-BNP、CRP及D-Dimer 較治療前均降低(均P<0.05),且觀察組D-Dimer更低于對照組(P<0.05),pro-BNP和CRP組間比較差異無統計學意義,見表2。
2.2 2組患者心絞痛療效評估 治療后,觀察組患者心絞痛治療的總有效率明顯高于對照組(χ2=4.036,P=0.037),見表3。

表3 2組患者心絞痛療效評估 例
3 討論
隨著人口老齡化,冠心病發病率的升高使冠心病的治療方法也越來越受關注,介入和手術治療費用高且對于高齡老年患者存在很大風險,藥物治療及物理治療相對經濟安全。對于采用不同壓力的高壓氧治療冠心病存在很大爭議,本研究采用0.13MPa高壓氧低于常規0.20MPa高壓氧,減少吸入高壓純氧時引起血管痙攣的風險,同時又提高常規吸氧情況下心臟等各臟器的氧含量。有研究顯示0.20MPa高壓氧與0.15MP高壓氧對改善腦損傷大鼠的預后無顯著差異[7],且使用0.16MP高壓氧治療耳聾療效顯著且副作用明顯小于0.20MPa高壓氧[8],使用較低且安全的治療壓力是一種趨勢。雖然使用0.13MPa高壓氧治療冠心病缺少大規模循證醫學證據,但0.20MPa高壓氧治療過程中更易引起患者血壓升高、心動過緩、血管痙攣,特別是加壓減壓時間長不利急癥的搶救。本研究結果顯示0.13MPa高壓氧聯合藥物治療能有效減輕冠心病不穩定心絞痛的疼痛程度及時間,降低D-Dimer的水平,減輕炎癥反應。
UA發病的病理基礎是在冠脈粥樣硬化的基礎上,板塊松動或破裂,使斑塊內致血栓形成的物質暴露于血液中導致血管病變,其特征是心肌供氧和需氧之間平衡失調[9]。高壓氧治療冠心病的原理為:在高氣壓的環境下讓患者在氧艙中吸入純氧,能夠增加患者血液中氧的溶解量,從而使缺血的心肌獲得充足的氧供應,改善心肌的有氧代謝和能量供應[10-11];其次,高壓氧環境下可減輕心律失常,心率減少可保護心臟,另一方面高壓氧使梗死部位的環磷酰胺腺苷及生物胺水平降低,減少心律失常的發生[12];高壓氧還能降低心肌氧耗,保護缺氧心肌,改善心肌側支循環以及保護內皮細胞[13-15],高壓氧還能改善無癥狀患者心臟的收縮功能,可用于心衰患者的治療[16]。pro-BNP反應患者的心功能,入組的患者大多數不合并心功能衰竭(即pro-BNP<150pg/ml),故治療前后pro-BNP的變化無顯著性差異。CRP是炎癥指標,炎癥反應在動脈粥樣硬化中起著關鍵作用,故認為CRP可反應冠脈粥樣硬化的程度[17],但其敏感性低于超敏C反應蛋白(hs-CRP),CRP<0.05mg/dl時無法統計具體數值。研究顯示pro-BNP,CRP降低未達到統計學意義,可能與納入人數少、CRP敏感性偏低、高壓氧治療療程短有關。

表2 2組患者心絞痛發作次數、持續時間及血清學指標比較 M(Q1,Q3)
綜上所述,0.13MPa高壓氧聯合常規藥物治療,能有效改善冠心病的療效,降低D-Dimer,改善患者的預后,減少患者住院時間及費用,是一種經濟有效的輔助治療。

