基于網絡藥理學探討防風-辛夷藥對治療變應性鼻炎的作用機制
李宇思 謝慧 劉艷 李清韻 肖旭
變應性鼻炎(Allergic Rhinitis,AR),俗稱過敏性鼻炎,患病率為10%~25%,是由于機體針對變應原產生過量的特異性IgE而誘發(fā),導致鼻腔黏膜水腫、噴嚏、鼻癢、分泌物增多等一系列癥狀。變應性鼻炎屬祖國醫(yī)學“鼻鼽”的范疇,目前臨床尚無特效藥治療,西醫(yī)主要使用抗組胺藥、糖皮質激素等治療[1]。中藥在預防和治療變應性鼻炎中具有很大的優(yōu)勢和潛力。
防風、辛夷是導師謝慧治療變應性鼻炎的常用藥對,長期的臨床觀察發(fā)現(xiàn)該藥對的應用能緩解變應性鼻炎鼻塞、鼻癢、噴嚏、流清涕的癥狀,并能減少其發(fā)作。劉金壘等通過對治療變應性鼻炎國家專利中藥復方的挖掘發(fā)現(xiàn),治療變應性鼻炎最多的對藥為防風-辛夷[2]。防風辛、甘,溫,歸膀胱、肝、脾經,功擅解表祛風,勝濕,止痙。辛夷辛,溫,歸肺、胃經,功擅散風寒,通鼻竅。變應性鼻炎的主要病機是肺氣虛弱,風寒外襲[2],防風、辛夷合用,可增強祛風散寒通鼻竅之用,但兩藥配伍治療變應性鼻炎的藥效機制尚不明了,有待進一步闡明,本文運用網絡藥理學,對防風-辛夷藥對治療變應性鼻炎的活性成分、關鍵靶點、作用機制等進行初步探索,為后續(xù)研究提供依據與思路。
1 材料與方法
1.1藥效成分收集篩選
以防風、辛夷為研究對象,通過中藥系統(tǒng)藥理數(shù)據庫和分析平臺(TCMSP)(http://tcmspw.com/tcmsp.php)進行化學成分的查詢及篩選[3]。選取口服利用度(oral bioavailability,OB)≥30%且類藥性(drug-likeness,DL)≥0.18[4]的化學成分作為潛在有效成分。
1.2藥效成分靶點預測
繼續(xù)通過TCMSP數(shù)據庫檢索防風和辛夷的所有成分的靶點,并與已得到的潛在成分相映射,獲得潛在靶點,利用 Drugbank數(shù)據庫(https://www.drugbank.ca/)和Uniprot 數(shù)據庫(http://www.uniprot.org/)將防風和辛夷有效靶點與人類相關基因相對應,獲得藥物的潛在靶點。
1.3疾病靶點預測
通過GeneCards數(shù)據庫(https://www.genecards.org/)、OMIM數(shù)據庫(http://www.omim.org/)、Drugbank數(shù)據庫(https://www.drugbank.ca/)搜索“allergic rhinitis”,合并3個疾病數(shù)據庫的靶點,刪除重復值作為疾病候選靶點。在Unitprot數(shù)據庫中查詢靶點的基因名,對候選靶點進行標準化處理。
1.4構建“藥物-活性成分-靶點”網絡
將藥物疾病映射的共同靶點與藥物的有效活性成分導入 Cytoscape 3.8.0軟件,構建藥物-活性成分-靶點網絡圖。
1.5獲取藥物與疾病的共同靶點
借助Venny 2.1(https://bioinfogp.cnb.csic.es/tools/venny/index.html)將藥物潛在靶點與疾病作用靶點取交集,獲得防風-辛夷藥對治療變應性鼻炎的關鍵靶點,繪制韋恩圖。
1.6構建關鍵靶點蛋白相互作用(protein-protein interaction, PPI)網絡
為了進一步獲取關鍵靶點,利用 STRING 數(shù)據庫(https://string-db.org/),將藥對和疾病的共同靶點導入該數(shù)據庫,并限定物種為人類物種(Homo sapiens),獲得蛋白互作網絡圖(PPI),檢索研究相關文獻,為確保可信度,將交互分數(shù)限定為>0.4,去除無相互作用的單一蛋白,獲得最終的PPI網絡圖。
1.7GO功能、KEGG通路富集分析
在DAVID6.8數(shù)據平臺(https://david.ncifcrf.gov/)傳關鍵靶點,進行GO分析[由細胞組成(cellular component, CC)、分子功能(molecular function, MF)、生物過程(biological process, BP)三部分組成]和KEGG分析,并通過微生信在線平臺分別繪制高級氣泡圖。
1.8構建“成分-關鍵靶點-通路”網絡圖
應用 Cytoscape 3.8.0 軟件對防風、辛夷藥對預測的44個靶點及相對應的32種化學成分,以及靶點相對應的主要通路進行分析,構建核心藥物組合成分-關鍵靶點-通路網絡圖。
2 結果
2.1藥物活性成分及靶點篩選
通過TCMSP數(shù)據庫,根據OB≥30%和DL≥0.18原則,共篩選得到36種候選藥效成分,其中防風18種,辛夷19種,其中共有成分1種,詳細信息如表1所示。36個有效成分經進一步搜集共得到潛在有效靶點80個,運用Cytoscape3.8.0繪制“藥物-活性成分-靶點”網絡圖,見圖1 ,該網絡共包含111個節(jié)點,342條邊,其中34個節(jié)點代表藥效成分,77個節(jié)點代表與藥效成分相關的靶點基因。

表1
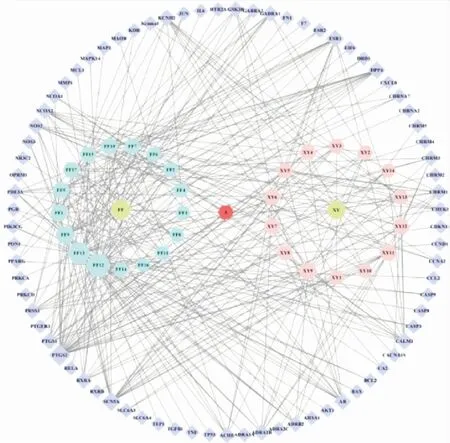
圖1
2.2變應性鼻炎靶點的獲取及藥物與疾病交集靶點的獲取
在Genecards數(shù)據庫中搜集變應性鼻炎靶點2073個,考慮靶點基因過多,按Relevance Score分數(shù)由高到低進行排序,經兩次篩選大于中位數(shù)的靶點后,獲939個靶點。結合Drugbank、OMIM數(shù)據庫補充變應性鼻炎靶點,合并去重,共獲得疾病靶點1147個。在Venny2.1.0中將篩選出的防風-辛夷活性成分靶點與變應性鼻炎靶點取交集,得到44個共同關鍵靶點,為CHRM1、CHRM2、CHRM3、CHRM4、CHRM5、SLC6A4、SLC6A3、PTGS1、PGR、NR3C2、PTGS2、GABRA2、IL6、PTGER3、TGFB1、TNF、CXCL8、CCL2、ADRB2、NOS2、FN1、CASP3、MMP1、NOS3、PIK3CG、MAPK14、ESR1、RELA、CASP8、PPARG、AKT1、JUN、BCL2、KDR、PRKCA、DPP4、PON1、HTR2A、RXRB、ADRA1A、AR、KCNH2、ESR2、PRKCD,見圖2。
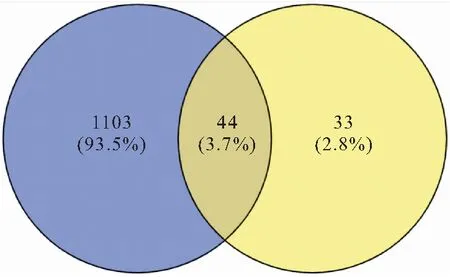
圖2
2.3防風-辛夷藥對治療變應性鼻炎的關鍵靶點PPI網絡
為了更好地分析靶點蛋白間的相互作用,將疾病和藥對的共同靶點導入String數(shù)據庫,限定物種為人,為確保數(shù)據的可靠性,選擇0.4的高置信度,繪制蛋白互作關系網絡圖,去除無相互作用的單一蛋白,獲得最終的PPI網絡圖,結果見圖3。該網絡包括44個節(jié)點,285條邊。根據Degree值篩選出排名前五的靶點分別是AKT1、IL6、NOS3、JUN、MAPK14。
2.4GO功能和KEGG通路富集分析
為進一步闡明關鍵靶點的可能作用,應用DAVID 6.8數(shù)據平臺對關鍵靶點進行GO及KEGG通路富集分析,共有321個GO術語條目,其中細胞組成27個,分子功能49個,生物過程245個,KEGG富集顯示92條通路。按P值排序后,取前20條通過通過微生信在線平臺分別繪制高級氣泡圖,見圖4。
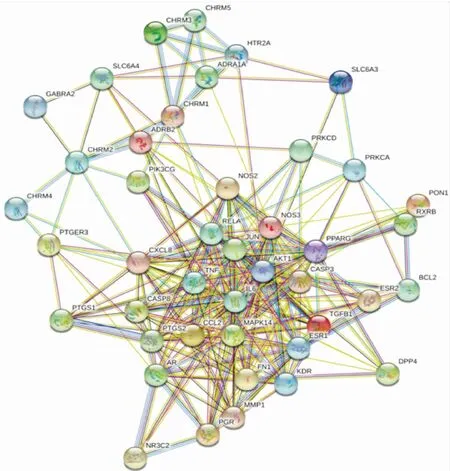
圖3
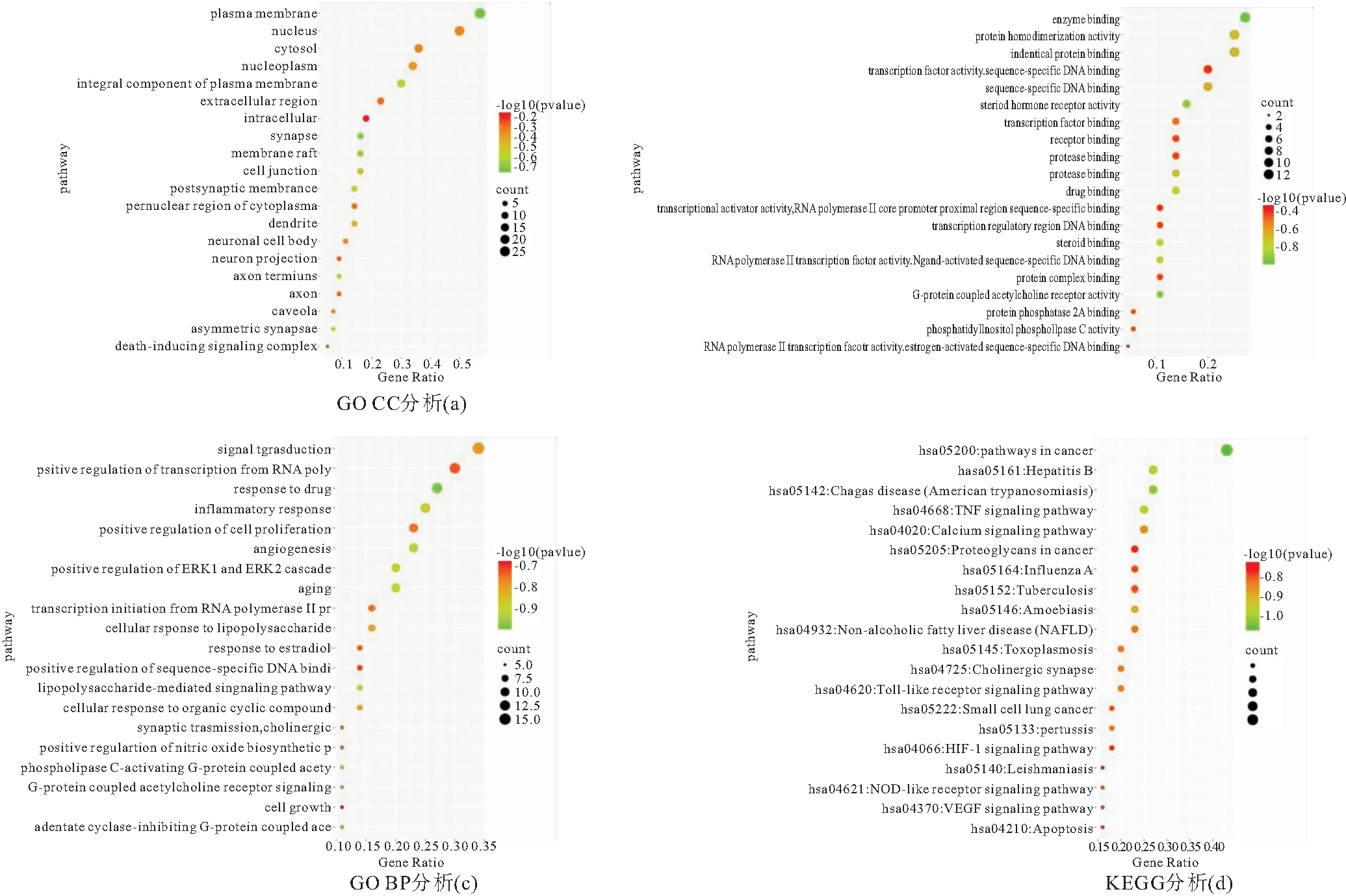
圖4
GO功能富集分析結果顯示,細胞組成(CC)主要集中于質膜(plasma membrane)、突觸(synapse)、膜筏(membrane raft)、質膜的組成部分(integral component of plasma membrane)、突觸后膜(postsynaptic membrane)等部位,見圖4a;分子功能(MF)主要集中于酶結合(enzyme binding)、G蛋白偶聯(lián)乙酰膽堿受體活性(G-protein coupled acetylcholine receptor activity)、類固醇激素受體活性(steroid hormone receptor activity)、類固醇結合(steroid binding)等方面,見圖4b;生物過程(BP)主要集中于脂多糖介導的信號通路(lipopolysaccharide-mediated signaling pathway)、細胞對脂多糖的反應(cellular response to lipopolysaccharide)、ERK1和ERK2級聯(lián)的正調節(jié)(positive regulation of ERK1 and ERK2 cascade)等方面,見圖4c。KEGG 通路富集分析結果顯示,鈣信號通路(Calcium signaling pathway)、Toll樣受體信號通路(Toll-like receptor signaling pathway)、NOD樣受體信號通路(NOD-like receptor signaling pathway)、膽堿能突觸(Cholinergic synapse)、腫瘤壞死因子信號通路(TNF signaling pathway)、血管內皮生長因子信號通路(VEGF signaling pathway)等20條通路與防風-辛夷治療變應性鼻炎可能相關,見圖4d。
2.5成分-靶點-通路網絡圖
應用 Cytoscape 3.8.0 軟件對防風、辛夷藥對預測的44個靶點及相對應的32種化學成分,以及靶點相對應的主要通路進行分析,構建成分-靶點-通路網絡圖,結果見圖5。
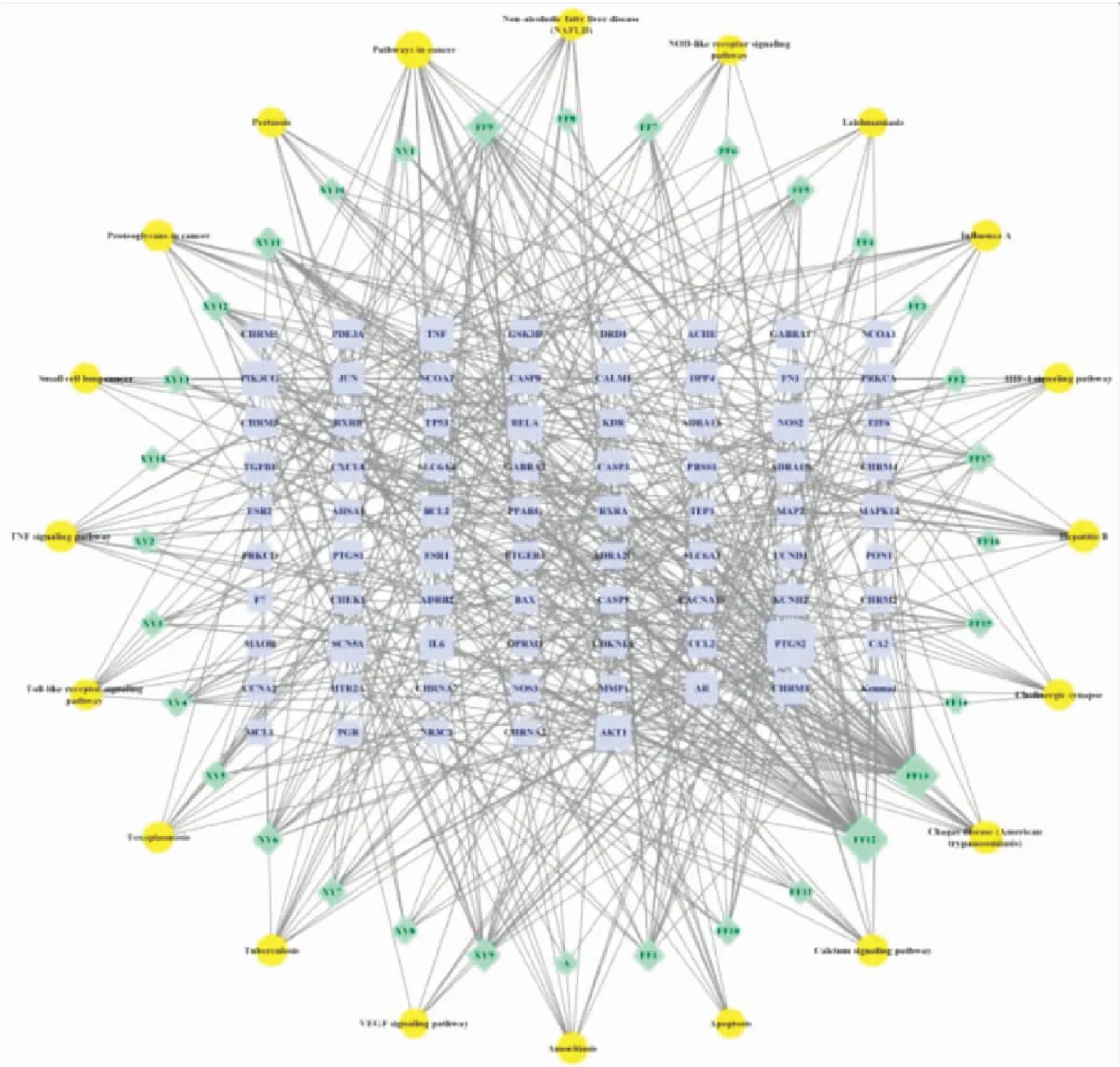
圖5
3 討論
防風、辛夷中色原酮、5-O-甲維阿斯米醇、歐前胡素、木蘭脂素、Galgravin能匹配到較多的靶點,提示著可能是防風、辛夷治療變應性鼻炎的關鍵有效成分。歐前胡素可顯著抑制RBL-2H3細胞脫顆粒,并降低組胺及各炎癥指標的釋放,促進IFN-γ表達,通過免疫調節(jié)降低細胞的炎癥反應[5]。色原酮能降低血清的IL-1β,IL-6和TNF-α水平,降低炎癥反應[6],從而減輕變應性鼻炎的癥狀。5-O-甲維阿斯米醇能顯著抑制二甲苯引起的皮膚腫脹, 降低炎癥反應[7]。木蘭脂素具有較強的抗過敏作用,對炎癥早起有明顯的抑制作用,其抗炎機制與其抑制IL—la的作用有關[8-9]。而Galgravin作為一種有效的抗PAF化合物[10],對PAF導致的變應性鼻炎可能具有較好的治療效果。
蛋白質相互作用網絡表明,44個關鍵靶點中,IL6的連接度最高。IL-6是炎癥發(fā)生最關鍵的炎癥因子,在適應性免疫和慢性炎癥等病理過程中起重要作用[11]。王鑫等[12]研究表明,IL6與變應性鼻炎的發(fā)病密切相關,Kimura等[13]認為IL-6增強B淋巴細胞的終末分化,放大IgE合成的信號,促使B淋巴細胞成熟為高效合成IgE的細胞,并最終分泌IgE。除此之外,AKT1、NOS3、JUN、MAPK14,這些關鍵靶點參與多種生物過程,PI3K/AKT 信號通路可以抑制肥大細胞活性和變應性鼻炎的變應性反應,而在此通路中,AKT 發(fā)揮著關鍵的作用[14]。MAPK14參與調控T細胞受體、輔助性T細胞(Th1、Th2、Th17細胞分化)信號通路從而參與機體免疫應答[15],并且參與細胞的生長分化過程[16]。JUN蛋白質能調節(jié)免疫細胞的增殖和分化,且涉及炎癥細胞的激活和細胞因子和趨化因子的釋放[17]。NOS3的活性被抑制,可控制某些炎癥因子所介導的通透性增加[18],從而減少滲出。
通過GO生物功能富集分析,發(fā)現(xiàn)其可以通過影響酶結合、類固醇結合、藥物結合、蛋白酶結合、蛋白質復合物結合、受體結合、G蛋白偶聯(lián)乙酰膽堿受體活性、類固醇激素受體活性、轉錄因子活性、蛋白酶活性,直接配體調控序列特異性DNA結合、血管生成、突觸傳遞等的作用來治療變應性鼻炎。KEGG 通路富集分析顯示了防風-辛夷療變應性鼻炎的主要信號通路。研究表明TLRs信號可能通過參與誘導產生Th1和/或 Th2型細胞因子調節(jié)過敏性炎癥[19-20]。鈣信號通路與變應性鼻炎中的T細胞分化有關[21]。NOD樣受體信號通路能介導炎癥反應,引起Th2細胞因子的釋放,加重或維持AR狀態(tài),并且能增強免疫應答[22]。因此,Toll受體信號通路、NOD樣受體信號通路、鈣離子通道可能是防風-辛夷治療過變應性鼻炎的的潛在靶信號通路。
本研究通過網絡藥理學研究方法,對防風-辛夷治療變應性鼻炎的化學成分、靶點、通路之間進行研究,體現(xiàn)了防風、辛夷藥對多成分、多靶點、多通路協(xié)同作用的特點。但防風-辛夷藥對治療變應性鼻炎的作用機制有待于進一步動物實驗或細胞實驗的證實。

