“素養為本”指導下的高三化學復習策略
—— 以“合成氨工業”為例
黃瓊玉
(江蘇省張家港市沙洲中學 215600)
一、問題的提出
2016年,教育部考試中心權威發布“一體四層四翼”,從頂層設計上回答了高考“為什么考”“考什么”“怎么考”,其中對“學科素養”考查要求是:學生能夠在不同情境下綜合利用所學知識和技能處理復雜任務,具有扎實的學科觀念和寬闊的學科視野,并體現出自身的實踐能力、創新精神等內化的綜合學科素養.《普通高中化學課程標準(2017年版)》中提到:高中化學學科素養反映了社會主義核心價值觀下化學學科育人的基本要求,全面展現了化學課程學習對學生未來發展的重要價值.新高考、新課程標準都推動了廣大化學教師要在“素養為本”的視域下進行化學教學.
傳統的高三化學的復習教學注重知識點的反復梳理,雖然也有方法歸納和遷移應用,但少了新意和生趣,不能很好地激發學生的求知欲望,以致于在有限的復習時間里沒有達到最好的復習效果.如何在化學核心素養要求下使高三復習課綻放精彩,值得每位高三化學教師思考與研究.
二、教學案例的選擇
筆者在多年的高三教學中關注到與化工工業相關的知識一直是考試的熱點,也是高三復習的重點,在實際教學中,通過各種嘗試,發現如果在化學核心素養指導下,將元素化合物知識結合化工生產,滲透物質結構和反應原理等知識,形成主題式復習模式,可以激發學生的主觀能動性,讓課堂更鮮活更有激情.下面筆者以“合成氨工業”為例,談談“素養為本”指導下的高三化學復習策略.
三、教學過程的實施
環節一:合成氨工業的原理
【創設情境】播放錄像:化學史—— 諾貝爾化學獎三次握手合成氨工業,介紹哈伯、博施、埃特爾的事跡.
【學生活動】
1. 寫出哈伯的合成氨工業的原理.
2.該反應過程中的能量變化如圖1所示.已知H—H鍵、N—H鍵、N≡N鍵鍵能分別為436、391、946 kJmol-1,請寫出其熱化學方程式____.
3.在25℃時該反應的化學平衡常數為5×108,可為什么常溫下氮氣、氫氣不能合成氨?
【設計意圖】體現了“宏觀辨識與微觀探析”的核心素養.通過化學方程式的書寫,認識元素從游離態到化合態的轉化,形成“元素觀”,以此建立起一種工業合成新物質的認識框架.通過化學反應能量圖的分析,能從“化學反應的本質是舊化學鍵的斷裂,同時新化學鍵的形成”這一微觀層面來認識宏觀的能量變化,并對物質及其變化進行分類和表征.
環節二:合成氨工業條件的選擇
【創設情境】合成氨工藝條件的成熟經歷了很多艱辛的研究過程,凝聚了很多科學家的心血,他們通過大量實驗來提煉資料,得到結論.
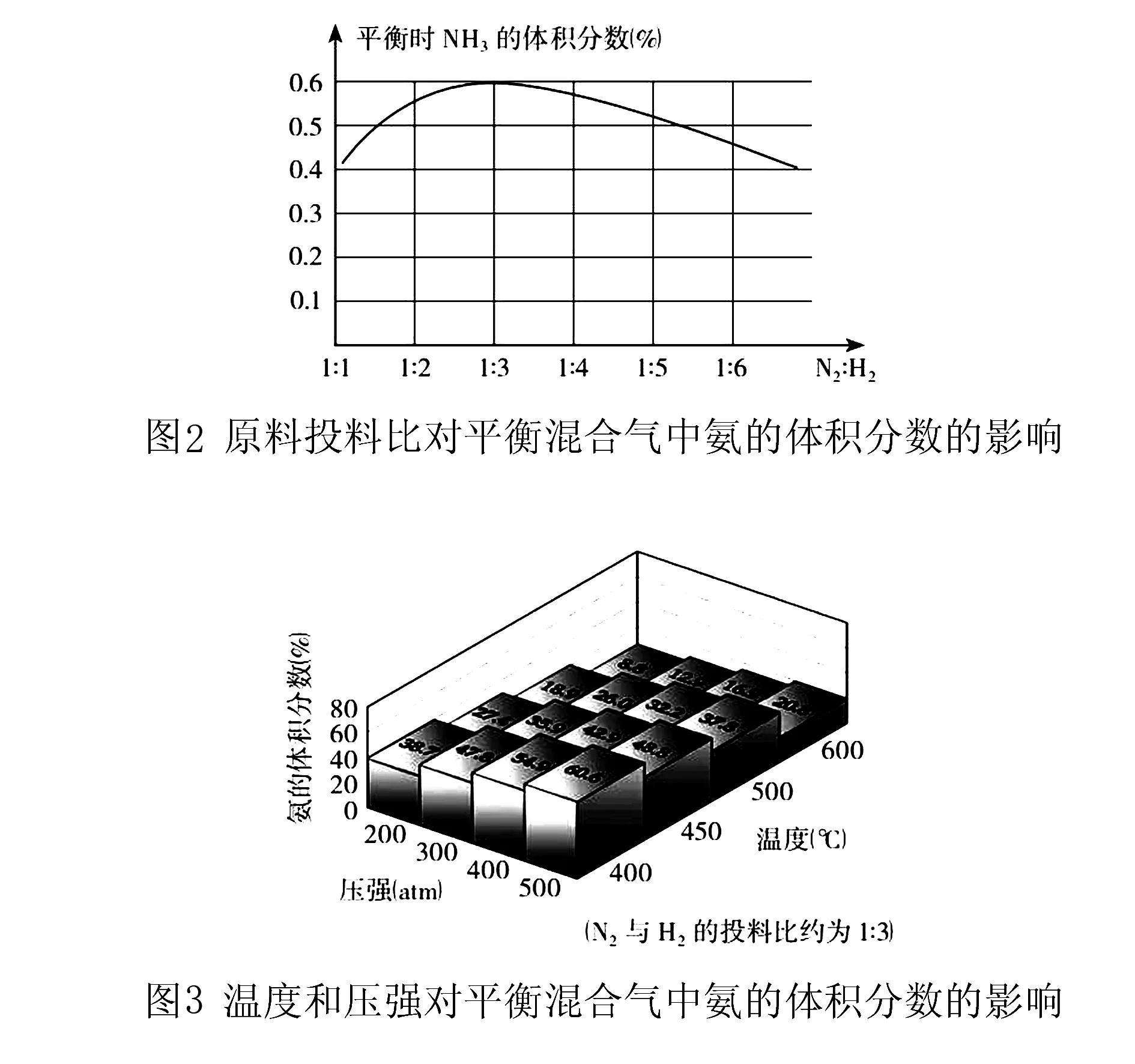
表1

研究者壓強/atm溫度/℃催化劑平衡混合氣中NH3所占的體積分數)能斯特50685鉑粉、錳粉等0.96%哈伯150~250550鋨或鈾8.25%
【學生活動】
1. 結合圖2、圖3和表1的信息,從化學反應速率和化學反應平衡的角度來選擇合成氨工業的條件.
2. 在密閉容器內的反應:

(1)若初始投入:N21mol、H23mol,則N2和H2的平衡濃度比是____.
(2)平衡時,等容容器中充入惰性氣體,平衡將____移動.
(3)平衡時,將3種物質的濃度同時增大1倍,平衡將____移動.

①氫氣的消耗速率與氨的生成速率為3∶2;
②N2、H2、NH3的分子數目比為1∶3∶2;
③N2、H2、NH3的濃度保持不變;
④混合氣體的總壓強不再改變.
【設計意圖】體現了“變化觀念與平衡思想”的核心素養.通過圖像和數據分析來概括合成氨工業的條件,認識反應條件對化學反應速率和化學平衡的影響,學會運用變量控制的方法研究化學反應;根據稀有氣體對該反應的影響以及平衡標志的判斷來理解化學反應中量變和質變的關系,學會運用對立統一思想和定性定量的方式揭示化學變化的規律,并運用于生產、生活實際中去.
環節三:合成氨化學平衡中的等效思想

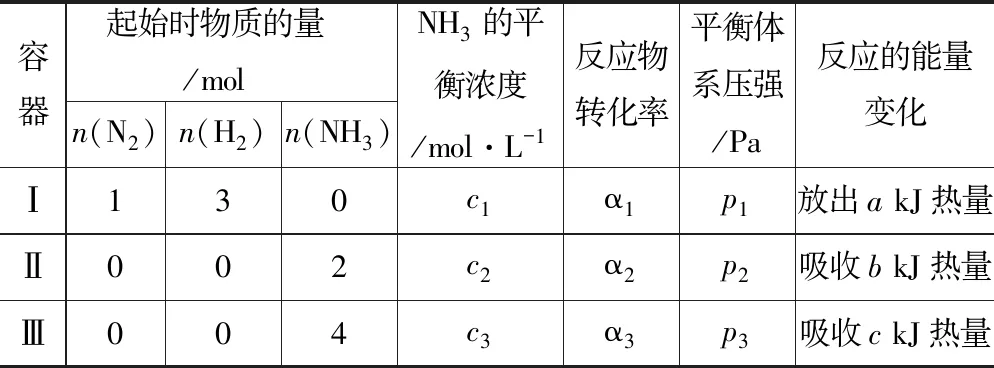
容器起始時物質的量/moln(N2)n(H2)n(NH3)NH3的平衡濃度/mol·L-1反應物轉化率平衡體系壓強/Pa反應的能量變化Ⅰ130c1α1p1放出a kJ熱量Ⅱ002c2α2p2吸收b kJ熱量Ⅲ004c3α3p3吸收c kJ熱量
【學生活動】構造解題模型(如圖4所示).一般先建立等效平衡(將恒容容器先變為恒壓容器),再確定反應過程中體積的變化,然后將體積復原,確定平衡移動的方向,分析平衡移動引起的量的變化.
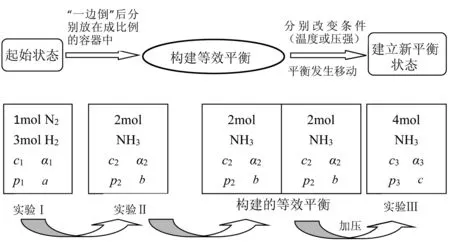
圖4
【設計意圖】體現了“證據推理與模型認知”的核心素養.面對復雜的等效平衡問題,幫助學生對情境中的關鍵要素(“一邊倒”后是否相同或成比例、等溫等壓、等溫等容、絕熱容器)進行分析以建構相應的模型.這是一種極其重要的思想方法,其一般步驟是:分析抽象問題→構建化學模型→建立化學關系→回歸解決問題.
環節四:合成氨工業的發展
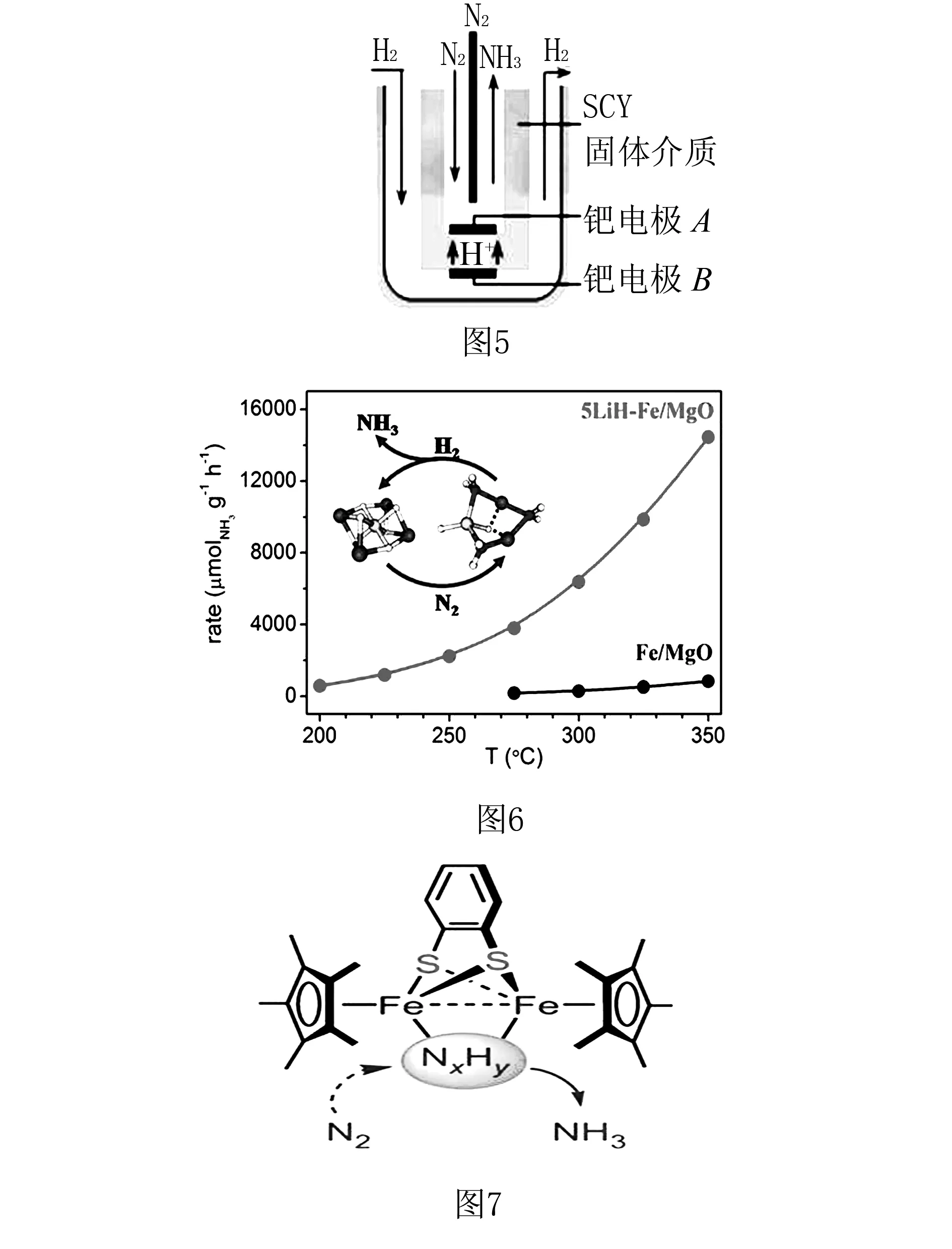
【創設情境】合成氨工業關系到全人類的生存和發展,常溫常壓下合成氨的探索一直是科學家研究的熱點.下面圖5是2001年兩位希臘化學家提出了采用高質子導電性的SCY陶瓷(能傳遞H+)為介質電解合成氨的方法.圖6是化學模擬生物固氮新的功能分子模型,實現了在雙鐵中心上,氮烯(NxHy)還原轉化成氨氣.圖7是大連化物所在合成氨反應機理中對復合催化劑的部分研究結果.
【學生活動】
1. 由圖5寫出電極反應式.
2. 由圖6選擇催化性能較好的催化劑.
3. 由圖7寫出生成NH3的化學方程式.
4. 請從原料氣的來源、凈化,催化劑的選擇,節能減排等方面談談你對合成氨工業未來發展的設想.
【設計意圖】體現了“科學探究與創新意識”的核心素養.科學技術是第一生產力,而只有創新才能推動科學技術的進步.這一環節通過對合成氨工業的創新發展歷史的學習和討論,培養學生的問題意識,讓學生能根據文獻和實際需要提出綜合性探究方案,善于合作,勇于創新.
環節五:合成氨工業與綠色化學
【創設情境】全世界每年約有15%的氨用于非化肥領域,如氨是固定裝置排放NOx的還原劑.利用NH3催化還原氮氧化物(SCR技術)是目前應用廣泛的煙氣脫硝技術.
【學生活動】
1.寫出SCR技術核心反應

的化學平衡常數表達式K=____.
若K隨溫度T的升高而減小,則該反應的ΔH____0.(填“>”、“<”或“=”).
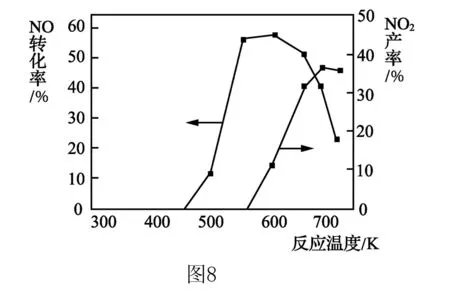
2.如圖8所示,在有氧及Ag2O催化下,還會發生:

ΔH=-1627.2 kJ·mol-1
試分析當溫度為550~700℃,NO轉化率下降、NO2產率上升的可能原因____.
【設計意圖】體現“科學態度與社會責任”的核心素養.通過了解合成氨的產品氨氣能參與含氮污水的處理,樹立“綠色化學”理念.解決社會熱點問題,逐步形成節約成本、循環利用、保護環境等觀念.
四、教學反思
本節課依托“合成氨工業”進行主題式復習,從諾貝爾化學獎到合成氨工藝的條件及平衡狀態,再挖掘發展前景及參與綠色化學等,將元素化合物知識、化學反應與能量變化、等效平衡、電化學等知識串聯起來,打破了原有知識的孤立性和零散性,拓展了復習的廣度和深度,不僅提高了學生綜合解決問題的能力,還樹立了學生的社會責任意識.這樣的高三復習課既迎合了高考“一體四層四翼”的高層要求,又體現了五大化學核心素養,真正讓化學課堂成為落實立德樹人根本任務、發展素質教育、弘揚科學精神、提升學生核心素養的重要載體.這種“素養為本”的主題式高三復習課,要求教師在課前花費大量的時間去思考如何最大限度地將各知識點結成一張立體的大網,再創設情境,構思問題,設計成一堂不斷迸發思維火花的課堂.筆者相信,在高考“一體四層四翼”和化學學科核心素養的正確指導下,通過廣大化學教師不懈的努力,肯定能讓原本枯燥的高三化學復習課大放異彩!

