桃葉珊瑚苷通過(guò)激活ERβ途徑抑制心肌細(xì)胞凋亡
李春曉,張璐莎,張麗媛,馬璐璐,王倩怡,方樂(lè)玉,楊文杰,孫 偉,冷雨澤,陳 璐,王 虹
(天津中醫(yī)藥大學(xué)中西醫(yī)結(jié)合學(xué)院、方劑學(xué)教育部重點(diǎn)實(shí)驗(yàn)室、天津市中藥藥理學(xué)重點(diǎn)實(shí)驗(yàn)室、天津中醫(yī)藥大學(xué)中醫(yī)藥研究院,天津 301617)
抑制心肌細(xì)胞凋亡發(fā)揮抗心肌缺血損傷從而改善急性心肌梗死后心功能的作用,其部分作用機(jī)制與ERβ通路的激活有關(guān)。
缺血性心臟病(ischemic heart disease,IHD)是全球死亡率最高的疾病之一[1]。急性心肌梗死(acute myocardial infarction,AMI)能夠?qū)е虏豢赡娴男募〖?xì)胞損傷或繼發(fā)的心肌供血不足。雖然現(xiàn)有的治療方法能夠改善冠狀動(dòng)脈血流,增加缺血區(qū)域的血液供應(yīng)從而達(dá)到治療效果[2],但其發(fā)病率和死亡率依然居高不下。氧化應(yīng)激損傷是缺血性心臟病的主要發(fā)病機(jī)制[3],活性氧的積累導(dǎo)致心肌細(xì)胞的壞死和凋亡,其中細(xì)胞凋亡貫穿心肌梗死發(fā)生的整個(gè)病程[4],因此減少心肌梗死后的心肌細(xì)胞凋亡對(duì)限制心肌梗死患者的組織損傷程度及改善心臟功能具有重要意義。
雌激素受體β(estrogen receptor β,ERβ)在調(diào)節(jié)正常生理、衰老和多種疾病中發(fā)揮重要作用[5]。ER最典型的功能為配體激活的轉(zhuǎn)錄因子,介導(dǎo)激素調(diào)節(jié)的組織和器官中的基因轉(zhuǎn)錄[6]。研究表明[7],絕經(jīng)后婦女急性心肌梗死的增加可能與體內(nèi)雌激素水平下降和ERβ表達(dá)下降有關(guān)。在心肌梗死中,ERβ通過(guò)調(diào)節(jié)PI3K/AKT信號(hào)通路改善急性心肌梗死患者的心功能及MI后的心肌纖維化[8-9],是預(yù)防及治療圍絕經(jīng)期綜合征患者急性心肌梗死的潛在靶點(diǎn)之一。
桃葉珊瑚苷(aucubin,AU)又稱(chēng)β-D-吡喃葡萄糖苷,是杜仲、車(chē)前草、地黃等中藥材的有效成分之一。近年來(lái)研究表明,AU具有抗氧化、抗炎、抗纖維化等多種藥理作用[10-11],對(duì)免疫、心腦血管、神經(jīng)系統(tǒng)均有保護(hù)作用,但其對(duì)心肌細(xì)胞凋亡的作用機(jī)制尚不清楚。本課題組前期研究發(fā)現(xiàn)AU具有植物雌激素樣作用[12],能夠激活雌激素受體。本研究旨在探討AU對(duì)心肌凋亡的影響及其機(jī)制,為AU防治缺血性心臟病提供新的實(shí)驗(yàn)依據(jù)。
1 材料與方法
1.1 材料
1.1.1細(xì)胞與動(dòng)物 大鼠H9c2,購(gòu)于美國(guó)ATCC公司,8周齡雄性C57BL/6J小鼠購(gòu)自北京維通利華實(shí)驗(yàn)動(dòng)物研究中心,許可證號(hào):SCXK(京)2016-0006。
1.1.2藥物與試劑 AU購(gòu)于成都曼斯特生物科技有限公司(批號(hào):DST190907-004),純度為99.93%,分子量為346.33,分子式:C15H22O9;腫瘤壞死因子-α(Tumor necrosis factor-α,TNF-α,貨號(hào):315-01A)購(gòu)于PeProTech;放線菌酮(Cycloheximide, CHX,貨號(hào):M4881)、MTT(貨號(hào):M8180)購(gòu)于Solaibro;MPP dihydrochloride(貨號(hào)7A/198343)、(R,R)-THC(貨號(hào):6A/192678)購(gòu)于tocris公司;DCFH-DA粉末(貨號(hào):D6883)購(gòu)于Sigma;DMEM(貨號(hào):SH30022.01)購(gòu)于Hyclone;胎牛血清(FBS,貨號(hào):04-001-1ACS)、雙抗(青鏈霉素,貨號(hào):03-031-1B)、胰蛋白酶(貨號(hào):03-052-1A)購(gòu)于Biological Industries;β-Actin (3E5) Rabbit mAb(貨號(hào):4970)、caspase-3 Antibody(貨號(hào):9662)、Akt Antibody(貨號(hào):4691)、 p-Akt Antibody(貨號(hào):4060)、Bcl2 Antibody(貨號(hào):3498)、Bax Antibody(貨號(hào):2772)購(gòu)于CST;Goat anti-Rabbit IgG (H+L) Alexa Fluor?594 conjugate(貨號(hào):A-11012)購(gòu)于Invitrogen;In Situ Cell Death Detection Kit(貨號(hào):11684817910)購(gòu)于Roche。
1.2 方法
1.2.1動(dòng)物及給藥 小鼠在體實(shí)驗(yàn)經(jīng)天津中醫(yī)藥大學(xué)倫理委員會(huì)(中國(guó)天津)批準(zhǔn),在體研究方法均按照指南操作。所有動(dòng)物實(shí)驗(yàn)均按照美國(guó)指南(NIH出版物#85-23,1985年修訂)和赫爾辛基宣言的原則進(jìn)行。將小鼠飼養(yǎng)于溫度(22±2) ℃和濕度55%±5%房間中,12 h照明/12 h黑暗晝夜交替,在進(jìn)行實(shí)驗(yàn)前適應(yīng)性喂養(yǎng)1周。研究中使用的AU為10 mg·kg-1·d-1,辛伐他汀作為陽(yáng)性藥,使用劑量為10 mg·kg-1·d-1。將AU和辛伐他汀溶解在生理鹽水中灌胃給藥。
1.2.2手術(shù) 腹腔注射三溴乙醇麻醉小鼠,結(jié)扎左前降支冠狀動(dòng)脈建立急性MI模型。手術(shù)后將小鼠隨機(jī)分為4組:假手術(shù)組,模型(生理鹽水)組,AU組和Sim組。從d 0開(kāi)始,將小鼠隨機(jī)分組給藥。
1.2.3超聲心動(dòng) 在術(shù)前1 d,術(shù)后7、14和28 d,用Vevo 2100TM高分辨率超聲生物顯微鏡(VisualSonics Inc.,Canada)和Vevo分析軟件(Vevo 2.2.3,[VisualSonics Inc.])進(jìn)行超聲心動(dòng)圖測(cè)量。麻醉小鼠后,記錄M-模式短軸圖像和B-模式長(zhǎng)軸圖像。測(cè)量左心室收縮末期容積(LVESV)和舒張末期容積(LVEDV)。計(jì)算左心室射血分?jǐn)?shù)(LVEF)(LVEF=[LVEDV-LVESV]/LVEDV)。
1.2.4Masson染色 在造模28 d超聲心動(dòng)圖分析后取材,用體積分?jǐn)?shù)0.04多聚甲醛固定后包埋在石蠟中,并在縫合線下方500 mm距離處切片。通過(guò)Masson's Trichrome染色評(píng)估心臟組織的梗死面積。
1.2.5細(xì)胞培養(yǎng) 細(xì)胞培養(yǎng)所用培基為DMEM加入體積分?jǐn)?shù)0.1的胎牛血清,及體積分?jǐn)?shù)0.01的青鏈霉素混勻,4 ℃存放。細(xì)胞于體積分?jǐn)?shù)0.05的CO2、0.95空氣、37 ℃、飽和濕度的培養(yǎng)箱內(nèi)培養(yǎng)。細(xì)胞融合至0.8~0.9時(shí)進(jìn)行傳代。
1.2.6細(xì)胞活力檢測(cè) 正常培養(yǎng)細(xì)胞融合至0.8時(shí),以8×103個(gè)細(xì)胞每孔接種于96孔板中,分別為Control(0.1%DMSO)組;model組(10 μg·L-1TNF-α,5 mg·L-1CHX,0.1%DMSO);AU 10 μmol·L-1組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 10 μmol·L-1);AU 20 μmol·L-1組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1);AU 50 μmol·L-1組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 50 μmol·L-1),共5組,每組6個(gè)復(fù)孔。造模同時(shí)用AU處理心肌細(xì)胞6 h后進(jìn)行MTT檢測(cè)。MTT使用濃度為0.5 g·L-1,每孔加入20 μL并在37 ℃下孵育4 h。除去含MTT的培養(yǎng)基后,每孔加入200 μL DMSO,用酶標(biāo)儀檢測(cè)490 nm處各孔的OD值。
1.2.7IncuCyte活細(xì)胞成像系統(tǒng) H9c2細(xì)胞以含體積分?jǐn)?shù)0.1的FBS的DMEM完全培養(yǎng)基常規(guī)培養(yǎng),當(dāng)細(xì)胞生長(zhǎng)覆蓋到培養(yǎng)皿的0.9后用胰酶消化,細(xì)胞計(jì)數(shù)后,以8×103個(gè)細(xì)胞每孔接種于96孔板中。用顯微鏡觀察細(xì)胞情況后置于培養(yǎng)箱中培養(yǎng)。將實(shí)驗(yàn)分為6組,每組3個(gè)復(fù)孔,分別為分別為Control(0.1% DMSO)組;model組(10 μg·L-1TNF-α,5 mg·L-1CHX,0.1%DMSO);AU 20 μmol·L-1組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1);E2組(10 μg·L-1TNF-α,5 mg·L-1CHX,E2 10 nmol·L-1);AU+MPP組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1,MPP 100 nmol·L-1);AU+MPP組(10 μg·mL-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1,MPP 100 nmol·L-1);AU+(R,R)-THC組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1,(R,R)-THC 100 nmol·L-1)。細(xì)胞培養(yǎng)24 h后,細(xì)胞貼壁良好,鋪展生長(zhǎng),此時(shí)吸棄培養(yǎng)液,置換成體積分?jǐn)?shù)0.01的FBS的完全培養(yǎng)液進(jìn)行血清饑餓。血清饑餓24 h后,依據(jù)上述分組置換成含有TNF-α及CHX的的完全培養(yǎng)液中。造模6 h后,進(jìn)行TUNEL染色,置于Incucyte中拍照。
1.2.8Western blot 正常培養(yǎng)細(xì)胞融合至0.8時(shí),以2.4×105個(gè)細(xì)胞每孔接種于6孔板中,分別為Control(0.1% DMSO)組;model組(10 μg·L-1TNF-α,5 mg·L-1CHX,0.1%DMSO);AU 20 μmol·L-1組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1);E2組(10 μg·L-1TNF-α,5 mg·L-1CHX,E2 10 nmol·L-1),共4組,每組3個(gè)復(fù)孔。培養(yǎng)24 h待細(xì)胞貼壁生長(zhǎng)良好后,按分組加入培基,造模給藥6 h后提取總蛋白。用BCA法進(jìn)行蛋白濃度測(cè)定,取等量蛋白進(jìn)行SDS-PAGE,半干法轉(zhuǎn)膜,與相應(yīng)一抗二抗結(jié)合反應(yīng)后,用化學(xué)發(fā)光法檢測(cè)抗原抗體結(jié)合區(qū)帶。用凝膠成像分析儀進(jìn)行電泳條帶的拍照與分析。實(shí)驗(yàn)中以β-actin為內(nèi)參,分別檢測(cè)了caspase-3、Bax、Bcl2、p-Akt、Akt。
1.2.9TUNEL染色 正常培養(yǎng)細(xì)胞融合至0.8時(shí),以8×103個(gè)細(xì)胞每孔接種于96孔板中,將實(shí)驗(yàn)分為6組,每組3個(gè)復(fù)孔,分別為分別為Control(0.1% DMSO)組;model組(10 μg·L-1TNF-α,5 mg·L-1CHX,0.1%DMSO);AU 20 μmol·L-1組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1);E2組(10 μg·L-1TNF-α,5 mg·L-1CHX,E2 10 nmol·L-1);AU+MPP組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1,MPP 100 nmol·L-1);AU+MPP組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1,MPP 100 nmol·L-1);AU+(R,R)-THC組(10 μg·L-1TNF-α,5 mg·L-1CHX,AU 20 μmol·L-1,(R,R)-THC 100 nmol·L-1)。細(xì)胞培養(yǎng)24 h后,細(xì)胞貼壁良好,鋪展生長(zhǎng),此時(shí)吸棄培養(yǎng)液,24 h后置換成含有TNF-α(10 μg·L-1)、CHX(5 mg·L-1)的完全培養(yǎng)液6 h后使用In Situ Cell Death Detection Kit試劑盒進(jìn)行染色,DAPI復(fù)染細(xì)胞核。
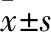
2 結(jié)果
2.1 AU能夠改善心肌梗死小鼠的心功能超聲心動(dòng)檢測(cè)術(shù)前1 d,術(shù)后給藥7 d、14 d和28 d左心室短軸縮短率和射血分?jǐn)?shù)。結(jié)果顯示,心肌梗死前組間的短軸縮短率和射血分?jǐn)?shù)無(wú)顯著差異,兩者均具有正常的心肌功能。心肌梗死后,心肌梗死的C57BL/6小鼠隨機(jī)分組,在d 7、14和28進(jìn)行相關(guān)指標(biāo)的檢測(cè)。結(jié)果顯示,模型組、AU組及陽(yáng)性藥組相較于假手術(shù)組的EF%和FS%明顯降低。給藥后7 d,AU及陽(yáng)性藥組與模型組之間沒(méi)有顯著差異。但給藥后d 14、28,AU組給藥效果良好,明顯優(yōu)于模型組(Fig 1A, B)。連續(xù)給藥28 d后,對(duì)來(lái)自小鼠的心臟組織進(jìn)行Masson染色。結(jié)果顯示正常心室結(jié)構(gòu)完整,心肌纖維化不明顯,梗死部位無(wú)藍(lán)色,無(wú)心室壁變薄。在模型組中,心室壁嚴(yán)重梗塞,纖維化,變薄和心室腔擴(kuò)大,纖維化程度占整個(gè)心室壁的約40%~50%。非梗塞區(qū)域有松散的組織細(xì)胞和增加的空隙。給藥組與模型組相比,給藥組的心室壁纖維化及心室腔的變化得到改善(Fig 1C, D)。
2.2 AU能夠減少急性心肌梗死小鼠心肌細(xì)胞凋亡連續(xù)給藥28 d后,對(duì)來(lái)自小鼠的心臟組織進(jìn)行TUNEL染色。心肌細(xì)胞的凋亡可以通過(guò)TUNEL+/DAPI雙色熒光重合信號(hào)確認(rèn),TUNEL+ cell為紅色,DAPI為藍(lán)色。結(jié)果顯示AU給藥組與生理鹽水組相比,TUNEL+(red)信號(hào)明顯減少(Fig 2)。
2.3 AU提高TNF-α/CHX損傷模型中的心肌細(xì)胞活力課題組前期結(jié)果表明,TNF-α/CHX能夠成功誘導(dǎo)心肌細(xì)胞損傷,為了確定藥物濃度,本研究采用MTT法檢測(cè)不同濃度下AU對(duì)模型中細(xì)胞活力的影響,結(jié)果顯示AU在20 μmol·L-1及50 μmol·L-1時(shí),能夠明顯在TNF-α/CHX損傷模型中增加細(xì)胞活力,差異具有統(tǒng)計(jì)學(xué)意義(Fig 3)。預(yù)處理24 h能夠增強(qiáng)其保護(hù)作用。
2.4 AU能夠減少TNF-α/CHX損傷模型中的細(xì)胞凋亡為了進(jìn)一步證明AU的抗凋亡作用,本研究采用Western blot法檢測(cè)TNF-α/CHX損傷模型中6 h時(shí)caspase-3、Bcl2、Bax、Akt以及p-Akt蛋白的表達(dá),結(jié)果顯示造模6 h時(shí),模型組與對(duì)照組相比,caspase-3蛋白表達(dá)增加,差異具有統(tǒng)計(jì)學(xué)意義;AU組與模型組相比,caspase-3蛋白表達(dá)減少,Bcl2/Bax比例上調(diào),其結(jié)果差異具有統(tǒng)計(jì)學(xué)意義(Fig 4)。
2.5 AU能夠促進(jìn)ERα以及ERβ的表達(dá)確定AU的抗凋亡作用后,本研究進(jìn)一步對(duì)AU如何影響凋亡做了進(jìn)一步的探討,采用Western blot方法檢測(cè)AU對(duì)心肌細(xì)胞中ERα以及ERβ的表達(dá)的影響,結(jié)果顯示AU能夠明顯促進(jìn)心肌細(xì)胞中ERα以及ERβ的表達(dá),差異具有統(tǒng)計(jì)學(xué)意義(Fig 5)。

Fig 1 AU improves cardiac function and reduces infarct size after MI

Fig 2 AU inhibits apoptosis of myocardial cells after MI
2.6 ERβ抑制劑能夠減弱AU的抗凋亡作用為了探討AU是否通過(guò)激活雌激素受體抑制細(xì)胞凋亡,本研究采用TUNEL法檢測(cè)ERα的抑制劑MPP和ERβ的抑制劑(R,R)-THC對(duì)給藥后TNF-α/CHX損傷模型中凋亡的影響。結(jié)果顯示, MPP對(duì)AU的心肌細(xì)胞保護(hù)作用無(wú)明顯影響;而加入(R,R)-THC后,細(xì)胞凋亡數(shù)量較AU組有明顯上升,其結(jié)果差異具有統(tǒng)計(jì)學(xué)意義(Fig 6)。本研究證明,AU能夠激活ERβ發(fā)揮心肌保護(hù)作用。

Fig 3 AU improves myocardial cell viability against TNF-α/CHX treatment

Fig 4 AU inhibits apoptosis induced by TNF-α/CHX

Fig 5 AU promotes ERα and ERβ expression
3 討論
AU是杜仲等中藥的活性成分之一,本研究發(fā)現(xiàn)AU可使ERβ表達(dá)升高,抑制心肌細(xì)胞凋亡,并且加入ERβ抑制劑可阻斷AU的抗凋亡作用。表明AU可以通過(guò)激活ERβ通路,發(fā)揮抗心肌缺血損傷從而改善急性心肌梗死后心功能的作用。
植物雌激素是對(duì)具有雌激素相似結(jié)構(gòu),能夠作用于雌激素受體的一類(lèi)化合物的統(tǒng)稱(chēng)。課題組前期研究證實(shí)AU是一種具有植物雌激素樣作用的小分子,能夠激活雌激素受體[12]。雌激素受體ER于發(fā)現(xiàn)于1958年,其中ERβ分布于卵巢、中樞神經(jīng)系統(tǒng)、心血管系統(tǒng)、肺、結(jié)腸、腎臟和免疫系統(tǒng)中[13]。心血管系統(tǒng)功能異常是臨床絕經(jīng)期綜合征表現(xiàn)的重要方面之一,Zhang等[9]研究發(fā)現(xiàn),Tg-ERβ轉(zhuǎn)基因小鼠的心肌組織Ⅰ型膠原、α-SMA、TGF-β mRNA的表達(dá)水平明顯低于野生型小鼠,說(shuō)明ERβ有助于抑制心肌梗死后心肌纖維化和重塑過(guò)程,提高心肌抗纖維化能力。同時(shí),Wang也研究發(fā)現(xiàn)將ERβ敲除后,PI3K和Akt磷酸化水平下調(diào),caspase-3和caspase-8的表達(dá)增加,Bcl-2蛋白表達(dá)水平降低,證明ERβ可能是通過(guò)調(diào)節(jié)PI3K/Akt信號(hào)通路改善急性心肌梗死患者的心功能[8]。
本研究采用TNF-α和CHX共同誘導(dǎo)心肌細(xì)胞損傷模型,探討了AU抗心肌細(xì)胞損傷作用及其與ER信號(hào)通路的相關(guān)性。TNF-α能夠與膜受體TNFR I或TNFR II結(jié)合,激活凋亡通路,同時(shí)刺激TNF抗凋亡因子(TNF apoptosis protection fraction,TAPF)的生成,而CHX能夠抑制TAPF阻斷TNF-α激活的保護(hù)途徑[14]。有研究表明TNF-α/CHX模型誘導(dǎo)凋亡的主要因素是由于ROS上調(diào)誘發(fā)細(xì)胞內(nèi)氧化應(yīng)激和凋亡[15],課題組成功構(gòu)建了TNF-α/CHX心肌細(xì)胞損傷模型,并發(fā)現(xiàn)了AU的抗心肌損傷作用,為了進(jìn)一步探討其抗凋亡作用是否與雌激素受體相關(guān),本研究選用MPP作為ERα的拮抗劑,(R,R)-THC作為ERβ的拮抗劑[16],表明AU是通過(guò)干預(yù)ERβ途徑發(fā)揮抗凋亡作用。

Fig 6 ERβ inhibitor reduces antiapoptotic effect of AU
綜上所述,AU可以通過(guò)抑制心肌細(xì)胞凋亡發(fā)揮抗心肌缺血損傷從而改善急性心肌梗死后心功能的作用,其部分作用機(jī)制與激活ERβ信號(hào)通路有關(guān)。本研究為AU應(yīng)用于急性心肌梗死的治療提供了實(shí)驗(yàn)依據(jù)。
(致謝 本實(shí)驗(yàn)完成于天津中醫(yī)藥大學(xué)中西醫(yī)結(jié)合學(xué)院、方劑學(xué)教育部重點(diǎn)實(shí)驗(yàn)室、天津市中藥藥理學(xué)重點(diǎn)實(shí)驗(yàn)室、天津中醫(yī)藥大學(xué)中醫(yī)藥研究院,感謝給予的幫助!)