高考中化學反應機理的考查研究
◇ 山東 孫振法
描述一個化學反應有多種形式,化學方程式和離子方程式是兩種常見形式,常用來表示化學反應中的明顯變化.除此之外,涵蓋所有基元反應的反應機理也可用來表示化學反應.高中階段學生對反應機理的學習并不深入,是學生繼續(xù)深造時才會系統(tǒng)學習的化學知識.但在2020年高考試題中卻出現(xiàn)了有關(guān)化學反應機理的考查,這既是新高考制度實施的體現(xiàn),也是對學生核心素養(yǎng)培養(yǎng)成果的考查.
1 反應機理概述
反應機理描述的是詳細的化學反應過程,在一個完整的反應機理圖示中,通常以箭頭為主要表現(xiàn)方式,電子的流向、反應物參加反應的時機、生成物產(chǎn)生的過程都有詳細的表示,箭尾的一方表示將要參加下一歷程的反應物,箭頭的一方表示上一歷程的產(chǎn)物和下一歷程的反應物,首尾相連,形成一個完整的循環(huán).由于化學反應中催化劑在反應前后能保持化學性質(zhì)不變,因此處于循環(huán)主線上的常是化學反應的催化劑.
反應機理并不是化學專家根據(jù)化學反應推理出來的,而是由很多實驗事實總結(jié)得出的.反應機理的提出既可解釋化學實驗現(xiàn)象,又可預測即將發(fā)生的化學反應,在實際生產(chǎn)中有著廣泛的應用.
2 反應機理考查方式
2020年因新冠病毒的肆虐,高考在時間上延遲了一個月,形式上也進行了新的嘗試,如某些地區(qū)在本校進行、由本校老師監(jiān)考等,此外在高考試題上也有大膽的創(chuàng)新.就高考化學試題而言,反應機理的出現(xiàn)是近年來的新題型,對學生的能力是一大考驗,同時也是對新課程改革和核心素養(yǎng)教育理念所取得成果的考查.
例(2020年全國卷Ⅰ)銠的配合物離子[Rh(CO)2I2]-可催化甲醇羰基化,反應過程如圖1所示.下列敘述錯誤的是( ).
A.CH3COI是反應中間體
B.甲醇羰基化反應為
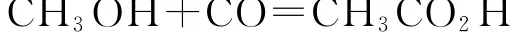
C.反應過程中Rh的成鍵數(shù)目保持不變
D.存在反應CH3OH+HI=CH3I+H2O
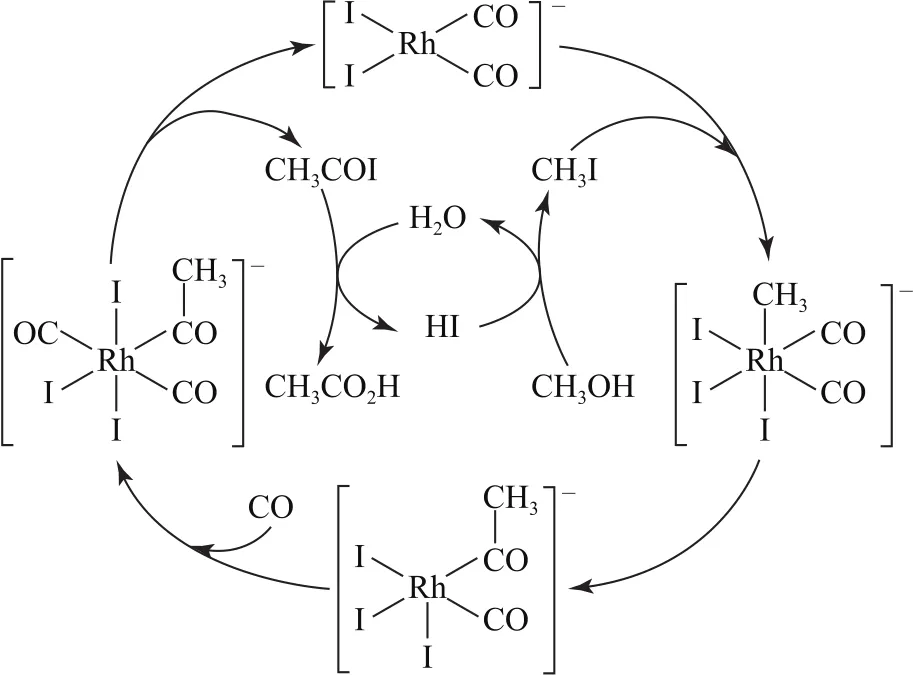
圖1
分析學生在初看這道題時,很可能會被看似復雜的反應機理圖所“嚇”到,心理上產(chǎn)生畏懼,也就很難靜下心來解讀題意.在遇到該類試題時學生首先要保持良好的心態(tài),可以這么想:高考中考查的知識肯定是學過的,不會“超綱”,即使出現(xiàn)偏差,也一定不會只有我一個人不會,如果我做對了就比其他人的分數(shù)高了.然后認真審讀試題.解答本題的關(guān)鍵是了解反應機理圖示的本質(zhì):在反應機理圖示中,反應物是隨著箭頭加入的物質(zhì),產(chǎn)物是隨著箭頭產(chǎn)生的物質(zhì),處于循環(huán)系統(tǒng)中的物質(zhì)都是反應的中間產(chǎn)物.由題意知銠的配合物離子[Rh(CO)2I2]-是催化劑,此反應機理表示的是甲醇羰基化反應.依據(jù)反應機理圖示本質(zhì)分析,CH3COI既不隨著箭頭進入反應體系,也不隨箭頭脫離反應體系,則屬于反應中間體,選項A說法正確.由整個反應機理圖示可看出,隨著箭頭進入體系的物質(zhì)是CH3OH和CO,隨著箭頭脫離體系的物質(zhì)是CH3CO2H,因此,甲醇羰基化反應為CH3OH+CO=CH3CO2H,選項B說法正確.由反應機理圖示可知,Rh的成鍵數(shù)目分別為4、5、6,選項C說法錯誤.由圖示可知,在CH3OH剛進入反應體系時發(fā)生的反應是CH3OH+HI=CH3I+H2O,選項D說法正確.答案為C.
由此可知,解答反應機理類試題難度并不大,關(guān)鍵是要找出化學反應中的反應物、生成物和催化劑.雖然此類試題只在2020年的高考試題中出現(xiàn),但隨著新高考制度的逐步實施,此類試題或新的考查方式還會出現(xiàn),且難度會有所增加.因此,在新一輪的復習中,教師有必要對高中化學知識進行適當延伸,以拓寬學生視野.

