我院2011年4月至2021年4月β-內酰胺酶抑制劑復方制劑不良反應分析報告
朱朝艷 魯廣先 丁信園 沈欣 過曉蕾


[摘要] 目的 分析我院β-內酰胺酶抑制劑復方制劑所致藥品不良反應(ADR)發生的特點及其規律,提醒臨床用藥注意,促進臨床合理用藥。 方法 從國家藥品不良反應監測系統中收集我院2011年4月至2021年4月使用β-內酰胺酶抑制劑復方制劑的不良反應報告,利用Excel 2010對200例不良反應進行數據匯總,對其年齡、性別、用藥原因及使用情況、發生不良反應的藥物及數量、不良反應發生的臨床表現、不良反應發生的嚴重程度等進行統計分析。 結果 200例不良反應報告中,女性發生比例高于男性;0~13歲的患者發生不良反應最為常見,構成比高達50.00%;不良反應發生率最高的是注射用阿莫西林鈉舒巴坦鈉,發生67例,構成比高達33.50%,占比前3的第二位和第三位分別為注射用美洛西林鈉舒巴坦鈉(28.00%)及注射用哌拉西林舒巴坦鈉(25.00%);給藥方式均為靜脈滴注;臨床表現以皮膚及其附件損害最為常見。 結論 β-內酰胺酶抑制劑復方制劑所致的不良反應與多種因素有關,醫護人員在臨床用藥過程中應加強不良反應監測并及時處理、減少或避免不良反應的發生,保障患者用藥安全。
[關鍵詞] β-內酰胺酶抑制劑;不良反應;復方制劑;合理用藥
[中圖分類號] R969.3? ? ? ? ? [文獻標識碼] B? ? ? ? ? [文章編號] 1673-9701(2021)35-0117-04
Adverse reaction analysis report of β-lactamase inhibitor compound preparation in our hospital from April 2011 to April 2021
ZHU Chaoyan? ?LU Guangxian? ?DING Xinyuan? ?SHEN Xin? ?GUO Xiaolei
Department of Pharmacy, Suzhou Hospital Affiliated to Nanjing Medical University, Suzhou? ?215001, China
[Abstract] Objective To analyze the characteristics and regularity of ADR caused by β-lactamase inhibitor compound preparation in our hospital, to remind clinical medication attention, and to promote clinical rational drug use. Methods The adverse reaction reports of β-lactamase inhibitor compound preparation in our hospital from April 2011 to April 2021 were collected from the national adverse drug reaction monitoring system. Excel 2010 was used to summarize the data of 200 patients of adverse reactions, and statistical analysis was made on their age, gender, medication reasons and usage, drugs and quantity of adverse reactions, clinical manifestations of adverse reactions, and severity of adverse reactions. Results Among 200 patients of adverse reactions reported, the proportion of female was higher than that of male. Adverse reactions were most common in patients aged 0-13 years, with a constituent ratio of up to 50.00%.The highest incidence of adverse reactions was amoxicillin sodium and sulbactam sodium for injection, with 67 cases, accounting for 33.50%. The second and third place in the top 3 were mezlocillin sodium and sulbactam sodium for injection (28.00%) and piperacillin and sulbactam sodium for injection (25.00%), respectively.The methods of administration were all intravenous drip.The most common clinical manifestations were skin and accessory lesions. Conclusion The adverse reactions caused by β -lactamase inhibitor compound preparations are related to a variety of factors, so medical staff should strengthen the monitoring of adverse reactions and timely deal with, reduce or avoid the occurrence of adverse reactions in clinical medication to ensure the drug safety of patients.
[Key words] β-lactamase inhibitor; Adverse reaction; Compound preparation; Rational use of drugs
β-內酰胺酶抑制劑復方制劑因抗菌范圍廣、毒性低等優點被臨床廣泛使用,也成為臨床治療耐β-內酰胺類抗生素細菌所致感染性疾病的重要措施之一。然而一部分患者使用該類藥物會發生不良反應(Adverse reaction,ADR)癥狀[1],ADR一般與藥物的劑型、給藥方法、藥品質量、個體差異等相關,為研究β-內酰胺酶抑制劑復方制劑不良反應產生的規律特點,減少該類藥物的ADR發生率,保證患者的用藥安全。本研究對我院2011年4月至2021年4月使用的6種β-內酰胺酶抑制劑復方制劑發生不良反應的病例進行分析總結,為臨床合理使用β-內酰胺酶抑制劑復方制劑提供參考,現報道如下。
1 資料與方法
1.1 一般資料
本研究抽取我院2011年4月至2021年4月在全國不良反應監測系統中上報的關于β-內酰胺酶抑制劑復方制劑的不良反應報告共計200例,按照不良反應因果關系評價方法[2]逐一檢索,將判斷為“肯定”“很可能”及“可能”的病例作為研究對象;排除病歷內容記錄不全,不良反應相關內容缺失的病例。本研究符合我院醫學倫理委員會規定。
1.2 方法
利用Excel 2010對200例ADR報告的信息進行數據匯總,對其年齡、性別、用藥原因及使用情況、發生ADR的藥物以及數量、不良反應發生的臨床表現、不良反應發生的嚴重程度等進行統計分析。
2 結果
2.1 一般資料分析
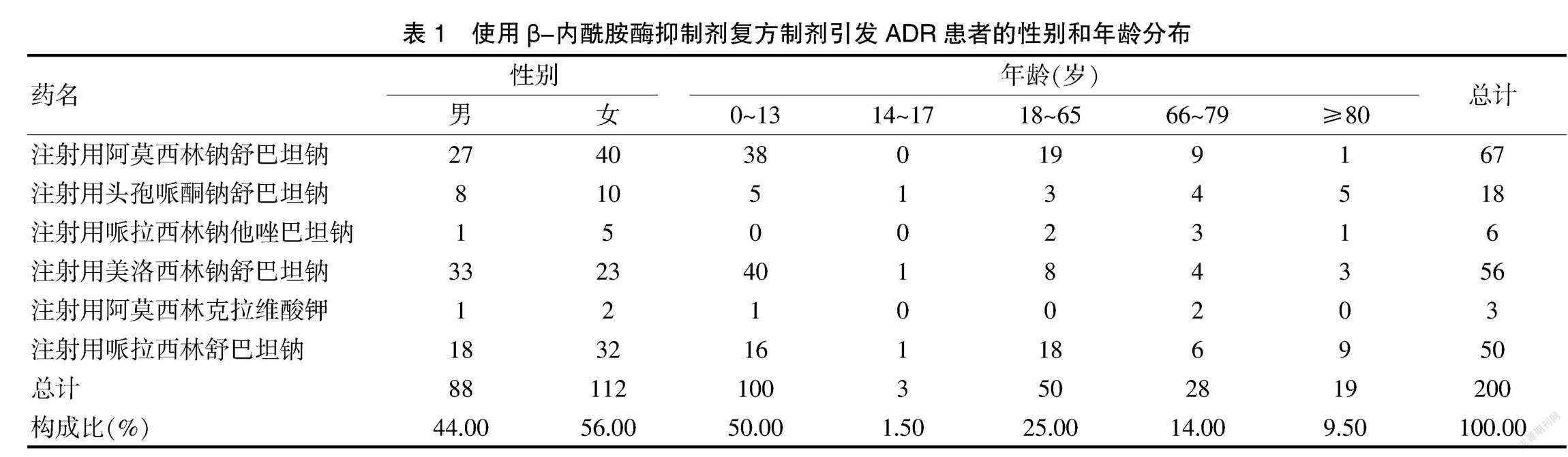
因使用β-內酰胺酶抑制劑復方制劑而導致不良反應的患者累計200例,其中男88例,女112例,女性病例略多于男性病例,男女比例為1∶1.27,年齡1~93歲,平均(33.3±31.5)歲,其中0~13歲的ADR發生率最高,有100例,構成比為50.00%,14~17歲處于青春期,該類藥物的ADR發生率最小,僅有1.50%,≥80歲、66~79歲、18~65歲該類藥物的ADR發生率依次為9.50%、14.00%和25.00%。性別、年齡具體情況見表1。
2.2 引起藥物不良反應的藥品統計
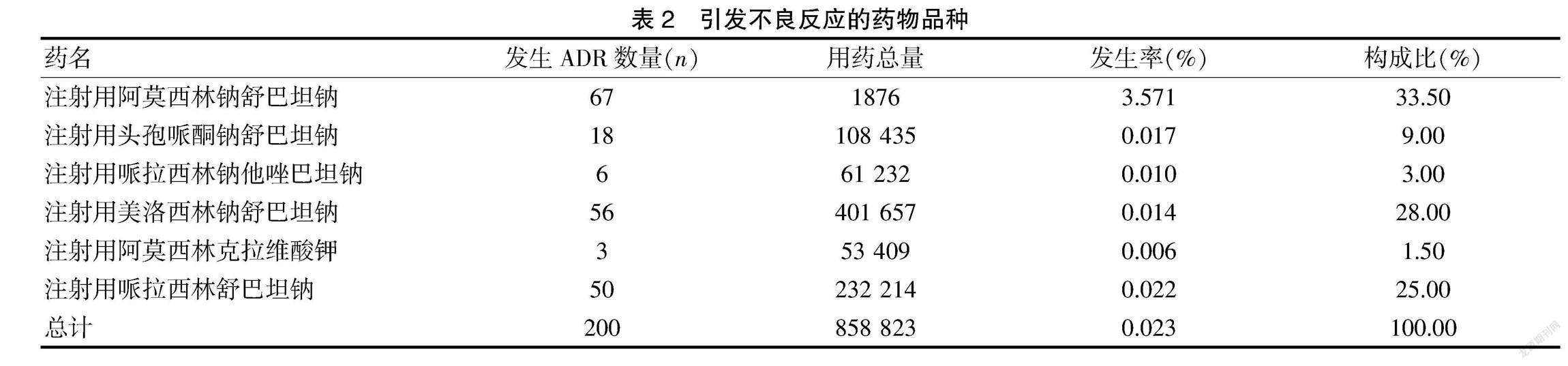
在本院抽取的200個病例中,我院使用了6種β-內酰胺酶抑制劑復方制劑,均是靜脈滴注,分別為①注射用阿莫西林鈉舒巴坦鈉;②注射用阿莫西林克拉維酸鉀;③注射用美洛西林鈉舒巴坦鈉;④注射用頭孢哌酮鈉舒巴坦鈉;⑤注射用哌拉西林鈉他唑巴坦鈉;⑥注射用哌拉西林舒巴坦鈉。在200例ADR報告中,ADR發生率最高的是注射用阿莫西林鈉舒巴坦鈉,發生了67例,構成比高達33.50%,占比前3的第二位和第三位分別為注射用美洛西林鈉舒巴坦鈉和注射用哌拉西林舒巴坦鈉。從用藥的總量來看,注射用阿莫西林鈉舒巴坦鈉的ADR發生率高達3.571%,仍然處于6個藥品中的ADR發生率第一位。而注射用阿莫西林克拉維酸鉀和注射用哌拉西林鈉他唑巴坦鈉的ADR報告發生率較低,分別為1.50%和3.00%,兩個藥品用藥總量的ADR發生率也較低。發生ADR的β-內酰胺酶抑制劑復方制劑具體情況見表2。
2.3 用藥原因及使用情況
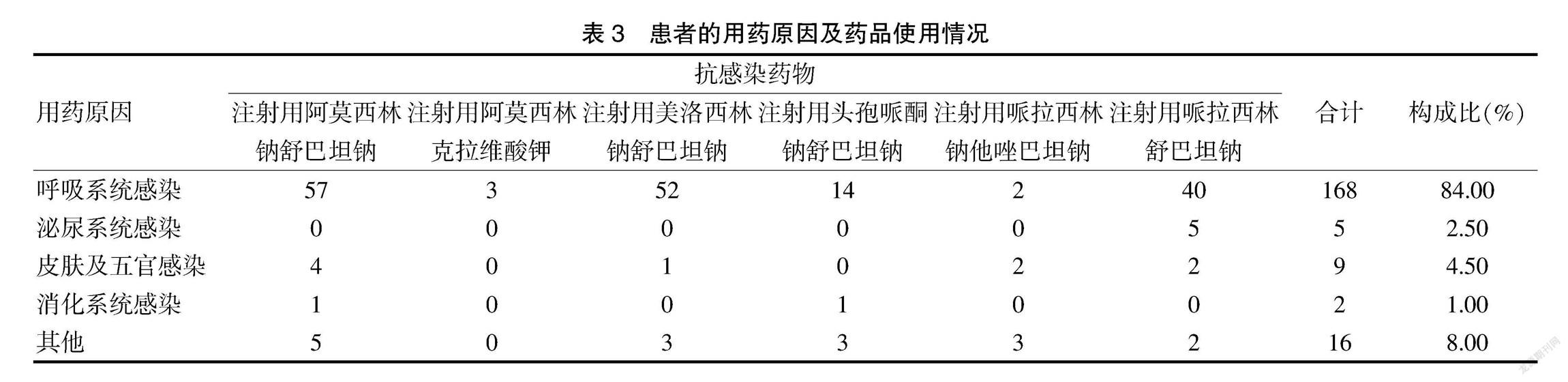
將收集的200例ADR報告中的病例分為以下幾個系統:①呼吸系統感染;②泌尿系統感染;③消化系統感染;④皮膚及五官系統感染;⑤其他疾病,其中因呼吸系統感染而使用β-內酰胺酶抑制劑復方制劑的患者最多,合計168例,構成比高達84.00%,在這168例中,應用注射用阿莫西林鈉舒巴坦鈉治療呼吸系統感染的患者最多,為57例,其次為使用注射用美洛西林鈉舒巴坦鈉和注射用哌拉西林舒巴坦鈉的患者,分別為52例和40例。因泌尿系統感染、消化系統感染和皮膚及五官系統感染而使用β-內酰胺酶抑制劑復方制劑的例數較少,其構成比分別為2.50%、1.00%和4.50%;⑥其他疾病共收集16例,包括后腹膜囊腫、抗感染、腫瘤相關性疾病、金黃色葡萄球菌感染等,除注射用阿莫西林克拉維酸鉀沒有使用,其他藥品均有3次使用。藥物用藥原因及使用情況見表3。
2.4 ADR累及的器官及主要臨床表現
在收集的200例本院β-內酰胺酶抑制劑復方制劑ADR報告中,共統計出216例ADR累及系統-器官(由于某些患者出現兩種或兩種以上的ADR反應,累及的系統也不止一個)根據統計數據,將累及的系統-器官分為:①皮膚性疾病;②消化系統反應;③全身性反應;④呼吸系統反應;⑤心血管系統;⑥泌尿系統;⑦神經系統;⑧血液系統,其中出現ADR臨床表現最多的是皮膚性疾病,共計144例,占比66.67%,具體表現為皮疹、蕁麻疹、皮膚瘙癢等。全身性反應出現28例,占比12.96%,患者主要的臨床ADR表現為過敏性反應、發熱、藥物熱等,消化系統反應出現26例,占比12.04%,患者的主要臨床ADR表現為惡心嘔吐、腹痛、腹瀉等。而呼吸系統、泌尿系統、心血管系統、神經系統、血液系統出現的臨床ADR例數較少,患者臨床ADR表現分別為胸悶、干咳、呼吸困難,排尿困難、急性腎衰竭、心悸心慌、頭暈乏力煩躁不安,血小板減少。見表4。
2.5 不良反應嚴重的程度
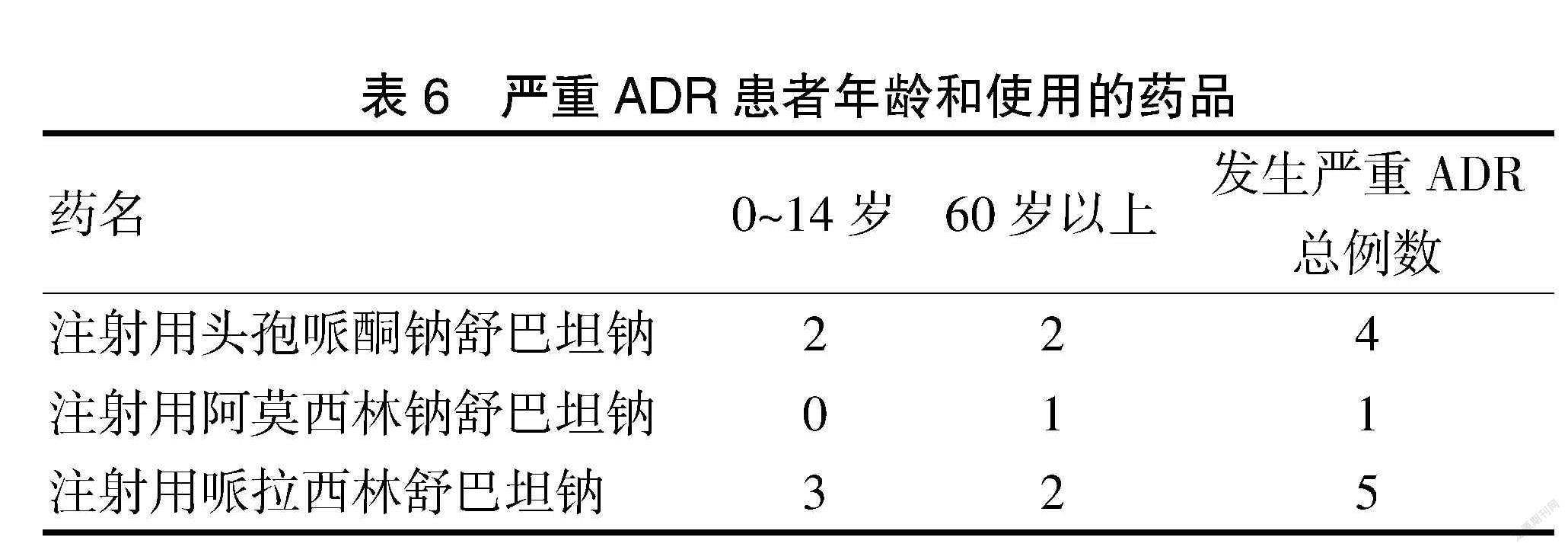
根據統計的200例ADR報告,10例患者注射β-內酰胺酶抑制劑復方制劑后出現嚴重的不良反應,190例患者出現的ADR嚴重程度為一般。10例出現嚴重ADR反應的患者中,有4例是使用注射用頭孢哌酮鈉舒巴坦鈉,1例使用注射用阿莫西林鈉舒巴坦鈉,5例使用注射用哌拉西林舒巴坦鈉。患者的年齡也趨于兩極分化,只出現在0~14歲的兒童和60歲以上的老年人,各5例,出現ADR的嚴重程度和年齡分布具體情況見表5~6。
表5? ?出現ADR的嚴重程度
表6? ?嚴重ADR患者年齡和使用的藥品
3 討論
3.1 性別與年齡
從本次統計的200例ADR報告來看,男性患者發生ADR的人數少于女性,男女比例為1∶1.27,此結果與國內的部分報告一致[3-4],原因可能來自很多方面,如雌激素不但會使女性身體中的脂肪比男性身體中的脂肪多,而且還會影響脂肪在身體內的分布情況,使進入體內的藥物與蛋白結合產生差異,而且女性因為體內缺乏某些肝藥酶,所以會使某些藥物在體內清除速度明顯慢于男性患者,還可能與女性的特殊生理周期有關,這需要進一步的討論。ADR報告的年齡分布也較為廣泛,其中0~13歲的患兒構成比最高,達50.00%,這說明兒童使用β-內酰胺酶抑制劑出現ADR較多,與此年齡段使用抗感染藥物的機會多有關,患者的年齡較小,其中樞神經系統、肝膽系統、內分泌系統、免疫系統、腎臟等都未發育完全,對藥物還未形成對應的耐受性,另外一般三期臨床試驗都沒有兒童實驗階段,兒童的專用藥物嚴重短缺,導致“成人藥兒童用”成為普遍現象。大量的兒童患兒使用未標注兒童用法用量、未進行過系統性兒科臨床研究的成人藥,這無疑會增加患兒用藥產生不良反應的風險,一旦患兒出現不良反應往往伴隨一系列的并發癥,不僅會影響治療效果,而且患兒還會出現發育不良的問題,因此兒科醫生需要根據患兒的病情合理給藥[5-6],并且在出現ADR時要采取相應的處理措施。60歲以上的老年人發生ADR例數61例,占200例中的30.00%,老年人藥物ADR發生率較高與多種因素有關,如老年人基礎疾病較多、生物轉化減慢、免疫機制變差等[7]。兒童和老年人均是ADR高發人群[8],因此臨床醫生在使用β-內酰胺酶抑制劑復方制劑時應提防此類藥物可能引起的不良反應,細致觀察患兒用藥過程,如果出現異常,應立即停藥并給予及時處理,以免造成嚴重不良反應發生。
3.2 用藥原因
在200例ADR報告中,168例是在治療呼吸系統感染性疾病時發生,占84.00%,可能由于本院臨床醫生普遍使用β-內酰胺酶抑制劑復方制劑來治療呼吸道感染疾病,所以該病所占比例最高[9]。
3.3 發生ADR的藥物品種
在引發ADR的6個β-內酰胺酶抑制劑復方制劑中,注射用阿莫西林鈉舒巴坦鈉的ADR發生率最高,其次為注射用美洛西林鈉舒巴坦鈉和注射用哌拉西林舒巴坦鈉。檢索有關注射用阿莫西林鈉舒巴坦鈉所致不良反應的文獻較少,主要有皮疹、腹瀉、蕁麻疹等一般嚴重程度的ADR,但統計數據中該藥的ADR報告與用藥總量的比值最高,提醒臨床改選其他藥物,或者此類藥物在使用前應該仔細詢問患者的用藥史和過敏史,建議用相應的原藥液做皮試,并配以抗組胺藥物治療過敏[10-11]。注射用美洛西林鈉舒巴坦鈉發生的ADR的病理報告高居第二,根據病例逐一檢索,詢問部分住院患者,以及檢索的文獻,接近半數的患者存在聯合使用藥物的情況,可能會引起臟器損傷,如果多種藥品混合靜脈滴注則可能產生白色渾濁物,另外與過敏體質、原患者疾病、給藥濃度過高、滴速過快等因素有關[12-13]。注射用哌拉西林舒巴坦鈉發生ADR的數量與用藥總量的比值位列6個藥品首位,達0.022%,哌拉西林鈉和舒巴坦鈉在強酸或強堿條件下均不穩定,易發生變態反應。β-內酰胺類抗菌藥物引發的速發型變態反應與藥物中存在的高分子雜質有密切聯系,其含量的高低與臨床不良反應發生率相關性很高[14-15]。注射用哌拉西林鈉他唑巴坦鈉和注射用阿莫西林克拉維酸鉀發生的ADR數量則較少,與患者自身體質相關性較高,無明顯規律特點。注射用頭孢哌酮鈉舒巴坦鈉發生的ADR為18例,需要特別注意的是使用頭孢哌酮鈉舒巴坦鈉后飲酒或食用含有乙醇的物質后會發生雙硫侖樣反應[16-17],用該藥前應詢問患者12 h內是否飲酒或服用含有乙醇成分的藥物。
3.4 ADR主要臨床表現
主要以皮膚感染性疾病為主,表現為皮疹、蕁麻疹及皮膚瘙癢等,過敏性休克作為最嚴重的藥物不良反應屬于Ⅰ型變態反應[18],其發生機制是變應原通過各種途徑進入機體刺激β細胞產生IgE類抗體,IgE以Fc段與肥大細胞和嗜堿性粒細胞上的IgE的Fc段受體結合,使機體處于致敏狀態。當相應變應原再次進入機體直接與肥大細胞或嗜堿性粒細胞上的IgE結合,致細胞脫顆粒,釋放生物活性介質作用于效應器官,引起平滑肌痙攣。建議此類藥物按原藥300~500 mg/mL進行皮膚過敏試驗。注意首次靜脈滴注β內酰胺酶抑制劑復方制劑時應控制滴速,密切關注患者用藥過程中有無異常反應,如果出現不良反應及時處理[16-17]。
綜上所述,β-內酰胺酶抑制劑復方制劑在臨床上應用廣泛,療效顯著,但其不良反應屢見不鮮,臨床醫護人員在應用此類藥物時應特別注意兒童、老年人、孕婦等特殊人群,做好皮試工作,密切關注患者用藥情況,發現ADR及時處理,最大程度的保障患者的生命安全。
[參考文獻]
[1] 楊澍,崔艷麗,高秀清,等.β-內酰胺酶抑制劑復合制劑的不良反應文獻分析[J].現代藥物與臨床,2016,31(1):107.
[2] Yang H,Wei J,Wang JY,et al. Study on methods of adverse drug reaction/event reporting assessment[J]. Chinese Journal of Pharmacovigilance,2009,6(10):581-584.
[3] 王維忠,馬瑩,禇文靜.306例β-內酰胺類抗菌藥物不良反應報告分析[J].實用藥物與臨床,2012,15(5):290-293.
[4] 白姜花.住院患者靜脈抗菌藥物使用情況及不良反應分析[J].齊齊哈爾醫學院學報,2019,40(18):2292-2293.
[5] 劉春紅.兒童抗生素用藥不良反應發生及防治的調查研究[J].醫藥前沿,2017,7(18):373-374.
[6] 鐘鳳宜.50例兒童β-內酰胺類抗生素不良反應分析[J].中國民族民間醫藥,2010,19(18):106.
[7] 黎海姣,朱遂明.抗菌藥物引起128例老年人不良反應的回顧性分析[J].貴陽中醫學院學報,2013,35(1):89.
[8] 廖元園.老年人藥物不良反應報告分析[J].醫藥前沿,2020,10(17):233-235.
[9] 楊澍,崔艷麗,高秀清,等.β-內酰胺酶抑制劑復合制劑的不良反應文獻分析[J].現代藥物與臨床,2016,31(1):106-110.
[10] 黃猛.抗菌藥物不良反應分析與合理應用探討[J].中國衛生標準管理,2020,11(16):94-96.
[11] 李忠忠,劉亞非.注射用阿莫西林-舒巴坦鈉致過敏性休克1例[J].中國現代應用藥學,2006,23(3):192.
[12] 李鳳榮,梁紅英,尹德芬,等.278例注射用美洛西林鈉舒巴坦鈉藥物不良反應分析[J].藥學研究,2017,36(7):429-431.
[13] 王靜.注射用美洛西林鈉舒巴坦鈉在臨床中引發的不良反應1例[J].醫學理論與實踐,2011,24(2):182.
[14] 劉彥儒,金諾楠,龔婧如.哌拉西林鈉/舒巴坦鈉致藥物熱及白細胞減少1例[J].醫藥導報,2018,37(9):1145-1146.
[15] 馬超,于凝,張樹榮.注射用哌拉西林鈉/舒巴坦鈉致過敏性休克1例[J].醫藥導報,2013,32(12):1668.
[16] 徐琦.探討注射用頭孢哌酮鈉舒巴坦鈉的不良反應[J].中國現代藥物應用,2017,11(20):102-103.
[17] 喻鋒,王麗,陳麗明,等.注射用頭孢哌酮鈉舒巴坦鈉的不良反應分析[J].中國繼續醫學教育,2020,12(12):119-121.
[18] 趙曙剛,汪林嬌.基于藥品說明書對β-內酰胺類抗生素皮膚過敏試驗臨床意義的探討和建議[J].中國醫藥科學,2020,10(5):27-31.
(收稿日期:2021-08-24)

