中度嗜鹽菌S61生防因子分析及其對(duì)馬鈴薯干腐病的防效


摘要:【目的】測(cè)定中度嗜鹽菌S61對(duì)馬鈴薯干腐病病原菌的抑菌活性及對(duì)干腐病的防效,為馬鈴薯干腐病的生物防治及綠色防控提供科學(xué)依據(jù)。【方法】以來源于青海察爾汗鹽湖的1株中度嗜鹽菌S61為材料,采用形態(tài)學(xué)、生理生化特征及分子生物學(xué)方法對(duì)菌株S61進(jìn)行鑒定。通過對(duì)峙培養(yǎng)法和馬鈴薯活體試驗(yàn),進(jìn)行菌株S61及其發(fā)酵液有機(jī)溶劑萃取物抑制馬鈴薯干腐病病原菌活性測(cè)定及對(duì)儲(chǔ)藏期馬鈴薯安全性評(píng)價(jià)。采用平板透明圈法和排油圈法,分別測(cè)定菌株S61發(fā)酵液分泌抑菌蛋白和產(chǎn)生脂肽類物質(zhì)的能力。【結(jié)果】結(jié)合菌株S61的形態(tài)特征、生理生化特征和系統(tǒng)發(fā)育進(jìn)化樹分析結(jié)果,將菌株S61鑒定為特氏鹽芽孢桿菌(Halobacillus trueperi)。其發(fā)酵液能產(chǎn)生蛋白酶、淀粉酶和纖維素酶,并能產(chǎn)生脂肽類物質(zhì)。菌株S61及其有機(jī)溶劑萃取物對(duì)3株馬鈴薯干腐病病原菌(青9A-4-13、青9A-5-2和65B-2-6)均有不同程度的抑菌活性,其中對(duì)青9A-4-13的抑菌活性最強(qiáng),對(duì)峙培養(yǎng)7 d后的抑制率為55.67%。菌株S61發(fā)酵液不同濃度(1、5、10和20 mg/mL)正丁醇萃取物對(duì)青9A-4-13的抑菌活性最高,抑制率分別為61.50%、63.00%、64.00%和66.00%。菌株S61發(fā)酵液及其正丁醇萃取物對(duì)馬鈴薯儲(chǔ)藏安全。【結(jié)論】中度嗜鹽菌S61在體外和馬鈴薯活體上均對(duì)干腐病病原真菌具有抑制作用,其發(fā)酵產(chǎn)物的正丁醇萃取物活性最高,并存在生防因子,能產(chǎn)生一些具有抑菌活性的次級(jí)代謝產(chǎn)物,具有較好的馬鈴薯干腐病生物防治潛力。
關(guān)鍵詞: 中度嗜鹽菌;生防因子;馬鈴薯干腐病;防效;安全性評(píng)價(jià)
中圖分類號(hào): S435.32;S476? ? ? ? ? ? ? ? ? ? ? ? ?文獻(xiàn)標(biāo)志碼: A 文章編號(hào):2095-1191(2021)10-2619-13
Abstract:【Objective】The inhibitory activity and control effect of moderate halophilic bacteria S61 against pathogenic fungi of potato dry rot was determinedto provide a scientific basis for the biological control and green prevention and control of potato dry rot. 【Method】A moderately halophilic strain S61 from Qarhan Salt Lake in Qinghai was used as material and was was identified by morphology, physiological and biochemical characteristics and molecular biology methods. The inhibitory activity of strain S61 and its organic solvent extract from fermentation against potato dry rot pathogens and the safety assessment were determined by confrontation culture method and potato experiment in vivo. The capacity of producing lipopeptides and proteins of strain S61’s fermentation was determined by transparent circle and oil drain ring methods. 【Result】Combining the morphological characteristics, physiological and biochemical characteristics and phylogenetic tree analysis results, the strain S61 was identified as Halobacillus trueperi. Its fermentation could produce protease, amylase, cellulose, and lipopeptides. S61 and its organic solvent extract had different inhibitory activities against 3 potato dry rot pathogenic fungi (Qing 9A-4-13, Qing 9A-5-2 and 65B-2-6). S61 had the highest inhibitory activity against pathogen Qing9A-4-13, with an inhibition rate 55.67% (7 d). Its N-butyl alcohol extract at the different concentrations (1, 5, 10 and 20 mg/mL) had the highest inhibitory activity against pathogen Qing 9A-4-13, with inhibition rates 61.50%, 63.00%, 64.00%? and 66.00%, respectively. The strain S61 and its N-butyl alcohol extract were safe for potato in storage. 【Conclusion】The moderate halophilic bacterium S61 has inhibitory activity against potato dry rot pathogenic fungi both in vitro and in vivo. The N-butyl alcohol extract has the highest inhibitory activity. It has biocontrol factors and could produce metabolic products with anti-fungi activity. It proves that S61 has good biocontrol potential in potato dry rot.
Key words: moderate halophilic bacterium; biocontrol factor; potato dry rot; control effect; safety assessment
Foundation item: General Project of Qinghai Natural Science Foundation(2019-ZJ-914); Major Science and Techno-logy Project of Qinghai(2019-NK-A1); Special Funds for National Modern Agricultural Industrial Technology System (CARS-10)
0 引言
【研究意義】馬鈴薯干腐病是馬鈴薯貯藏期主要真菌性病害之一,由多種鐮刀菌(Fusarium spp.)的種或變種引起(Delaplace et al.,2008;李金花等,2011)。馬鈴薯干腐病對(duì)馬鈴薯貯藏期造成的產(chǎn)量損失最高可達(dá)60%(Bojanowski et al.,2013;雷婭紅等,2016;許苗等,2018)。采用化學(xué)防治手段對(duì)馬鈴薯進(jìn)行防腐保鮮處理是當(dāng)前減少馬鈴薯腐爛損失的重要手段,但長(zhǎng)期使用化學(xué)藥劑防治會(huì)造成菌株抗藥性、環(huán)境污染和農(nóng)藥殘留等問題(Romualdo et al.,2010;王麗麗等,2016;Krüsemann et al.,2017;孫清華等,2019)。目前,多利用具有安全無毒、不污染環(huán)境和不易產(chǎn)生抗藥性等優(yōu)點(diǎn)的生物防治手段進(jìn)行植物病害防治(Gerbore et al.,2014;Krüsemann et al.,2017)。因此,生物防治尤其是利用微生物等天然資源及其產(chǎn)生的天然產(chǎn)物對(duì)馬鈴薯干腐病進(jìn)行防治,對(duì)馬鈴薯產(chǎn)業(yè)的健康發(fā)展具有重要意義。【前人研究進(jìn)展】目前,有關(guān)馬鈴薯干腐病拮抗菌的研究主要集中在拮抗菌的篩選及活性物質(zhì)的抑菌活性研究方面。馬鈴薯干腐病拮抗菌篩選結(jié)果顯示,生防菌大部分為木霉菌(Trichoderma spp.)(崔巖,2013)、芽孢桿菌(Bacillus spp.)、放線菌(Actinomyces spp.)(孫現(xiàn)超等,2013;牛世全等,2017)和假單胞菌(Pseudomonas spp.)(Ramlawi et al.,2021)。王愛軍(2013)研究發(fā)現(xiàn),萎縮芽孢桿菌(B. atrophaeus)能同時(shí)抑制馬鈴薯干腐病菌接骨木鐮刀菌(F. sambucinum)和茄病鐮刀菌(F. solani),并采用AFLP技術(shù)對(duì)其遺傳多樣性進(jìn)行了研究;賈鵬莉等(2020)研究發(fā)現(xiàn)貝萊斯芽孢桿菌(B. velezensis)的正丁醇萃取物對(duì)馬鈴薯干腐病病原菌尖孢鐮刀菌(F. oxysporum)的抑菌活性高達(dá)80.07%,同時(shí)該拮抗菌能產(chǎn)生蛋白酶、淀粉酶、纖維素酶及脂肽類物質(zhì);胡英杰等(2021)通過生長(zhǎng)速率法測(cè)定發(fā)現(xiàn),地衣芽孢桿菌(B. licheniformis)的正丁醇萃取物對(duì)馬鈴薯干腐病病原菌的抑制率高達(dá)78.57%;賈鵬莉和沈碩(2021)通過平板對(duì)峙法及穩(wěn)定性評(píng)價(jià)發(fā)現(xiàn),暹羅芽孢桿菌(B. siamensis)和貝萊斯芽孢桿菌對(duì)馬鈴薯干腐病病原鐮刀菌具有較高的抑菌活性。在次級(jí)代謝產(chǎn)物的研究方面,發(fā)現(xiàn)來源于藍(lán)桉的藍(lán)桉葉精油及其主要單體組分能抑制馬鈴薯干腐病致病菌菌絲生長(zhǎng),其對(duì)黃色鐮刀菌(F. culmorum)和擬枝鐮刀菌(F. sporotrioides)的抑制效果更好(韓峰,2017);來源于真菌寡雄腐霉(Pythium oligandrum)的寡雄蛋白(Oligandrin)對(duì)馬鈴薯塊莖干腐病的擴(kuò)展有一定控制效果,其能提高馬鈴薯塊莖組織苯丙烷代謝相關(guān)的酶活及相關(guān)基因的表達(dá),從而提高馬鈴薯塊莖的抗病性(劉筱等,2017);殼聚糖能抑制尖孢鐮刀菌的生長(zhǎng)和孢子萌發(fā),增強(qiáng)馬鈴薯對(duì)該病原菌的抗性(Ren et al.,2021)。在嗜鹽菌研究方面,由于嗜鹽菌在特殊鹽堿生境下生長(zhǎng),其中必然存在著特殊活性的次級(jí)代謝產(chǎn)物(任培根和周培瑾,2003;Mathabatha,2010;談峰等,2021)。目前國(guó)內(nèi)外有關(guān)來源于鹽湖的嗜鹽菌研究主要包括新菌種的發(fā)現(xiàn)及鑒定、群落結(jié)構(gòu)及多樣性分析、耐鹽堿能力及防治植物病害等。王錢福(2007)從青島和甘肅河西走廊地區(qū)的高鹽環(huán)境樣品中分離到中度和極端嗜鹽菌菌株,并對(duì)分離到的菌株進(jìn)行形態(tài)學(xué)、生理生化特征、細(xì)胞化學(xué)組分分析及16S rDNA序列分析等多相分類學(xué)研究。沈碩(2017)從察爾汗鹽湖樣品中分離到中度嗜鹽菌421株,并對(duì)其群落結(jié)構(gòu)和多樣性進(jìn)行分析,發(fā)現(xiàn)該鹽湖中度嗜鹽菌具有豐富的遺傳多樣性,存在可分離的新物種。王艷紅等(2017)成功克隆了中度嗜鹽菌Halobacillus Y5的甘氨酸甜菜堿轉(zhuǎn)運(yùn)蛋白o(hù)pu D基因,對(duì)其結(jié)構(gòu)及蛋白功能進(jìn)行分析,驗(yàn)證了該菌的耐鹽堿特性。【本研究切入點(diǎn)】目前,針對(duì)馬鈴薯干腐病拮抗菌的研究多為從馬鈴薯薯塊病樣病健交界處分離得到拮抗菌,而且都為對(duì)馬鈴薯干腐病病原菌的體外活性測(cè)定;針對(duì)嗜鹽菌的研究方面多集中在嗜鹽菌的多樣性、群落結(jié)構(gòu)及嗜鹽機(jī)制方面。有關(guān)利用特殊環(huán)境微生物中的中度嗜鹽菌及其次級(jí)代謝產(chǎn)物進(jìn)行馬鈴薯窖藏病害生物防治、以及利用生防菌發(fā)酵液有機(jī)溶劑萃取物及次級(jí)代謝產(chǎn)物抑制馬鈴薯干腐病病原菌的馬鈴薯活體防效及安全性評(píng)價(jià)的研究尚未見報(bào)道。【擬解決的關(guān)鍵問題】通過體外對(duì)峙培養(yǎng)法與馬鈴薯活體試驗(yàn)相結(jié)合,對(duì)來源于青海察爾汗鹽湖的1株中度嗜鹽菌S61及其發(fā)酵液有機(jī)溶劑萃取物抑制馬鈴薯干腐病病原菌的活性和干腐病活體防效進(jìn)行評(píng)價(jià),對(duì)生防因子進(jìn)行分析,旨在尋找高效、低毒的馬鈴薯干腐病生防菌劑、生防制劑及其先導(dǎo)化合物,以期為馬鈴薯干腐病的生物防治及綠色防控提供科學(xué)依據(jù)。
1 材料與方法
1. 1 試驗(yàn)材料
1. 1. 1 生防菌 中度嗜鹽菌S61分離自青海察爾汗鹽湖(東經(jīng)99°02′~99°02′,北緯36°18′~36°45′)湖水樣品,由青海省農(nóng)林科學(xué)院微生物研究室分離并保存。
1. 1. 2 植物病原真菌 馬鈴薯干腐病病原真菌青9A-4-13(F. acuminatum)和青9A-5-2(F. solani)分離自馬鈴薯青薯9號(hào)薯塊病樣,65B-2-6(F. tricinctum)分離自馬鈴薯下寨65薯塊病樣。供試菌株均由青海省農(nóng)林科學(xué)院微生物研究室分離并保存。
1. 1. 3 馬鈴薯品種 供試馬鈴薯品種為青薯2號(hào),由青海省農(nóng)林科學(xué)院生物技術(shù)研究所提供。
1. 1. 4 培養(yǎng)基 中度嗜鹽菌S61分離培養(yǎng)于ATCC 213改良培養(yǎng)基(沈碩,2017),所有馬鈴薯干腐病病原菌培養(yǎng)于PDA培養(yǎng)基(沈碩和王艦,2013)。
1. 2 試驗(yàn)方法
1. 2. 1 菌株S61形態(tài)學(xué)與生理生化特征鑒定 根據(jù)《伯杰氏細(xì)菌鑒定手冊(cè)》(Buchanan and Gibbons,1999)和《常見細(xì)菌系統(tǒng)鑒定手冊(cè)》(東秀珠和蔡妙英,2001)對(duì)菌株S61進(jìn)行形態(tài)學(xué)和生理生化特征鑒定。
1. 2. 2 菌株S61可利用碳源分析 采用Biolog細(xì)菌鑒定系統(tǒng),菌株S61經(jīng)革蘭氏染色和酶活性測(cè)定后,在Biolog微生物鑒定系統(tǒng)專用的平板培養(yǎng)基(Biolog,USA)上劃線培養(yǎng)12 h,取單菌落用稀釋液稀釋至合適濁度,透光率為90%~98%,將稀釋液加至Biolog全自動(dòng)生化鑒定板中,每孔加100 μL,30 ℃培養(yǎng)20 h后上機(jī)讀數(shù),記錄讀數(shù)結(jié)果,并進(jìn)行菌株S61對(duì)95種碳源的利用特征分析。
1. 2. 3 菌株S61分子生物學(xué)鑒定 菌株S61的DNA提取根據(jù)生工生物工程(上海)股份有限公司的柱式細(xì)菌DNA提取試劑盒的程序操作。選擇細(xì)菌16S rDNA通用引物F27(5'-AGAGTTTGATCCTGGCT CAGG-3')和P1541(5'-AAGGAGGTGGTGATCCA GCCGCA-3')。PCR反應(yīng)體系25.0 μL:10×Buffer 2.5 μL,dNTP(10 mmol/L) 2.0 μL,DNA模板1.0 μL,上、下游引物各1.0 μL,Taq DNA聚合酶0.2 μL,無菌水補(bǔ)足至25.0 μL。擴(kuò)增程序:94 ℃預(yù)變性5 min;94 ℃ 40 s,55 ℃ 45 s,72 ℃ 80 s,進(jìn)行35個(gè)循環(huán);72 ℃延伸10 min。反應(yīng)結(jié)束后,取5.0 μL PCR產(chǎn)物進(jìn)行瓊脂糖凝膠電泳檢測(cè),回收產(chǎn)物送至生工生物工程(上海)股份有限公司測(cè)序。將得到的16S r DNA序列登錄NCBI網(wǎng)站通過BLAST進(jìn)行序列比對(duì),運(yùn)用MEGA 7.0中的鄰接法(Neighbor-joining,NJ)(Bootstrap值為1000次)構(gòu)建菌株S61 16S rDNA序列的系統(tǒng)發(fā)育進(jìn)化樹。
1. 2. 4 菌株S61發(fā)酵液制備及其萃取物制備? 將菌株S61接種至裝瓶量為400 mL的ATCC213改良液體培養(yǎng)基中,置于37 ℃ 180 r/min恒溫?fù)u瓶柜中振蕩培養(yǎng)5~7 d,收集發(fā)酵液,然后將其經(jīng)布氏漏斗減壓過濾去除菌體,得到去菌體發(fā)酵液,備用。
取去菌體發(fā)酵液600 mL于3000 mL的分液漏斗中,依次用等體積的氯仿、乙酸乙酯和正丁醇對(duì)發(fā)酵液進(jìn)行萃取,萃取液經(jīng)旋轉(zhuǎn)蒸發(fā)得萃取物;將萃取物預(yù)溶于二甲基亞砜(≤0.1%),并用無菌水分別將其配成質(zhì)量濃度為1.00、5.00、10.00和20.00 mg/mL的萃取物溶液,溶液經(jīng)0.22 μm微孔濾膜抽濾,備用。
1. 2. 5 菌株S61生防因子分析 采用平板透明圈法(潘曉梅等,2019),用直徑6 mm的打孔器分別在淀粉、酪蛋白、葡聚糖酶和羧甲基纖維素培養(yǎng)基上打取3個(gè)孔,向每孔中加入菌株S61發(fā)酵液100 μL,每個(gè)培養(yǎng)基處理設(shè)3次重復(fù)。將培養(yǎng)基平板置于30 ℃培養(yǎng)箱中培養(yǎng)48~72 h,向淀粉酶培養(yǎng)基中加入2 mL碘液,使碘液均勻覆蓋平板,靜置10 min,觀察平板上出現(xiàn)透明圈情況;同時(shí)觀察酪蛋白酶、葡聚糖酶和羧甲基纖維素培養(yǎng)基平板出現(xiàn)透明圈的情況。
采用排油圈法(魏新燕等,2017),取適量橄欖油加入蘇丹Ⅲ染色劑混勻,向直徑為9 cm的培養(yǎng)皿中加入60 mL純水,并緩慢加入染色后的橄欖油,水面形成一層油膜,向培養(yǎng)皿油膜中心持續(xù)滴加菌株S61發(fā)酵液,觀察是否形成排油圈,檢測(cè)菌株S61發(fā)酵液是否有脂肽類物質(zhì)生成。
1. 2. 6 菌株S61及其萃取物抑菌活性測(cè)定 采用平板對(duì)峙法(Sadfi et al.,2001),在直徑9 cm的培養(yǎng)皿底部用十字交叉法劃線,并以交叉點(diǎn)為中心,在中心點(diǎn)接種菌株S61,在距離中心點(diǎn)2.5 cm處呈對(duì)稱分布的4個(gè)點(diǎn)接種直徑為5 mm的同一種病原菌菌餅。每個(gè)培養(yǎng)皿為1個(gè)處理,每處理3次重復(fù),以只接種病原菌的培養(yǎng)皿為對(duì)照。7 d后測(cè)定菌株S61的抑菌活性。計(jì)算公式:抑菌率(%)=(對(duì)照菌落直徑-處理菌落直徑)/對(duì)照菌落直徑×100。
采用牛津杯法(吳海霞和田志芳,2020)測(cè)定發(fā)酵液有機(jī)溶劑萃取物的抑菌活性。計(jì)算公式:抑制率(%)=(對(duì)照菌落直徑-處理菌落直徑)/對(duì)照菌落直徑×100。
1. 2. 7 菌株S61發(fā)酵液及其萃取物對(duì)活體馬鈴薯上干腐病病原菌的抑制效果和馬鈴薯儲(chǔ)藏的安全性評(píng)價(jià) 參照Sadfi等(2001)的方法,首先將活化后的菌株S61接種于ATCC213改良液體培養(yǎng)基中,在37 ℃ 200 r/min的搖瓶柜中振蕩培養(yǎng)2 d,收獲發(fā)酵液,用血球計(jì)數(shù)板將菌株S61發(fā)酵液的濃度調(diào)至1.0×108 CFU/mL;將3株供試馬鈴薯干腐病病原菌接種于PDB液體培養(yǎng)基中,在28 ℃ 200 r/min的搖瓶柜中振蕩培養(yǎng)2 d,收獲發(fā)酵液,用血球計(jì)數(shù)板分別將3株病原菌發(fā)酵液的孢子濃度調(diào)整為1.0×107 個(gè)/mL。然后在已消毒處理的馬鈴薯上用直徑為5 mm的打孔器打造2個(gè)深3 mm的孔口,每個(gè)孔口先接入40 μL病原菌發(fā)酵液,隨后接入40 μL菌株S61發(fā)酵液,將接種完成的馬鈴薯用封口膜包扎放入自封袋中,并在28 ℃、相對(duì)濕度75%左右的恒溫培養(yǎng)箱中培養(yǎng)14 d;以接病原菌發(fā)酵液和等量無菌水的處理作為陽(yáng)性對(duì)照,以接等量無菌水和菌株S61發(fā)酵液的處理為陰性對(duì)照,以只接等量無菌水的處理為空白對(duì)照。每處理接種1個(gè)馬鈴薯,重復(fù)3次。
菌株S61發(fā)酵液萃取物對(duì)活體馬鈴薯上干腐病防效測(cè)定方法與發(fā)酵液防效測(cè)定方法一致。
培養(yǎng)14 d后,分別測(cè)定發(fā)酵液和萃取物溶液處理下馬鈴薯塊莖的壞果率、病斑深度及抑制率,并進(jìn)行菌株S61發(fā)酵液及其萃取物對(duì)貯藏期馬鈴薯的安全性評(píng)價(jià)(李永才等,2009;劉筱等,2017)。計(jì)算公式:抑制率(%)=LP-LA/LP×100;其中,LP=未經(jīng)中度嗜鹽菌處理的馬鈴薯塊莖原質(zhì)量-鐮刀菌侵染后質(zhì)量,LA=中度嗜鹽菌處理后的馬鈴薯塊莖原質(zhì)量-鐮刀菌侵染后質(zhì)量。馬鈴薯儲(chǔ)藏安全性評(píng)價(jià)中無需計(jì)算抑制率。
1. 3 統(tǒng)計(jì)分析
試驗(yàn)數(shù)據(jù)運(yùn)用SPSS 19.0進(jìn)行統(tǒng)計(jì)分析,應(yīng)用Duncan’s新復(fù)極差法進(jìn)行各處理間的差異顯著性分析。
2 結(jié)果與分析
2. 1 菌株S61的鑒定
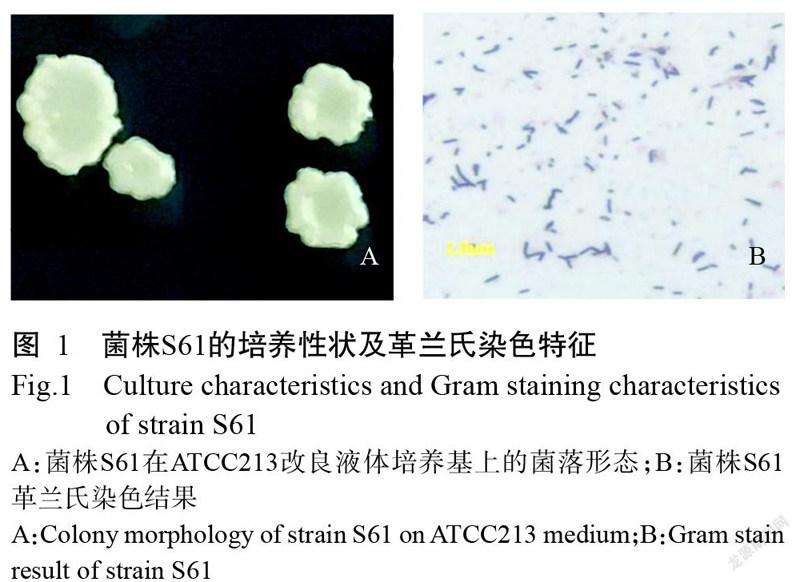
2. 1. 1 形態(tài)學(xué)鑒定 如圖1所示,菌株S61菌落呈乳黃色,不透明,表面褶皺,邊緣不規(guī)則;革蘭氏染色后鏡檢呈藍(lán)紫色,桿狀,表明該菌株為陽(yáng)性菌。
2. 1. 2 生理生化特征 菌株S61過氧化氫酶、氧化酶、β-半乳糖苷酶、硝酸鹽還原、明膠液化、淀粉水解和酪蛋白測(cè)定呈陽(yáng)性,精氨酸雙水解酶、精氨酸脫羧酶、H2S產(chǎn)生、水楊酸、吲哚試驗(yàn)、溶血試驗(yàn)、厭氧試驗(yàn)和脲酶呈陰性(表1)。
2. 1. 3 菌株S61可利用碳源 采用Biolog細(xì)菌鑒定系統(tǒng)進(jìn)行菌株S61對(duì)95種碳源利用情況分析,結(jié)果見表2。
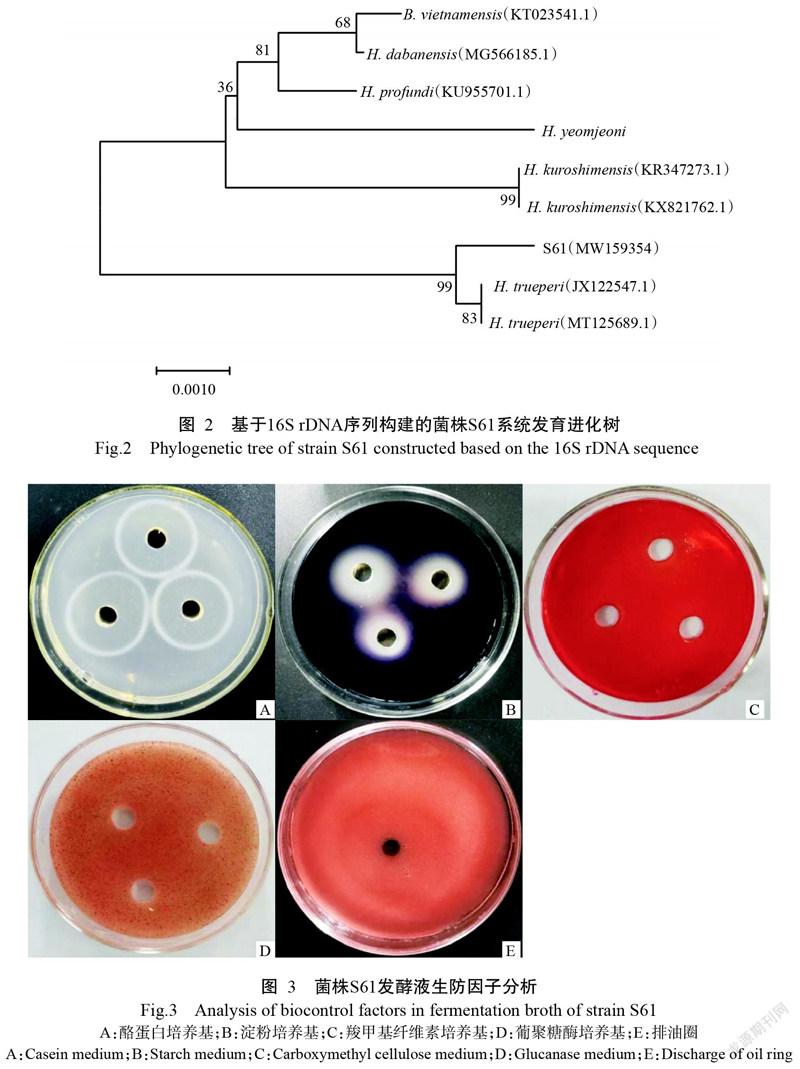
2. 1. 4 分子生物學(xué)鑒定 將菌株S61測(cè)序得到的16S rDNA序列提交至NCBI數(shù)據(jù)庫(kù),登錄號(hào)為MW 159354。經(jīng)BLAST序列比對(duì)分析,菌株S61與H. trueperi(MT125689.1)和H. trueperi(JX122547.1)的親緣關(guān)系最近,同源性達(dá)99.78%。使用MEGA 7.0中的鄰接法,以菌株S61與其他同源性相近的菌株16S rDNA序列構(gòu)建系統(tǒng)發(fā)育進(jìn)化樹,結(jié)果(圖2)顯示,菌株S61的16S rDNA序列與H. trueperi(MT125689.1)和H. trueperi(JX122547.1)聚類為同一分支。結(jié)合菌株S61的形態(tài)特征、生理生化特征和系統(tǒng)發(fā)育進(jìn)化樹結(jié)果,將菌株S61鑒定為特氏鹽芽孢桿菌(H. trueperi)。
2. 2 菌株S61生防因子分析
采用透明圈法測(cè)定菌株S61發(fā)酵液的產(chǎn)酶能力,結(jié)果(圖3)顯示,菌株S61發(fā)酵液在酪蛋白培養(yǎng)基(圖3-A)、淀粉培養(yǎng)基(圖3-B)和羧甲基纖維素培養(yǎng)基(圖3-C)上均產(chǎn)生了明顯的酶解圈,其中在酪蛋白培養(yǎng)基和淀粉培養(yǎng)基上酶解圈邊緣界限清晰;在酪蛋白培養(yǎng)基上酶解圈明顯較大;在羧甲基纖維素培養(yǎng)基上酶解圈邊緣界限模糊。說明菌株S61發(fā)酵液產(chǎn)蛋白酶較多,淀粉酶次之。菌株S61發(fā)酵液在葡聚糖酶培養(yǎng)基上未產(chǎn)生透明圈(圖3-D),說明菌株S61發(fā)酵液不具有產(chǎn)葡聚糖酶的能力。
采用排油圈法測(cè)定菌株S61發(fā)酵液是否具有產(chǎn)生表面活性功能的脂肽類物質(zhì)的能力,結(jié)果(圖3-E)顯示,菌株S61發(fā)酵液產(chǎn)生了明顯的排油圈,但排油圈較小,說明菌株S61發(fā)酵液能產(chǎn)少量脂肽類物質(zhì)。
2. 3 菌株S61抑菌活性測(cè)定結(jié)果
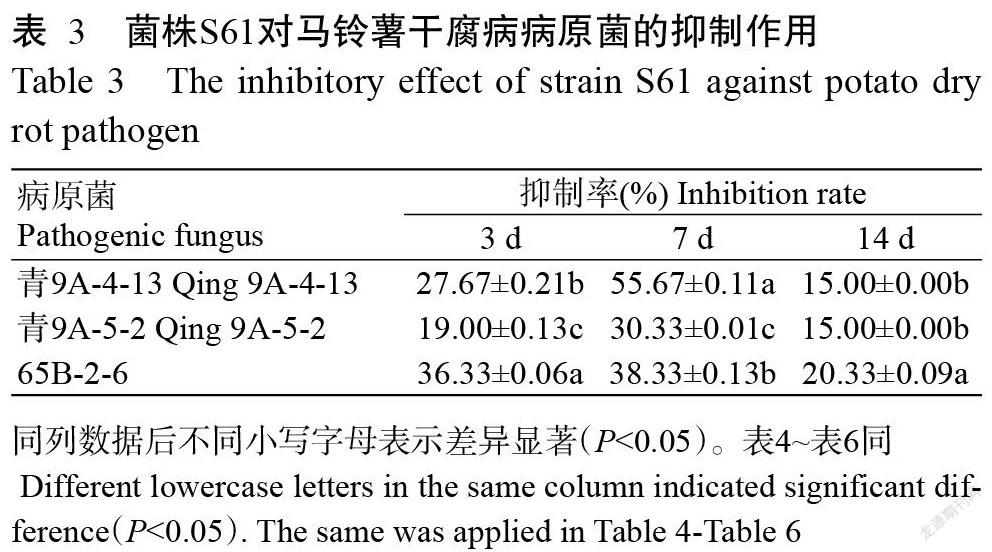
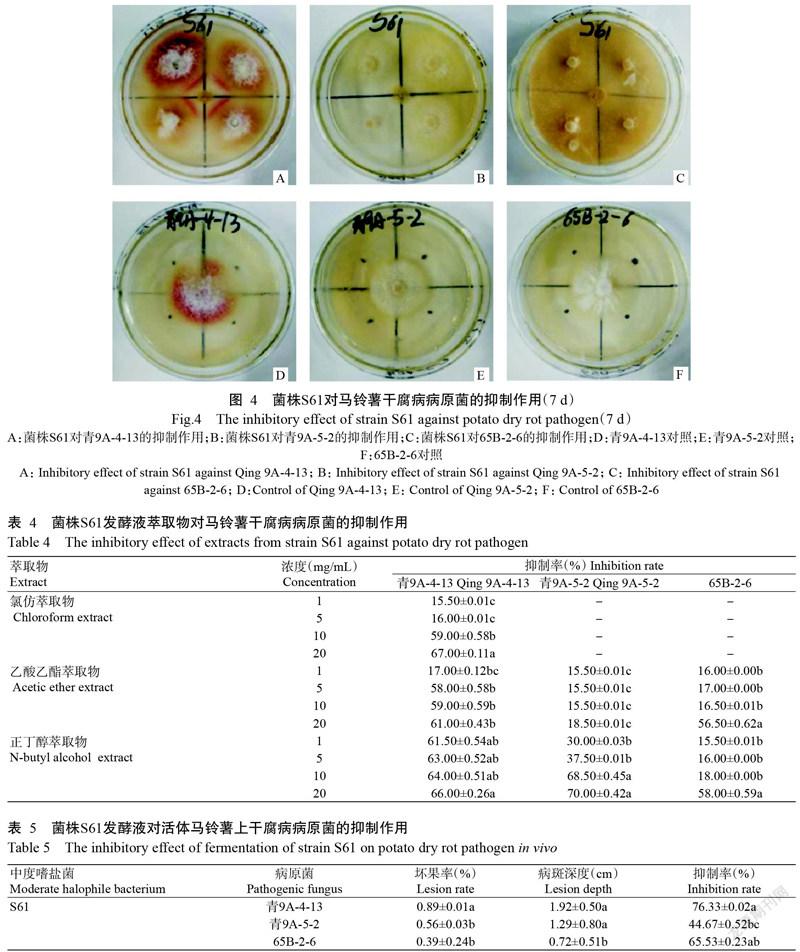
由表3可知,菌株S61與3株馬鈴薯干腐病病原菌在培養(yǎng)皿中分別對(duì)峙培養(yǎng)3 d后,對(duì)青9A-4-13、青9A-5-2和65B-2-6的抑制率分別27.67%、19.00%和36.33%;培養(yǎng)7 d后,抑制率升高,分別為55.67%、30.33%和38.33%;培養(yǎng)14 d后,對(duì)3株病原菌的抑制效果相當(dāng),抑制率分別為15.00%、15.00%和20.33%。由此可見,培養(yǎng)7 d后,菌株S61對(duì)病原菌的抑制效果最強(qiáng),其中對(duì)青9A-4-13的抑制活性最好(圖4)。
2. 4 菌株S61發(fā)酵液萃取物的抑菌活性測(cè)定結(jié)果
由表4可知,菌株S61的正丁醇萃取物對(duì)3株馬鈴薯干腐病病原菌的抑制活性最高,乙酸乙酯萃取物活性次之,氯仿萃取物活性最低。就正丁醇萃取物而言,1和5 mg/mL萃取物僅對(duì)青9A-4-13具有高抑菌活性,抑制率分別為61.50%和63.00%;10 mg/mL萃取物對(duì)青9A-4-13和青9A-5-2具有高抑菌活性,抑制率分別為64.00%和68.50%;20 mg/mL萃取物對(duì)青9A-4-13、青9A-5-2和65B-2-6均具有較高的抑菌活性,抑制率分別為66.00%、70.00%和58.00%。就乙酸乙酯萃取物而言,5和10 mg/mL萃取物僅對(duì)青9A-4-13具有較高的抑菌活性,抑制率分別為58.00%和59.00%;20 mg/mL萃取物對(duì)青9A-4-13和65B-2-6具有較高的抑菌活性,抑制率分別為61.00%和56.50%。就氯仿萃取物而言,僅10和20 mg/mL萃取物對(duì)青9A-4-13具有較高的抑菌活性,抑制率分別為59.00%和67.00%。
由此可見,3種不同的菌株S61發(fā)酵液萃取物對(duì)青9A-4-13的抑菌活性最高;同時(shí),正丁醇和乙酸乙酯萃取物對(duì)3株馬鈴薯干腐病病原菌均具有不同的抑菌活性,且正丁醇萃取物的抑菌活性更高。
2. 5 菌株S61發(fā)酵液對(duì)活體馬鈴薯上干腐病病原菌的抑制效果
由表5可知,菌株S61發(fā)酵液對(duì)活體馬鈴薯上干腐病病原菌青9A-4-13的抑菌活性最高,壞果率為0.89%,病斑深度為1.92 cm,抑制率達(dá)76.33%;對(duì)65B-2-6的抑菌活性次之,抑制率為65.53%;對(duì)青9A-5-2的抑菌活性最弱,抑制率為44.67%。
2. 6 菌株S61發(fā)酵液萃取物對(duì)活體馬鈴薯上干腐病病原菌的抑制效果
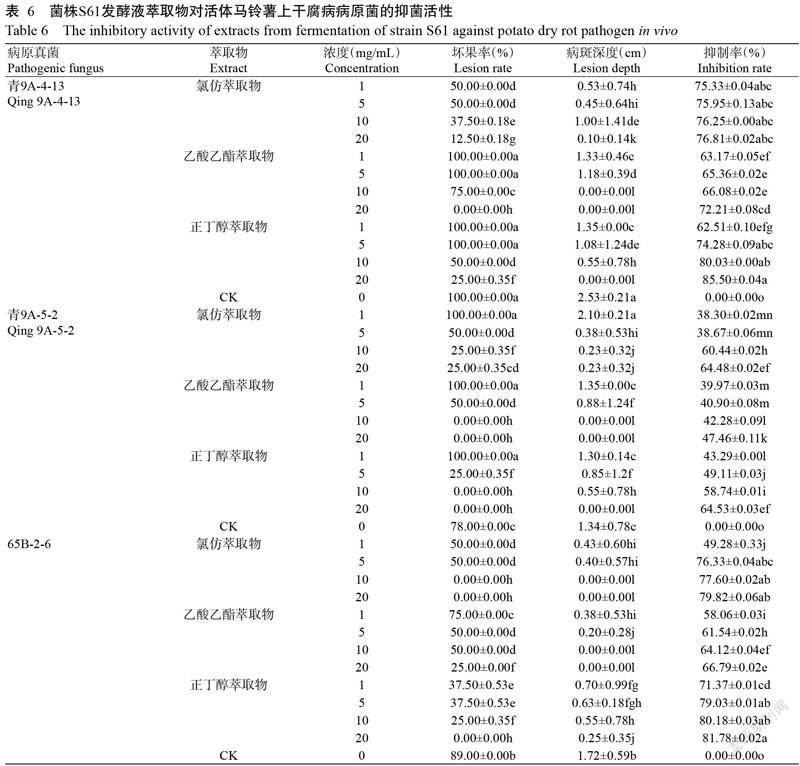
由表6可知,菌株S61發(fā)酵液萃取物對(duì)活體馬鈴薯上干腐病病原菌有明顯的抑制活性,其中對(duì)青9A-4-13具有高抑菌活性,抑制率為62.51%~85.50%;對(duì)65B-2-6的抑菌活性次之,抑制率為49.28%~81.78%;對(duì)青9A-5-2的抑菌活性最低,抑制率為38.30%~64.53%。此外,菌株S61發(fā)酵液的正丁醇萃取物對(duì)青9A-4-13和65B-2-6的抑菌活性最高,各供試濃度下對(duì)2株病原菌的抑制率均高于60.00%,濃度為10和20 mg/mL的正丁醇萃取物對(duì)2株病原菌的抑制率均高于80.00%。同時(shí),濃度為10和20 mg/mL的正丁醇和乙酸乙酯萃取物作用下的壞果率和病斑深度均較低。
2. 7 菌株S61發(fā)酵液及其有機(jī)溶劑萃取物對(duì)馬鈴薯儲(chǔ)藏的安全性評(píng)價(jià)
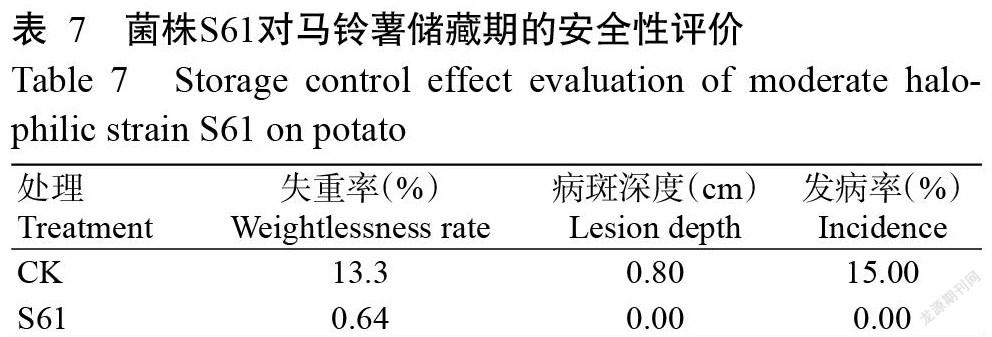
由表7可知,馬鈴薯接種青9A-4-13后,經(jīng)菌株S61發(fā)酵液及其正丁醇萃取物處理,馬鈴薯表現(xiàn)出一定程度的失重,但馬鈴薯塊莖創(chuàng)傷處無任何病害癥狀,病斑深度及發(fā)病率均為零。說明菌株S61發(fā)酵液及其正丁醇萃取物對(duì)馬鈴薯儲(chǔ)藏安全。
3 討論
中度嗜鹽菌特殊的生存環(huán)境使其具有極為特殊的生理結(jié)構(gòu)和代謝機(jī)制,并且還產(chǎn)生了許多具有特殊功能的天然活性物質(zhì),是一類具有生物技術(shù)潛能的自身利益資源,因而其應(yīng)用已引起人們的廣泛關(guān)注。目前對(duì)中度嗜鹽菌應(yīng)用方面的研究主要集中在對(duì)其產(chǎn)生的酶、一些功能性分子和大分子多聚物以及生物環(huán)保等方面(馮二梅等,2009)。除此之外,也有學(xué)者對(duì)來源于青海察爾汗鹽湖的中度嗜鹽菌萃取物對(duì)辣椒疫霉菌的抑菌活性進(jìn)行了研究(韓峰,2017)。本研究利用青海察爾汗鹽湖的中度嗜鹽菌S61及其發(fā)酵液萃取物對(duì)馬鈴薯干腐病的抑制作用進(jìn)行了評(píng)價(jià),結(jié)果表明,菌株S61及其發(fā)酵液萃取物對(duì)3株馬鈴薯干腐病病原菌具有不同程度的抑制作用;在對(duì)馬鈴薯塊莖的安全性評(píng)價(jià)中,馬鈴薯接種病原菌青9A-4-13后,經(jīng)菌株S61發(fā)酵液及其正丁醇萃取物處理,馬鈴薯塊莖創(chuàng)傷處無任何病害癥狀,菌株S61及其發(fā)酵液萃取物對(duì)馬鈴薯儲(chǔ)藏安全。可見菌株S61具有作為馬鈴薯儲(chǔ)藏期間干腐病生防制劑的潛力。關(guān)于其發(fā)酵液提取物中活性物質(zhì)的分離、結(jié)構(gòu)鑒定以及尋找具有高效抑制馬鈴薯干腐病病害的化合物是下一步研究工作的重點(diǎn)。
截至目前,大量的國(guó)內(nèi)外學(xué)者將芽孢桿菌作為多種植物病原真菌潛在的生防制劑在培養(yǎng)皿中和生物活體上進(jìn)行了研究(Sadfi et al.,2002;van den Boogert and Luttikholt,2004;王穎等,2014;Chen? et al.,2016;程歡歡等,2019)。本研究對(duì)中度嗜鹽菌S61進(jìn)行了生理生化鑒定及基于16S rDNA序列分析的分子生物學(xué)鑒定,將菌株S61鑒定為特氏鹽芽孢桿菌。大量研究顯示,芽孢桿菌中的短小芽孢桿菌可對(duì)小麥根腐病病原菌(崔云龍等,1995)、番茄細(xì)菌性青枯病(連玲麗等,2009)、大豆疫病(曹舜,2015)、煙草赤星病菌、黑脛病菌和白粉病菌(王靜等,2010,2015)等多種植物病害及病原物具有生防作用;簡(jiǎn)單芽孢桿菌對(duì)根結(jié)線蟲和胞囊線蟲的生防作用顯著(劉冬梅等,2006;李永才等,2009)。但有關(guān)特氏鹽芽孢桿菌在生物防治方面的研究還處于空白狀態(tài);而本研究中特氏鹽芽孢桿菌S61及其發(fā)酵液萃取物對(duì)3種不同馬鈴薯干腐病病原菌均有一定的抑制作用,為開發(fā)防治植物病害的新型生物源農(nóng)藥打下基礎(chǔ)。
菌株S61在體外對(duì)峙培養(yǎng)和馬鈴薯活體試驗(yàn)中均對(duì)干腐病病原菌表現(xiàn)出明顯的抑制作用,經(jīng)生理生化試驗(yàn)發(fā)現(xiàn)可產(chǎn)生過氧化氫酶、氧化酶、β-半乳糖苷酶、硝酸鹽還原酶、淀粉水解酶和酪蛋白酶等多種酶活性;同時(shí),其發(fā)酵產(chǎn)物的3種不同有機(jī)溶劑萃取物在體外和馬鈴薯活體試驗(yàn)中對(duì)干腐病病原菌均表現(xiàn)出一定的抑制作用,其中,正丁醇萃取物活性最高。由此可見,菌株S61會(huì)產(chǎn)生一些具有抑菌活性的次級(jí)代謝產(chǎn)物,如抗生素(Korsten,1995)、生物表面活性劑(梅雨薇等,2020)、酶類物質(zhì)(Sadfi et al.,2001;劉郵洲等,2017)、嗜鐵素(Zhang et al.,2016)和酯肽類(Isabel et al.,2015;魏新燕等,2017;車建美等,2017)等。此外,菌株S61發(fā)酵液及其萃取物在體外和馬鈴薯活體試驗(yàn)中對(duì)馬鈴薯干腐病病原菌的抑菌活性相當(dāng),說明生防制劑的有效性通常受到生防菌和病原菌類型、寄主植物對(duì)病原菌的抗性以及環(huán)境等多種因素的影響(Recep et al.,2009)。后續(xù)課題組將進(jìn)一步探究菌株S61的活性組分對(duì)干腐病病原菌的相關(guān)生防作用機(jī)制,以期為生防菌劑、生防制劑及其先導(dǎo)化合物的開發(fā)提供理論依據(jù)和技術(shù)支持。
4 結(jié)論
中度嗜鹽菌S61在體外和馬鈴薯活體上均對(duì)干腐病病原菌具有抑制作用,其發(fā)酵產(chǎn)物的正丁醇萃取物活性最高,并存在生防因子,能產(chǎn)生一些具有抑菌活性的次級(jí)代謝產(chǎn)物,具有較好的馬鈴薯干腐病生物防治潛力。
參考文獻(xiàn):
曹舜. 2015. 短小芽孢桿菌BS-4菌株對(duì)大豆疫病的生防作用及其機(jī)制研究[D]. 合肥:安徽農(nóng)業(yè)大學(xué). [Cao S. 2015. Biological control and mechanism of Bacillus pumilus strain BS-4 against soybean blight(Phytophthorasojae)[D]. Hefei:Anhui Agriculture University.]
車建美,劉波,陳冰冰,劉國(guó)紅,葛慈斌,藍(lán)江林. 2017. 短短芽胞桿菌產(chǎn)抗菌物質(zhì)——羥苯乙酯發(fā)酵培養(yǎng)基的優(yōu)化[J]. 中國(guó)生物防治學(xué)報(bào),33(2):248-257. [Che J M,Liu B,Chen B B,Liu G H,Ge C B,Lan J L. 2017. Medium optimization for the production of antimicrobial ethylparaben from Brevi bacillus brevis FJAT-0809-GLX using response surface methodology[J]. Chinese Journal of Biological Control,33(2):248-257.] doi:10.16409/j.cnki.2095-039x.2017.02.016.
程歡歡,余水,姚偉偉,李忠,彭麗娟,丁海霞. 2019. 辣椒炭疽病生防芽孢桿菌的篩選及田間防效[J]. 河南農(nóng)業(yè)大學(xué)學(xué)報(bào),53(4):568-573. [Cheng H H,Yu S,Yao W W,Li Z,Peng L J,Ding H X. 2019. Screening of antagonistic Bacillus strains and control effect against pepper anthracnose in field trial[J]. Journal of Henan Agricultural University,53(4):568-573.] doi:10.16445/j.cnki.1000-2340.2019. 04.012.
崔巖. 2013. 馬鈴薯干腐病與黑痣病菌拮抗木霉菌的篩選及木霉菌遺傳多樣性分析[D]. 蘭州:甘肅農(nóng)業(yè)大學(xué). [Cui Y. 2013. Screening of antagonistic Trichoderma strains against pathogens of Fusarium dry rot and black scurf in potato in Gansu and its analysis of genetic diversity[D]. Lanzhou:Gansu Agricultural University.]
崔云龍,姬金紅,衣海青. 1995. 短小芽孢桿菌D82對(duì)小麥根腐病原菌拮抗的研究[J]. 中國(guó)生物防治,11(3):114-118. [Cui Y L,Ji J H,Yi H Q. 1995. Antagonism of Bacillus pumillus D82 to Helminthosporium sativum,a common root rot pathogen of wheat[J]. Chinese Journal of Biological Control,11(3):114-118.] doi:10.16409/j.cnki. 2095-039x.1995.03.005.
東秀珠,蔡妙英. 2001. 常見細(xì)菌系統(tǒng)鑒定手冊(cè)[M]. 北京:科學(xué)出版社. [Dong X Z,Cai M Y. 2001. Common bacterial system identification manual[M]. Beijing:Science Press.]
馮二梅,宿紅艷,王磊. 2009. 中度嗜鹽菌的研究進(jìn)展[J]. 安徽農(nóng)業(yè)科學(xué),37(31):15125-15126. [Feng E M,Su H Y,Wang L. 2009. Reseach progress of moderately halophilic bacteria[J]. Anhui Agriculture Science,37(31):15125-15126.] doi:10.13989/j.cnki.0517-6611.2009.31. 005.
韓峰. 2017. 藍(lán)桉精油的高效分離及對(duì)馬鈴薯干腐病鐮刀菌抑制作用的研究[D]. 哈爾濱:東北林業(yè)大學(xué). [Han F. 2017. Efficient separation of essential oil from Eucalyptus globulus and the study of inhibitory effect of potato Fusarium dry rot[D]. Harbin:Northeast Forestry University.]
胡英杰,沈碩,賈鵬莉,陳菲兒. 2021. 中度嗜鹽菌抑制馬鈴薯干腐病病原菌活性的篩選及活性菌株的鑒定[J]. 青海大學(xué)學(xué)報(bào),39(1):24-30. [Hu Y J,Shen S,Jia P L,Chen F E. 2021. Screening of moderate halophiles against the pathogen activity of potato dry rot and identification of active strains[J]. Journal of Qinghai University,39(1):24-30.] doi:10.13901/j.cnki.qhwxxbzk.2021.01.004.
賈鵬莉,沈碩. 2021. 拮抗馬鈴薯干腐病病原菌活性菌株的篩選及鑒定[J]. 青海大學(xué)學(xué)報(bào),39(2):34-41. [Jia P L,Shen S. 2021. Screening and identification of active strains against the pathogen of potato dry rot[J]. Journal of Qing-hai University,39(2):34-41.] doi:10.13901/j.cnki.qhwxxbzk.2021.02.005.
賈鵬莉,沈碩,胡英杰. 2020. 一株馬鈴薯干腐病拮抗菌芽孢桿菌的篩選、鑒定及生防因子初探[J]. 福建農(nóng)業(yè)學(xué)報(bào),35(12):1336-1345. [Jia P L,Shen S,Hu Y J. 2020. Screening,identification,and preliminary analysis on antagonistic Bacillus sp. against potato dry rot[J]. Fujian Journal of Agricultural Sciences,35(12):1336-1345.] doi:10.19303/j.issn.1008-0384.2020.12.007.
雷婭紅,況衛(wèi)剛,鄭春生,李秀璋,高文娜,李春杰. 2016. 基于DNA條形碼技術(shù)對(duì)鐮刀菌屬的檢測(cè)鑒定[J]. 植物保護(hù)學(xué)報(bào),43(4):544-551. [Lei Y H,Kuang W G,Zheng C S,Li X Z,Gao W N,Li C J. 2016. Detection and identification of the genus Fusarium by DNA barcoding[J]. Journal of Plant Protection,43(4):544-551.] doi:10.13802/j.cnki.zwbhxb.2016.04.003.
李金花,王蒂,柴兆祥,Burgess L W. 2011. 甘肅省馬鈴薯鐮刀菌干腐病優(yōu)勢(shì)病原的分離鑒定[J]. 植物病理學(xué)報(bào),41(5):456-463. [Li J H,Wang D,Chai Z X,Burgess L W. 2011. Isolation and identification of the dominant pathogens causing potato Fusarium dry rot in Gansu Province[J]. Acta Phytopathologica Sinica,41(5):456-463.] doi:10.13926/j.cnki.apps.2011.05.002.
李永才,畢陽(yáng),胡潔,張春園. 2009. 真菌菌絲細(xì)胞壁提取物對(duì)馬鈴薯塊莖組織抗干腐病的誘導(dǎo)效應(yīng)[J]. 西北植物學(xué)報(bào),29(4):749-753. [Li Y C,Bi Y,Hu J,Zhang C Y. 2009. Induced resistance in potato tuber tissue against Fusarium sulphureum infection by hyphal cell wall extract from Trichothecium roseum[J]. Acta Botanica Boreali-Occidentalia Sinica,29(4):749-753.] doi:10.3321/j.issn:1000- 4025.2009.04.016.
連玲麗,謝荔巖,鄭璐平,林奇英. 2009. 短小芽孢桿菌EN16誘導(dǎo)番茄對(duì)細(xì)菌性青枯病的抗性[J]. 福建農(nóng)林大學(xué)學(xué)報(bào)(自然科學(xué)版),38(5):460-464. [Lian L L,Xie L Y,Zheng L P,Lin Q Y. 2009. Induced resistance to bacterial wilt of tomato by Bacillus pumilus strain EN16[J]. Journal of Fujian Agriculture and Forestry University(Natural Science Edition),38(5):460-464.] doi:10.13323/j.cnki.j.fafu (nat.sci.).2009.05.012.
劉冬梅,李理,楊曉泉,梁世中. 2006. 用牛津杯法測(cè)定益生菌的抑菌活力[J]. 食品研究與開發(fā),27(3):110-111. [Liu D M,Li L,Yang X Q,Liang S Z. 2006. Determination of the antimicrobial activity of probiotic by oxford plate assay system[J]. Food Research and Development,27(3):110-111.] doi:10.3969/j.issn.1005-6521.2006.03.044.
劉筱,潘靜宇,李永才,楊蘭,高春麗,畢陽(yáng). 2017. 寡雄蛋白(Oligandrin)處理對(duì)馬鈴薯塊莖干腐病及苯丙烷代謝的影響[J]. 食品工業(yè)科技,38(6):297-302. [Liu X,Pan J Y,Li Y C,Yang L,Gao C L,Bi Y. 2017. Effects of Oligandrin treatment on dry rot and phenylpropanoid pathway metabolism of potato tubers[J]. Science and Technology of Food Industry,38(6):297-302.] doi:10.13386/j.issn1002-0306.2017.06.056.
劉郵洲,梁雪杰,喬俊卿,劉永鋒,邵明燦. 2017. 梨果貯藏期病害拮抗細(xì)菌的篩選、鑒定和評(píng)價(jià)[J]. 中國(guó)生物防治學(xué)報(bào),33(1):121-127. [Liu Y Z,Liang X J,Qiao J Q,Liu Y F,Shao M C. 2017. Screening,identification and evalua-tion of antagonistic bacteria for the control of pear ring rot and anthracnose during storage[J]. Chinese Journal of Biological Control,33(1):121-127.] doi:10.16409/j.cnki. 2095-039x.2017.01.017.
梅雨薇,楊子云,于樊,龍旭偉. 2020. 生物表面活性劑脂肽的發(fā)酵生產(chǎn)及抑菌應(yīng)用研究進(jìn)展[J]. 中國(guó)生物工程雜志,40(5):105-116. [Mei Y W,Yang Z Y,Yu F,Long X W. 2020. Recent progress on fermentation and antibacterial applications of surfactin[J]. China Biotechnology,40(5):105-116.] doi:10.13523/j.cb.1912023.
牛世全,李渭娟,李海云,惠娜娜,龍洋. 2017. 河西走廊鹽堿土壤中抗馬鈴薯干腐病放線菌的篩選鑒定[J]. 西北師范大學(xué)學(xué)報(bào)(自然科學(xué)版),53(2):94-98. [Niu S Q,Li W J,Li H Y,Hui N N,Long Y. 2017. Screening of Actinomyces on antagonism to Fusariun spp. isolated from saline-alkali soils in Hexi corridor[J]. Journal of Northwest Normal University(Natural Science),53(2):94-98.] doi:10.16783/j.cnki.nwnuz.2017.02.017.
潘曉梅,李昭煜,石曉玲,林勝紅,李佳佳,田永強(qiáng). 2019. 番茄灰霉生防菌XF的篩選、鑒定及生防因子的初步探索[J]. 西北農(nóng)業(yè)學(xué)報(bào),28(11):1888-1895. [Pan X M,Li Z Y,Shi X L,Lin S H,Li J J,Tian Y Q. 2019. Screening,identification and biocontrol effects of antagonistic bacterial strain XF and preliminary exploration of biocontrol factors[J]. Acta Agriculturae Boreali-occideotalis Sinica,28(11):1888-1895.] doi:10.7606/j.issn.1004-1389.2019. 11.018.
任培根,周培瑾. 2003. 中度嗜鹽菌的研究進(jìn)展[J]. 微生物學(xué)報(bào),43(3):427-431. [Ren P G,Zhou P J. 2003. Reseach progress of moderately halophilic eubacteria[J]. Acta Microbiologica Sinica,43(3):427-431.] doi:10.13989/j.cnki.0517-6611.2009.31.005.
沈碩. 2017. 青藏高原察爾汗鹽湖地區(qū)可培養(yǎng)中度嗜鹽菌的群落結(jié)構(gòu)與多樣性[J]. 微生物學(xué)報(bào),57(4):490-499. [Shen S. 2017. Community structure and diversity of culturable moderate halophilic bacteria isolated from Qrhan salt lake on Qinghai-Tibet plateau[J]. Acta Microbiologica Sinica,57(4):490-499.] doi:10.13343/j.cnki.wsxb. 20160232.
沈碩,王艦. 2013. 青海鹽湖地區(qū)嗜鹽菌的分離純化及抑制植物病原菌的活性初探[J]. 廣東農(nóng)業(yè)科學(xué),40(1):79-81. [Shen S,Wang J. 2013. Isolation,petrifaction and inhibitory activity against plant pathogenic fungi of halophilic strains from Qinghai salt lake[J]. Guangdong Agriculture Science,40(1):79-81.] doi:10.16768/j.issn.1004-874x. 2013.01.041.
孫清華,任向宇,馮志文,杜密茹,張若芳. 2019. 貯藏期馬鈴薯干腐病防治藥劑篩選及其安全性評(píng)價(jià)[J]. 中國(guó)馬鈴薯,33(6):364-371. [Sun Q H,Ren X Y,F(xiàn)eng Z W,Du M R,Zhang R F. 2019. Screening and safety evaluation of fungicides for control of potato dry rot during storage[J]. Chinese Potato Journal,33(6):364-371.] doi:10. 3969/j.issn.1672-3635.2019.06.008.
孫現(xiàn)超,彭健芳,張寧,史夢(mèng)蝶,周常勇. 2013. 馬鈴薯干腐病菌拮抗放線菌JY-22的抑菌作用及菌株鑒定[J]. 植物保護(hù)學(xué)報(bào),40(1):38-44. [Sun X C,Peng J F,Zhang N,Shi M D,Zhou C Y. 2013. Inhibitory effect and identification of an antagonistic Actinomyces strain JY-22 against Fusarium solani causing potato dry rot[J]. Journal of Plant Protection,40(1):38-44.] doi:10.13802/j.cnki.zwbhxb. 2013.01.006.
談峰,王瑩,李玉娟. 2021. 1株可提高植物耐鹽能力菌株的分離[J]. 江西農(nóng)業(yè)學(xué)報(bào),33(4):52-58. [Tan F,Wang Y,Li Y J. 2021. Isolation of a strain specific for plant salt tole-rance[J]. Acta Agriculturae Jiangxi,33(4):52-58.] doi:10.19386/j.cnki.jxnyxb.2021.04.09.
王愛軍. 2013. 馬鈴薯干腐病和黑痣病菌拮抗芽孢桿菌的篩選及芽孢桿菌遺傳多樣性研究[D]. 蘭州:甘肅農(nóng)業(yè)大學(xué). [Wang A J. 2013. Screening of antagonistic Bacillus strains against pathogens of Fusarium dry rot and black scurf in potato and its AFLP analysis of genetic[D]. Lanzhou:Gansu Agricultural University.]
王靜,孔凡玉,秦西云,張成省,張秀玉. 2010. 短小芽孢桿菌AR03對(duì)煙草黑脛病菌的拮抗活性及其田間防效[J]. 中國(guó)煙草學(xué)報(bào),16(5):78-81. [Wang J,Kong F Y,Qin X Y,Zhang C S,Zhang X Y. 2010. Inhibition and bio-control activity of Bacillus pumilus AR03 against tobacco black shank[J]. Acta Tobacaria Sinica,16(5):78-81.] doi:10. 3969/j.issn.1004-5708.2010.05.015.
王靜,田華,孔凡玉,王貽鴻,張成省,馮超. 2015. 短小芽孢桿菌AR03對(duì)煙草赤星病菌和白粉病菌的防治[J]. 應(yīng)用生態(tài)學(xué)報(bào),26(10):3167-3173. [Wang J,Tian H,Kong F Y,Wang Y H,Zhang C S,F(xiàn)eng C. 2015. Inhibition of Bacillus pumilus AR03 on Alternaria alternata and Erysipheci choracearum on tobacco[J]. Chinese Journal of Applied Ecology,26(10):3167-3173.] doi:10.13287/j.1001-9332. 20150921.022.
王麗麗,徐韜,李琳,相陽(yáng),魏濤,李克梅. 2016. 馬鈴薯干腐病病菌生物學(xué)特性及室內(nèi)藥劑篩選[J]. 新疆農(nóng)業(yè)大學(xué)學(xué)報(bào),39(3):222-226. [Wang L L,Xu T,Li L,Xiang Y,Wei T,Li K M. 2016. Biological characteristics of the pathogens of the potato dry rot and fungicides selection in laboratory[J]. Journal of Xinjiang Agricultural University,39(3):222-226.] doi:10.3969/j.issn.1007-8614. 2016.03.009.
王錢福. 2007. 嗜鹽菌的分離及其多相分類學(xué)研究[D]. 蘭州:蘭州大學(xué). [Wang Q F. 2007. Studies on isolation and polyphasic taxonomy of halophiles[D]. Lanzhou:Lanzhou University.]
王穎,王玉琴,楊成德,姚玉玲,陳秀蓉,薛莉. 2014. 馬鈴薯貯藏期主要病害拮抗內(nèi)生細(xì)菌的篩選、鑒定及功能評(píng)價(jià)[J]. 草業(yè)學(xué)報(bào),23(3):269-275. [Wang Y,Wang Y Q,Yang C D,Yao Y L,Chen X R,Xue L. 2014. Screening,identification and biological function evaluation of endophytic bacteria against potato storage disease[J]. Acta Prataculturae Sinica,23(3):269-275.] doi:10.11686/cyxb20140332.
王艷紅,曹寧,賈桂燕,余麗蕓,姜巨全. 2017. 中度嗜鹽菌Halobacillus Y5甘氨酸甜菜堿轉(zhuǎn)運(yùn)蛋白o(hù)pu D基因的克隆及功能分析[J]. 中國(guó)生物制品學(xué)雜志,30(3):258-263. [Wang Y H,Cao N,Jia G Y,Yu L Y,Jiang J Q. 2017. Cloning and functional identification of glycine betaine-cholinecarnitine transporter opu D gene from Halobacillus Y5[J]. Chinese Journal of Biologicals,30(3):258-263.] doi:10.13200/j.cnki.cjb.001680.
魏新燕,黃媛媛,黃亞麗,杜克久. 2017. 拮抗灰霉菌的海洋細(xì)菌甲基營(yíng)養(yǎng)型芽胞桿菌的篩選、鑒定及其抑菌活性物質(zhì)的研究[J]. 中國(guó)生物防治學(xué)報(bào),33(5):667-674. [Wei X Y,Huang Y Y,Huang Y L,Du K J. 2017. Screening,identification of antagonistic ocean bacteria Bacillus methylotrophicus and its antimicrobial substances to botrytis cinerea pres[J]. Chinese Journal of Biological Control,33(5):667-674.] doi:10.16409/j.cnki.2095-039x.2017.05. 013.
吳海霞,田志芳. 2020. 銀杏果實(shí)(白果)多糖提取工藝優(yōu)化及其抑菌活性分析[J]. 江蘇農(nóng)業(yè)學(xué)報(bào),36(6):1551-1558. [Wu H X,Tian Z F. 2020. Optimization of extraction technology of polysaccharides from Ginkgo biloba L.Fruit(Ginkgo biloba seed) and antibacterial activity[J]. Jiangsu Journal of Agricultural Sciences,36(6):1551-1558.] doi:10.3969 /j.issn.1000-4440.2020.06.027.
許苗,葉文武,王淑琛,馮慧,鄭小波. 2018. 快速檢測(cè)馬鈴薯干腐病病原接骨木鐮孢的環(huán)介導(dǎo)等溫?cái)U(kuò)增技術(shù)[J]. 植物病理學(xué)報(bào),48(1):55-60. [Xu M,Ye W W,Wang S C,F(xiàn)eng H,Zheng X B. 2018. Rapid diagnosis of potato dry rot caused by Fusarium sambucinum using a loop-mediated isothermal amplification assay[J]. Acta Phytopathologica Sinica,48(1):55-60.] doi:10.13926/j.cnki.apps. 000038.
Bojanowski A,Avis T J,Pelletier S,Tweddell R J. 2013. Mana-gement of potato dry rot[J]. Postharvest Biology and Technology,84:99-109. doi:10.1016/j.postharvbio.2013. 04.008.
Buchanan R E,Gibbons N E. 1999. Bergey’s manual of systematic bacteriology[M]. The 9th Edition. Baltimore:Williams & Wilkins Company.
Chen X Y,Zhang Y Y,F(xiàn)u X C,Li Y,Wang Q. 2016. Isolation and characterization of Bacillus amyloliquefaciens PG12 for the biological control of apple ring rot[J]. Postharvest Biology and Technology,115(1):113-121. doi:10.1016/j.postharvbio.2015.12.021.
Delaplace P,Rojas-Beltran J,F(xiàn)rettinger P,Jardin P D,F(xiàn)auconnier M L. 2008. Oxylipin profile and antioxidant status of potato tubers during extended s torage at room temperature[J]. Plant Physiology and Biochemistry,46(12):1077-1084. doi:10.1016/j.plaphy.2008.09.001.
Gerbore J,Benhamou N,Vallance J,F(xiàn)loch G,Grizard D,Regnault-Roger C,Rey P. 2014. Biological control of plant pathogens:Advantages and limitations seen through the case study of Pythium oligandrum[J]. Environmental Scien-ce and Pollution research,21(7):4847-4860. doi:10. 1007/s 11356-013-1807-6.
Isabel M,Jordi C,Emilio M,Vittorio V. 2015. Cyclic lipopeptide biosynthetic genes and products,and inhibitory acti-vity of plant-associated Bacillus against phytopathogenic bacteria[J]. PLoS One,10(5):e0127738. doi:10.1371/journal.pone.0127738.
Korsten L. 1995. Evaluation of bacterial epiphytes isolated from avocado leaf and fruit surfaces for biocontrol of avocado postharvest diseases[J]. Plant Disease,79(11):1149-1156. doi:10.1094/PD-79-1149.
Krüsemann E J Z,Cremers J W J M,Visser W F,Punter P H,Talhout R. 2017. The sensory difference threshold of menthol odor in flavored tobacco determined by combining sensory and chemical analysis[J]. Chemical Senses,42(3):233-238. doi:10.1093/chemse/bjw123.
Mathabatha E S. 2010. Diversity and industrial potential of hydrolase producing halophilic/halotolerant eubacteria[J]. African Journal of Biotechnology,9(11):1555-1560. doi:10.5897/AJB10.051.
Ramlawi S,Chiu J O,Cloutier A,Avis T J. 2021. Suppression of Fusarium dry rot of potato using beneficial bacterial treatments[J]. Journal of Plant Pathology,103:269-281. doi:10.1007/s42161-020-00731-y.
Recep K,F(xiàn)ikrettin S,Erkol D,Cafer E. 2009. Biological control of the potato dry rot caused by Fusarium species using PGPR strains[J]. Biological Control,50(2):194-198. doi:10.1016/j.biocontrol.2009.04.004.
Ren J,Tong J,Li P H,Huang X Q,Dong P,Ren M Z. 2021. Chitosan is an effective inhibitor against potato dry rot caused by Fusarium oxysporum[J]. Physiological and Molecular Plant Pathology,113(16):101601. doi:10. 1016/J.PMPP.2021.101601.
Romualdo C,Gemma C,Lourdes A M,Rosa B M,Javier C F. 2010. Thiabendazole resistance and mutations in the β-tubulin gene of Penicillium expansum strains isolated from apples and pears with blue mold decay[J]. FEMS Microbiology Letters,297(2):189-195. doi:10.1111/j.1574-6968.2009.01670.x.
Sadfi N,Chérif M,F(xiàn)liss I,Antoun H. 2001. Evaluation of bacterial isolates from salty soils and Bacillus thuringiensis strains for the biocontrol of fusarium rot of potato tubers[J]. Journal of Plant Pathology,83(2):101-117. doi:10. 2307/41998046.
Sadfi N,Chérif M,Hajlaoui M R,Boudabbous A. 2002. Biological control of the potato tubers dry rot caused by Fusarium roseum var. sambucinum under greenhouse,field and storage conditions using Bacillus spp. isolates[J]. Journal of Phytopathology,150(11-12):640-648. doi:10. 1046/j.1439-0434.2002.00811.x.
van den Boogert P H J F,Luttikholt A. 2004. Compatible biological and chemical control systems for Rhizoctonia solani in potato[J]. European Journal of Plant Pathology,110(2):111-118. doi:10.1023/B:EJPP.0000015325.332 99.e0.
Zhang W W,Liang W K,Li C H. 2016. Inhibition of marine Vibrio sp. by pyoverdine from Pseudomonas aeruginosa PA1[J]. Journal of Hazardous Materials,302(2):217-224. doi:10.1016/j.jhazmat.2015.10.003.
(責(zé)任編輯 麻小燕)

