多模態超聲評估甲狀腺微小乳頭狀癌頸部淋巴結轉移的臨床價值
章曉妍 周敏俐 楊江東
甲狀腺微小乳頭狀癌(papillary thyroid microcarcinoma,PTMC)是指腫瘤最大徑≤1 cm的甲狀腺乳頭狀癌(papillary thyroid carcinoma,PTC),其作為一種惰性腫瘤,預后較好[1]。但PTMC常伴有早期頸部淋巴結轉移,并且頸部淋巴結轉移被認為是PTMC局部復發的重要危險因素[2-3]。因此,對于PTMC患者,術前準確評估頸部淋巴結情況有助于臨床選擇合適的手術方式。超聲檢查是評估頸部淋巴結轉移的重要影像學手段之一。PTMC的常規二維超聲征象如微鈣化、不規則邊界等具有預測頸部淋巴結轉移的臨床價值[1,4]。但是其對頸部淋巴結轉移診斷的敏感性較低,約為15%~30%[5]。國內外研究指出結節內的中央血流模式及結節的高彈性值是評估甲狀腺癌的重要指標[6-7]。因此,本研究分析了PTMC的二維超聲圖像、剪切波彈性成像(SWE)及超微血管顯像(SMI)技術模式的超聲特征,探討其與頸部淋巴結轉移的相關性,為臨床術前評估及術后干預提供方案。
1 對象和方法
1.1 對象 選取2017年5月至2019年8月永康市第一人民醫院和浙江大學醫學院附屬第一醫院經術后病理確診的373例PTMC患者(384個病灶)的臨床資料。納入標準:術前行頸部多模態超聲檢查(二維超聲、SMI、SWE);(2)術前結節均行超聲引導下的細針穿刺(FNA)。排除圖像質量不佳及臨床影像資料不完整的29例,最終納入324例患者(355個病灶,永康市第一人民醫院213個,浙江大學醫學院附屬第一醫院142個),其中252例患者進行了頸部中央區淋巴結清掃,72例患者進行了中央區和頸側區淋巴結清掃。本研究經本院醫學倫理委員會審批同意,患者均知情同意。
1.2 方法 使用Toshiba Aplio 500型高分辨率彩色多普勒超聲診斷儀,線陣探頭,頻率為4~15 MHz,配有聲輻射力脈沖VTIQ成像軟件和SMI軟件。
患者仰臥,頸部略墊高,充分暴露頸前區。選擇甲狀腺檢查條件。二維超聲檢查:掃查目標結節,觀察結節超聲特征并記錄結節數目、大小、形態、內部回聲、邊界、是否存在微鈣化等。SMI檢查:二維超聲檢查后行SMI檢查,觀察結節內血流分布情況。SWE檢查:二維超聲檢查后在SWE模式下繪制感興趣區,包含整個結節和周圍組織,測定結節的彈性指數Emean。所有圖像均由2位工作10年以上且能熟練應用上述技術的超聲診斷醫師進行圖像分析,意見不統一時,共同討論得出統一意見。
1.3 分型標準 血流的分型標準參考Kim等[8]半定量方法,對甲狀腺實性結節血流模式進行分型:(1)無血流型:結節內未探及血流信號;(2)周邊型:結節周邊可見血流信號;(3)中央型:結節內可見血流信號;(4)混合型:結節周邊及內部均可見血流信號。
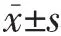
2 結果
2.1 病理檢查結果 經手術病理檢查證實355個PTMC病灶中,144個(59.4%)發生中央區淋巴結轉移,41個(11.5%)發生頸側區淋巴結轉移。
2.2 PTMC二維超聲特征與頸部中央區、頸側區淋巴結轉移相關性的單因素分析 在預測頸部淋巴結轉移的單因素分析中,腫瘤大小、腫瘤位置、微鈣化、邊緣、血流分型模式及Emean均與中央區淋巴結轉移和頸側區淋巴結轉移相關(均P<0.05),見表1。
2.3 PTMC二維超聲特征與頸部中央區、頸側區淋巴結轉移相關性的多因素logistic回歸分析 在多因素回歸分析中,微鈣化、中央型血流及Emean是中央區淋巴結轉移的獨立危險因素;腫瘤大小、腫瘤位置、微鈣化、邊緣、中央型血流及Emean是頸側區淋巴結轉移的獨立危險因素,見表2。
2.4 不同模式對超聲檢查PTMC頸部中央區區淋巴結轉移的預測效能比較 從ROC曲線計算Emean預測中央區淋巴結轉移的最佳截斷值為125 kPa(圖1)。根據最佳截斷值計算不同超聲模式預測頸部中央區淋巴結轉移的效能。與二維超聲模式相比,二維超聲與SWE聯合模式預測中央區淋巴結轉移風險的靈敏度和陰性預測值較高,差異有統計學意義(P<0.05);二維超聲與SMI聯合模式預測中央區淋巴結轉移風險的靈敏度和陽性預測值較高,差異有統計學意義(P<0.05);3者聯合模式的靈敏度、特異度、陰性預測值、陽性預測值均高于其他模式,差異均有統計學意義(均P<0.05)。見表3。
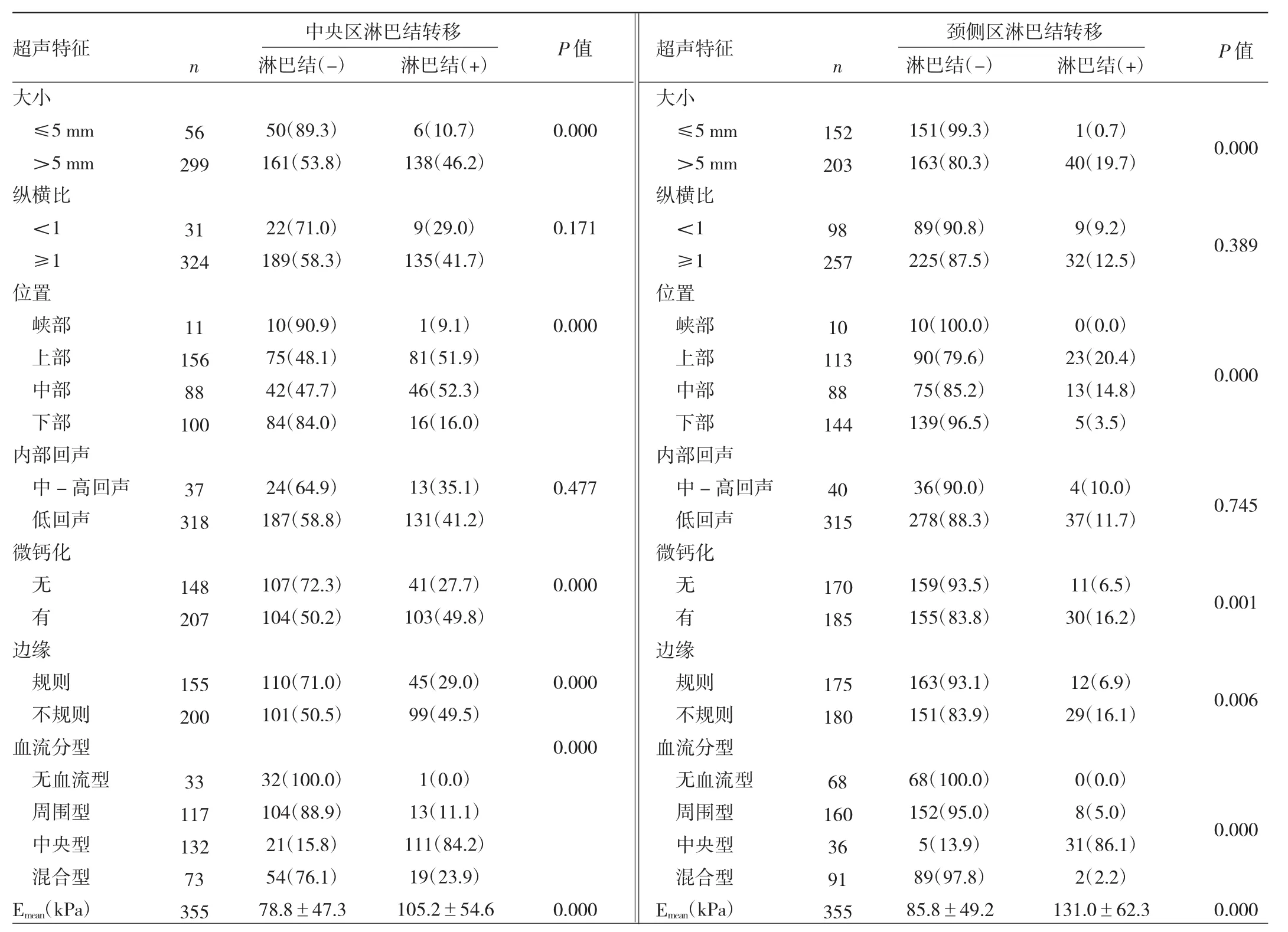
表1 PTMC二維超聲特征與頸部中央區淋巴結轉移、頸側區淋巴結轉移的單因素分析[個(%)]
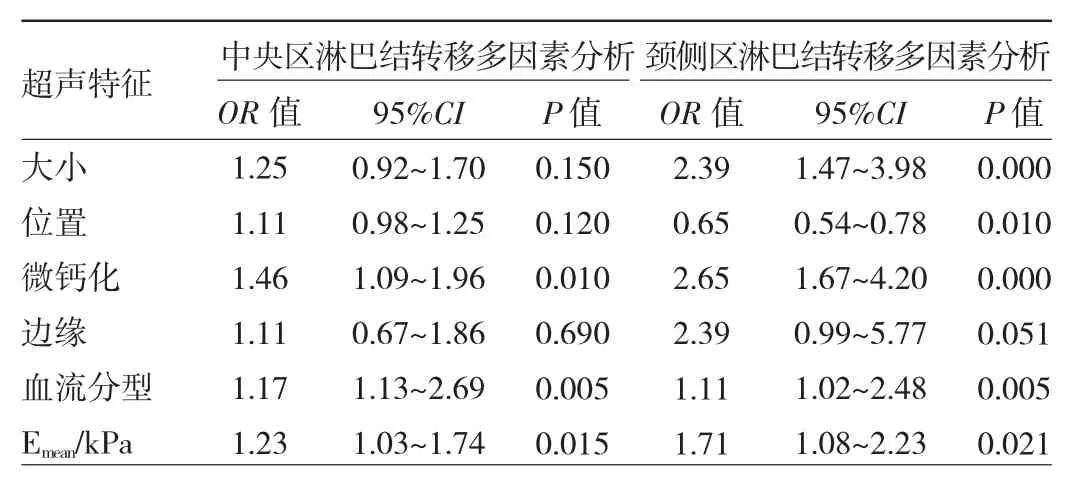
表2 PTMC二維超聲特征與頸部中央區、頸側區淋巴結轉移的多因素logistic回歸分析
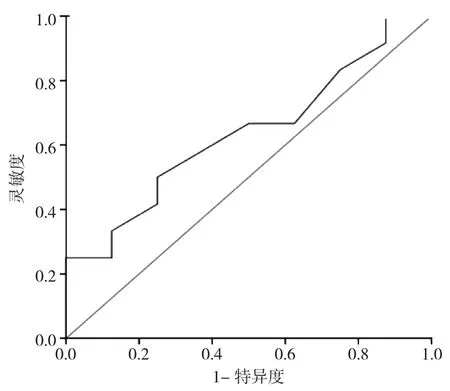
圖1 中央區淋巴結轉移超聲檢查診斷ROC曲線
2.5 不同診斷模式對PTMC頸側區淋巴結轉移的預測效能比較 ROC曲線計算Emean預測頸側區淋巴結轉移的最佳截斷值為129 kPa(圖2)。與二維超聲比較,二維超聲與SWE聯合模式預測頸側區淋巴結轉移風險的靈敏度、特異度、陽性預測值和陰性預測值較高,差異有統計學意義(P<0.05);二維超聲與SMI聯合模式預測頸側區淋巴結轉移風險的靈敏度較高,差異有統計學意義(P<0.05),3者聯合模式的靈敏度、特異度、陰性預測值和陽性預測值均高于其他模式,差異有統計學意義(P<0.05)。見表 4。
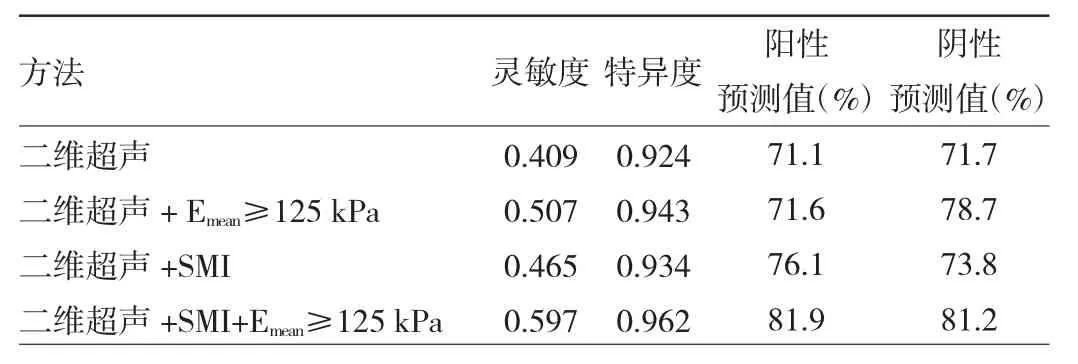
表3 不同診斷模式對PTMC頸部中央區淋巴結轉移的預測效能
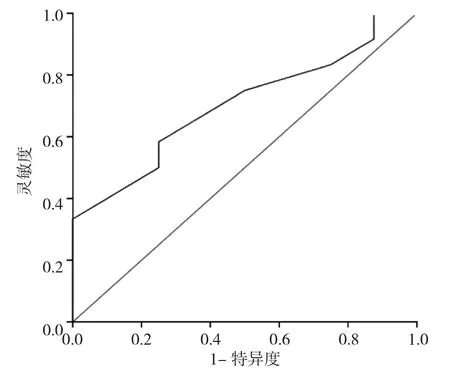
圖2 頸側區淋巴結轉移超聲檢查的ROC曲線
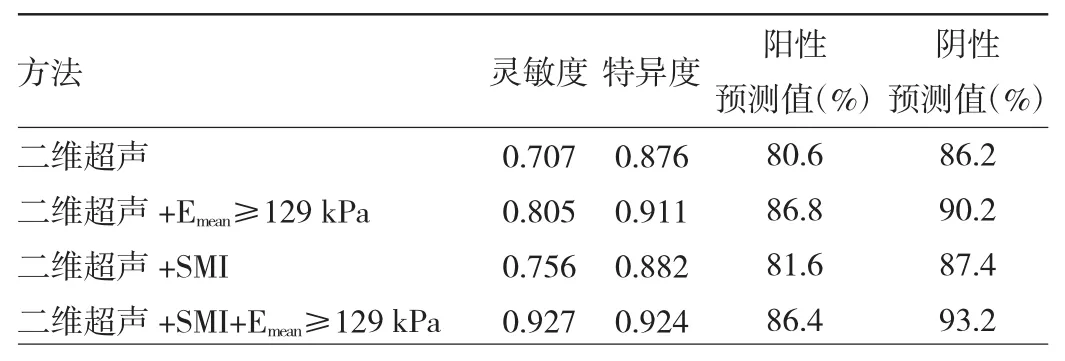
表4 二維超聲、SMI、SWE其聯合模式對PTMC頸側區淋巴結轉移的預測效能
3 討論
近年來,隨著高分率超聲及超聲引導下穿刺活檢技術的廣泛使用,全球甲狀腺癌檢出率呈逐年上升趨勢,尤其是PTMC。盡管PTMC預后較好,但其頸部淋巴結轉移的發病率高達24%~64%。同時,頸部淋巴結轉移也是PTMC患者復發和死亡的重要危險因素。手術切除原發灶及中央區淋巴結清掃是改善患者預后的關鍵。但是對于術前未發現中央區淋巴結轉移的PTMC患者是否常規行頸部中央區淋巴結清掃尚存在較大爭議。2015美國甲狀腺協會(ATA)的指南建議,對于沒有淋巴結轉移的患者,單純的腺葉切除術是安全的。因此準確預測PTMC患者術前頸部淋巴結情況是臨床手術方式及術后管理的重要依據。
超聲檢查是PTMC術前頸部淋巴結情況評估的首選檢查方法。本研究通過對355例PTMC的二維超聲特征進行單因素分析得出腫瘤大小、腫瘤位置、微鈣化、邊緣均與中央區頸部淋巴結轉移和頸側區淋巴結轉移相關,與Wei等[1]研究結果一致。同時本研究多因素回歸分析結果顯示微鈣化是中央區淋巴結轉移的獨立危險因素。Huang等[9]對PTMC術前超聲特診進行多因素回歸分析時同樣得出微鈣化是預測中央區淋巴結轉移的獨立危險因素,與本研究結果一致。對于頸側區淋巴結轉移,本研究得出腫瘤大小、腫瘤位置、微鈣化為其獨立危險因素。同時,本研究依據上述超聲特征分別評估頸部中央區及頸側區淋巴結轉移的預測效能,結果表明,僅依據二維超聲預測頸部淋巴結轉移的靈敏度較低,中央區淋巴結僅為0.409,頸側區淋巴結為0.707,與Park等[5]研究結果一致。
SMI是一種多普勒成像新技術,能夠顯示更多的微血管。本研究采用SMI技術分析PTMC的血流分型模式,并將其納入預測PTMC頸部淋巴結轉移評估指標,結果發現無論是在預測頸部中央區淋巴結轉移還是頸側區淋巴結轉移,中央型血流均是獨立危險因素。二維超聲聯合SMI將預測中央區淋巴結轉移的靈敏度從0.409提升0.465,將預測頸側區淋巴結轉移的靈敏度從0.707提升至0.756。Hong等[10]報道采用CDFI技術檢測的PTC血流分型和淋巴結轉移無相關性,可能的原因是確定血流分型模式采用的技術不同,SMI技術較CDFI技術對微小血管的檢測更敏感。同時,該研究認為超聲造影表現為等或高增強的患者頸部淋巴結轉移率高于低增強的患者。等或高增強的PTC意味著腫瘤組織內部血供較周圍組織血供豐富,腫瘤的生物學行為可能受血供的影響。SMI與超聲造影具有良好的一致性,相較于超聲造影,SMI存在一定的優勢,其無需應用對比劑,耗時短,更適合應用于臨床日常篩查工作中[11-12]。
SWE技術可以有效的反映組織彈性特征。生物力學研究證實甲狀腺惡性結節的彈性值要高于甲狀腺正常實質和良性結節[13]。Jung等[14]報道指出Emean與Emax均可以用于評估PTC中央區淋巴結轉移情況,彈性指數Emean預測PTC中央區淋巴結轉移的準確性高于彈性指數Emax。基于此本研究采用彈性指數Emean預測PTMC頸部淋巴結轉移情況。本研究發現PTMC的高彈性值Emean與中央和頸側區淋巴結轉移獨立相關。與單純二維超聲相比,二維超聲與SWE聯合模式可以提高對頸部淋巴結轉移的預測價值。在預測頸部中央區淋巴結轉移時,二維超聲和SWE聯合模式可將靈敏度由0.409提高到0.507;在預測頸側區淋巴結轉移時,二維超聲和SWE聯合模式可將靈敏度由0.707提高到0.805。Park等[5]在一項包含363例甲狀腺乳頭狀癌的研究中表明剪切波彈性成像可以提高對頸淋巴結轉移的預測能力。張微等[15]研究表明甲狀腺癌超聲彈性指數比值在有淋巴結轉移和無淋巴結轉移中的差異有統計學意義,上述報道均與本研究結果一致。細胞外基質交聯是癌細胞生物學的重要組成部分,與組織纖維化中的組織硬化有關。組織纖維化通過調節可溶因子來影響腫瘤進展,這些可溶因子可誘導炎癥和血管生成,并刺激細胞生長和侵襲[16-17]。依據SWE技術檢測腫瘤組織的的硬度可以反映細胞增殖和纖維化的進展,預測淋巴結轉移。
綜上所述,PTMC表現出中央型血流及高彈性指數的超聲特征是頸部淋巴結轉移的獨立危險因素,與二維超聲聯合使用可以提高淋巴結轉移預測效能。但是本研究仍有些不足之處:(1)本研究為回顧性研究,納入的樣本量較少;(2)本研究對SWE及SMI的檢查存在主觀性,未進行觀察者之間的比較。

