馬波沙星的研究進展
彭文繡
(中國獸醫藥品監察所,北京 100081)
馬波沙星(Marbofloxacin,MBF),又稱麻保沙星,是由瑞士羅氏公司研制開發的一種新型動物專用氟喹諾酮類抗菌藥,具有抗菌譜廣、殺菌活性強、與其他抗菌藥物交叉耐藥少等特點[1]。1995年,該藥首次在英國上市,主要用于貓、犬細菌性疾病的防治[2]。我國于2014年批準該藥為國家二類新獸藥,用于敏感菌所致的犬呼吸道感染。已有文獻主要圍繞MBF在不同動物體內的藥動學特征進行報道[3-9],這些研究表明,MBF內服及腸外給藥后吸收迅速且完全,體內分布廣泛,生物利用度高,提示了該藥在畜禽泌尿道、皮膚及深部組織感染等方面的防治具有巨大潛力。為滿足今后工作需求,促進MBF標準物質的研制,獸醫臨床用藥的規范以及檢驗檢測方法的建立與選擇,本文從MBF的理化性質、合成途徑、作用機制與體外抗菌活性、安全性以及含量或殘留檢測方法等方面進行綜述,以期為我國深入開展其相關研究與應用提供參考。
1 理化性質
MBF化學名為9-氟-2,3-二氫-3-甲基-10-(4-甲基-1-哌嗪基)-7-氧代-7H-吡啶-[3,2,1-ij](4,1,2)苯并噁二嗪-6-羧酸,結構式見圖1,分子式C17H19FN4O4,分子量362.35,為黃色或淡黃色結晶粉末,熔點為268~269 ℃,微溶于水,略溶或微溶于二氯甲烷,極微溶于96%的乙醇[10]。
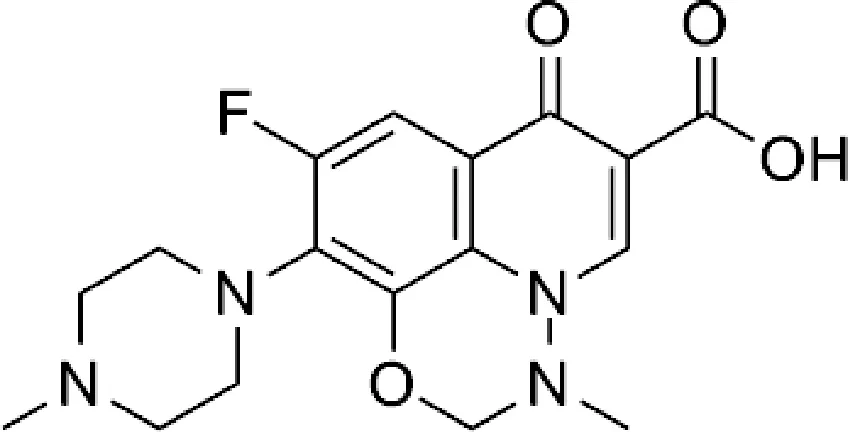
圖1 馬波沙星的化學結構式
2 合成途徑
傳統工藝中以2,3,4,5-四氟苯甲酸為原料,經酰氯化、縮合、水解、環合等9步反應得到目標化合物,總收率為32%[11]。嚴智等[12]進一步改進工藝,將2,3,4,5-四氟苯甲酸酰氯化后產物與3-(N-甲基-甲酰肼基)-丙烯酸乙酯偶聯、環合,再與4-甲基哌嗪縮合、水解、環合,氨水中和,經7步反應制得最終產物,總收率為47.7%。單國洋等[13]以2,3,4,5-四氟苯甲酰氯為起始原料,與3-(4-甲基哌嗪-1-基)-丙烯酸乙酯反應,再與N-甲基甲酰基肼胺化,胺化物再經環合、縮哌、堿解,最后環合得到MBF。該方法安全高效,關鍵步驟可采用一鍋法技術,廢水廢氣排放減少,總收率可提高到51%,所得產物質量符合要求,純度≥99.9%,具有較高的工業化價值。
3 作用機制與體外抗菌活性
MBF是通過抑制細菌DNA回旋酶(又稱II型拓撲異構酶)A亞基活性,阻止細菌DNA的合成和復制而導致細菌死亡。除II型拓撲異構酶外,MBF還對細菌細胞內的IV型拓撲異構酶具有抑制作用[10,14]。這一作用機制不同于其他抗菌藥物,故MBF產生交叉耐藥的可能性很小。
MBF抗菌譜廣,對革蘭氏陽性菌具有較強的抗菌活性,對大多數革蘭氏陰性桿菌和球菌、某些厭氧菌也比較敏感。Josef Bolte等[15]通過研究牛乳腺炎病原體對常用抗生素的敏感性發現,MBF抑制50%與90%克雷伯氏菌屬生長的最低藥物濃度(50% minimun inhibitory concentration, MIC50; 90% minimun inhibitory concentration, MIC90)分別為0.03 μg/mL與0.125 μg/mL,對大腸埃希氏菌的MIC50、MIC90分別為0.03 μg/mL與1.0 μg/mL,明顯低于頭孢喹肟、阿莫西林克拉維酸鉀、磺胺甲噁唑/甲氧芐氨嘧啶的MIC值。A.Bousquet-Melou等[16]對馬臨床分離的病原菌體外抑菌活性進行研究后發現,MBF對腸桿菌科(包括沙門氏菌、大腸埃希氏菌、肺炎桿菌)的MIC范圍為0.008~0.03 μg/mL,MIC90為0.027 μg/mL;對鏈球菌科(包括獸疫鏈球菌、馬鏈球菌)的MIC范圍為0.5~2.0 μg/mL,MIC90為1.667 μg/mL;對金黃色葡萄球菌的MIC范圍和MIC90分別為0.12~0.25 μg/mL、0.21 μg/mL;對銅綠假單孢菌的MIC范圍為0.12~2.0 μg/mL。Aude A.Ferran等[17]報道了MBF對犬源性金黃色葡萄球菌的MIC為0.125 mg/L,假中間葡萄球菌的MIC為0.25 mg/L。M.Grobbel等[18]首次研究了MBF對牛和豬臨床分離的病原體體外抗菌活性(表1),測得其對牛曼氏桿菌、大腸埃希氏菌、支氣管炎博德特菌的活性明顯強于恩諾沙星。Peter Silley等[19]報道了MBF對貓、犬厭氧菌的體外抗菌活性(表2),其活性相當或略強于恩諾沙星、二氟沙星和依巴沙星。岳永波等[20]報道MBF對豬臨床分離病原菌大腸桿菌、金黃色葡萄球菌和鏈球菌均有較低的最小抑菌濃度,其MIC50和MIC90分別為8和64 μg/mL、4和64 μg/mL、1和16 μg/mL,對臨床分離大腸桿菌、金黃色葡萄球菌和鏈球菌的抑菌活性明顯高于諾氟沙星、環丙沙星、慶大霉素和強力霉素,對臨床分離大腸桿菌的抑菌活性高于恩諾沙星。
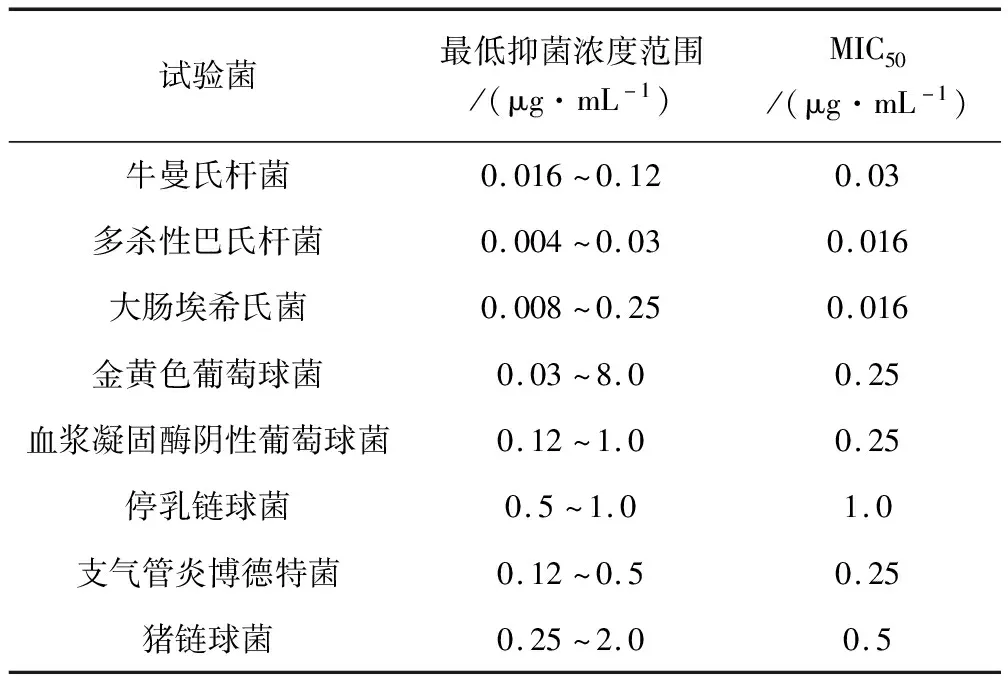
表1 馬波沙星對牛和豬臨床分離的病原菌的體外抗菌活性
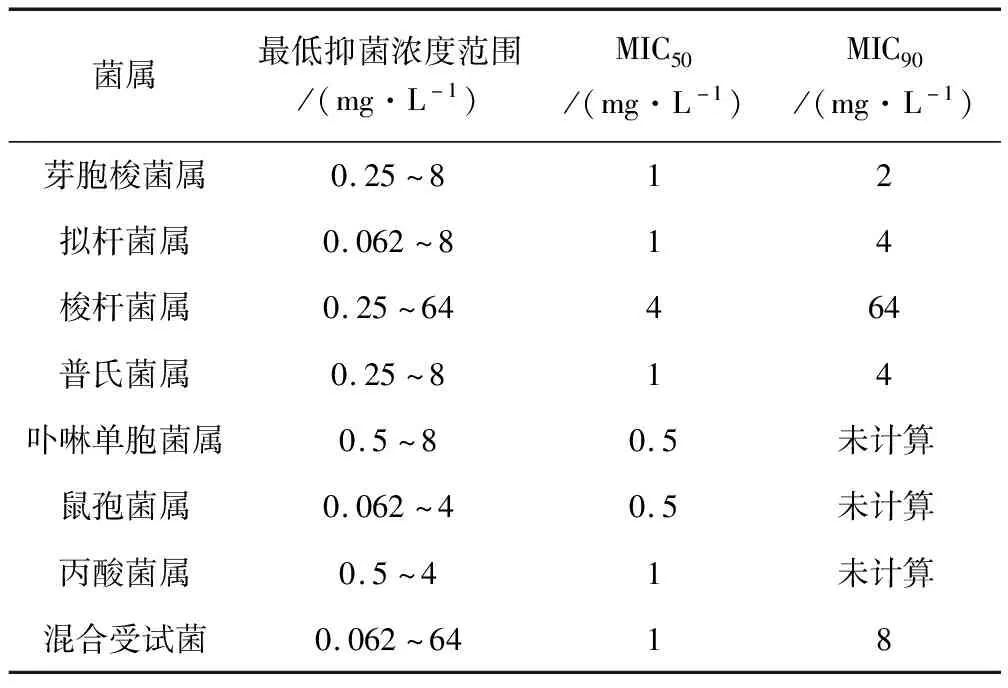
表2 馬波沙星對貓、犬厭氧菌的體外抗菌活性
4 安全性
沈建忠等[21]選用Wistar大鼠和昆明系小鼠對MBF的遺傳毒性進行研究。試驗結果表明,MBF對Wistar大鼠口服半數致死量(median lethal dose,LD50)大于5000 mg/kg,對昆明系小鼠口服 LD50為1000 mg/kg。該藥在抑菌劑量之下對鼠傷寒沙門氏菌無致突變作用;以低、中、高三組劑量(125、250和500 mg/kg)灌胃給藥,小鼠骨髓有微核多染紅細胞率未顯著升高且不會導致因雄性小鼠生殖細胞染色體畸變而造成的早期胚胎死亡。20 mg/kg和100 mg/kg劑量的MBF對母鼠的生殖機能和胎鼠的生長發育無明顯影響,對胎鼠不產生致畸作用,500 mg/kg劑量MBF對胎鼠體長和骨骼發育有一定影響,但不存在劑量反應關系。這些結果表明,MBF無明顯的致突變性和致畸性。
張玲玲等[22]對國產MBF的體外毒性進行了研究,分別對小鼠進行急性經口毒性試驗、急性毒性試驗、精子畸形試驗、骨髓微核試驗和亞慢性毒性試驗。結果顯示,國產MBF經口LD50為887.8 mg/kg,屬低毒物質,精子畸形試驗和骨髓微核試驗結果均為陰性,說明MBF無致突變作用。當按照178、89和18 mg/kg的劑量連續灌胃30 d,小鼠未見死亡,臟器系數、血常規及生化指標較陰性對照組雖有顯著變化,但均在正常值范圍內,國產MBF按推薦劑量使用安全,無致畸和致突變作用。
魏麗娟等[23]評價了MBF注射液在靶動物豬中的安全性。從試驗結果可以看出,使用1~5倍推薦劑量的10% MBF注射液的受試母豬均未出現明顯的臨床癥狀,血常規及生化指標未發生顯著改變,各推薦劑量組對母豬的組織/器官均無明顯影響,在2.5~50.0 mg/kg的劑量范圍內,MBF安全有效。
5 含量或殘留檢測方法
為了客觀、科學地評價MBF在動物體內的消除規律,制定合理的臨床給藥方案以及保證動物源性食品的質量安全,已有研究者建立方法對MBF的藥物含量或殘留進行檢測。
5.1 酶聯免疫檢測法 酶聯免疫法特異性和靈敏度高,不需要昂貴的儀器設備,適用于大量樣品的快速篩選。目前,還未見MBF殘留快速檢測試劑盒上市。已有的研究中[24],以MAR-HRP為異源酶標抗原建立的直接競爭酶聯免疫法,可以同時檢測牛奶中氧氟沙星、MBF、氟羅沙星三種喹諾酮類藥物的含量。若以諾氟沙星為抗體,通過條件優化,抗體包被量為1 μg/mL,酶標抗原稀釋比例為1∶50000,0.5%乳粉作為封閉液,封閉和競爭時間各為30、60 min,建立的諾氟沙星直接競爭酶聯免疫檢測方法,可同時檢測牛奶中包含MBF在內的十六種喹諾酮類藥物的殘留。趙貴山等[25]利用制備的MBF單克隆抗體與稀釋的MBF溶液混合均勻,通過間接競爭法檢測藥物殘留,檢測的MBF濃度范圍為100~5000 pg/mL。該方法制備出針對MBF的特異性強和親和力高的單克隆抗體,為MBF酶聯免疫檢測法的推廣提供了物質基礎。
5.2 熒光分光光度法 MBF核心部分為喹啉,具有較大的共軛結構和剛性,可產生較顯著的熒光,適合采用熒光分光光度法進行測定。該方法具有專屬性強、樣品用量少、操作簡便等特點,常用于微量甚至痕量物質的定量分析。謝軍[26]利用陽離子表面活性劑十六烷基三甲基溴化銨增強MBF體系的熒光強度,在pH 5.0的鹽酸-檸檬酸鈉緩沖液中,以303 nm為最大激發波長、506 nm為最大發射波長測定血液中MBF含量。檢測線性范圍為5.5×10-8~3.0×10-6mol/L,檢測限為4.6×10-8mol/L,相對標準偏差1.5%。
5.3 膠體金免疫層析技術 膠體金免疫層析技術是以膠體金作為示蹤標志物應用于抗原抗體的一種新型的免疫標記技術。它具有使用方便快速,便于基層和現場使用;成本低,不需要特殊的儀器設備;不需要使用有潛在致癌性的酶顯色底物或放射性同位素等優點,適用于藥物殘留的快速篩查。
孫曉崢等[27]將環丙沙星與牛血清白蛋白偶聯制備人工抗原,免疫小鼠后篩選得到特異性單克隆抗體。以純化后的單克隆抗體標記膠體金顆粒作為金標墊,以環丙沙星-牛血清白蛋白偶聯物和兔抗鼠 IgG作為檢測限和質控限,組裝檢測氟喹諾酮類抗生素殘留的膠體金免疫層析試紙條,用于臨床氟喹諾酮類抗生素殘留的快速檢測和大量樣品的篩選。該法特異性強、靈敏度高、廣譜性好、臨床適用性強,肉眼于10 min內即可判定結果。
5.4 超高液相色譜法 超高效液相色譜法的原理與高效液相色譜法基本相同,但其分析速度、靈敏度及分離度高于高效液相色譜,大大縮短了分析時間,減少了溶劑用量,降低了分析成本。趙莉等[28]建立了超高效液相色譜法檢測豬肉中MBF殘留。該方法以氧氟沙星為內標,樣品經三氯甲烷提取后吹干、復溶,正己烷除脂,紫外檢測器檢測,方法的線性范圍為10~1000 μg/kg(r=0.9994),檢出限為5 μg/kg,定量限為10 μg/kg,平均回收率為85.80%~103.20%,其分析速度、靈敏度及分離度分別是高效液相色譜法的9、3、1.7倍。
5.5 高效液相色譜法、高效液相色譜串聯質譜法 高效液相色譜法是檢測此類藥物殘留分析方法中最重要和最基本的方法,液質聯用則有助于提供混合物的相對分子質量與結構信息。賈國賓等[29]建立的高效液相色譜法可測定豬肝臟、肌肉、腎臟、脂肪等組織中MBF的殘留量。惠蕓華等[30]建立的方法可以同時測定水產品中包含MBF在內的9種氟喹諾酮類藥物殘留量。宮小明等[31]優化樣品前處理方法,采用梯度洗脫和程序波長建立了一種能夠同時檢測8種氟喹諾酮類多殘留的高效液相色譜法。這些方法采用的儀器均比較普及,通用性強,可滿足基層檢測需求。錢卓真等[32]建立的水產品中19種喹諾酮類藥物的液相色譜-串聯質譜法,可涵蓋所有用于魚類病害防治的喹諾酮類藥物。該方法用酸化乙腈提取水產品中喹諾酮類藥物,正己烷脫脂,在電噴霧電離源,正離子掃描模式下運用外標法定量檢測。19種藥物的標準曲線線性回歸系數均在0.99以上,線性范圍為2~200 ng/mL,MBF的檢出限為0.5 μg/kg、定量限為1.0 μg/kg,可滿足實驗室批量樣品分析的需求。
6 結 論
從長期積累的經驗以及在畜禽、寵物領域的研究結果可以看出,MBF具有給藥方便,廣譜、低毒、高效等特點,已成為繼恩諾沙星之后,畜禽及寵物疾病領域又一動物專用氟喹諾酮類抗菌新藥[33],在防治動物疾病方面發揮著極為重要的作用。
盡管研究已證實,MBF安全劑量范圍寬,極少引起諸如惡心、嘔吐、腹瀉、痙攣等不良作用[34],且無明顯生殖和遺傳毒性,長期使用,對動物血常規、生化指標、組織/器官形態無顯著影響,但張福濤發現[35],MBF在24 h內能夠以劑量和時間依賴方式引起體外幼齡犬關節軟骨細胞存活率下降,凋亡升高。目前,未見針對這一潛在不良反應所進行的系統性研究,建議后續可開展相關動物試驗,補充完善MBF的安全性資料。
文獻報道的MBF對不同細菌的體外抗菌活性和MIC值對該藥抗菌譜的界定、給藥劑量的選擇具有一定參考價值,有助于臨床獸醫經驗性治療的開展。需要注意的是,隨著藥物長期使用,細菌耐藥性也不斷發生變化,為確保治療安全有效,有條件的地區應定期更新抗菌藥對不同細菌體外抗菌活性的研究資料,或在疾病治療前進行藥敏性試驗,優先選擇有效的窄譜藥物,按照療程規范使用,避免頻繁換藥,以延緩抗菌藥物耐藥性的產生。
有關MBF在動物組織殘留的問題已引起人們的關注,尋找更為方便快捷的檢測方法尤為重要。文獻中,不同研究者建立的含量或殘留檢測方法具有藥物涵蓋范圍廣、操作簡便、靈敏度高的優點,可滿足不同領域、不同層面、不同場合的工作需求,為后續研究奠定基礎。現有公告及《食品安全國家標準 食品中獸藥最大殘留限量》(GB 31650-2019)還未對MBF限量值作出明確規定,有關部門應加快制定完善獸藥殘留檢測的程序和依據,加強MBF的使用監管,促進藥物科學合理應用,進一步保障畜禽養殖業的穩態發展。

