非編碼RNA在索拉非尼治療肝細胞癌耐藥中的作用機制
陳國想, 周 茉, 陳 圣, 王 元, 周元龍, 楊季紅
河北大學附屬醫院 肝膽外科, 河北 保定 071000
肝細胞癌(HCC)是臨床上常見的、最具侵襲性的消化系統惡性腫瘤之一,從全球范圍來看,HCC的發病率在所有惡性腫瘤疾病中位居第6位。由于我國的HBV感染率較高,全世界約50%的HCC發生在我國[1]。由于早期HCC癥狀不典型,患者就診時已經失去最佳手術時機。對于這些患者來說,系統性治療是十分必要的,索拉非尼在控制HCC細胞增殖以及血管生成過程具有重要作用。研究[2]表明,索拉非尼能使晚期HCC患者的中位生存時間延長2~3個月,較高的耐藥率是制約索拉非尼效益的主要原因之一,所以為有效延長晚期HCC患者生存時間,索拉非尼耐藥是目前急需解決的問題。目前研究顯示,非編碼RNA(non-coding RNA ,ncRNA)與索拉非尼耐藥存在相關性,本文將對與HCC索拉非尼耐藥相關的ncRNA進行總結,并對其在索拉非尼耐藥的作用機制進行探討,以期為解決HCC索拉非尼耐藥提供新的思路。
1 ncRNA簡介
人類基因組中有20 000~25 000個基因,但其中98%的基因轉錄產物并不能翻譯出蛋白質,這類轉錄出來的RNA統稱為ncRNA。其中大于200個核苷酸的稱為長鏈非編碼RNA(long noncoding RNA,lncRNA),而目前研究較多的微小RNA(microRNA,miRNA)則屬于短鏈ncRNA[3],過去認為ncRNA在機體中并沒有明確的生物學功能,是基因轉錄過程中的“噪聲”,但隨著近些年的研究,ncRNA在腫瘤疾病中存在的作用逐漸顯現出來,它們作為功能性調節分子,參與各種細胞活動,包括轉錄、翻譯、染色質重塑、基因表達及調控[4]。近期研究[5]發現,ncRNA還參與腫瘤疾病的化療耐藥。如lncRNA H19通過增強多藥耐藥基因1/P-糖蛋白(P-gp)的表達,促進化療藥物外排,來介導肝癌出現阿霉素耐藥;lncRNA HOTAIR通過增加STAT3的水平,促進STAT3磷酸化,使癌細胞將藥物外排能力增強,導致肝癌細胞出現順鉑耐藥[6]。
2 索拉非尼治療HCC中的耐藥機制
索拉非尼通過抑制Raf/MEK/ERK和PI3K/AKT/mTOR信號通路來抑制腫瘤細胞的增殖,從而抑制肝癌的進展。此外,索拉非尼還具有抑制血管內皮生長因子受體和血小板衍生生長因子受體的能力,進一步阻斷腫瘤血管的形成,從而間接抑制腫瘤的生長[7-8]。索拉非尼作為HCC診療指南推薦的晚期HCC的一線治療藥物,能夠延長晚期HCC患者3個月的生存時間,但多數患者在服藥后會出現索拉非尼耐藥。索拉非尼耐藥機制復雜,隨著對ncRNA研究的深入,發現ncRNA對HCC出現索拉非尼耐藥存在調控作用,作為ncRNA的代表,lncRNA及miRNA通過誘導HCC細胞自噬、HCC細胞上皮-間質轉化、激活PI3K/AKT通路、促進肝癌干細胞增殖以及調節腫瘤微環境等生物學活動參與索拉非尼耐藥[9]。
2.1 ncRNA通過誘導HCC細胞自噬導致索拉非尼耐藥
ncRNA在調控HCC細胞自噬方面有著重要作用,ncRNA通過調節相應自噬相關蛋白的表達、激活AKT信號通路,促進HCC細胞自噬,導致HCC細胞出現索拉非尼耐藥。
2.1.1 ncRNA通過調節自噬相關蛋白促進索拉非尼耐藥 細胞自噬是真核生物進化過程中出現的一種依賴自身溶酶體消化自身蛋白質的過程,研究[10-12]發現,自噬是HCC出現耐藥的重要機制之一,ncRNA可以通過調控腫瘤細胞胞內自噬相關蛋白表達,促進HCC細胞保護性自噬,進而導致HCC出現索拉非尼耐藥。研究[13]發現,lncRNA CRNDE在HCC中的高表達能夠使HCC細胞對索拉非尼的敏感性降低,其通過抑制miRNA-543上調自噬相關蛋白ATG4B,促進HCC細胞自噬,導致HCC出現索拉非尼耐藥,通過敲低CRNDE能夠使HCC細胞重新獲得對索拉非尼的敏感性。Jing等[14]發現對索拉非尼耐藥的腫瘤組織中SNHG16普遍高表達,SNHG16已經被證實參與多種腫瘤疾病的發生及發展。在耐索拉非尼的HCC細胞系Hep3B(Hep3B/SO)中,SNGH16通過上調EGR1的表達來抑制miRNA-23b-3p導致自噬相關蛋白LC3-Ⅱ及LC3-Ⅰ表達增多,來促進Hep3B/SO的存活和自噬,在Hep3B/SO中沉默SNHG16可以明顯提高Hep3B/SO對索拉非尼的敏感性。lncRNA NEAT1通過海綿樣吸附miRNA-204 來上調自噬相關蛋白ATG3的表達,NEAT1通過調控miRNA-204/AGT3促進HCC細胞自噬,增強細胞對索拉非尼的耐藥性[15]。而miRNA-142-3p則通過靶向自噬相關基因5(ATG5)和ATG16L1抑制索拉非尼誘導的自噬并使HCC細胞對索拉非尼的敏感性增加。miRNA-142-3p的上調可能是克服HCC細胞索拉非尼耐藥性的有前途的治療措施[16]。由此可見,ncRNA參與調節多種自噬相關蛋白的表達,并通過調節它們來促進HCC細胞的保護性自噬行為,導致HCC細胞出現索拉非尼耐藥。
2.1.2 ncRNA激活AKT通路促進HCC細胞自噬 ncRNA誘導AKT通路激活在HCC細胞出現索拉非尼耐藥中具有重要作用。AKT是一類AGC家族的絲氨酸/蘇氨酸激酶,它在調控細胞生長、增殖、存活、轉錄以及蛋白質合成中發揮著重要作用。研究[17-18]發現過表達的lncRNA SNHG1通過調節SLC3A2(一種溶質轉運蛋白)激活AKT通路,從而參與索拉非尼的耐藥,去除SNHG1可通過抑制AKT通路的激活而增強索拉非尼耐藥HCC細胞凋亡,并且SNHG1受miRNA-21正向調節,miRNA-21可以直接下調PTEN的表達,導致AKT通路的激活,進而調節HCC細胞自噬行為,介導HCC細胞的索拉非尼耐藥。
2.2 ncRNA通過促進HCC細胞增殖導致索拉非尼耐藥
實體腫瘤中存在少量未分化,能夠進行持續分裂的具有多細胞分化能力的細胞,稱為腫瘤干細胞。研究發現,腫瘤干細胞在腫瘤的發生、增殖、復發以及耐藥中均具有重要作用。ncRNA可以與調節腫瘤干細胞的因子結合,激活相關信號通路,促進腫瘤干細胞激活以及增殖,導致HCC對索拉非尼的敏感性降低。研究發現,上皮-間質轉化作為腫瘤惡性行為的標志,不僅有助于細胞遷移,還有助于腫瘤細胞耐藥行為的產生。Van等[19]發現,與上皮性HCC細胞相比,間葉性HCC細胞對索拉非尼的耐藥性更強。
2.2.1 ncRNA促進肝癌干細胞增殖導致索拉非尼耐藥 研究[20]發現,肝癌干細胞在HCC產生耐藥性的過程中起到關鍵作用,lncRNA ROR通過影響肝癌干細胞的生長抑制索拉非尼誘導的HCC細胞凋亡,促進HCC細胞出現索拉非尼耐藥。除此之外,部分ncRNA通過調節以下信號通路來影響肝癌干細胞的增殖,導致HCC細胞出現索拉非尼耐藥。(1)通過活化轉錄激活因子3(signal transducer and activator of transcription 3,STAT3)通路誘導肝癌干細胞增殖。STAT3是STAT家族中的一個功能蛋白,激活后的STAT與胞核中靶基因的轉錄密切相關。lncRNA ARSR通過激活下游的STAT3通路,促進STAT3磷酸化,使HCC中的肝癌干細胞增殖,導致HCC細胞出現索拉非尼耐藥[21]。(2)通過抑制腺嘌呤核苷酸轉運子2(ANT2)及Ras相關的C3肉毒毒素底物1(RAC1)的表達促進誘導HCC出現索拉非尼耐藥。Lu等[22]在研究中發現,ANT2可以誘導Huh7細胞形成肝癌干細胞表型,并且促進HCC轉移及耐藥,miRNA-137表達使Huh7細胞中ANT2蛋白表達下調,抑制Huh7細胞中肝癌干細胞的形成,使耐藥細胞重新獲得對索拉非尼的敏感性。miRNA-194、miRNA-365通過調節RAC1來抑制肝癌干細胞增殖,并且miRNA-194的過表達可以使HCC細胞對索拉非尼更敏感[23-24]。(3)通過調節SOX9信號通路促進肝癌干細胞增殖。SOX9是由SOX9基因編碼的轉錄因子,目前已發現它廣泛參與細胞調節,并且在肺癌、HCC以及乳腺癌中作為癌基因發揮作用。Li等[25]研究發現,表面標志物CD24或OV6陽性的肝癌干細胞中,miRNA-613的表達顯著降低,miRNA-613的表達下調促進HCC細胞的去分化以及促進肝癌干細胞的自我更新。進一步研究發現miRNA-613通過靶向SOX9信號通路抑制HCC細胞去分化及肝癌干細胞增殖,從而使HCC細胞對索拉非尼的敏感性增強。總之,肝癌干細胞在HCC的生長、轉移及耐藥中存在著重要作用,多種ncRNA通過調節肝癌干細胞的增殖調控HCC細胞對索拉非尼的敏感性。
2.2.2 ncRNA誘導HCC細胞上皮-間質轉化過程導致索拉非尼耐藥 上皮-間質轉化是指細胞從上皮細胞通過特定程序向間質細胞轉化的過程,表現為細胞極性消失,細胞間連接能力下降,研究發現,腫瘤細胞上皮-間質轉化過程與腫瘤的轉移、抗凋亡以及出現耐藥存在相關性。
近年來研究者發現ncRNA可以通過以下幾種機制來介導HCC細胞出現索拉非尼耐藥:(1)激活PI3K/AKT及TGFβ通路誘導HCC細胞上皮-間質轉化過程導致HCC索拉非尼耐藥。Zhang等[26]研究發現,lncRNA SNHG3的高表達與HCC細胞的增殖以及耐藥有關,進一步機制研究發現,SNHG3作為內源競爭RNA(ceRNA)參與miRNA-128/CD151反饋環的抑制,并且激活PI3K信號通路,誘導HCC細胞上皮-間質轉化,從而促進HCC細胞的侵襲性以及對索拉非尼的耐藥性;miRNA-93、miRNA-216a/217的過表達對TGFβ通路和PI3K/AKT信號激活的典型通路起正反饋調節作用,并且miRNA-216a/217的過表達參與了PI3K/AKT信號的激活并導致HCC細胞出現對索拉非尼的獲得性耐藥,通過阻斷TGFβ以及PI3K/AKT信號通路的激活則能逆轉miRNA-216a/217誘導的索拉非尼耐藥[27-28]。(2)通過抑制Notch-1通路介導HCC索拉非尼耐藥。Notch-1通路激活促進腫瘤細胞的上皮-間質轉化過程,并誘導腫瘤細胞抗凋亡。研究[29]發現,miRNA-34a表達增加能夠抑制Notch-1通路激活,增加HCC耐藥細胞株對索拉非尼的敏感性; ncRNA通過干擾TGFβ、PI3K/AKT及Notch通路,調節HCC細胞上皮-間質轉化過程,誘導HCC細胞出現索拉非尼耐藥。
2.3 ncRNA通過干擾HCC細胞凋亡調節索拉非尼耐藥 細胞凋亡是一種程序性的細胞死亡過程,阻礙細胞凋亡過程是腫瘤細胞出現耐藥的重要原因,多種ncRNA通過調控以下信號通路阻礙腫瘤細胞的凋亡,從而出現藥物耐藥。研究[30]發現,miRNA-222能夠促進HepG2細胞的增殖、遷移、侵襲及細胞周期的G1/S轉換,并阻礙細胞凋亡,機制研究發現,miRNA-222通過激活PI3K/AKT信號通路,減少細胞凋亡,增強HCC細胞對索拉非尼的耐藥性;miRNA-494通過抑制PTEN的表達,上調PI3K和AKT的表達,從而促進HCC細胞的增殖、遷移和侵襲,增加索拉非尼對HCC細胞的耐藥性[31]。在Fornari等[32]的研究中發現,miRNA-221的過表達與索拉非尼耐藥有關,Casepase-3是細胞凋亡過程中最主要的終末剪切酶,參與細胞的凋亡過程,它通過剪切多聚聚合酶PARP,使其與DNA結合的兩個鋅指結構與羧基端的催化區域分離,調控細胞凋亡過程。miRNA-221通過下調Casepase-3抑制HCC細胞凋亡過程,導致HCC細胞對索拉非尼的敏感性下降。lncRNA NEAT1通過抑制藥物誘導的凋亡增加HCC細胞的索拉非尼耐藥性,NEAT1負向調控miRNA-335,減輕其對c-MET-AKT的抑制作用,從而促進HCC生長[33]。Azumi等[34]在其研究中指出,miRNA-181a通過抑制RAS結合結構域家族成員1(RASSF1),誘導HCC細胞對索拉非尼耐藥。miRNA-34a通過與抗凋亡蛋白Bcl-2 mRNA的3′-UTR結合從而抑制其翻譯,miRNA-34a的表達降低了HCC細胞的存活率,促進了細胞的凋亡,并通過抑制Bcl-2的表達增強了索拉非尼誘導的HCC細胞的凋亡和毒性[35]。Xu等[36]發現,在正常肝臟中表達的miRNA-122在HCC中表達顯著降低,過表達的miRNA-122可以使耐藥細胞對索拉非尼敏感,進一步研究發現,miRNA-122表達減少通過靶向激活胰島素樣生長因子1受體(IGF-1R),激活Ras/RAF/ERK信號通路,導致HCC細胞對索拉非尼耐藥。
2.4 ncRNA調節腫瘤微環境介導索拉非尼耐藥 惡性腫瘤生長迅速,導致腫瘤微環境缺氧,腫瘤內部缺氧是惡性腫瘤的共同特征,也是產生耐藥的重要因素。缺氧誘導轉錄因子-1(HIF-1)是一種轉錄因子,通過調節一系列與血管生成、代謝和細胞增殖相關的基因來介導細胞對缺氧的適應性[37]。HIF-1α是其功能亞單位,研究[38-40]表明,HIF-1α與多種腫瘤的化療耐藥有關。在Xu等[41]的研究中發現,miRNA-338-3p通過抑制HIF-1α,下調其下游的血管內皮生長因子、葡萄糖轉運蛋白-1及P-gp的表達,減少HCC細胞對索拉非尼的外排,抑制HCC細胞生長以及增強HCC細胞對索拉非尼的敏感性。研究[42]發現lincRNA-VLDLR在HCC中顯著高表達,使用索拉非尼后,HCC細胞及其釋放的lincRNA-VLDLR表達增加,進一步研究發現,lincRNA-VLDLR通過調控乳腺癌耐藥蛋白(ABCG2)的表達,促進HCC細胞藥物外排,從而導致HCC出現索拉非尼耐藥。總結相關研究報道多種lncRNA和miRNA參與HCC索拉非尼耐藥詳見表1。

表1 HCC索拉非尼耐藥相關ncRNA
3 總結與展望
越來越多的證據證明ncRNA參與了HCC索拉非尼耐藥,圖1總結了ncRNA在HCC索拉非尼耐藥中的作用機制,靶向調控這些ncRNA可能是逆轉索拉非尼耐藥的一種方法。例如,針對致癌miRNA或腫瘤抑制因子miRNA的合成寡核苷酸進行納米顆粒遞送,或者與調節miRNA的天然藥物一起給藥,已經被作為HCC治療的概念驗證進行了研究[44-45]。Tang等[46]人工設計了針對多種miRNAs的lncRNA 用于治療HCC細胞對索拉非尼的耐藥, 取得了良好效果。靶向ncRNA聯合索拉非尼治療HCC可能是逆轉耐藥和改善晚期HCC患者預后的一種有前途的選擇。而且同一種ncRNA可以從不同的信號通路或者靶點調節HCC細胞索拉非尼耐藥。如miRNA-34a既可以通過抑制Notch-1通路抑制HCC細胞的上皮-間質轉化過程也可以通過與抗凋亡蛋白Bcl-3的3’-UTR結合,從而促進耐索拉非尼的HCC細胞凋亡。眾多ncRNA之間是否存在協同作用,也許在未來能夠成為研究索拉非尼耐藥研究的一個方向。可以看到多種ncRNA通過激活PI3K/AKT通路來介導HCC細胞對索拉非尼耐藥,該信號通路可能是逆轉索拉非尼耐藥的關鍵通路。
另外,聯合用藥也許是克服索拉非尼耐藥的一種途徑,目前免疫治療已經成為腫瘤治療的新方向,Chen等[47]研究發現,在索拉非尼治療后的小鼠模型中,其PD-L1表達增加,使用PD-1受體阻滯劑聯合CXCR4抑制劑和索拉非尼可延緩HCC的生長,但聯合用藥的效果仍需要進一步來證實。盡管將ncRNA作為治療靶標具有良好前景,但基于ncRNA的治療方式尚未進行臨床實踐,并且目前已知的ncRNA可能僅代表HCC中功能相關的ncRNA的一小部分。更好的了解ncRNA介導的HCC出現索拉非尼耐藥的分子機制將為HCC的治療帶來巨大裨益。在基于ncRNA的治療方式成為HCC的治療方法以前,仍有很多挑戰亟待解決,如需要更多的研究來進一步了解及證實ncRNA與索拉非尼耐藥之間的分子機制,如何靶向治療效果好,安全性高、長期治療效果好的ncRNA進行臨床試驗等。雖然目前關于ncRNA與索拉非尼的研究仍停留在體外階段,但ncRNA為逆轉索拉非尼耐藥提供了新的方向,為HCC的治療提供了新的策略。
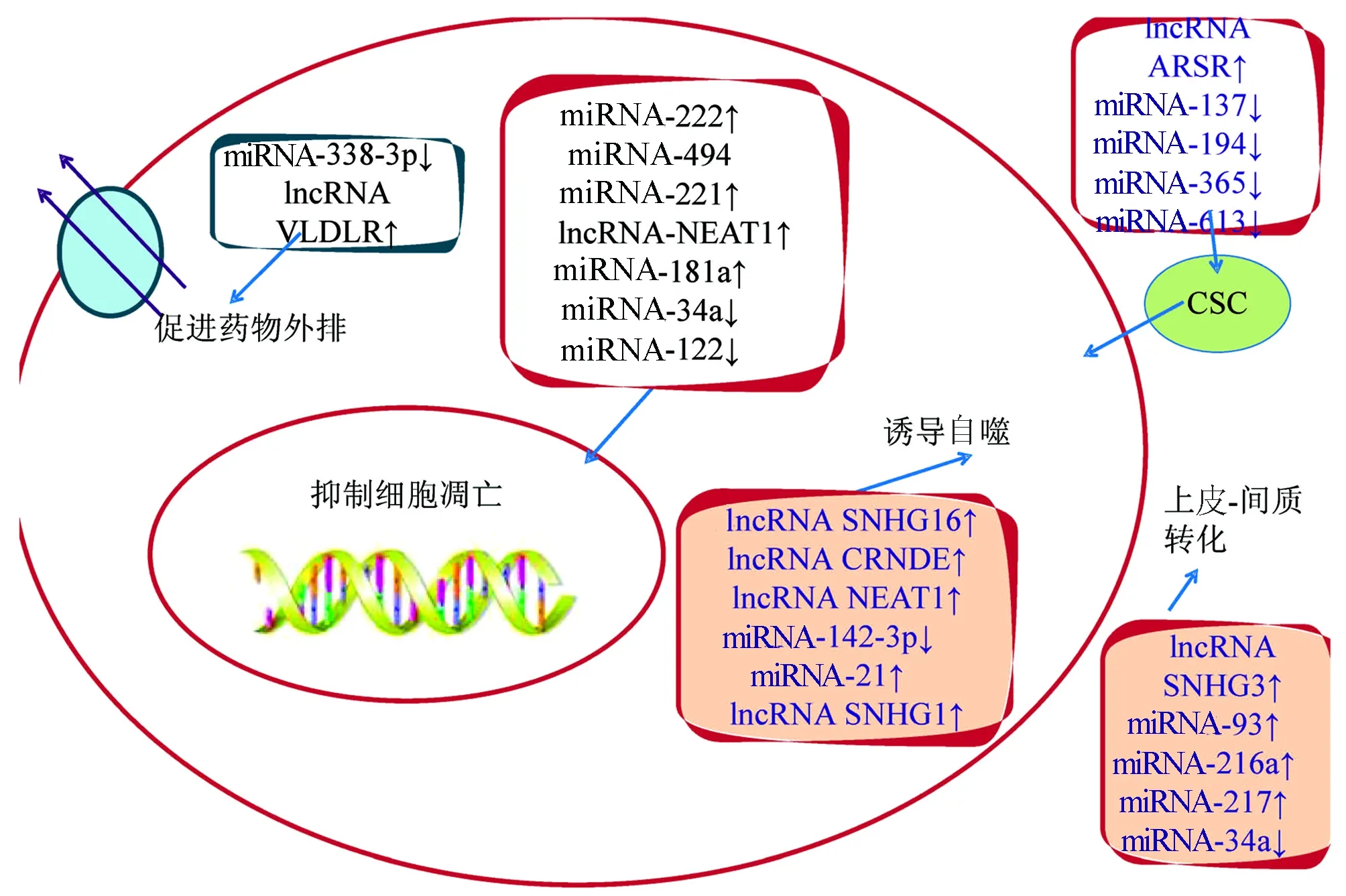
圖1 ncRNA在HCC索拉非尼耐藥中的效應機制
利益沖突聲明:所有作者均聲明不存在利益沖突。
作者貢獻聲明:陳國想、周茉負責查找閱讀及總結文獻,分析資料,撰寫論文;陳圣、王元、周元龍負責指導文章撰寫;楊季紅負責擬定寫作思路,指導撰寫文章并最后定稿。

