不同中藥對NaV1.7離子通道的抑制率比較
申小年 彭俊宇 戴儉華
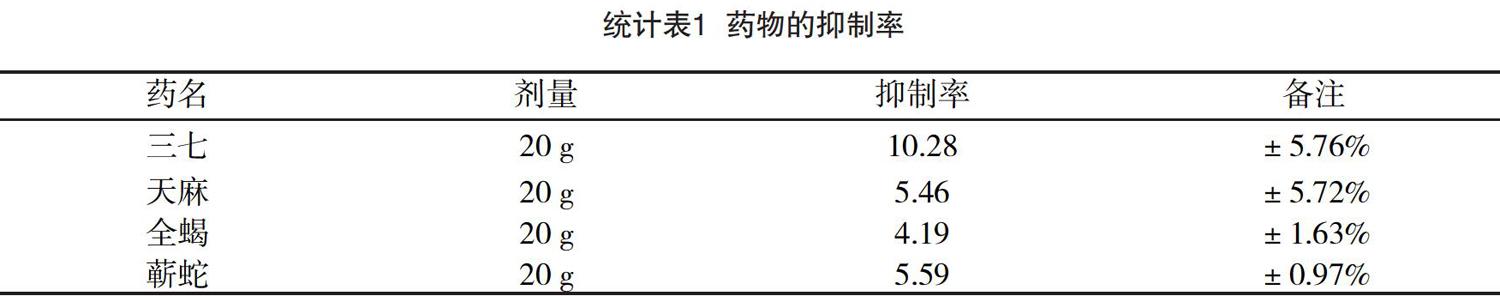
摘? 要:目的? 分別用NaV1.7離子通道測試的常用中藥的抑制率,比較這些常用藥物的療效,為臨床處方治療疼痛提供理論指導。方法? 選擇三七、天麻、全蝎、蘄蛇各20 g,根據2015版中藥藥典通則2201的40 g對應1 000 mL水的方法,冷凝水煎提取。然后過0.22 μm濾膜,使用全細胞膜片鉗技術,研究這些藥物分別對NaV1.7離子通道抑制作用。結果? 抑制率的比較的結果:三七的抑制率最高,臨床有統計學意義。結論 對于臨床骨科常用藥物止痛效果有一定的指導意義。
關鍵詞:疼痛? 膜片鉗? 離子通道? 中藥鎮痛
中圖分類號:R73??????????? 文獻標識碼:A? ???????????? 文章編號:1672-3791(2021)01(a)-0250-03
Comparison of Inhibition Rates of Different Traditional Chinese Medicine on Nav1.7 Ion Channel
SHEN Xiaonian1? PENG Junyu2? DAI Jianhua2
(1.Anhui College of Traditional Chinese Medicine; 2. Anhui Wuhu Hospital of Traditional Chinese Medicine Affiliated to Anhui College of Traditional Chinese Medicine, Wuhu, Anhui Province, 241000 China)
Abstract: Objective The inhibition rates of commonly used traditional Chinese medicines tested with NaV1.7 ion channels were compared, and the therapeutic effects of these commonly used medicines were compared to provide theoretical guidance for the clinical prescription of pain. Methods 20 g each of Panax notoginseng, Gastrodia elata, whole scorpion, and cypris were selected. According to the method of 2015 edition of the General Principles of Chinese Medicine Pharmacopoeia 2201, 40 g corresponded to 1 000 mL of water,condensate decoction extraction. Then through a 0.22 μm filter, using whole-cell patch-clamp technology to study the inhibitory effects of these drugs on NaV1.7 ion channels. Results? The result of the comparison of the inhibition rate: Panax notoginseng has the highest inhibition rate, which is statistically significant. Conclusion It has certain guiding significance for the analgesic effect of commonly used drugs in clinical orthopedics.
Key Words: Pain; Patch clamp; Ion channel; Analgesia with traditional Chinese medicine
疼痛是一種在軀體或內臟組織中產生的具有潛在傷害性或受到有害刺激之后的令人不快的感覺。炎癥和神經性疼痛與急性疼痛不同,如關節炎和偏頭痛,在大部分人身上往往表現出的是持久的慢性狀態,醫療保健費用花費達數十億美金并且造成生產力損失[1]。鈉離子通道的表達異常可能與炎性痛、神經病理性痛和癌痛等多種慢性痛的發病機制相關[2]。電壓門控鈉通道是完整的跨膜蛋白,為興奮性細胞的快速去極化提供電流通路,并且它們在傳遞傷害感受器對背角突觸的反應中起關鍵作用[3]。NaV1.7離子通道主要集中分布于感覺神經的背根神經節和交感神經的神經節中,同時也分布于傷害性刺激密切相關的傳入神經纖維Aβ纖維和C纖維中表達[4]。
近年來,基于幾項顯著的人類遺傳學研究,NaV1.7已成為一種極有研究價值的鎮痛靶點。調控編碼NaV1.7α亞基基因為SCN9A,研究指出SCN9A基因不同位點突變導致了疼痛相關疾病的發生:如紅斑性肢痛癥(Inherited Erythro Melalgia,IEM)、先天性無痛癥(Congenital Insensitivity to Pain,CIP)和陣發性劇痛癥(Paroxysmal Extreme Pain Disorder,PEPD)。特異性NaV1.7阻斷劑是當前靶向鈉通道的鎮痛藥物研發的熱點。
藥物治療為神經病理性疼痛的主要治療方案之一,但不良反應使其在臨床應用中受到一定限制。因此尋找新的藥物治療思路顯得尤為重要。臨床上中醫藥的止痛使用范圍極為廣泛,但是一直沒有一個統一的檢測衡量標準,通過該實驗希望能夠建立一種檢測標準使中藥止痛的療效有一個比較,指導臨床使用中藥。
1? 材料和方法
1.1 水提液的制備
精密稱量三七、天麻、全蝎、蘄蛇各20 g,濃度按40 g藥物/1 000 mL超蒸水進行提取,冷浸60 min,在115 ℃下冷凝提取,熱煮沸60 min,濃縮液約為500 mL。將液袋封放置于冰箱在-20 ℃下儲存冷藏室待用。用時用濾網(0.22 μm)的濾器儲備溶液濃度分別為0.1 g/mL和0.25 g/mL。
1.2 細胞培養
NaV1.7通道穩定表達在人胚腎(HEK 293)細胞上,NaV1.7通道(山東維真生物醫藥科技有限公司,濟南,中國)分別生長于DMEM(DMEM,Gibco,USA),100 U/mL青霉素,100 U/mL鏈霉素和400 μg/mL G418(Sigma-Aldrich,USA)的培養基,且放置在37 ℃,5%CO2培養箱中進行培養。用胰蛋白酶溶液消化細胞,然后在膜片鉗實驗前將細胞接種在無菌玻璃蓋玻片上12~36 h。
1.3 全細胞膜片鉗記錄
用于NaV通道記錄的標準浴液包含:70 mM NaCl、1 mM MgCl2、4 mM CsCl、10 mM葡萄糖、10 mM HEPES、1.8 mM CaCl2、用NaOH將pH調節至7.4,用蔗糖將摩爾滲透壓濃度調節至300 mOsm。用于NaV通道記錄的標準電極內液包含40 mM CsCl、100 mM CsF、2 mM MgCl2、5 mM EGTA、10 mM HEPES,用CsOH將pH調節至7.4,用蔗糖將溶液摩爾滲透壓濃度調節至300 mOsm。
2? 數據分析
使用Clampfit(Axon,USA)軟件對電流進行分析。通過使用非線性回歸方程分析擬合到模式方程的數據(SSPS)。組數據表示為平均值±標準差(),使用單樣本t檢驗統計學比較。P<0.05被認為具有統計學意義。
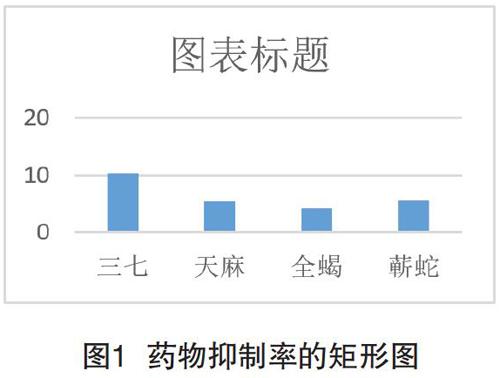
Fig.1.抑制率比較:抑制率均值單樣本t檢驗,(P=0.018),P<0.05。抑制率的比較的結果:三七的抑制率最高,臨床有統計學意義。三七對NaV1.7離子通道的抑制率比天麻、全蝎、蘄蛇更有效。
3? 討論
神經病理性疼痛的病理生理機制復雜,現代研究認為主要是外周敏化(Peripheral Sensitization)和中樞敏化(Central Sensitization)引起疼痛。現在對于神經病理性疼痛的發病機制主要是通過動物模型進行研究。動物實驗為理解人類神經病理性疼痛提供了非常有價值的工具。常見的動物模型有坐骨神經慢性壓迫(Chronic Constriction Injury, CCI)模型、坐骨神經分支選擇損傷(Spared Nerve Injury, SNI)模型、背根神經節慢性壓迫(Chronic Compression of Dorsal Root Ganglion, CCD)模型、坐骨神經部分結扎(Partial Sciatic Nerve Injury, PSNI)模型、脊神經結扎(Spinal Nerve Ligation, SNL)模型。這些動物模型可表現痛覺過敏、痛覺異常以及自發痛等NP癥狀,主要通過機械刺激痛、熱刺激痛和冷刺激痛確定模型是否成功。電壓門控鈉(NaV)通道是完整的跨膜蛋白,為可興奮細胞的快速去極化提供電流通路,并且它們在傳遞傷害感受器對背角突觸的反應中起關鍵作用。特異性NaV1.7阻斷劑是當前靶向鈉通道的鎮痛藥物研發的熱點。通過該研究發現,三七在這幾味中藥中對NaV1.7離子通道抑制率最高,有統計學意義;表明三七比天麻、全蝎和蘄蛇在疼痛的止痛方面更有效果;進一步解釋了三七止痛是抑制了對NaV1.7離子通道的抑制,提供了臨床三七止痛的藥理基礎。還需要進一步研究三七止痛的主要成份和量效關系。
參考文獻
[1]?Steven J McKerrall,DanieL P Sutherlin. Nav1.7 inhibitors for the treatment of chronic pain[J].Bioorganic & Medicinal Chemistry Letters,2018,28(19):3141-3149.
[2]?Waxman SG. Transcriptional channelopathies: an emerging class of disorders[J].Nature Reviews Neuroscience,2017,2(9):652-659.
[3]?Ednard Emery, Ana Paula Luiz, John N Wood. Nav1.7 and other voltage-gated sodium channels as drug targets for pain relief[J].Expert Opin Ther Targets,2016,20(8):975-983.
[4]?Hoeijmakers JGJ, Merkies ISJ, Gerrits MM, et al. Genetic aspects of sodium channelopathy in small fiber neuropathy[J].Clin Genet,2018,82(4):351-358.
[5]?岳子皓.糖皮質激素受體調節鈉離子通道Nav1.7參與神經病理性疼痛[D].鄭州大學,2016.
[6]?宋珍源.電壓門控性鈉離子通道NaV1.7和NaV1.8參與糖尿病大鼠腸道痛覺過敏的外周機制研究[D].蘇州大學,2015.

