伊貝沙坦的合成
應佳妮,王興飛,萬浩芳*
(1.浙江中醫藥大學 中醫藥科學院,浙江 杭州 310051;2.浙江嵐之山科技發展有限公司,浙江 湖州 313200)
隨著老齡化社會的到來,高血壓患者數目呈逐年上升的趨勢。高血壓會帶來包括卒中、心梗等心腦血管并發癥,給社會和家庭造成較重的醫療負擔。伊貝沙坦[1-2]作為一種高選擇性血管緊張素II(Ang II)受體拮抗藥,在治療原發性高血壓上療效顯著,且有治療充血性心力衰竭、左心室肥厚、糖尿病腎病等作用,患者耐受性好,給藥方便,降壓安全、有效、平穩,適合治療老年高血壓患者,符合我國國情,有較好的市場前景。
目前對伊貝沙坦的合成報道較多[3-7]。Kumar等[8]以環戊酮為起始原料,與氰化鈉、氨水反應生成1-氨基環戊腈草酸鹽,再經濃硫酸水解成酰胺后,與正戊酰氯發生脫水關環反應,得到2-丁基-1-二氮雜螺[4.4]壬-1-烯-4-酮,該化合物又與4′-(溴甲基)-2-氰基聯苯偶聯,最后與疊氮化鈉發生疊氮化反應得到伊貝沙坦。本路線中用到劇毒品氰化鈉以及疊氮化鈉,另外使用了大量的濃硫酸進行水解,該工藝產生大量酸性廢水,不符合綠色生產要求。許偉等[9]以環亮氨酸為起始原料,與正戊酰氯進行反應后,再與4-氨甲基-2′-氰基-聯苯進行縮合環化,制得伊貝沙坦中間體,最后再與疊氮化鈉反應獲得伊貝沙坦。該方法避免了氰化鈉的使用,且為伊貝沙坦合成提供了新的思路。但該法中所用原料成本偏高,不利于工業化的生產。
本文在文獻[10-12]方法基礎上,開發了一條以環戊酮為起始原料的合成工藝路線,經氰化、戊酰化、水解、環合、縮合、疊氮化等6步反應最終合成目標產物伊貝沙坦(Scheme 1),其結構經1H NMR、13C NMR和HR-MS(ESI)確證。
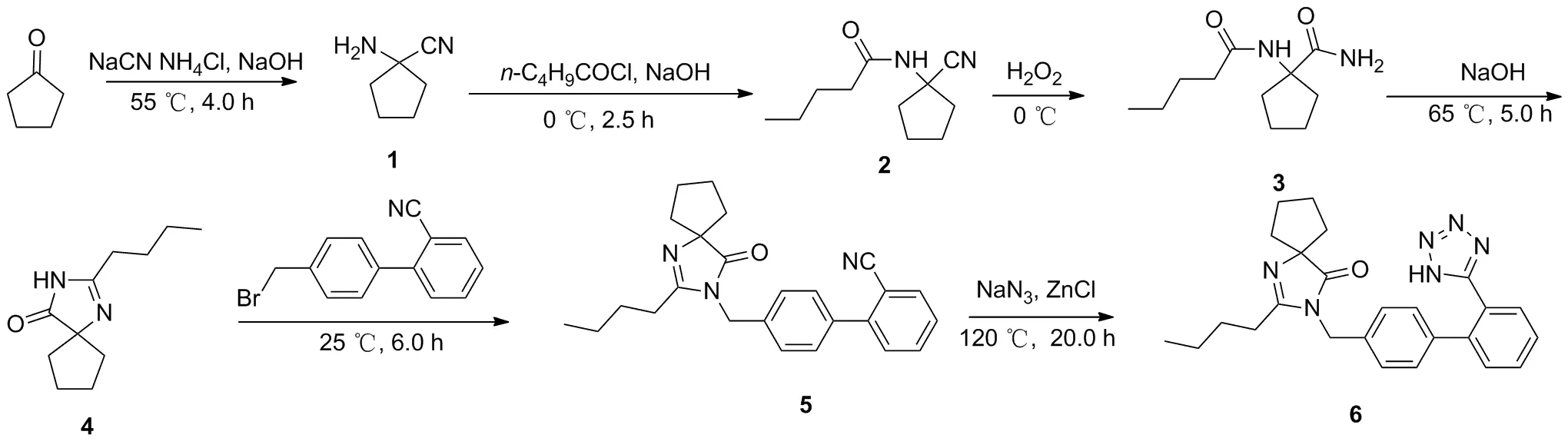
Scheme 1
1 實驗部分
1.1 儀器與試劑
Bruker 500 MHz型核磁共振儀(TMS為內標);Agilent ITQ 110型離子阱質譜儀;Agilent GC-2014 型氣相色譜儀;Agilent 1260型高效液相色譜儀。
氰化鈉,含量98%,安慶市曙光化工股份有限公司;環戊酮,含量>99%,氯化銨,含量99.5%,正戊酰氯,含量98%,上海阿拉丁試劑有限公司;其余所用試劑均為分析純或工業品。
1.2 合成
(1)N-(1-氰基環戊基)戊酰胺(2)的合成
向裝有機械攪拌的三口燒瓶中加入7.9 g(0.161 mol)氰化鈉,9.2 g(0.172 mol)氯化銨和45.0 mL水,攪拌溶解完全后,依次加入60.0 mL甲醇,12.0 g(0.143 mol)環戊酮,12.0 g(0.341 mol)的20%氨水,于45 ℃反應4 h(GC檢測)。分液,用CH2Cl2(2×50 mL)萃取水層,合并有機層,旋干回收溶劑,干燥得淡黃色液體化合物M。在三口燒瓶中加入M和120 mLCH2Cl2,攪拌使其完全溶解,于0 ℃加入16.7 g(0.157 mol)碳酸鈉,緩慢滴加19.0 g(0.157 mol)戊酰氯,滴完,保溫反應2 h(HPLC檢測)。加水淬滅反應,分液,用CH2Cl2(2×50 mL)萃取水層,合并有機層,旋干回收溶劑,干燥得黃棕色油狀液體224 g,HPLC檢測純度97.5%,收率87.0%(以環戊酮計);1H NMR(400 MHz,Chloroform-d)δ:7.52(s,1H),2.37~2.31(m,2H),2.14(dd,J=13.4 Hz,6.7 Hz,2H),1.84(s,3H),1.69~1.56(m,3H),1.36(h,J=7.4 Hz,3H),0.93(t,J=7.5 Hz,4H);13C NMR(101 MHz,Chloroform-d)δ:174.05,121.44,54.80,38.69,35.60,27.61,22.96,22.18,13.70;HR-MS(ESI)m/z:Calcd for C11H18N2ONa{[M+Na]+}217.2623,found 217.2678。
(2) 1-戊酰胺基環戊烷-1-羥酰胺(3)的合成
向裝有機械攪拌的三口燒瓶中加入20 g(0.103 mol)化合物2,1.5 g(0.037 mol)氫氧化鈉,120 mL甲醇,攪拌使其完全溶解,于0 ℃緩慢滴加21.0 g(0.618 mol)雙氧水與20 mL甲醇的混合液,滴畢,保溫反應6 h(HPLC檢測)。分液,用CH2Cl2(2×50 mL)萃取水層,合并有機層,旋干回收溶劑得白色固體320.2 g,HPLC檢測純度98.0%,收率92.5%(以化合物2計),m.p.169~171 ℃(m.p.170~171℃[13]);1H NMR(400 MHz,DMSO-d6)δ:7.79(s,1H),6.89(s,1H),6.74(s,1H),2.15(t,J=7.5 Hz,2H),2.00(dt,J=12.7 Hz,8.0 Hz,2H),1.89~1.76(m,2H),1.60(td,J=8.4 Hz,7.5 Hz,5.0 Hz,4H),1.47(p,J=7.5 Hz,2H),1.27(hept,J=7.8 Hz,7.3 Hz,2H),0.87(t,J=7.4 Hz,3H);13C NMR(101 MHz,DMSO-d6)δ:176.48,172.73,66.46,36.51,35.60,27.74,24.38,22.29,14.24;HR-MS(ESI)m/z:Calcd for C11H20N2O2Na{[M+Na]+}235.2810,found 235.2810。
(3) 2-丁基-1,3-二氮雜螺環[4.4]壬-1-烯-4-酮(4)的合成
向裝有機械攪拌的三口燒瓶中加入20 g(0.094 mol)化合物3,11.3 g(0.282 mol)氫氧化鈉,120 mL甲醇,升溫至65 ℃,保溫反應5 h(HPLC檢測)。旋干回收溶劑,用100 mL水洗滌,分液,用CH2Cl2(2×50 mL)萃取水層,合并有機層,旋干回收溶劑得黃色油狀液體413.9 g,HPLC檢測純度98.5%,收率76.0%(以化合物3計);1H NMR(400 MHz,DMSO-d6)δ:2.80(t,J=7.7 Hz,2H),2.30~1.59(m,11H),1.36(h,J=7.4 Hz,2H),0.92(t,J=7.3 Hz,3H);13C NMR(101 MHz,DMSO-d6)δ:180.10,173.73,72.60,36.99,27.83,27.05,25.44,21.91,13.86;HR-MS(ESI)m/z:Calcd for C11H18N2ONa{[M+Na]+}217.2701,found 217.2678。
(4) 4′-[(2-丁基-4-氧-1,3-二氮雜螺環[4.4]壬-1-烯-3-基)甲基]聯苯-2-甲腈(5)的合成
向裝有機械攪拌的三口燒瓶中加入10.0 g(0.051 mol)化合物4,13.8 g(0.051 mol)4′-(溴甲基)-2-氰基聯苯,0.5 g四丁基溴化銨,6.5 g(0.061 mol)碳酸鈉和100 mL甲苯,升溫至80 ℃,保溫反應6.0 h(HPLC檢測)。加入100 mL水,旋干回收溶劑,分液,用CH2Cl2(2×50 mL)萃取水層,合并有機層,旋干回收溶劑,殘余物用混合溶劑[V(乙酸乙酯)/V(石油醚)=1/6]重結晶得白色固體516.8 g,HPLC檢測純度98.3%,收率85.5%(以化合物4計);m.p.93~95 ℃(m.p.92~93℃[14]);1H NMR(400 MHz,DMSO-d6)δ:7.95(dd,J=7.9 Hz,1.4 Hz,1H),7.79(td,J=78 Hz,1.5 Hz,1H),7.68~7.53(m,4H),7.33(d,J=8.1 Hz,2H),4.79(s,2H),2.37(t,J=7.6 Hz,2H),1.87(q,J=5.3 Hz,4.8 Hz,6H),1.77~1.61(m,2H),1.50(p,J=7.6 Hz,2H),1.35~1.18(m,2H),0.80(t,J=7.4 Hz,3H);13C NMR(101 MHz,DMSO-d6)δ:186.21,161.50,138.25,137.42,134.30,133.96,130.53,129.64,128.71,127.21,110.64,76.35,42.77,37.29,27.98,27.14,25.94,22.01,14.06;HR-MS(ESI)m/z:Calcd for C25H27N3NaO{[M+Na]+}408.4992,found 408.5008。
(5) 伊貝沙坦(6)的合成
向裝有機械攪拌的三口燒瓶中加入15.0 g(0.039 mol)化合物5,5.6 g(0.041 mol)氯化鋅,5.0 g(0.078 mol)疊氮鈉,0.5 g四丁基溴化銨和120 mL二甲苯,與120 ℃保溫反應20.0 h(HPLC檢測)。冷卻至室溫,緩慢滴加20 mL 30%氫氧化鈉溶液,攪拌0.5 h;分液,用水(2×30 mL)萃取有機層,合并水層,緩慢滴加10 %鹽酸至pH=3.5,攪拌0.5 h;加入飽和碳酸鈉溶液至pH=7.5,過濾,濾餅用95%乙醇重結晶得白色固體613.0 g,HPLC檢測純度99.5%,收率78.0%(以化合物5計);m.p.179~181 ℃(m.p.180~181 ℃[14]);1H NMR(400 MHz,DMSO-d6)δ:7.71~ 7.64(m,2H),7.57(dd,J=18.2 Hz,7.4 Hz,2H),7.10(s,4H),2.53~2.47(m,1H),2.30(t,J=7.6 Hz,2H),1.84(d,J=8.0 Hz,6H),1.74~1.61(m,2H),1.49(p,J=7.6 Hz,2H),1.27(h,J=7.4 Hz,2H),0.81(t,J=7.4 Hz,3H);13C NMR(101 MHz,DMSO-d6)δ:155.49,136.79,131.56,131.05,129.73,128.31,126.75,123.95,42.70,37.26,27.93,27.05,25.90,21.98,14.07;HR-MS(ESI)m/z:Calcd for C25H28N6ONa{[M+Na]+}451.5230,found 451.5298。
2 結果與討論
2.1 合成2的反應條件優化
(1) 反應溫度
反應過程中,其他條件同1.2(1),考察不同的反應溫度對酰化反應的影響。該反應為親核取代反應,反應為放熱反應,溫度過高,反應越劇烈,將導致反應過度酰化,溫度過低,反應速度減慢,因此控制合適的溫度有利于反應的正常進行,由表1可知,反應溫度為0 ℃時反應收率最高,因此優選0 ℃為反應溫度。

表 1 反應溫度對收率的影響Table 1 The influences of reaction temperature on yield
(2) 戊酰氯用量
反應過程中,其他條件同1.2(1),考察戊酰氯的用量對反應的影響。反應過程中,當戊酰氯的量較少時,因溶劑以及空氣中有部分水,戊酰氯部分水解,隨著戊酰氯的量增加,將導致反應過度酰化,副產物增加,收率降低,由表2可知,當環戊酮與戊酰氯的物質量比(r)為1.00/1.10時,反應收率最高,因此該反應的最佳摩爾比為1.00/1.10。
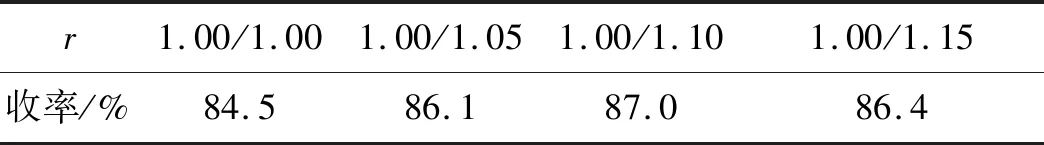
表 2 戊酰氯的量對反應收率的影響Table 2 Effect of the amount of valeryl chloride on the reaction yield
2.2 合成3的反應條件優化
(1) 反應溫度
反應過程中,其他條件同1.2(2),考察不同的反應溫度對水解反應的影響。溫度是該反應的關鍵因素,溫度過高,將導致化合物2過度水解生成羧酸,同時溫度過高將加速雙氧水的分解,因此控制合適的反應溫度有利于提高產物產率及純度。由表3可知,反應溫度為0 ℃時反應收率最高,因此優選0 ℃為反應溫度。

表 3 反應溫度對收率的影響Table 3 The influences of reaction temperature on yield
(2) 雙氧水用量
反應過程中,其他條件同1.2(2),考察雙氧水的用量對反應的影響。由表4可知,當環化合物2與雙氧水的物質量比(r)為1.00/6.00時,反應收率最高。這是因為雙氧水的堿性條件下,雙氧水易分解,當雙氧水量小于6摩爾當量時,反應不完全,產率較低,當雙氧水量過高時,致化合物2進一步水解生成羧酸。

表 4 雙氧水的量對反應收率的影響Table 4 Effect of the amount of valeryl chloride on the reaction yield
2.3 合成化合物5的反應條件優化
反應過程中,其他條件同1.2(4),考察不同的堿對反應的影響,該反應歷程中,每分子原料反應會生成一分子HBr,需要用堿中和生成的HBr加快反應速度,結果見表5。由表5可知,氫氧化鈉,乙醇鈉堿性過強,長時間反應下,易造成化合物4的水解,生成副產物,三乙胺為有機堿,該反應條件下催化效果不明顯,故采用堿性適中,收率較高的碳酸鈉作為縛酸劑。

表 5 堿對5收率的影響Table 5 Effect of base on the yield of 5
2.4 合成6的反應條件優化
(1) 催化劑用量
反應過程中,其他條件同1.2(5),考察不同的催化劑的量對反應的影響,具體結果見表6。由表6可知,當化合物5與氯化鋅的物質量比(r)為1.00/1.05時,反應達到較佳條件,此時繼續增加催化劑用量收率不再有明顯改變,但是催化劑用量低于該值時,收率降低。因此,催化劑投料比r=1.00/1.05為較優的反應條件。

表 6 戊酰氯的量對反應收率的影響Table 6 Effect of the amount of valeryl chloride on the reaction yield
以環戊酮為起始原料,經氰化、戊酰化、水解、環合、縮合、疊氮化反應合成伊貝沙坦,總收率40.7%,純度99.5%。

