SDF-1基因修飾的真皮多能干細胞移植修復脊髓損傷*
鮑全偉,宗兆文,,楊家治,葉 釗,呂明銳,譚 丹△
1.陸軍軍醫大學新橋醫院 急診科(重慶 400037);2.陸軍軍醫大學 衛勤訓練基地戰救技能培訓教研室(重慶 400038)
脊髓損傷(spinal cord injury, SCI)是創傷中較為嚴重的損傷,常伴有較為嚴重的神經功能障礙,嚴重影響患者的功能恢復。目前,對于SCI尚無有效的治療方案,干細胞移植被認為是修復SCI功能損傷最有前景的方法之一[1-2]。研究[3]證實,脊髓中存在神經干細胞(neural stem cells, NSCs),并可參與SCI修復。如何增強內源性NSCs的修復功能,成為SCI修復的策略之一。基質源性因子-1(stromal-derived factor-1, SDF-1)可刺激NSCs遷移,顯示出良好的運用前景[3],但如何局部高效運用尚缺乏有效手段。本研究擬探討SDF-1基因修飾的大鼠真皮多能干細胞(dermal multipotent stem cells, dMSCs)移植后對SCI修復的影響。
1 材料與方法
1.1 實驗動物
Wistar大鼠購自陸軍軍醫大學動物中心[合格證號:SCXK(渝)20170004],動物實驗、尸體處理按照陸軍軍醫大學動物倫理委員會(執行標準SYXK軍2002032)標準實施。
1.2 主要試劑
pAdEasy腺病毒表達載體構建系統由本校解剖教研室董世武博士饋贈,Tripure和DOTAP脂質轉染試劑盒購自瑞士Roche公司。細胞培養用培養基、培養瓶、血清等購自美國Hyclone公司。Transwell細胞培養小室購自美國Costar公司,3H-TdR購自中國科學院上海原子核研究所。兔抗SDF-1一抗、藻紅蛋白(phycoerythrin, PE)和異硫氰酸熒光素(fluoresceine isothiocyanate, FITC)結合的二抗均購自美國Santa-Cruz公司。維甲酸、地塞米松、IBMX、胰島素、吲哚美辛購自美國Sigma-Aldrich公司,免疫組化試劑盒購自美國Boster公司。SDF-1 ELISA試劑盒購自德國Phoenix公司。
1.3 大鼠dMSCs的分離培養
采用前期建立的早期貼壁法分離dMSCs[4]。新生1 d Wistar大鼠,引頸處死,酒精消毒,剪取皮膚置于0.25%胰酶消化過夜。次日,磷酸緩沖鹽溶液(phosphate buffer saline, PBS)清洗后,去除表皮和皮下組織,將真皮組織剪成細胞碎片并吹打成細胞懸液,過濾后接種于培養瓶中。6 h后,棄培養液和懸浮細胞,繼續培養早期貼壁細胞。反復傳代至有集落樣細胞群體生成,按常規方法接種和選取細胞克隆,傳代備用。
1.4 Adv-SDF-1的構建
采用前期建立的方法使用pAdEasy腺病毒表達載體系統構建Adv-SDF-1[4]。Tripure提取大鼠骨髓的總RNA,擴增SDF-1的全長cDNA,然后亞克隆至穿梭質粒pAdTrack-CMV中,再與pAdEasy-1質粒在大腸桿菌BJ5183中進行同源重組產生含有SDF-1的骨架質粒。將驗證正確的骨架質粒用PacⅠ酶切后轉染293 細胞,從而包裝出Adv-SDF-1。然后大量擴增,空斑實驗測定病毒滴度后備用。
1.5 Adv-SDF-1感染dMSCs
向dMSCs 培養基中加入0.2 mL Adv-SDF-1病毒原液,病毒滴度約為2.0×1010PFU/mL,其中PFU為空斑形成單位(plaque-formating unit,PFU)。繼續培養12 h后,采用免疫熒光組織化學檢測SDF-1的表達。加入95%乙醇固定細胞20 min,PBS漂洗加入兔抗SDF-1,4 ℃孵育過夜,PBS漂洗,加入PE結合的熒光二抗,室溫孵育約30 min,PBS,漂洗,4′,6-二脒基-2-苯基吲哚(4,6-diamino-2-phenyl indole, DAPI)復染細胞核,熒光顯微鏡下觀察。此外,按照SDF-1 ELISA試劑盒的說明檢測培養基中SDF-1濃度。
1.6 制備SCI模型及分組
采用改良Allen 重物打擊法制作SCI模型[5]。將麻醉的大鼠俯臥位固定后顯露T10節段的脊髓,用重20 g、打擊頭直徑為2.5 mm的打擊器自2.5 cm高度自由落下,造成T10節段脊髓打擊傷。將損傷后的成年大鼠36只隨機分為Adv-SDF-1感染dMSCs移植組(A組),未感染dMSCs移植組(B組),生理鹽水注射組(C組),每組12只。收集Adv-SDF-1感染和未感染的dMSCs,將密度調整為1×107個/mL,A組大鼠用Hamilton注射器于損傷脊髓上、下各1 mm處注射100 μL Adv-SDF-1感染dMSCs,并保留注射器3 min防止細胞外漏;B組大鼠注射100 μL 未感染的dMSCs;C組大鼠注射100 μL生理鹽水。其中,病毒感染dMSCs的步驟同1.5。為防止膀胱感染,術后每日行人工擠壓膀胱排尿2 次。SCI 3、7 d后,取損傷處脊髓取材后4%甲醛固定,免疫熒光組織化學檢測損傷脊髓中央導水管及其附近的脊髓組織dMSCs的成活及分化情況,Nestin陽性細胞的分布情況。
1.7 行為學檢測
SCI 7 d后參照Ferguson等[6]Basso Beattie Bresnahan(BBB)評分法評定大鼠的功能恢復情況。觀察SCI大鼠早、中、晚期的后肢運動評分,總共分為21個等級,后肢全癱為0分,完全正常為21分。
1.8 統計學方法
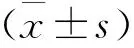
2 結果
2.1 Adv-SDF-1的構建及其感染dMSCs后SDF-1表達的變化
因SDF-1在大鼠骨髓中高水平表達,故選擇從大鼠骨髓中提取RNA擴增SDF-1,然后用pAd Easy腺病毒表達載體系統成功構建了Adv-SDF-1。用其感染dMSCs后,可見dMSCs呈現綠色熒光,而細胞形態未發生明顯改變(圖1A)。免疫熒光組織化學檢測可發現,Adv-SDF-1感染dMSCs后幾乎所有細胞均為SDF-1陽性(紅色熒光),陽性細胞數量多于沒有感染的dMSCs(圖1B、C)。而酶聯免疫吸附測試結果顯示,感染病毒載體的dMSCS培養基中SDF-1的濃度為(23.8±0.58) μg/L,明顯高于對照的(1.35±0.23 ) μg/L,差異有統計學意義(t=16.235,P=0.006)。上述結果提示,Adv-SDF-1感染可上調dMSCs中SDF-1的表達水平,并可分泌到細胞外培養基中。

圖1 Adv-SDF-1感染dMSCs前、后SDF-1表達變化(100×)
2.2 Adv-SDF-1感染的dMSCs移植后dMSCs存活情況
SCI后3 d,可見SCI處DAPI標記陽性dMSCs(圖2A),傷后7 d陽性細胞數量增多(圖2B),提示Adv-SDF-1感染的dMSCs移植后能夠正常存活并增殖。

圖2 Adv-SDF-1感染后dMSCs的存活情況(100×)
2.3 Adv-SDF-1感染后對Nestin陽性細胞的調動及修復作用
3組大鼠功能評估結果顯示,移植細胞后7 d A組(6.70±0.52)分,高于B組(4.30±0.44)分及C組(4.10±0.48)分,差異有統計學意義(tA組VS B組=12.26,tA組VS C組=13.28,P<0.05)。
SCI后3 d,A組大鼠脊髓室管膜細胞Nestin陽性增加,SCI后7 d時其數量繼續增加,中央導水管周圍的脊髓組織內有Nestin陽性細胞,提示其可能是室管膜細胞遷移至損傷組織。而B、C組大鼠SCI后3、7 d在中央導水管及其周圍的脊髓組織均未見到明顯的Nestin陽性細胞(圖3)。

圖3 移植后損傷脊髓中Nestin免疫熒光染色(200×)
3 討論
SCI指外界因素所致的脊髓受損,導致損傷區域的感覺、運動信號的傳導改變,肌張力異常、出現病理反射,可表現為損傷節段以下肢體嚴重功能障礙,嚴重者可累及呼吸、泌尿等系統,甚至危及生命;SCI的治療方法有手術治療及非手術治療,手術治療主要在于手術解除壓迫、內固定穩定脊柱;非手術治療主要在于穩定脊柱、避免并發癥及二次損傷,現有的治療策略主要為減少SCI后的繼發性損傷、應用刺激神經生長的因子和(或)阻斷抑制軸突生長的物質促進軸突的再生、組織或細胞移植重建損傷脊髓的解剖連接、修復損傷的髓鞘和恢復損傷區神經纖維沖動傳導以及促進中樞神經的可塑性變化[1-2]。現有的治療措施對于急性及陳舊性SCI具有一定臨床治療效果,但目前對于SCI后如何促進神經功能恢復,促進神經再生修復尚無有效措施。
近年來, 隨著干細胞技術的不斷發展,應用干細胞治療SCI的臨床研究日益增多。一般認為,脊髓中的NSCs存在于軟膜表面的放射狀膠質細胞和位于中央管的室管膜細胞,且功能有可能不完全相同。目前,常用的內源性神經干細胞的標記有Nestin、Sox-2等,其中以Nestin最常用[7-9],故在本研究中以Nestin 陽性的細胞來代表NSCs。SCI后脊髓白質中Nestin 陽性的細胞可能來源于放射狀膠質細胞,而脊髓灰質中Nestin 陽性的細胞可能來源于中央管的室管膜細胞[7-9]。
SCI發生后,Nestin 陽性細胞可遷移到損傷局部參與損傷修復,但其數量相對有限,如何更多的得到NSCs及使其遷移至損傷部位是本研究的重點。為了提高內源性NSCs的修復效果,一些學者進行了有益的探索。Fan等[7]發現,在SCI局部注射粒細胞-巨噬細胞克隆刺激因子或移植樹突狀細胞可動員脊髓內源性NSCs參與損傷修復;Tashiro等[8]發現,SCI后功能鍛煉可增加損傷脊髓中Nestin陽性細胞的數量,并同功能恢復呈正相關;而Bambakidis等[9]證實,SCI局部注射或靜脈注射音猬因子后,可增加SCI局部內源性NSCs的數量。
研究[4,10-11]發現,SDF-1屬于CXC 族趨化性細胞因子,在脊髓等多種損傷組織局部上調表達,可趨化表達其受體CXCR4的干細胞到損傷局部參與損傷修復。骨髓間充質干細胞、dMSCs和NSCs等多種干細胞均表達SDF-1的唯一受體CXCR4。因此,設想在SCI局部高表達SDF-1進而驅使脊髓本身NSCs向損傷局部遷移而達到脊髓修復的目的。由于具有取材方便、來源豐富、可進行自體移植等特點,皮膚來源的干細胞移植具有神經干細胞和胚胎干細胞等不具備的優勢[12]。目前,已有多種類型的干細胞從皮膚中分離,如dMSCs、真皮纖維母細胞等[12],dMSCs獲得較為方便,因此本實驗運用dMSCs來進行操作。
綜上所述,本研究發現Adv-SDF-1感染dMSCs后SDF-1的表達明顯上調,再將Adv-SDF-1感染的dMSCs移植到大鼠SCI局部, SCI局部高表達SDF-1。SDF-1修飾的dMSCs移植后在SCI局部有更多的NSCs,BBB評分也顯示擁有更好的功能恢復。本研究僅就SDF-1對Nestin陽性細胞的吸引進行了初步觀察,但很多問題仍需要進一步觀察,如基因轉染的安全性和致癌性問題等,將在以后的研究中對這些問題進行深入探討。

