人少突膠質前體細胞移植對腦白質損傷大鼠的保護作用
鐘欣 欒佐 臧靜 管倩 楊印祥 王倩 史源
(1.重慶醫(yī)科大學附屬兒童醫(yī)院新生兒科/國家兒童健康與疾病臨床醫(yī)學研究中心/兒童發(fā)育疾病研究教育部重點實驗室/重慶市干細胞治療工程技術研究中心,重慶 400014;2.解放軍總醫(yī)院第六醫(yī)學中心,北京 100048)
隨著圍生醫(yī)學的發(fā)展,幾乎所有國家的早產率都在上升。不幸的是,早產兒大腦發(fā)育過程特別容易遭受缺氧缺血和炎癥感染,其發(fā)生腦白質損傷(white matter injury, WMI)的風險很高[1]。WMI常導致遠期認知障礙和腦性癱瘓等后遺癥[1],給家庭和社會經濟造成了巨大負擔。腦室周圍白質軟化(periventricular leukomalacia, PVL)是WMI的主要表現形式[2],它干擾少突膠質細胞譜系的發(fā)育[3-4]。然而,目前還沒有針對WMI 治療的特異性方法。
少突膠質前體細胞(oligodendrocyte precursor cells, OPCs)是中樞神經系統(tǒng)少突膠質細胞的前體,在胚胎發(fā)育和出生后早期的神經發(fā)育過程中發(fā)揮著重要作用。髓鞘脫失是PVL 的病理標志,隨著OPCs 向有髓少突膠質細胞的增殖和分化減少而增加[5-6]。越來越多的研究表明,在WMI 中,OPCs 對于潛在的髓鞘重塑活動驅動也發(fā)揮了關鍵作用[7]。此外,實驗室先前的研究表明通過側腦室移植人少突膠質前體細胞(human oligodendrocyte precursor cells, hOPCs)后可對WMI 大鼠模型起神經保護和修復作用,增強髓鞘再生能力,并維持正常的神經功能[8]。因此,hOPCs 具有很大的移植潛力。
通過腦立體定位儀移植細胞到胼胝體和側腦室,或者通過動靜脈注射移植等途徑都是目前干細胞動物實驗中常用的方法。但是將這些干細胞研究轉化為臨床應用,需要改善細胞遞送方式從而避免對腦組織的損傷,同時需要克服中樞神經系統(tǒng)存有血腦屏障的難題。經小腦延髓池注射細胞至蛛網膜下腔的移植方式是非侵入性的,操作簡單方便,不良反應小,可反復操作。細胞可以進入腦脊液,快速彌散于蛛網膜下腔,并且直接接觸腦組織。
本實驗的目的是研究經蛛網膜下腔移植hOPCs 至WMI 大鼠模型是否能促進髓鞘再生和改善其遠期行為能力。
1 材料與方法
1.1 動物
從北京維通利華購買清潔級Sprague-Dawley孕鼠。將孕鼠單獨關在籠子里,自由進食。待產子后,選取生后3 d 的新生大鼠作為實驗對象。根據實驗要求,將新生大鼠隨機分為假手術組、模型組、hOPCs 移植組(移植組),每組10 只,其中雄性大鼠5 只,雌性大鼠5 只,30 日齡時分籠。90 日齡時,進行水迷宮實驗后,每組隨機選取3只大鼠進行電鏡觀察。
1.2 主要試劑
多聚甲醛和牛血清白蛋白(A1992,美國Sigma 公司),兔抗鼠神經節(jié)苷脂(ganglioside,A2B5)抗體(MAB1416,美國R&D Systems 公司),兔抗鼠少突膠質細胞轉錄因子-2(oligodendrocyte transcription factor-2, Olig2)抗體(AB9610,美國Millipore 公司),驢抗兔IgG 488 二抗(AB175649,英國Abcam 公司)。
1.3 細胞培養(yǎng)
本研究中采用的hOPCs 從人類自然流產的11周胎兒腦中分離的神經干細胞誘導分化產生。細胞來源已獲得解放軍總醫(yī)院第六醫(yī)學中心醫(yī)學倫理審查委員會批準(20170812),并在術前與供者簽訂知情同意書。按照文獻所述[9],通過反復的機械分散、離心、分離,將提取的胎兒腦組織分離成單細胞懸液。然后將這些細胞種植到專用的神經干細胞培養(yǎng)基中,誘導其在體外分化得到hOPCs。用hOPCs 特異性標記物A2B5 和Olig2 進行染色,鑒定并檢測細胞純度。細胞移植時,將hOPCs 濃縮在磷酸緩沖0.9%氯化鈉溶液中制成細胞懸液(1.8×106/20 μL PBS)。
1.4 PVL 動物模型的建立
參照文獻建造PVL 動物模型[10-11],將出生后(P)3 d 的大鼠放置在冰上15 min 行冰凍麻醉,待其對有害刺激無反應。大鼠取仰臥位用膠布固定,消毒頸部皮膚。在顯微鏡下沿正中線切開皮膚約0.5 cm,剝離其右側頸總動脈,用電凝筆離斷后,縫合皮膚。建造模型過程中,排除模型組出血過多的大鼠1 只。術后,立即將新生大鼠放回母鼠籠中復溫2 h,然后將幼鼠置于密封的37℃恒溫缺氧箱中,暴露于缺氧(94%N2+6%O2)環(huán)境中2 h。假手術組大鼠僅在冰凍麻醉后游離右側頸總動脈,但不予離斷,也不對其進行缺氧處理。
1.5 細胞移植
給予戊巴比妥(60 mg/kg)腹腔注射麻醉P8 d大鼠,并用立體定位儀將其固定在俯臥位,頭部在水平線下以大約30°的角度彎曲。沿中線切開后頭皮,用鑷子對肌肉進行鈍性分離。在枕骨與寰椎的交界處,暴露出寰枕膜。將寰枕膜晾干,用漢密爾頓進樣針從中間向左側刺穿。觀察到腦脊液流出,以確保針尖位于小腦延髓池內[12]。將20 μL hOPCs 細胞懸液(移植組)或20 μL PBS(模型組及假手術組)緩慢注射到小腦延髓池,此過程大約10 min。然后將針尖停留在蛛網膜下腔內10 min 以防止細胞泄漏。移植期間,大鼠沒有明顯的不良反應。拔針后立即將1 滴0.9%氯化鈉溶液滴于針頭處,以避免移植細胞與腦脊液一起從第四腦室流出。最后縫合皮膚。移植組大鼠無出血、無死亡。移植前3 d 開始對大鼠腹腔注射環(huán)孢素(每日10 mg/kg),直到移植后1 個月。
1.6 行為測試
按照文獻所述方法[13],在移植后第12 周對所有大鼠進行Morris 水迷宮實驗。在實驗中,將大鼠依次緊靠側壁放置在每個象限內。連續(xù)訓練5 d進行定位航行實驗,記錄定位目標平臺所用的總時間(延遲截止時間60 s),評估大鼠的學習能力。在測試的第6 天,進行空間探索實驗,將平臺移出迷宮,測量60 s 內的目標平臺穿越次數、目標象限穿越次數和目標象限停留時間,評估大鼠的遠期記憶功能。
1.7 免疫熒光染色
取狀態(tài)良好的6 孔板培養(yǎng)的hOPCs 進行免疫熒光染色鑒定。hOPCs 用4%多聚甲醛室溫固定5 min,PBS 洗3 次;每孔加入3%BSA 在28~30℃的三氣培養(yǎng)箱中封閉2 h,吸棄封閉液后加入一抗A2B5(1 : 50)和Olig2(1 : 100),于4℃孵育過夜;PBS 洗3 次,每次5 min;加入二抗驢抗兔IgG 488(1 : 500),室溫避光孵育2 h,PBS 洗3 次,每次5 min;DAPI 復 染10 min,PBS 洗3 次,每 次5 min;在熒光顯微鏡下拍照。
1.8 電鏡
移植后第12 周,每組各取3 只大鼠經心臟灌注。從每只鼠右半腦同一位置取總面積為1 mm2的胼胝體樣本。2.5%戊二醛固定30 min,PBS 室溫洗滌3 次。四氧化鋨固定后,用丙酮脫水并包埋在環(huán)氧樹脂中。然后將標本切成70 nm 的超薄切片,再用電鏡觀察軸突的超微結構。通過Image J 軟件,從低倍率圖像(6 000 倍)中隨機選取100個有髓軸突,計算g-ratio(軸突總直徑/纖維總直徑),g-ratio 值越大,說明髓鞘厚度越小[14]。
1.9 統(tǒng)計學分析
采用GraphPad Prism 8 和SPSS 11.0 統(tǒng)計軟件對數據進行統(tǒng)計學分析。計量資料采用均數±標準差()表示。水迷宮定位航行實驗采用重復測量方差分析,同一時間點組間兩兩比較采用LSD-t檢驗。其他結果采用單因素方差分析,組間兩兩比較采用LSD-t檢驗。P<0.05 為差異有統(tǒng)計學意義。
2 結果
2.1 從神經干細胞分化制備hOPCs
采用hOPCs 特異性標記物(Olig2、A2B5)進行免疫熒光染色,驗證移植細胞純度。免疫熒光分析顯示,移植細胞為Olig2+、A2B5+細胞(圖1),陽性百分率分別為92.5%、95.1%,即為hOPCs。該結果表明hOPCs 純度較高,可用于本實驗研究。
2.2 hOPCs 移植對WMI 大鼠神經功能的影響
移植后第12 周對大鼠進行Morris 水迷宮測試。在Morris 水迷宮定位航行實驗中,從第1 天到第5 天,模型組的逃避潛伏期明顯長于假手術組(P<0.05)。但是,與模型組相比,除第2 天外,移植組的逃避潛伏期均縮短(P<0.05)。在水迷宮空間探索實驗中,與假手術組相比,模型組大鼠的目標平臺和目標象限穿越次數均減少,目標象限停留時間縮短(P<0.05)。移植組大鼠的目標象限停留時間長于模型組(P<0.05);模型組與移植組之間的目標平臺和目標象限穿越次數差異均無統(tǒng)計學意義(P>0.05)。這些結果表明,hOPCs 移植在一定程度上減輕了WMI 大鼠的認知功能障礙,改善了神經系統(tǒng)的預后。見表1~2。

圖1 分化培養(yǎng)hOPCs 移植到WMI 大鼠中(免疫熒光染色,×200) 上圖綠色熒光為神經節(jié)苷脂(A2B5)的陽性表達,藍色熒光為DAPI 標記的細胞核;下圖綠色熒光為少突膠質細胞轉錄因子-2(Olig2)的陽性表達;藍色熒光為DAPI 標記的細胞核。
表1 各組大鼠定位航行實驗逃避潛伏期比較 (,s)
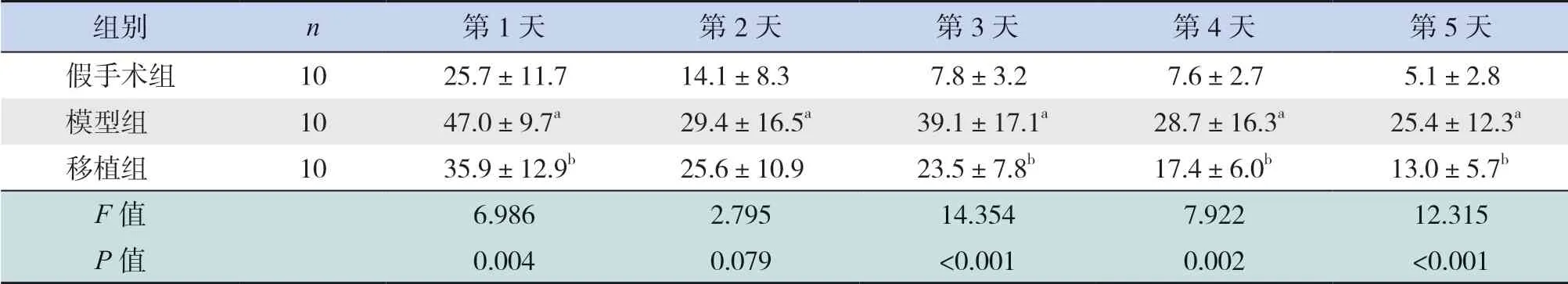
表1 各組大鼠定位航行實驗逃避潛伏期比較 (,s)
注:重復測量方差分析顯示了時間因素差異(F=26.736,P<0.001);分組因素差異(F=13.718,P<0.001);時間因素與分組因素無交互作用(F=1.349,P>0.05)。a 示與假手術組比較,P<0.05;b 示與模型組比較,P<0.05。
組別 n 第1 天 第2 天 第3 天 第4 天 第5 天假手術組 10 25.7±11.7 14.1±8.3 7.8±3.2 7.6±2.7 5.1±2.8模型組 10 47.0±9.7a 29.4±16.5a 39.1±17.1a 28.7±16.3a 25.4±12.3a移植組 10 35.9±12.9b 25.6±10.9 23.5±7.8b 17.4±6.0b 13.0±5.7b F 值 6.986 2.795 14.354 7.922 12.315 P 值 0.004 0.079 <0.001 0.002 <0.001
表2 各組大鼠空間探索實驗測試結果比較 ()
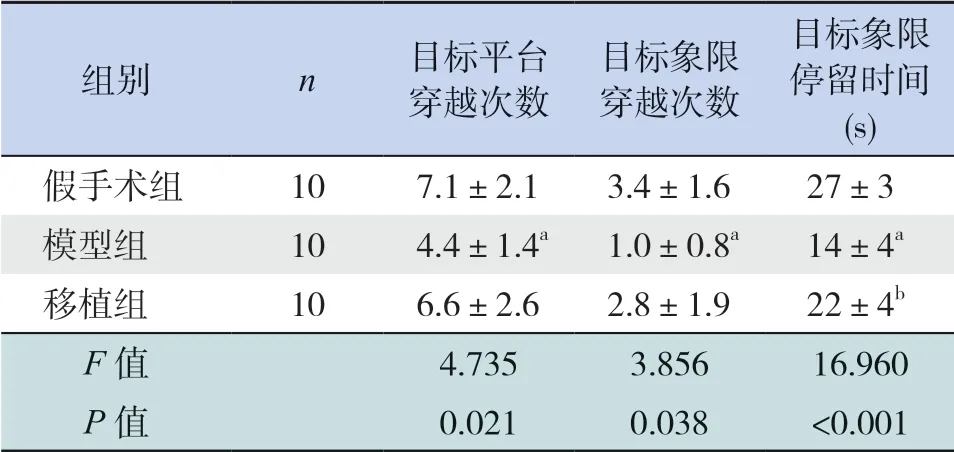
表2 各組大鼠空間探索實驗測試結果比較 ()
注:a 示與假手術組比較,P<0.05;b 示與模型組比較,P<0.05。
目標象限停留時間(s)假手術組 10 7.1±2.1 3.4±1.6 27±3模型組 10 4.4±1.4a 1.0±0.8a 14±4a移植組 10 6.6±2.6 2.8±1.9 22±4b F 值 4.735 3.856 16.960 P 值 0.021 0.038 <0.001組別 n 目標平臺穿越次數目標象限穿越次數
2.3 hOPCs 移植對WMI 大鼠髓鞘再生的影響
為了評估WMI,通過電鏡直接觀察軸突的超微結構(圖2)。模型組髓鞘呈松散、分離和崩解的形態(tài),有髓軸突數量減少;假手術組髓鞘完好,均勻,邊界清晰;移植組部分髓鞘局部分離,結構大致完整,有髓軸突數量增加。各組g-ratio 比較差異有統(tǒng)計學意義(F=153.100,P<0.001)。與假手術組(0.672±0.010)相比,模型組大鼠的g-ratio(0.857±0.020)升高(P<0.05),說明髓鞘厚度減小;與模型組相比,移植組的g-ratio(0.753±0.006)降低(P<0.05),說明髓鞘厚度增加。提示hOPCs 移植促進了WMI 模型大鼠的髓鞘再生。
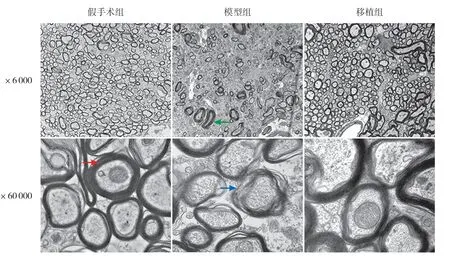
圖2 各組大鼠電鏡下髓鞘形態(tài) 電鏡圖像顯示,模型組髓鞘呈松散、分離和崩解的形態(tài)(藍色箭頭所示),有髓軸突(綠色箭頭所示)數量減少;假手術組髓鞘完好,均勻,邊界清晰,同心圓結構正常(紅色箭頭所示);移植組部分髓鞘局部分離,結構大致完整,有髓軸突數量增加。
3 討論
隨著早產兒的增加,容易引起遠期神經功能損害的WMI 的發(fā)生率也增加。許多研究報道WMI的典型表現是髓鞘脫失和髓鞘再生能力減弱[1]。人類多能干細胞hOPCs 被證明在髓鞘形成和損傷后的髓鞘再生中發(fā)揮關鍵作用。作為一種低侵入性的治療策略,小腦延髓池移植路徑容易應用于臨床。因此,為了探討蛛網膜下腔移植hOPCs 的治療效果,本研究通過小腦延髓池將hOPCs 移植到WMI 大鼠的大腦中,通過行為測試評估大鼠神經功能,并通過電鏡觀察和評估大鼠髓鞘水平。結果顯示,與模型組相比,移植hOPCs 明顯增強了移植組的髓鞘生成,改善了神經功能結局。這些結果提示,采用經蛛網膜下腔進行的hOPCs 移植可能成為將來治療WMI 的新策略。
過去,hOPCs 直接從人類胚胎干細胞誘導而來或使用流式細胞術檢測其特異的表面標記物從供體腦組織中獲得[15-16]。源自人類胚胎干細胞的細胞可能具有很強的致瘤性,而通過免疫分選則需要大量的供體腦組織以獲得足夠數量的細胞。在本實驗室先前的研究中[9],根據細胞分化方案產生了高純度的、特定神經細胞型的hOPCs,且此細胞培養(yǎng)方法具有高穩(wěn)定性和可重復性。考慮將來臨床使用,這些特性是必要的。因此,我們研究了hOPCs 增強髓鞘再生和減輕WMI 后神經功能障礙的能力。
細胞的腦移植有幾種不同的途徑,包括動靜脈注射,腰椎穿刺后鞘內注射,腦實質內和腦室內注射。腦實質內和腦室內注射可直接將細胞移植到病變處,但炎癥微環(huán)境會影響供體細胞的存活,并且有創(chuàng)的移植方式可能會對腦造成進一步損傷從而限制其臨床應用。雖然全身給藥如靜脈和動脈注射是微創(chuàng)的,但移植細胞似乎受到血腦屏障的影響,很難到達腦損傷部位。由于注射部位位于腦脊液循環(huán)的末端,通過腰椎穿刺后的鞘內注射將細胞遞送至目標區(qū)域的移植方式也可能受到限制。有研究報道[12],通過小腦延髓池移植后,大量的間充質干細胞可以遷移至腦實質并開始增殖。此外,也有研究發(fā)現[17],通過小腦延髓池移植的神經球細胞大約有三分之二出現在缺乏髓鞘纖維的區(qū)域。所以我們設想,炎癥微環(huán)境可能促進移植細胞遷移到受損的腦組織,即我們注射到蛛網膜下腔的hOPCs 可以選擇性地進入到腦缺血區(qū)域。小腦延髓池穿刺是臨床上用于腦脊液檢查的常規(guī)醫(yī)療程序,操作簡單、方便、安全。在臨床應用中,移植手術應由經驗豐富的醫(yī)生進行,以避免手術失誤造成損傷。
作為一種新的移植策略,通過小腦延髓池遞送細胞方式的有效性在本研究中得到了驗證。本研究結果顯示,與模型組大鼠相比,經蛛網膜下腔移植的hOPCs 促進了移植組大鼠認知功能的改善,與假手術組相比無明顯差別。此外,電鏡結果顯示,與模型組大鼠相比,通過小腦延髓池進行hOPCs 移植的大鼠髓鞘再生能力增強。同時,與假手術組相比,移植組g-ratio 也無明顯差異。這與先前報道的關于hOPCs 移植的效果相當[8,18]。
研究報道,hOPCs 在移植后通過分化成少突膠質細胞,促進髓鞘形成和改善神經功能預后[18]。但是,其他研究表明,移植的hOPCs 可以通過獨立于靶細胞分化的機制,對神經元和少突膠質細胞產生保護作用[19-20]。然而,移植的hOPCs 在體內遷移分化的情況和其改善行為功能的機制尚不清楚,有待于進一步的研究。

