冠心病患者CYP2C19基因多態(tài)性及臨床不良事件發(fā)生與氯吡格雷抵抗的關(guān)系*
郭元元,王麗英,張 宇,張文佳,廖 璞
中國科學(xué)院大學(xué)重慶醫(yī)院/重慶市人民醫(yī)院檢驗科,重慶 400014
氯吡格雷是常用于治療心血管疾病的抵抗血小板聚集的藥物,是二磷酸腺苷(ADP)受體拮抗劑,通過抑制ADP對血小板的誘導(dǎo)作用產(chǎn)生抗凝作用。氯吡格雷對于經(jīng)皮冠狀動脈介入治療(PCI)和急性冠狀動脈綜合征(ACS)的抗栓治療具有極為明顯的療效,但由于患者之間存在個體差異,血小板對氯吡格雷的反應(yīng)不同,對氯吡格雷缺乏反應(yīng)或反應(yīng)降低,稱之為氯吡格雷抵抗,也稱氯吡格雷無反應(yīng)、氯吡格雷低反應(yīng)等[1-2]。研究表明,氯吡格雷抵抗與遺傳因素、吸煙、年齡、糖尿病、高血壓等多種因素有關(guān),而且對氯吡格雷反應(yīng)較低的患者發(fā)生心血管不良事件的概率比反應(yīng)高的患者更高[3-4]。為了進一步深入探討氯吡格雷抵抗發(fā)生、發(fā)展的原因,本研究通過分析本院PCI術(shù)后冠心病患者的CYP2C19基因型、臨床相關(guān)危險因素和主要心血管不良事件發(fā)生情況對氯吡格雷抵抗的影響,為臨床治療提供有效依據(jù)。
1 資料與方法
1.1一般資料 收集2017年1月至2018年12月本院收治并進行過基因檢測的346例冠心病患者資料,分析其CYP2C19基因型和代謝型分布特征,最終篩選出251例患者做進一步分析。納入標準:(1)經(jīng)冠狀動脈造影確診為冠心病,且已行PCI術(shù)。(2)已完成人CYP2C19基因分型檢測(熒光PCR法)。(3)服用標準劑量(100 mg/d)阿司匹林,服用氯吡格雷75 mg/d抗血小板治療,持續(xù)用藥至少3 d,3 d后進行血小板聚集率檢查。排除標準:(1)對阿司匹林或氯吡格雷有禁忌。(2)病歷資料不完善。(3)經(jīng)冠狀動脈造影術(shù)證實不需行PCI術(shù)。(4)患有嚴重肝、腎疾病或凝血功能障礙。(5)貧血[血紅蛋白(Hb)水平<100 g/L],有出血史。(6)使用過西洛他唑或替格瑞洛等新型抗血小板藥物。
1.2儀器與試劑 血液基因組DNA提取試劑盒(潮州凱普生物化學(xué)有限公司)、CYP2C19基因分型檢測試劑盒(熒光PCR法)(蘇州曠遠生物分子技術(shù)有限公司);實時熒光擴增儀(7500 Real Time PCR System、7300 Plus Real-Time PCR System,美國ABI)、PL-Ⅱ血小板功能分析儀(江蘇英諾華醫(yī)療技術(shù)有限公司)、高速離心機、掌式離心機、漩渦振蕩器、恒溫金屬浴鍋。
1.3方法
1.3.1血小板聚集功能試驗 采用枸櫞酸鈉雙層真空采血管采血3~5 mL,采用連續(xù)計數(shù)法進行血小板聚集功能的檢測,將血液標本顛倒混勻后,檢測血小板計數(shù)、平均血小板體積等參數(shù)(血小板聚集前),然后儀器自動對血液標本加入40 μL誘聚劑誘導(dǎo)血小板聚集,并混勻,隨后繼續(xù)對血液標本中的血小板計數(shù)、平均血小板體積等參數(shù)進行連續(xù)檢測,最終比較血液標本加入誘聚劑前后標本中血小板參數(shù)變化,從而得到誘聚劑對血小板聚集水平影響的相關(guān)指標。
1.3.2基因組DNA的提取 血液采集和處理:采集靜脈血2~3 mL加至含乙二胺四乙酸二鉀(EDTA-K2)的紫色管中,不可用肝素抗凝全血,并充分搖勻,避免溶血或凝血,血液標本采集后應(yīng)立即送檢(如需存放可在8 ℃存放7 d以內(nèi))。按照試劑盒說明書,提取基因組DNA,未能及時檢測的DNA樣品于—20 ℃保存,保存時間不超過6個月。DNA水平應(yīng)為10~100 ng/μL,不能低于10 ng/μL;DNA的A260/A280值必須為1.7~2.0。
1.3.3采用熒光PCR法進行CYP2C19基因分型檢測 操作流程:PCR反應(yīng)體系配制、設(shè)置PCR程序、上機檢測、分析結(jié)果。PCR程序設(shè)置:(1)37 ℃2 min去污染;(2)95 ℃3 min預(yù)變性;(3)95 ℃30 s,56 ℃30 s,65 ℃45 s,10個擴增循環(huán);(4)95 ℃30 s,56 ℃30 s※,65 ℃45 s,30個擴增循環(huán),設(shè)置FAM和ROX雙通道采集熒光信號,其中“※”為信號采集點;(5)25 ℃ 1 min程序結(jié)束,機器冷卻至室溫。按照試劑盒說明書進行結(jié)果分析,此試劑盒檢測位點覆蓋CYP2C19基因*1(野生型)、*2(c.681G>A)和*3(c.636G>A),不包括*17位點。
1.4氯吡格雷抵抗定義 目前,國際上對于氯吡格雷抵抗尚無統(tǒng)一標準,不同的研究所采用的標準大多是根據(jù)經(jīng)驗得來的。有人將氯吡格雷抵抗定義為ADP誘導(dǎo)的血小板聚集率>50%,≤50%則為氯吡格雷敏感[5],但也有研究將血小板聚集率>46%或>70%等定義為氯吡格雷抵抗[6],從本研究的方法和臨床實用性考慮,本研究將臨界值定為血小板最大聚集率(MAR)50%,MAR≥50%則判定為氯吡格雷抵抗。
1.5觀察指標 (1)分析346例患者的CYP2C19基因型和代謝型分布特征。代謝型分為快代謝型(*1/*1)、中代謝型(*1/*2、*1/*3)、慢代謝型(*2/*2、*2/*3、*3/*3)。(2)比較最終入選的251例患者中不同CYP2C19代謝型患者的MAR。(3)將最終入選的251例患者,按照MAR進行進一步分組,MAR≥50%的患者納入氯吡格雷抵抗組,MAR<50%的患者納入氯吡格雷敏感組,比較氯吡格雷抵抗組與氯吡格雷敏感組不同代謝型的患者比例。(4)比較氯吡格雷抵抗組與氯吡格雷敏感組的患者年齡、性別比例,以及吸煙、糖尿病、高血脂、高血壓患者比例。(5)比較氯吡格雷抵抗組與氯吡格雷敏感組的臨床心血管不良事件發(fā)生情況,臨床心血管不良事件包括支架內(nèi)再狹窄、心源性疾病、心肌梗死、心絞痛。
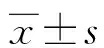
2 結(jié) 果
2.1CYP2C19基因型和代謝型分布 346例患者CYP2C19基因檢測結(jié)果顯示,CYP2C19基因型*1/*1有136例(39.3%),*1/*2有144例(41.6%),*1/*3有22例(6.4%),*2/*2有36例(10.4%),*2/*3有8例(2.3%),未檢測到*3/*3;代謝型分別為快代謝型136例(39.3%),中代謝型166例(48.0%),慢代謝型44例(12.7%)。
2.2不同CYP2C19代謝型患者的MAR比較 慢代謝型、中代謝型、快代謝型患者的MAR分別為(62.9±7.8)%、(48.7±6.5)%、(43.9±9.1)%,慢代謝型患者的MAR較中代謝型、快代謝型的MAR高,差異均有統(tǒng)計學(xué)意義(t=10.6、15.3,P<0.05)。
2.3CYP2C19代謝型與氯吡格雷抵抗的關(guān)系 入選的251例患者檢測出MAR≥50%的患者110 例(氯吡格雷抵抗組),MAR<50%的患者141例(氯吡格雷敏感組)。氯吡格雷抵抗組與氯吡格雷敏感組在快代謝型中的患者比例差異有統(tǒng)計學(xué)意義(χ2=4.741,P=0.029)。見表1。

表1 CYP2C19代謝型與氯吡格雷抵抗的關(guān)系[n(%)]
2.4兩組臨床相關(guān)危險因素比較 氯吡格雷抵抗組的患者年齡、男性比例,以及吸煙、糖尿病、高血脂患者比例與氯吡格雷敏感組比較,差異均無統(tǒng)計學(xué)意義(P>0.05),氯吡格雷抵抗組的高血壓患者比例與氯吡格雷敏感組比較,差異有統(tǒng)計學(xué)意義(P<0.05),見表2。

表2 兩組臨床相關(guān)危險因素比較
2.5兩組臨床心血管不良事件發(fā)生情況比較 氯吡格雷抵抗組臨床心血管不良事件發(fā)生率高于氯吡格雷敏感組,差異有統(tǒng)計學(xué)意義(P<0.05)。見表3。

表3 兩組臨床心血管不良事件發(fā)生情況比較 [n(%)]
3 討 論
目前,在已發(fā)現(xiàn)的25個CYP2C19等位基因中,中國人群主要以CYP2C19*1、CYP2C19*2、CYP2C19*3 為主,而且不同地域和種族人群之間CYP2C19基因型多態(tài)性的分布也不一致[7]。本研究分析了重慶地區(qū)346例患者CYP2C19的基因型和代謝型分布,快代謝型占39.3%、中代謝型占48.0%、慢代謝型占12.7%。這與重慶地區(qū)其他兩組研究報道結(jié)果[8-9]相似,但*2/*2的比例較文獻[9]報道的7.1%增加,*3/*3的比例較文獻[8]報道的1.3%減少,差異均有統(tǒng)計學(xué)意義(P<0.05);但與蒙古族人群的中代謝型和慢代謝型占比不完全一致[10]。與新疆地區(qū)維吾爾族和哈薩克族人群的CYP2C19代謝型相比,本研究快代謝型占比較低,中代謝型和慢代謝型占比較高,但與漢族人群的代謝型分布基本一致[11]。
本研究結(jié)果顯示,慢代謝型患者與快代謝型、中代謝型患者比較,具有較高的MAR,且快代謝型患者發(fā)生氯吡格雷抵抗的概率較小。進一步可推出非快代謝型(中代謝型和慢代謝型)患者發(fā)生氯吡格雷抵抗的可能性較大。CYP2C19酶是P450氧化酶系統(tǒng)的重要組成部分,對氯吡格雷的氧化起到關(guān)鍵性作用,而CYP2C19酶的活性受到CYP2C19基因的調(diào)控,因此CYP2C19基因突變可影響到機體對氯吡格雷的敏感程度[12-13]。中代謝型包括CYP2C19 *1/*2、*1/*3,慢代謝型包括CYP2C19 *2/*2、*2/*3、*3/*3,即CYP2C19攜帶了一個以上的突變位點;當CYP2C19基因發(fā)生突變,其酶的催化活性降低,從而降低體內(nèi)氯吡格雷活性代謝產(chǎn)物水平,導(dǎo)致血小板聚集率升高,氯吡格雷抵抗率也升高。故CYP2C19基因突變可能是氯吡格雷抵抗發(fā)生的一個危險因素。
有研究表明,CYP2C19rs12248560基因多態(tài)性能夠作為心力衰竭合并肺動脈高壓發(fā)生的危險因素,可以作為早期預(yù)防心力衰竭合并肺動脈高壓的指標[14]。本研究發(fā)現(xiàn),氯吡格雷抵抗與CYP2C19基因多態(tài)性和高血壓存在一定關(guān)系,因此,推薦對冠心病患者盡早進行CYP2C19基因檢測和血小板聚集功能試驗,根據(jù)檢測結(jié)果進行個體化用藥,避免氯吡格雷抵抗現(xiàn)象發(fā)生,從而預(yù)防臨床心血管不良事件的發(fā)生。PAN等[15]研究報道,在氯吡格雷治療的缺血性腦卒中或短暫性腦缺血發(fā)作的患者中,攜帶CYP2C19功能喪失等位基因的患者比非攜帶者具有更高的復(fù)發(fā)腦卒中和復(fù)合心血管事件風(fēng)險。余建萍等[16]研究發(fā)現(xiàn),氯吡格雷抗血小板治療患者攜帶CYP2C19*2基因是頸動脈血管內(nèi)支架置入術(shù)(CAS)后氯吡格雷抵抗組發(fā)生支架內(nèi)血栓的重要因素,并影響患者預(yù)后。本研究也發(fā)現(xiàn),氯吡格雷抵抗更容易發(fā)生臨床心血管不良事件,故可推測出攜帶CYP2C19雜合突變和純合突變的PCI術(shù)后患者更容易發(fā)生臨床心血管不良事件。CYP2C19基因突變可影響冠心病患者PCI術(shù)后的聯(lián)合心臟事件發(fā)生率,分析其中原因主要是突變純合型的血小板聚集率和氯吡格雷抵抗率較高,導(dǎo)致這部分患者未能達到預(yù)期的抗血小板聚集作用,進而導(dǎo)致其預(yù)后不良,增加聯(lián)合心臟事件發(fā)生率。
盡管本研究與多數(shù)的研究結(jié)果一致認為氯吡格雷抵抗與CYP2C19基因多態(tài)性及后續(xù)的心血管事件存在一定相關(guān)性,但也有研究發(fā)現(xiàn)中國PCI術(shù)后患者心血管不良事件發(fā)生率與經(jīng)氯吡格雷代謝途徑的基因變異無顯著相關(guān)[17],且也有研究支持氯吡格雷抵抗與CYP2C19的基因多態(tài)性無相關(guān)[4]。再加上目前血小板聚集功能檢測方法眾多但一致性不理想,不同種族間氯吡格雷治療后血小板高反應(yīng)性不同,患者如何通過試驗結(jié)果從抗血小板治療中獲益等問題尚未解決,因此對氯吡格雷抵抗及其相關(guān)影響因素的研究值得進一步探討。
綜上所述,本研究探討了重慶地區(qū)CYP2C19 基因多態(tài)性、臨床危險因素及不良心血管事件與氯吡格雷抵抗的關(guān)系,結(jié)果顯示,PCI術(shù)后攜帶CYP2C19慢代謝型的冠心病患者具有較高的MAR,且快代謝型患者發(fā)生氯吡格雷抵抗的概率較小;同時發(fā)現(xiàn)氯吡格雷抵抗的發(fā)生可能與高血壓有關(guān),且存在氯吡格雷抵抗患者更容易發(fā)生臨床心血管不良事件的可能。但本研究局限在于僅選擇某一時間段的本院PCI術(shù)后患者,可能不能完全代表本地區(qū)的整體情況,應(yīng)加大多中心合作,擴大樣本量,進一步證實本研究結(jié)論。
CYP2C19基因突變和高血壓可能是氯吡格雷抵抗發(fā)生的兩個重要影響因素,并且氯吡格雷抵抗增加了PCI術(shù)后患者臨床心血管不良事件的發(fā)生風(fēng)險。因此,對于PCI術(shù)后使用氯吡格雷的冠心病患者,應(yīng)及早進行CYP2C19基因多態(tài)性檢測,根據(jù)檢測結(jié)果個體化用藥,減少或避免臨床心血管不良事件的發(fā)生。

