當歸揮發油治療高血壓藥理機制的網絡分析
王 堯,張小飛,2*,鄒俊波,2,賈妍卓,王昌利,2*,史亞軍,2,郭東艷,2
1陜西中醫藥大學藥學院;2陜西中醫藥大學藥學院,陜西省中藥基礎與新藥研究重點實驗室,咸陽 712046
高血壓是一種常見的多發性疾病,其主要特征是全身動脈壓升高,由多基因遺傳、環境及其他危險因素相互作用而導致的全身性疾病[1]。理論和臨床實踐表明:可將高血壓病納入中醫的“頭痛”、“眩暈”、“肝風”等這類病證辨證論治。中醫憑借整體論治,標本兼顧等優勢,在對降低高血壓病患者血壓、保護靶器官、提高生活質量具有重要作用。
當歸是臨床中應用較為廣泛的一味中藥,味甘平、性溫,有“十方九歸”的說法。研究表明:當歸中含有揮發油、多糖類、水溶性、油脂類及維生素類等多種化學成分。當歸中的揮發油是對血管起解痙攣作用的主要活性成分,其中蒿本內脂是活性最強的成分[2,3]。然而當歸揮發油具有降壓作用的藥效物質以及其作用途徑尚不清楚。目前,利用網絡藥理學探索藥物的作用機理研究成熟,并獲得成功[3]。故采用網絡藥理學方法,探究當歸揮發油主要降壓的藥效物質和靶點通路,為臨床使用提供理論依據,本文研究流程見圖1.
1 方法
1.1 當歸揮發油化學成分的測定
本研究采用氣相色譜-質譜聯用(GC-MS)法測定當歸揮發油的化學成分。氣相色譜條件為:安捷倫HP-5ms(30 m×250 μm×0.25 μm)毛細管柱,高純He,進樣量1.5 μL,無分流,流速為1 mL/min,程序升溫80 ℃(保持時間:0 min),升溫3 ℃/min至167 ℃(保持時間:2.5 min),升溫2 ℃/min至202 ℃(保持時間:0 min),升溫4 ℃/min至280 ℃(保持時間:15 min)。
質譜條件為:EI離子源、電子能量70 ev、離子源溫度230 ℃、MS四極體溫度150 ℃、溶劑延遲2.5 min、質譜掃描模式全掃描、掃描范圍30~400 amu。
1.2 當歸揮發油化合物的鑒定
數據處理由Data Analysis軟件完成,將其閾值調整為14,對當歸揮發性化學成分進行篩選。所分辨的質譜在NIST14標準譜庫中檢索,根據匹配度、保留指數和文獻已報道物質進行核對。保留指數的測定采用相同的氣相色譜條件測定正構烷烴(C8~C40)的保留時間,自動質譜退卷積定性系統(AM-DIS)根據正構烷的保留時間,自動計算出當歸中各揮發性化合物的保留指數。
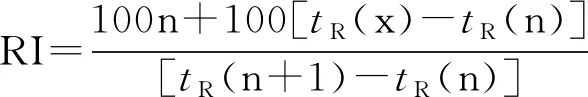
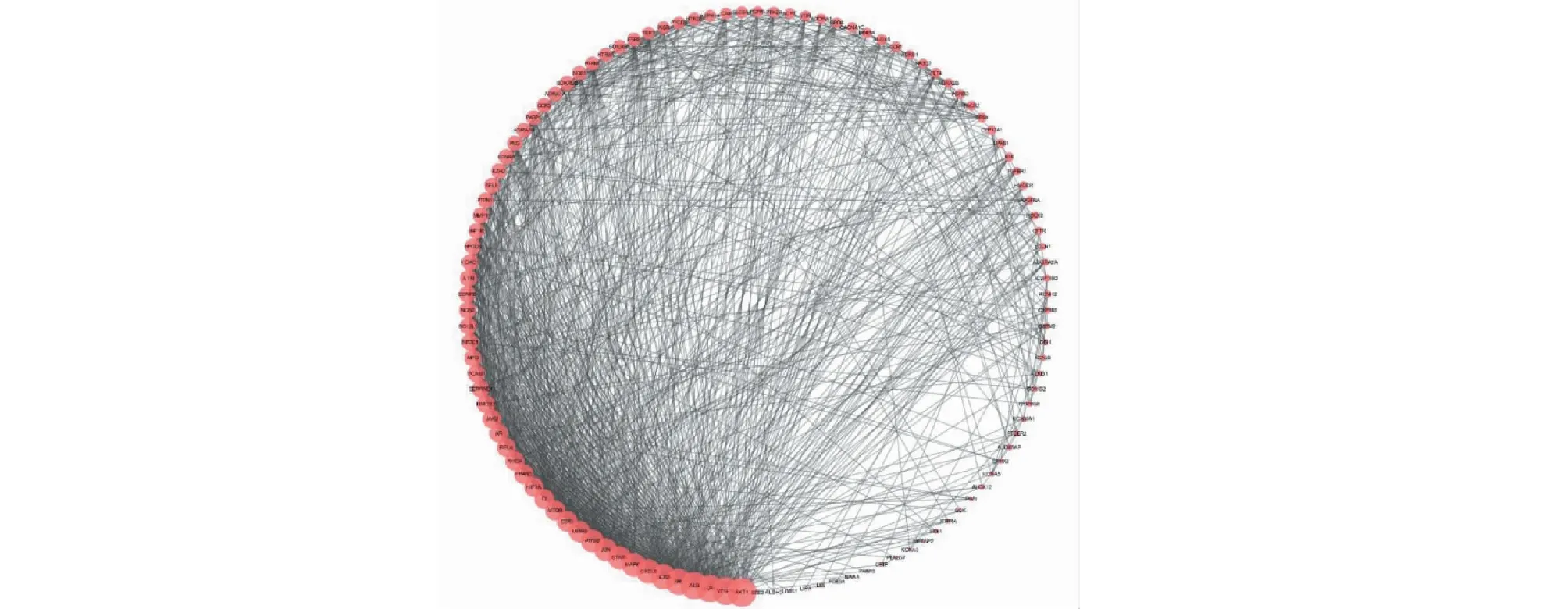
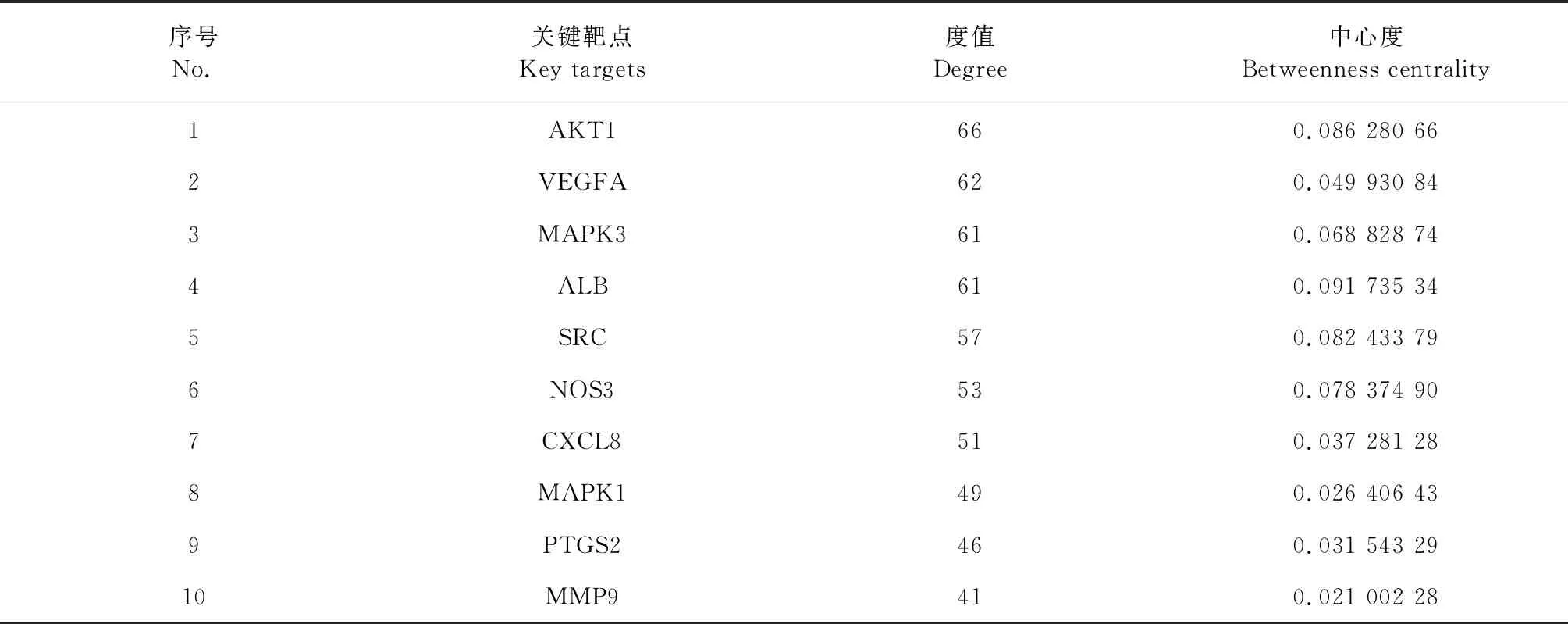
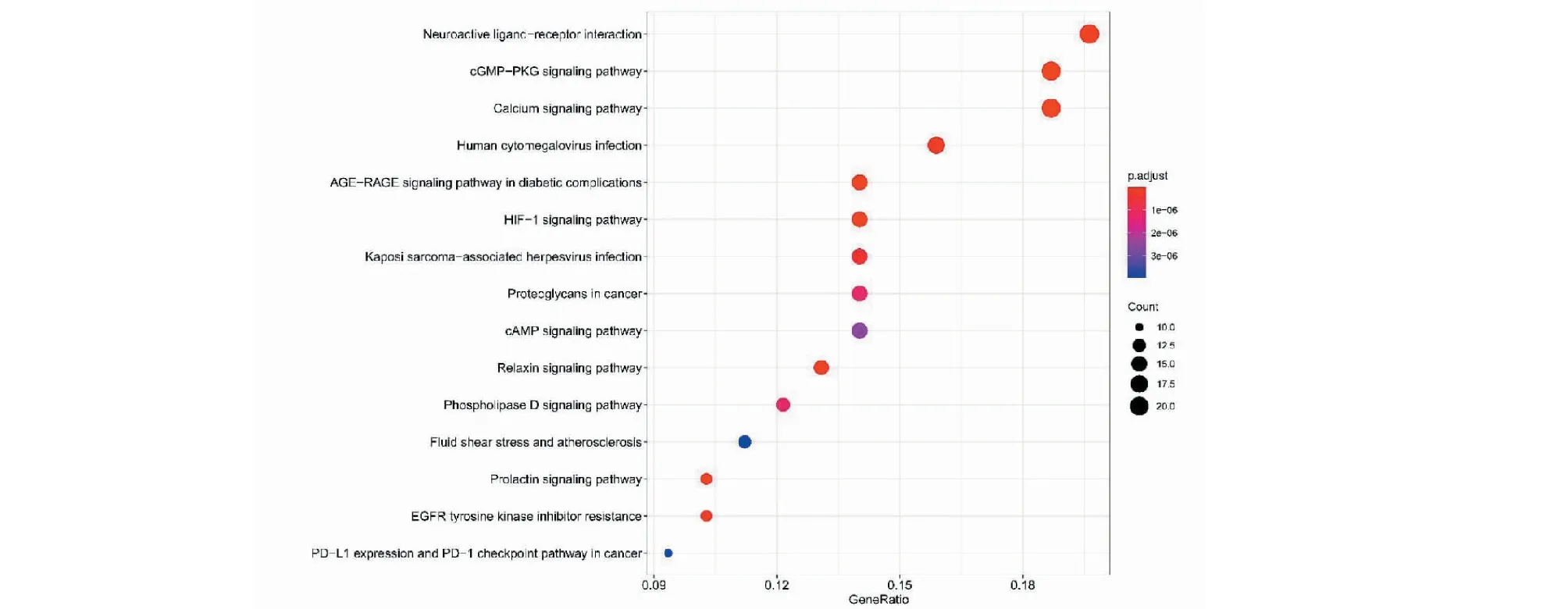
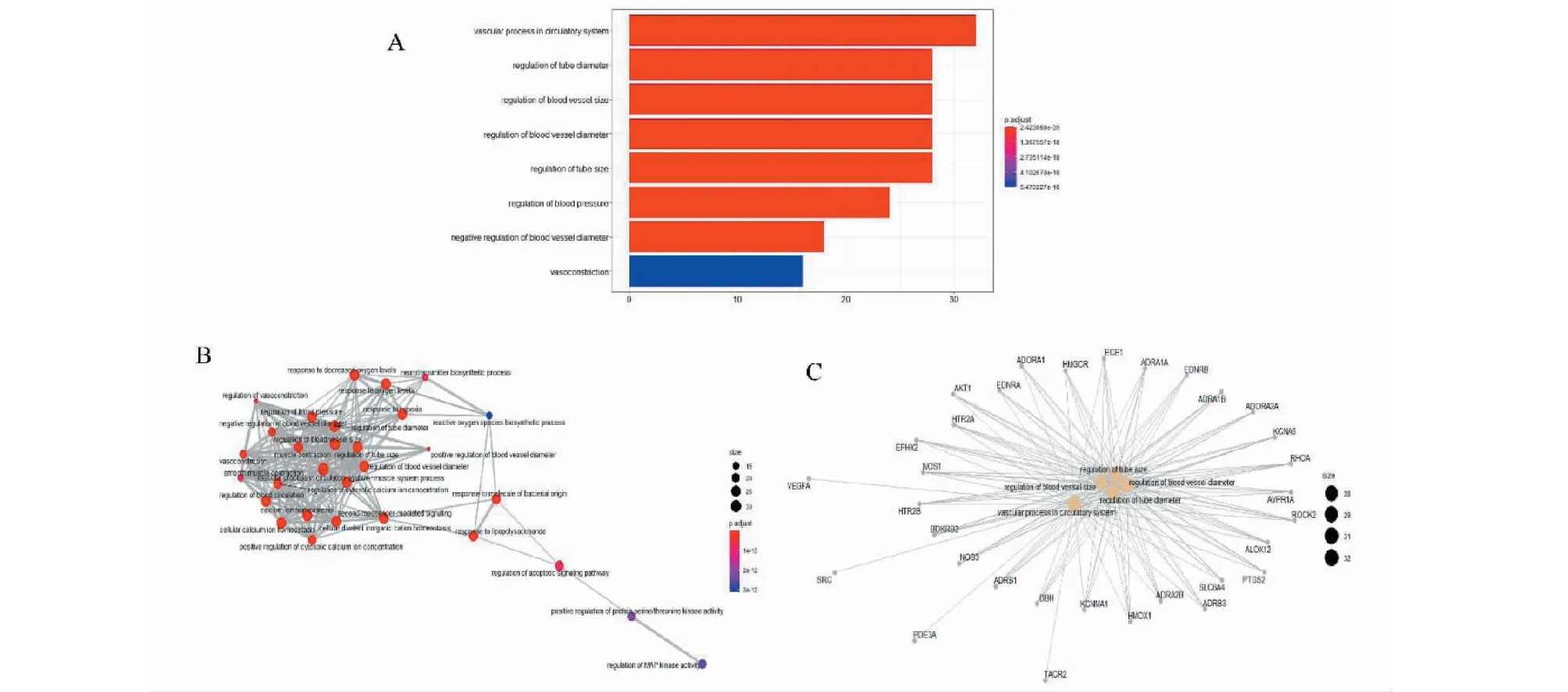
式中:tR(x)、tR(n)、tR(n+1)分別表示待測化合物,含碳數n和碳數n+1的正構烷烴的保留時間且tR(n) 利用SwissTargetPrediction數據庫(http://www.swisstargetprediction.ch/)獲取當歸揮發油相關成分靶點共計1 081個,剔除重復項625個。通過Mendelian人類基因和基因表型綜合數據庫OMIM(https://www.omim.org/)獲得高血壓相關靶點236個。DisGENET數據庫(https://www.disgenet.org/)獲得高血壓相關靶點723個;剔除重復項,共計高血壓相關靶點792個。并將高血壓相關靶點和當歸揮發油潛在作用靶點交互篩選出共同靶點。 通過Cytoscape v3.7.1建立當歸揮發油活性成分—高血壓靶點網絡圖。利用該軟件中的“Network analyzer”功能,分析其網絡拓撲屬性,主要考察其節點度值分布(node degree distribution)和介數中心性(betweenness centrality)2個重要的網絡拓撲參數。度值反映節點與其他節點之間的連接數;介數中心性是經過該節點的路徑數與網絡中最短路徑總數的比值;度值和介數是量化節點在網絡中重要性的拓撲參數[4]。最后,利用網絡拓撲屬性對當歸揮發油治療高血壓的主要成分進行分析。 為研究當歸揮發油與降壓靶點之間的相互作用,在STRING(https://string-db.org/cgi/input.pl)平臺構建其靶蛋PPI網絡。物種設為“Homo sapiens”,最低相互作用的閥值設為中等置信度0.4“Medium confidence”,其余參數保持默認設置,得到蛋白相互作用,下載其tsv文件。通過Cytoscape v3.7.1進行拓撲屬性分析篩選出PPI網絡中的關鍵靶蛋白。 運用Rstudio軟件R語言編程中的clusterProfiler程序包對當歸揮發油治療高血壓的靶基因進行KEGG信號通路富集分析和Gene Ontology(GO)生物過程富集,分析當歸揮發油治療高血壓作用靶點的主要信號通路和生物過程,并利用R語言編程進行繪圖分析。 分子對接(Molecular docking)是一種基于預測配體與其相結合受體位點的計算方法,是藥物設計的重要技術[5,6,7]。基于活性成分篩選出兩方中核心活性成分與靶標,采用Discovery Studio 4.5 Client軟件中的LibDock模塊進行分子對接,并得出對接得分(Score)值,得分值越大,配體與受體結合越穩定。蛋白下載于PDB數據庫(https://www.rcsb.org/),蛋白經加氫、準備、賦予力場后,定義活性位點。候選化合物下載于PubChem數據庫(https://pubchem.ncbi.nlm.nih.gov/),保存為SDF格式。分子對接為揭示核心成分作用機制、藥理復雜網絡分析及當歸揮發油功效機制奠定了基礎。 通過GC—MS測定出當歸揮發油化合物共20個(見表1),圖2所示為當歸揮發油離子質譜圖。 表1 當歸揮發油主要活性成分 續表1(Continued Tab.1) 圖2 當歸揮發油成分離子圖 將625個藥物靶點和792個高血壓相關靶點交互共得到115個共同靶基因(見圖3)。將115個靶基因作為當歸揮發油治療高血壓靶點,建立當歸揮發油活性成分—靶點網絡圖。如圖4所示,共有134個節點,398條邊;綠色節點為當歸揮發油化學成分,粉色節點為當歸揮發油對應的高血壓節點,398條邊代表了化學成分與靶點的相互作用。 圖3 當歸揮發油作用靶點與高血壓疾病靶點交集的韋恩圖 圖4 當歸揮發油成分-靶點網絡圖 當歸揮發油治療高血壓疾病靶蛋白PPI網絡有114個節點(其中有1個靶蛋白與其他蛋白未發生相互作用),1 080條相互作用連線(見圖5)。對排序均在前15的度值和介數的靶蛋白進行交集,共篩選出10個度值和介數的靶蛋白,提示這些靶蛋白在PPI網絡中起關鍵作用,可能是當歸揮發油治療高血壓的關鍵靶點(見表2)。 圖5 當歸揮發油治療高血壓的靶點PPI網絡圖 表2 關鍵靶點拓撲參數 將當歸揮發油115個高血壓疾病靶點在KEGG信號通路富集,根據P<0.05篩選到122條通路。如圖6所示列出了KEGG信號通路的前15條;其中有21個靶點參與了神經活性配體-受體相互作用通路,有20個靶點參與了cGMP-PKG信號通路,20個靶點參與了鈣信號通路,15個靶點參與了糖尿病并發癥中的AGE-RAGE信號通路,15個靶點參與了HIF-1信號通路。 圖6 KEGG信號通路圖 將當歸揮發油115個高血壓疾病靶點在GO生物過程富集,根據P<0.05篩選得:BP生物過程富集到1 779個結果,CC細胞組成富集到54個結果,MF分子功能富集到165個結果。GO分析顯示115個高血壓疾病靶點在生物過程中顯著富集(BP,圖7A~C),包括有32個靶點參與的血管循環系統(vascular process in circulatory system),有28個靶點參與的管徑的調節(regulation of tube diameter),有28個靶點參與的血管管徑的調節(regulation of blood vessel diameter),有28個靶點參與調節血壓(regulation of blood pressure),有24個靶點參與的血管內徑負調控(negative regulation of blood vessel diameter)等過程。細胞成分(CC,圖8ABC)分析表明,凹陷(caveola),質膜筏(plasma membrane raft),膜筏(membrane raft),膜微域(membrane microdomain),膜區(membrane region)等部分都是分類的。就分子功能而言(MF,圖9ABC),有12個靶點參與了血紅素結合(heme binding)以及四吡咯結合(tetrapyrrole binding),有11個靶點參與了氧化還原酶活性通過與分子氧的結合或還原,作用于成對的供體上(oxidoreductase activity,acting on paired donors,with incorporation or reduction of molecular oxygen),有7個靶點參與了核受體活性(nuclear receptor activity)和轉錄因子活性,直接配體調節的序列特異性DNA結合(transcription factor activity,direct ligand regulated sequence-specific DNA binding)等過程。 圖7 生物過程富集圖 圖8 細胞組成富集圖 圖9 分子功能富集圖 運用Discovery Studio 4.5 Client將篩選出來的關鍵靶點與對應核心成分進行對接。運用LibDock模式進行對接,對接結果如表3所示,其中度值最大的ATK1與成分1,4-Benzenediol,2,3,5-trimethyl-對接穩定,得分值為77.054 3,接近于陽性藥對接得分值。圖10A為靶點AKT1與成分1,4-Benzenediol,2,3,5-trimethyl-對接結果圖;B為靶點VEGFA與成分1,4-Benzenediol,2,3,5-trimethyl-對接結果圖;C為靶點MAPK3與成分(1R,4R,4aS,8aR)-4,7-dimethyl-1-(prop-1-en-2-yl)-1,2,3,4,4a,5,6,8a-octahydronaphthalene對接結果圖;D為靶點ALB與成分1,4-Benzenediol,2,3,5-trimethyl-對接結果圖;E為靶點SRC與成分(E)-3-butylidene-4,5-dihydroisobenzofuran-1(3H)-one對接結果圖。 圖10 核心成分與關鍵靶點對接結果圖 表3 分子對接結果 高血壓是導致心腦血管疾病的一個重要因素之一,常引起心、腦、腎三臟的并發癥。誘發血壓升高的機制相對比較復雜,有研究表明當歸揮發油對高血壓疾病的防治發揮一定的作用。主要通過抑制血管炎癥反應[8]、調節胰島素信號通路及血管內皮生長因子(VEGF)信號通路相關miRNA的表達[9];明顯降低SHRs的收縮壓,改善心肌組織形態等途徑對高血壓病起治療作用[10],而且當歸揮發油對血管內皮還具有一定的保護作用[11]。 本文利用分子對接技術將篩選出來的當歸揮發油核心活性成分與關鍵靶點進行對接,對接結果顯示對接穩定。其中(E)-3- butylidene-4,5-dihydroisobenzofuran-1(3H)-one(藁本內酯)含量最高,可通過降低氧化應激性損傷以及抗細胞凋亡、清除體內氧自由基、緩解腦細胞的損傷而發揮降壓作用[11]。此外本研究顯示tetrasiloxane,decamethyl-(十甲基四硅氧烷)、1,4-benzenediol,2,3,5-trimethyl-(三甲基氫醌)、butanoic acid,4-methoxy-,methyl ester(甲氧基丁酸甲酯)等成分也發揮降壓的作用,提示這些成分可能為當歸揮發油治療高血壓的新成分。 PPI網絡分析發現AKT1、VEGFA、MAPK3、ALB、SRC等是當歸揮發油降壓的關鍵靶點。AKT1是一種絲氨酸(蘇氨酸)激酶,在細胞代謝、存活、周期調節和轉錄調控中發揮重要作用。Miao等[12]在對高血壓心肌纖維化疾病的研究中:表明AKT1的表達和活化可以促進AngeⅡ誘導的心肌纖維化,提示AKT1在高血壓心肌纖維化中發揮作用。血管內皮生長因子A(VEGFA)是一種強效且具有特異性的內皮細胞有絲分裂劑,與其受體結合可以促進內皮細胞的分裂和增殖,增加微血管的通透性。Wang等[13]體內實驗表明:血管VEGF可以刺激血管的發生和生長,發現當歸揮發油能降低血清中VEGF的水平,說明其降壓作用于血清中的VEGF水平有關。尿ALB與高血壓性腎損害的進展密切相關,Li[14]研究表明:尿Alb水平有助于評估高血壓患者早期腎損傷;也有研究表明尿液UmAlb/Ucr 的變化比血清中Scr及BUN的變化發生更早,因此能準確、敏感地反映早期高血壓腎損害的情況[15]。SRC酪氨酸蛋白激酶是一個非受體型原癌基因酪氨酸激酶,Zeng等[16]論述:SRC通過不同信號途徑對血壓產生影響,對血壓具有雙向調節作用。 本研究為了分析當歸揮發油降壓的治療靶點所涉及的信號通路和生物過程,對靶基因進行了GO功能富集和KEGG信號通路分析,GO功能富集發現當歸揮發油治療高血壓的生物過程包括循環系統中的血管過程、管徑調節、血管大小的調節、血管直徑的調節、血壓調節、血管直徑負調節、血管收縮、血液循環調節、對氧含量的反應、第二信使介導的信號轉導,可以發現這些生物過程在降壓過程中發揮重要作用。KEGG通路富集到神經活性配體-受體相互作用通路、cGMP-PKG信號通路,鈣信號通路,糖尿病并發癥中的AGE-RAGE信號通路,HIF-1信號通路等多條通路。神經活性配體-受體相互作用通路是與細胞內和細胞外信號通路有關的所有受體和配體在質膜上的集合,調節生理節律、內分泌、情緒、學習、記憶等,內分泌紊亂是高血壓的常見病因;此外不良的情緒也會直接或間接的影響高血壓[17]。根據報道[18]:大多數組織中cGMP-PKG信號通路可調節血管平滑肌細胞收縮和舒張,抗高血壓。抗心肌肥大,抗動脈粥樣硬化,抗血管損傷/再狹窄。此外,鈣離子信號通路控制新陳代謝、分泌、平滑肌收縮、增殖等多種過程調節血壓[19],提示當歸揮發油可能通過調節平滑肌收縮來發揮藥效。高血壓合并糖尿病患者腎損害有很大可能性發生,研究表明:AGE通過RAGE可引起腎臟中NF-κB通路的激活,抑制NF-κB可以降低血壓并且部分減輕心肌肥厚[20]。提示當歸揮發油可能通過調節AGE-RAGE信號通路對高血壓伴糖尿病并發癥發揮治療作用。有研究顯示[21]:HIF-1介導的信號通路可能通過調節腎臟髓質功能和水鹽電解質平衡參與血壓調節。 綜上所述,本文運用網絡藥理學方法,對當歸揮發油的成分和作用靶點進行了系統性研究。利用Rstudio軟件R語言編程,從生物過程(biological process)、細胞組成(cellular component)與分子功能(molecular function)三個水平對其進行富集分析,同時也進行了KEGG富集分析。最后利用分子對接等手段,揭示其通過多組分、多靶點、多通路,從而發揮整體協同降壓的藥理機制。1.3 當歸揮發油主要活性成分作用靶點以及高血壓疾病相關靶點的獲取
1.4 當歸揮發油活性成分—高血壓疾病靶點網絡的構建
1.5 靶蛋白交互作用網絡(PPI)的構建
1.6 信號通路與生物過程分析
1.7 分子對接
2 結果
2.1 當歸主要活性成分


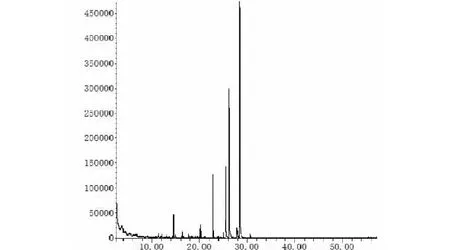
2.2 成分-靶點網絡圖的構建
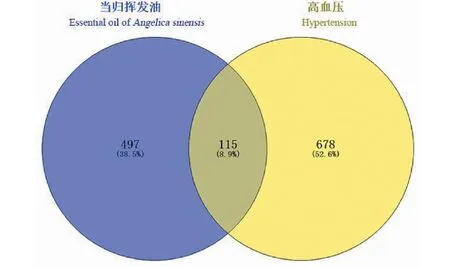
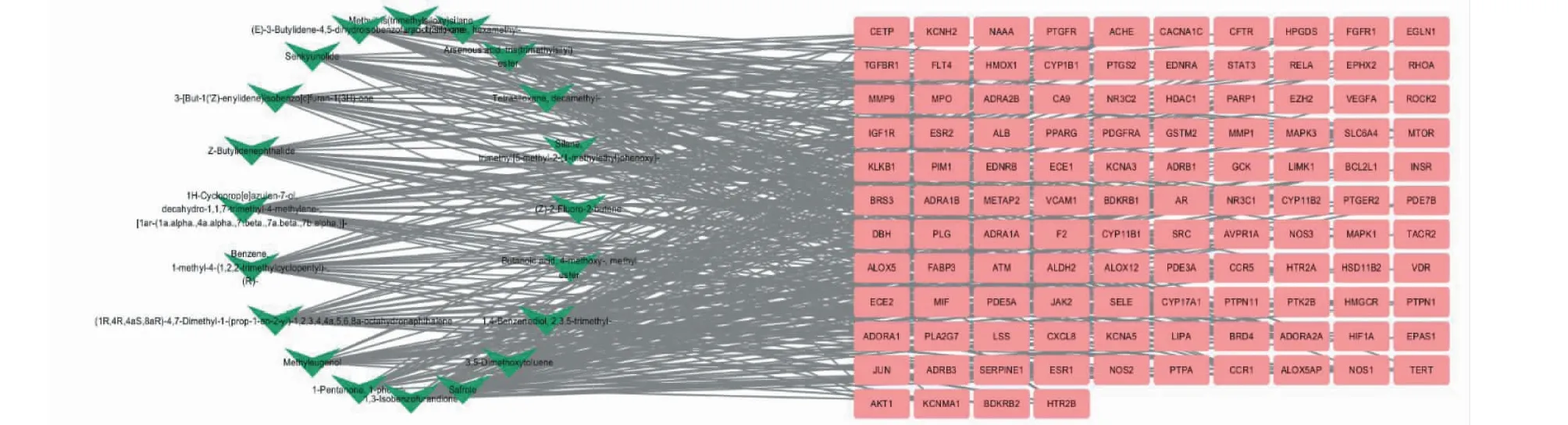
2.3 靶點PPI網絡分析
2.4 KEGG信號通路分析
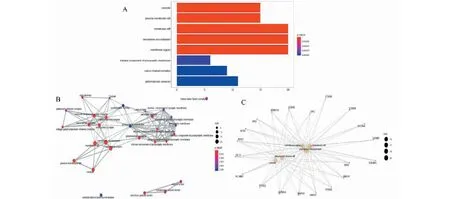
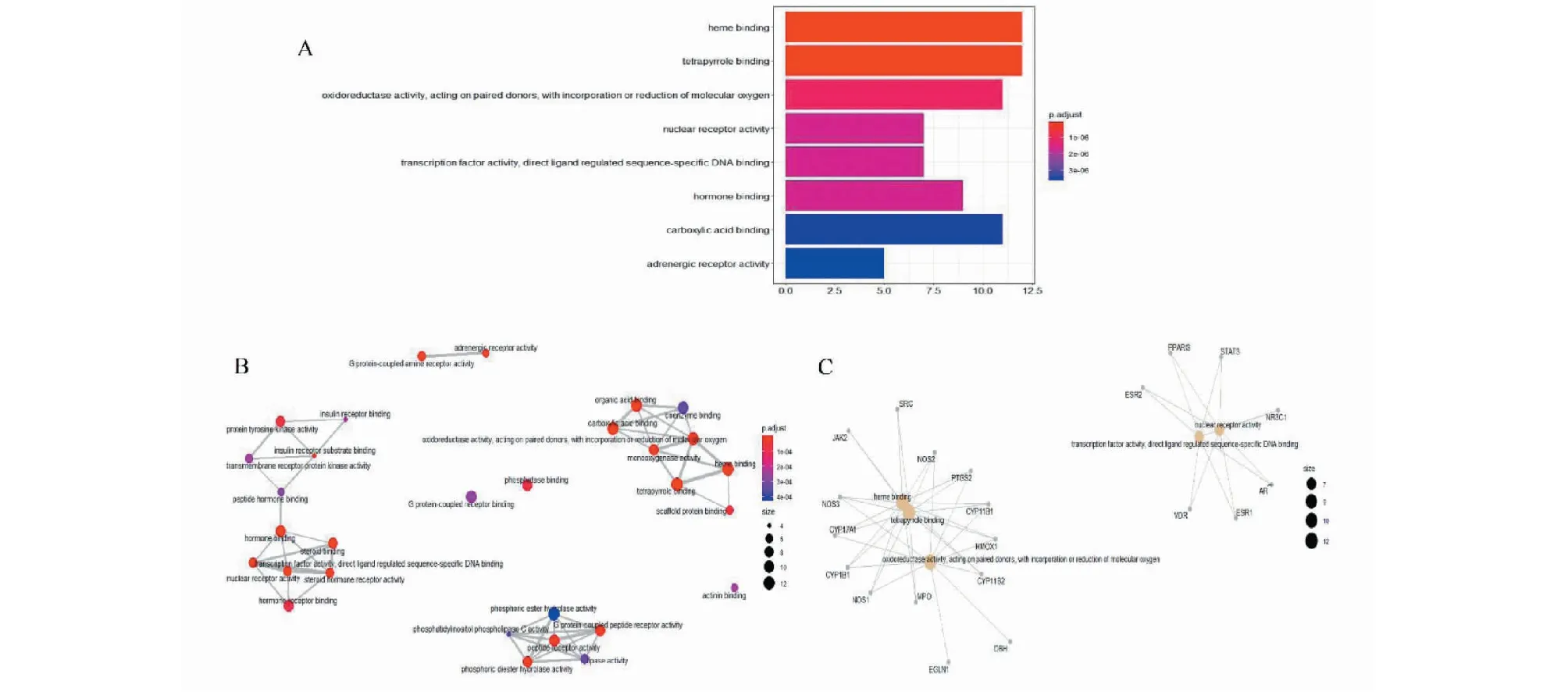
2.5 GO生物過程分析
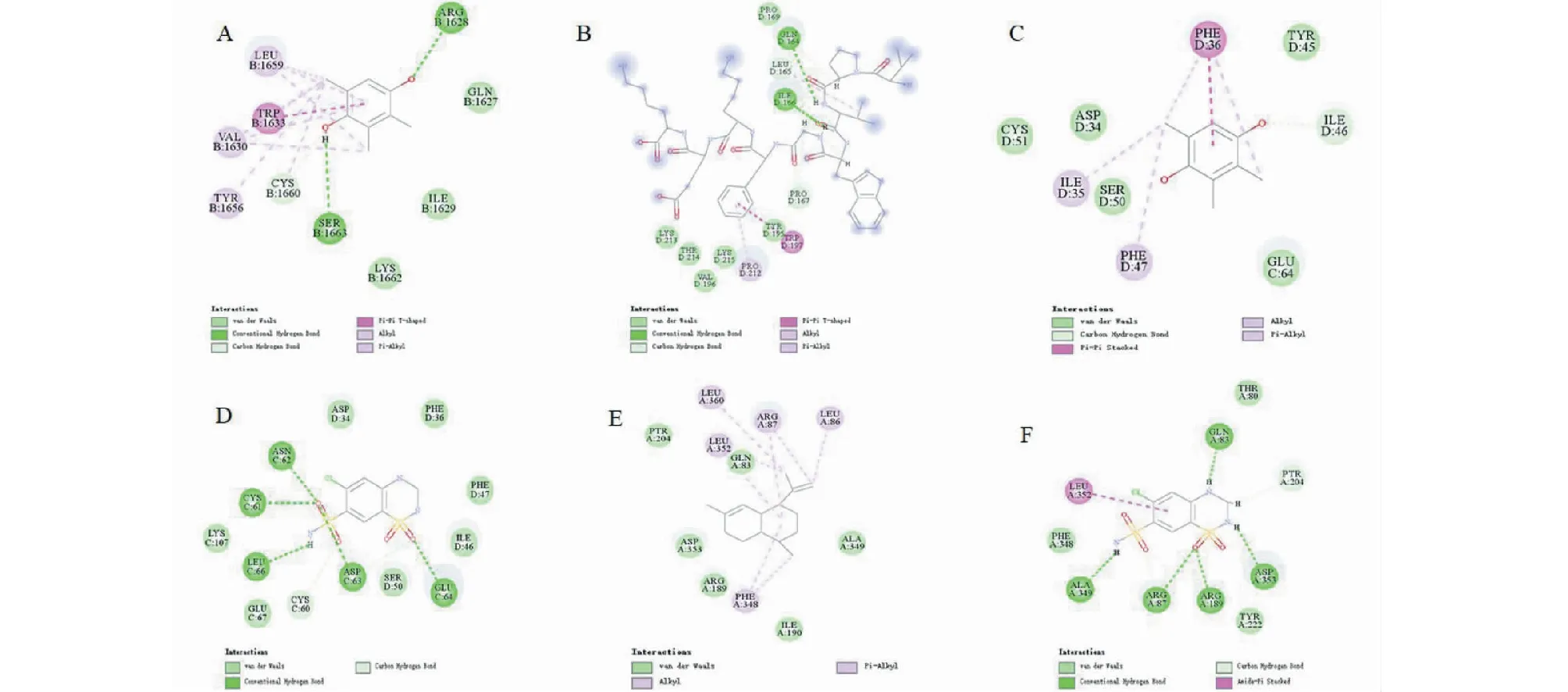
2.6 分子對接結果分析

3 討論

