炎性腸病合并視神經脊髓炎譜系疾病一例
徐康夏立建劉玉林于鵬 陳景波
炎性腸病是一種與免疫相關的腸道非特異性炎癥疾病,包括潰瘍性結腸炎(UC)、克羅恩病(CD)及未定型結腸炎[1]。視神經脊髓炎譜系疾病(neuromyelitis optica spectrum disorders,NMOSD)是一組與免疫相關的中樞神經系統炎性脫髓鞘疾病譜[2]。現將收治一例炎性腸病合并NMOSD患者進行報道。
一、病例資料
患者女性,67歲,因“腹痛、腹瀉1月余”于2019年2月8日入住山東第一醫科大學第一附屬醫院胃腸外科,患者曾于2019年2月1日至本院門診行結腸鏡檢查提示:升結腸占位合并不全性梗阻(圖1),活檢病理示:(升結腸)黏膜糜爛,急性發炎,見少量炎性滲出物,送檢標本中未查見惡性腫瘤組織。入院后查體:右下腹壓痛,無反跳痛,可觸及一大小約3 cm×3 cm腫塊。腹部CT提示:回盲部及升結腸腸壁異常增厚,考慮惡性腫瘤可能性大(圖2)。查無手術禁忌證后于2019年2月12日在全麻下行剖腹探查術,術中見:病變位于回盲部,大小約3 cm×3 cm,漿膜面明顯充血水腫,回盲部與側腹壁粘連致密,右側盆壁及側腹壁呈明顯充血水腫、炎性滲出改變。闌尾明顯充血水腫,系膜攣縮,闌尾頭包埋于盲腸和右側側腹壁粘連之間,系膜內未觸及腫大淋巴結,經探查決定行右半結腸切除術。術后病理回示:(1)(右半結腸)黏膜組織急慢性發炎,淋巴組織增生,腸壁可見透壁性炎癥,漿膜面見炎性滲出物,漿膜下大量漿細胞、嗜酸性粒細胞及中性粒細胞浸潤,局部可見膿腫形成,小動脈管壁增厚,局部黏液變性,小靜脈周圍淋巴單核細胞浸潤;(2)慢性闌尾炎,闌尾漿膜下急慢性炎;(3)(腹壁)纖維脂肪組織急慢性發炎;(4)腸系膜周圍淋巴結(13個)呈反應性增生(圖1)。患者于2019年2月23日出院。

圖1 結腸鏡檢查圖像及術后病理圖像。1A+1B(結腸鏡):升結腸一腫物,占腸腔約1周,表面糜爛,質硬,質脆,管腔狹窄,內鏡不能通過;1C(術后病理):結腸急慢性炎癥表現,淋巴組織增生,透壁性炎癥,漿膜下見漿細胞、嗜酸性粒細胞及中性粒細胞浸潤,局部可見膿腫形成(HE染色,×200倍)
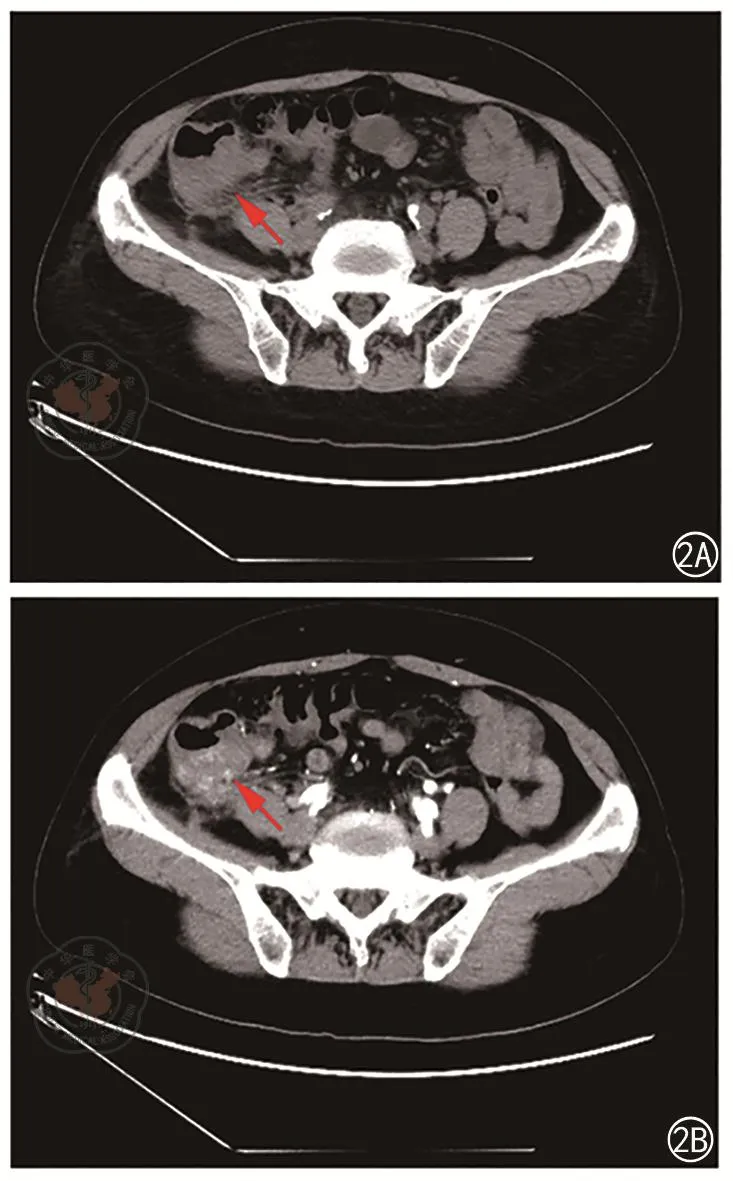
圖2 腹部平掃+增強CT成像圖。2A:平掃示回盲部管壁增厚;2B:增強示回盲部腸壁不均增厚
患者出院1周后,晨起出現頸肩部疼痛,持續酸痛,平臥時明顯。后癥狀加重,并伴有左側肢體麻木、無力,進行性加重,左手不能持物,下肢有“踩棉花感”,于2019年3月15日再次來院就診。入院完善相關檢查:降鈣素原7.418ng/mL,血沉27mm/h,C反應蛋白20.6mg/L,類風濕因子15.9IU/mL;抗核抗體測定:弱陽性,抗核抗體核型:均質+胞漿顆粒型;抗雙鏈DNA抗體陽性;ANCA陰性;腦脊液特殊蛋白:腦脊液IgG 58.50 mg/L,腦脊液白蛋白371.00 mg/L,抗AQP4抗體陽性,抗MBP抗體陰性,抗MOG抗體陰性;頸椎MRI診斷:頸2至胸1椎體水平脊髓內異常信號,考慮脊髓炎可能性大(圖3)。最終診斷為:NMOSD。給予激素沖擊、免疫抑制、改善循環、營養神經、抑酸護胃及對癥支持治療,患者病情好轉后出院。目前,術后隨訪18個月(2020年8月10日),患者一般情況可,大小便正常,神經系統臨床表現主要為行為反應遲鈍,未出現嚴重神經系統后遺癥。
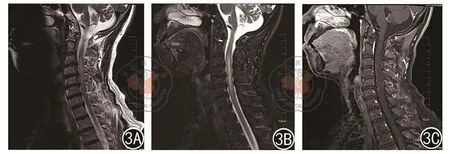
圖3 頸部磁共振成像圖。3A(T2):頸2至胸1水平脊髓略增粗,呈長T2信號;3B(T2脂肪抑制):呈高信號;3C(增強序列):輕度的片狀強化
二、討論
炎性腸病(inflammatory bowel disease,IBD)是一種非特異性、慢性的腸道炎癥性疾病[1]。目前于關于IBD的發病機制尚不明確,但是越來越多的研究表明,遺傳因素、環境因素、免疫因素及腸道菌群等在IBD的發病中發揮了重要作用[3]。對于IBD的診斷沒有金標準,主要依賴于病史、體格檢查、影像學檢查、實驗室檢查、內鏡、病理等信息。該患者有腹痛、腹瀉、腹部腫塊的臨床表現,腹部CT提示回盲部及升結腸腸壁增厚,術后病理提示:結腸透壁性炎癥、淋巴組織增生,漿膜下炎性細胞浸潤,并有膿腫形成,這些都符合炎性腸病的表現,因此,該患者最終診斷為炎性腸病。
NMOSD是一組免疫介導的中樞神經系統非特異性炎性脫髓鞘疾病[2],其致殘率較高,且易反復發作,主要包括6組核心臨床癥候:視神經炎、急性脊髓炎、延髓最后區綜合征、急性腦干綜合征、急性間腦臨床綜合征、大腦綜合征。水通道蛋白4抗體(AQP4-IgG)是NMOSD的特異性抗體[4],以AQP4-IgG作為診斷分層,分別制定了AQP4-IgG陽性診斷標準和AQP4-IgG陰性診斷標準,其中AQP4-IgG陽性診斷標準為:(1)至少符合一項核心臨床特征;(2)AQP4-IgG陽性;(3)排除其他可能的診斷[2]。NMOSD的具體發病機制尚不明確,但遺傳、環境、免疫因素同樣也在NMOSD的發病過程中發揮了重要的作用。另外,當合并其他自身免疫抗體陽性時,更傾向診斷為NMOSD[5],該患者腦脊液AQP4-IgG陽性,有頸部疼痛、肢體麻木無力等急性脊髓炎癥狀,頸椎MRI提示急性脊髓炎,類風濕因子、抗核抗體、抗雙鏈DNA抗體均陽性,綜合以上,該患者診斷NMOSD明確。
該患者在診斷為IBD后,短時間內出現NMOSD發作,并且這兩種疾病都與免疫相關,因此,我們猜想IBD和NMOSD之間是否存在聯系。通過查閱大量文獻,我們了解到,IBD與NMOSD的確關系密切。研究表明,當患有一種自身免疫性疾病時,會增加另一種免疫介導的疾病發病風險[6-7],有20%~30%的NMOSD患者會合并其他自身免疫性疾病,這些疾病可以在NMOSD診斷之前出現或者之后出現[8]。此前許多研究表明,在IBD患者中脫髓鞘疾病發生的風險會增加,這可能與IBD治療過程中免疫抑制劑應用有關[9-11]。Gupta等[10]在一項回顧性研究中發現,和非炎癥性腸病患者相比,脫髓鞘疾病在IBD患者中更常見,炎性腸病增加了患脊髓病或視神經炎的風險。Sadovnick等[11]研究報道,在IBD患者中,患多發性硬化癥的風險可增加3倍。另有研究表明,在血清AQP4-IgG陽性NMOSD患者中,胃腸道抗原抗體反應很常見[12],提示了胃腸道免疫反應與NMOSD自身免疫的潛在關系。此外,之前有關于NMOSD合并胃腸道自身免疫性疾病(乳糜瀉)的相關報道[13]。以上研究提示,IBD可能是NMOSD發病的危險因素。
該患者IBD與神經炎性脫髓鞘序貫發病,在IBD診療過程中并未發現明確的分子標志物或者特殊臨床表現提示神經炎性脫髓鞘的發生。因此IBD患者神經系統的檢查時機及檢測指標需要在未來的臨床實踐中重點觀察總結和進一步探討,以期建立一個風險評估模型預測NMOSD的發病風險。通過該病例的回顧,目的是讓臨床醫生在今后的診療活動中對該疾病有更好的認識,意識到IBD是一種全身性免疫性疾病,包括神經系統病變表現。在治療炎性腸病過程中要警惕另一種免疫性疾病NMOSD的發生可能,早發現、早治療,制定更加合理的診療方案,改善患者的預后。

