羥考酮聯合小劑量納美芬在預防瑞芬太尼誘發患者術后痛覺過敏的臨床價值*
林英 師雄 李明
(1.陸軍軍醫大學附屬第二醫院·新橋醫院,重慶 400037;2.重慶市中醫骨科醫院, 重慶 400010;3.武漢市第三醫院麻醉科,湖北 武漢 430060)
瑞芬太尼作為一種超短效μ受體激動劑,具有起效快、易于麻醉調控、持續用藥無蓄積等優點,被廣泛應用于各類患者的手術麻醉中[1-3]。然而有研究顯示,瑞芬太尼持續輸注容易誘發較強的術后痛覺過敏反應,且明顯強于其他阿片類藥物,導致患者對鎮痛藥物的需求增加[4-5]。近年來,有學者嘗試使用羥考酮來緩解瑞芬太尼引起的痛覺過敏,但效果仍然難以達到滿意水平。阿片受體雙向作用模式的提出,使越來越多的學者將目光投向了小劑量阿片受體拮抗劑與阿片類藥物聯合使用的研究中[6-7]。納美芬是一種阿片受體拮抗劑,是納曲酮的6-亞甲基類似物,對μ受體的親和力最強[8]。研究顯示[9],使用小劑量的納美芬有助于預防術后痛覺過敏。基于此,本研究探討羥考酮聯合小劑量納美芬用于治療瑞芬太尼誘發患者術后痛覺過敏的效果,為臨床提供數據參考。
1 資料與方法
1.1 一般資料 選取2017年9月~2019年3月陸軍軍醫大學附屬第二醫院擇期行婦科腹腔鏡子宮全切手術的患者184例為研究對象,采用隨機數字表法分為對照組、羥考酮組、納美芬組和聯合組,每組各46例。納入標準:①年齡25~55歲,體質量指數(body mass index,BMI)18~28 kg/m2。②美國麻醉醫師學會(American Society of Anesthesiologists,ASA)分級均為Ⅰ或Ⅱ級。③無麻醉藥物過敏史,無酗酒及藥物成癮史。④無精神病史。⑤患者及其家屬均知情同意并簽署知情同意書。排除標準:①伴支氣管哮喘者。②伴血液或神經系統疾病者。③嚴重心肝腎肺功能不全者。④預期插管困難者。⑤術前48 h內使用鎮痛藥物者。本研究經醫院道德倫理委員會審核批準。
1.2 方法 所有患者術前禁食12 h,禁飲8 h。患者進入手術室后常規監測心電圖、心率、無創收縮壓、舒張壓、脈搏血氧飽和度,建立靜脈通路。麻醉誘導藥物劑量:0.05 mg/kg咪達唑侖(宜昌人福藥業有限責任公司,國藥準字H20067040),4μg/kg芬太尼(宜昌人福藥業有限責任公司,國藥準字H42022076),1 mg/kg丙泊酚(四川國瑞藥業有限責任公司,國藥準字H20030115),0.15 mg/kg苯磺順阿曲庫銨(江蘇恒瑞醫藥股份有限公司,國藥準字H20060869)。麻醉維持藥物劑量:3~8 mg/(kg·h)丙泊酚,0.15~0.3 μg/(kg·min)瑞芬太尼(宜昌人福藥業有限責任公司,國藥準字H20030197,1 mg/瓶),微量泵泵注,根據手術刺激程度和血流動力學調節輸注速度,維持血流量動力學參數波動不高于基礎值的20%。維持呼吸末二氧化碳壓力35~45 mmHg。手術近結束時予曲馬多(石藥集團歐意藥業有限公司,國藥準字H10800001)1~2.5 mg/kg,帕瑞昔布鈉(輝瑞制藥有限公司,國藥準字J20130044)20~40mg。于手術結束縫皮前,羥考酮組靜脈緩慢注入羥考酮[萌蒂(中國)制藥有限公司,國藥準字J20180003]0.1 mg/kg,納美芬組靜脈緩慢注入納美芬(成都天臺山制藥有限公司,國藥準字H20184018)0.1 μg/kg,聯合組靜脈緩慢注入羥考酮0.1 mg/kg和納美芬0.1 μg/kg,對照組給予等量生理鹽水。患者術后送PACU觀察,均不予催醒藥、拮抗藥,待自主呼吸恢復,符合拔管指征后拔除氣管導管。術后鎮痛泵藥物配方:4~7 mg/kg曲馬多(1 d量),10 mg托烷司瓊,生理鹽水稀釋至100 mL,首劑量3 mL,維持2 mL/h,鎖時15 min。
1.3 觀察指標 ①記錄手術時間、術后患者呼吸恢復時間、拔管時間。②采用視覺模擬評分法(visual analogue scale,VAS)評估患者術前及術后30 min、90 min及180 min時的疼痛情況,總分10分,分數越高表示疼痛越強[10]。③記錄術后48 h內不良反應發生情況,包括惡心、嘔吐、嗜睡、頭暈、躁動、心動過速。
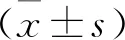
2 結果
2.1 4組患者一般資料比較 對照組:年齡26~55歲,平均年齡(44.32±5.11)歲;BMI為(24.15±1.57)kg/m2;ASA分級:Ⅰ級34例,Ⅱ級12例。羥考酮組:年齡 25~54歲,平均年齡(44.69±4.78)歲;BMI為(23.86±1.92)kg/m2;ASA分級:Ⅰ級32例,Ⅱ級14例。納美芬組:年齡 25~54歲,平均年齡(45.32±4.73)歲;BMI為(24.23±1.51)kg/m2;ASA分級:Ⅰ級33例,Ⅱ級13例。聯合組:年齡26~55歲,平均年齡(45.17±4.69)歲;BMI為(24.49±1.54)kg/m2;ASA分級:Ⅰ級34例,Ⅱ級12例。4組患者在年齡、BMI、ASA分級等方面比較差異無統計學意義(P>0.05)。
2.2 4組患者手術時間、意識恢復時間、拔管時間比較 4組患者的手術時間差異無統計學意義(P>0.05)。納美芬組、聯合組的意識恢復時間及拔管時間均顯著短于羥考酮組和對照組,差異具有統計學意義(P<0.05),但聯合聯合與納美芬組差異無統計學意義(P>0.05)。見表1。
2.3 4組患者各時間點VAS評分比較 4組患者術前的VAS評分差異均無統計學意義(P>0.05),術后30 min、90 min、180 min時的VAS評分均差異顯著(P<0.05)。經兩兩比較發現,聯合組在術后30 min、90 min、180 min時的VAS評分均顯著低于納美芬組、羥考酮組和對照組,且納美芬組、羥考酮組各時間VAS評分均低于對照組,差異具有統計學意義(P<0.05),見表2。

表1 4組患者的手術時間、意識恢復時間、拔管時間比較
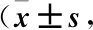
表2 4組患者各時間點VAS評分比較分)
2.4 4組不良反應發生情況比較 4組患者中,有部分患者出現惡心嘔吐、嗜睡、頭暈及躁動等不良反應,但均未出現心動過速情況,組間差異均無統計學意義(P>0.05)。見表3。

表3 4組患者不良反應發生情況比較(n)
3 討論
大量阿片類鎮痛藥的使用能誘發痛覺過敏反應,即阿片類藥物會激活體內的促傷害系統,大大提高機體對傷害性刺激的敏感性[11]。瑞芬太尼是一種人工合成的超短效μ受體激動劑,通過與Gi /Go蛋白偶聯產生鎮痛效應,同時對 k、δ受體也有活性。瑞芬太尼導致痛覺過敏的機制較為復雜,與內源性與外源性阿片類物質的快速失衡、阿片受體快速耐受以及有害物質進入脊髓、易化脊髓痛覺傳導等多種因素有關[12-13]。瑞芬太尼誘發的痛覺過敏主要發生在術后24 h之內,且以術后2 h內尤為明顯。臨床上,患者主觀感覺表現為手術后傷口疼痛更劇烈,嚴重者甚至會因輕微觸摸感到劇烈疼痛[14]。一方面,術后痛覺過敏所致的疼痛會引發患者中樞神經系統、心血管系統及內分泌系統等發生各種變化,對機體造成繼發傷害,影響患者病情的恢復。另一方面,痛覺過敏會增加患者對鎮痛藥物的需求,對機體造成不必要的負擔。因此,預防瑞芬太尼誘發患者術后痛覺過敏,保證患者正常的心理生理狀態,具有重要的臨床意義。
本研究行婦科腹腔鏡手術的患者,手術創傷疼痛程度中等,術后疼痛多以切口疼痛、外科創傷性疼痛為主,且排除了疼痛的性別差異,能夠更客觀地評估實驗藥物對于預防痛覺過敏的作用。
羥考酮屬于中效阿片類鎮痛藥,鎮痛機制主要為激動μ受體和κ受體,且對κ受體的結合力更強[15]。由于激動κ受體參與內臟痛的調節,因此羥考酮被認為是比純μ-受體激動劑更好的內臟痛止痛藥物[16]。納美芬則屬于純阿片受體拮抗劑,給藥后能迅速通過血-腦屏障,與其他阿片受體拮抗劑相比,其半衰期更長,可達10 h,且μ受體選擇性更強[17]。本研究結果顯示,聯合組的意識恢復時間及拔管時間均顯著短于羥考酮組和對照組,但與納美芬組無統計學差異,這可能由于納美芬能夠拮抗阿片類藥物作用,從而加快了患者拔管蘇醒時間。同時,本研究結果顯示,盡管與對照組相比,納美芬組、羥考酮組能一定程度減少患者術后疼痛感,但聯合組的術后各時間段VAS評分明顯優于單一使用納美芬或羥考酮。上述結果提示給患者應用羥考酮聯合小劑量納美芬對于拮抗瑞芬太尼引起的呼吸抑制具有積極意義,同時還能增強激動劑的鎮痛效能,從而預防瑞芬太尼誘發的痛覺過敏反應。推測聯合組較羥考酮效果更好的原因可能有以下幾點:①納美芬能夠將阿片受體激動藥物從Gs偶聯受體結合位點置換出來,通過影響信號系統、離子通道等途徑影響興奮性物質的釋放,阻斷激動藥物對GS偶聯受體的持續活化,以此阻斷痛覺過敏反應的發生[9]。②小劑量μ受體拮抗劑能夠通過抑制腦啡肽突觸前自我抑制系統,來增加內源性腦啡肽的自我釋放,從而發揮一定的鎮痛作用[18]。③阿片受體激動劑對Ca2+通道的興奮作用為細胞內Ca2+濃度升高或Ca2+通道的開放,而小劑量的納美芬可以通過影響Ca2+通道來分解痛覺過敏。此外,本組患者均未出現心動過速,聯合組患者發生惡心嘔吐、嗜睡、頭暈及躁動等不良反應的例數與羥考酮組及對照組無顯著差異。提示小劑量納美芬的使用不僅能夠達到滿意的鎮痛效果,且對不良反應發生的情況并無顯著影響,安全性較優。
4 結論
羥考酮聯合小劑量納美芬使用有助于預防婦科腹腔鏡手術患者瑞芬太尼誘發術后痛覺過敏,縮短術后拔管及蘇醒時間,且不增加不良反應發生風險,可在臨床推廣應用。

