改性毛竹生物炭復合材料對水中磷的動態吸附試驗
李艷紅, 王國豪, 張立浩, 梁 森, 朱義年
(1.桂林理工大學 a.環境科學與工程學院; b.廣西環境污染控制理論與技術重點實驗室; c.巖溶地區水污染控制與用水安全保障協同創新中心, 廣西 桂林 541006; 2.青島華高墨烯科技股份有限公司, 山東 青島 266000)
0 引 言
磷是植物和其他生物所必須的營養元素之一, 同時也是水體富營養化的關鍵因子[1-2]。由于人類活動的影響, 水體P含量過高導致的水體富營養化已成為全球環境問題之一, 有效控制水體中P含量已成為解決全球水體富營養化問題的關鍵[3-4]。目前處理含P廢水的方法有反滲透[5]、電滲析[6]、接觸過濾法[5, 7]、生物法[2]和沉淀法[5], 但其所需成本均較高、操作工藝復雜, 不宜大規模應用。吸附法因其具有工藝簡單、選擇性好、經濟性高的優點而被廣泛應用于水體凈化工程實踐中, 吸附法處理水體中磷主要依賴于吸附劑對磷的作用。目前在吸附法中應用眾多的吸附劑中, 生物炭具有可再生、來源廣、成本低等優勢而成為研究和工程應用的熱點[8]。近年來, 利用金屬氧化物對生物炭進行活化改性, 使生物炭能夠更高效地從水中去除磷酸鹽等污染物的研究引起了廣大學者們的關注。Delaney等[9]研究了多孔材料耦合金屬氧化物在化學工程中對于除磷的作用, 結果顯示多孔材料耦合金屬氧化物是磷酸鹽的有效吸附劑, 在適當的條件下去除率高達100%; Kralchevska等[10]使用高鐵酸鹽(Ⅵ)誘導核殼納米粒子進行原位吸附實驗, 結果表明, 通過對核殼納米粒子表面的吸附, 即可從水中去除磷酸鹽; Fytianos等[11]建立了使用三價鐵從廢水中去除磷的模型, 該模型解釋了加入三價鐵之后, 對水溶液和城市污水中磷酸鹽去除效果的差異; Zach-Maor等[12]建立了固化納米磁鐵礦固定磷酸鹽的Thomas模型, 證明了Thomas模型可以擬合固化納米磁鐵固定磷酸鹽的過程; Rafati等[13]使用含鐵納米粒子的樹脂從水中去除磷酸鹽, 當水體中磷酸鹽初始濃度為6 mg·L-1時, 含鐵納米離子樹脂對水體中磷酸鹽的去除率可達73%左右; 劉桂鳳等[14]以硝酸鐵為改性劑, 對白果殼進行改性制備成白果殼遺態Fe2O3/Fe3O4/C復合材料, 研究了其對Sb(Ⅲ)的去除性能, 結果表明,在初始 Sb(Ⅲ)濃度為 50 mg·L-1時, 其吸附量達9.23 mg·g-1, 吸附過程主要發生配位交換表面絡合反應。
中國是世界上的最大產竹國, 竹類資源豐富[15]。竹類的開采、加工和利用過程中會產生大量低價值的竹類廢棄物, 其有效利用率僅有35%~40%[16]。毛竹是具有復雜多級結構的生物材料, 適合制備生物炭[17-18]。目前, 利用毛竹制作的生物炭吸附劑的種類眾多[19-20], 但利用鐵改性毛竹制生物炭進行動態吸附的研究鮮有報道。本研究以農林廢棄物毛竹為植物模板, 利用鐵氧化物對毛竹生物炭改性, 制備改性的毛竹生物炭復合材料(PMC-Fe/C-B)。首先對原材料進行氨水抽提預處理, 可以有效去除原始材料中堵塞導管孔的侵填體組織、油脂和樹臘等, 浸提后的PMC-Fe/C-B可以完整地復制毛竹的分級多孔結構[21], 孔徑分布為20~50 μm(梯紋導管)、3~10 μm(梯紋導管、螺紋導管)和0.1~1.3 μm(纖維孔)。鐵溶液浸提后進行高溫焙燒, 毛竹模板中的纖維素經過了脫氫、脫氧的過程, 所吸附的Fe(NO3)3在高溫下分解為Fe2O3、NO2和O2。 在高溫含氧環境下, 部分Fe2O3被進一步轉化為磁性氧化鐵(Fe3O4)。通過金屬原位優化改性工藝, 成功負載了Fe2O3/Fe3O4鐵氧化物功能基團。
本文以PMC-Fe/C-B為吸附劑進行P(Ⅴ)溶液的動態吸附試驗, 研究初始濃度、流速、pH值、吸附劑投加量、吸附劑粒徑以及吸附溫度等因素對吸附過程的影響, 通過現代分析手段表征復合材料對水體中P(Ⅴ)吸附前后的變化, 探究吸附劑對水體中P(Ⅴ)的吸附行為和吸附機理。
1 實驗部分
1.1 實驗材料與儀器
實驗材料:磷酸二氫鉀、氨水、硝酸鐵、乙醇, 以上試劑均為分析純; 實驗用水為去離子水。
儀器:真空管式馬弗爐(RS120/750/11/P300, 德國納博熱儀器公司), 紫外分光光度計(UV2100, 尤尼柯上海儀器有限公司), 掃描電子顯微鏡(JSM-6380LV, 日本電子株式會社), 能譜儀(IE350, 英國牛津儀器國際市場有限公司), X射線光電子能譜儀(ESCALAB Mark II, 英國VG科學儀器公司), X射線衍射儀(X′Pert PRO, 荷蘭帕納科公司), 傅里葉變換紅外光譜儀(470 FT-IR, 美國熱電公司)。
1.2 實驗方法
1.2.1 改性材料制備 以農林廢棄物的毛竹旁枝為材料, 經抽提預處理、清洗、烘干、硝酸鐵溶液中循環浸泡、焙燒等工藝制得吸附劑PMC-Fe/C-B[22]。具體制備方法:①將毛竹碎化, 放入5%稀氨水中浸煮(100 ℃,6 h), 用超純水洗凈后烘干(80 ℃, 1 d); ②稱取硝酸鐵溶于乙醇超純水(V∶V=1∶1)混合溶劑中, 制備1.2 mol/L硝酸鐵前驅體溶液, 水浴保溫浸泡稀氨水浸煮烘干后的產物(60 ℃, 5 d)后取出烘干(80 ℃, 1 d); ③重復步驟②3次, 將水浴保溫浸泡的產物置于馬弗爐中焙燒(600 ℃, 3 h), 冷卻至常溫后研磨過篩, 獲得不同粒徑的PMC-Fe/C-B。
1.2.2 動態吸附試驗 將磷酸二氫鉀(KH2PO4)溶于超純水配制模擬含P(Ⅴ)廢水, 以PMC-Fe/C-B為吸附劑, 以含P(Ⅴ)廢水初始濃度、pH值、流速、PMC-Fe/C-B投加量、粒徑和溫度為影響因素開展動態吸附試驗, 研究PMC-Fe/C-B對P(Ⅴ)的動態吸附效果。采用動態吸附模型中較常用的Thomas模型探究改性吸附劑對P(Ⅴ)的吸附行為及其吸附機理。動態吸附試驗在自制小型固定床吸附裝置內進行(圖1)。

圖1 動態吸附實驗裝置圖Fig.1 Dynamic adsorption experimental device①—進水槽; ②—蠕動泵; ③—溫度調節池; ④—吸附柱; ⑤—溫度調節器; ⑥—出水槽; ⑦—循環水泵
PMC-Fe/C-B吸附柱④的長度為200 mm, 外徑為35 mm, 內徑為12 mm(當吸附劑投加量為0.5 g時, 吸附劑的高度為12.3 mm, 吸附體容積BV為1.4 mL)。為避免動態吸附過程中吸附劑的流失, 吸附柱的底部和頂部各設有纖維玻璃膜, 用蠕動泵控制進水流速, 使含P(Ⅴ)廢水自下而上進入吸附柱, 定時采集流出液, 運用過硫酸鉀-鉬銻抗分光光度法(GB 11893—1989)測定流出液中P(Ⅴ)的質量濃度。以《污水綜合排放標準》(GB 8978—1996)規定的P(Ⅴ)一級排放標準質量濃度為穿透點(Cb=0.5 mg·L-1), 以占溶液初始質量濃度90%的流出液P(Ⅴ)質量濃度作為衰竭點。P(Ⅴ)平衡吸附量為
(1)
式中:qtotal為吸附劑對P(Ⅴ)的平衡吸附總量,mg;qe為單位質量吸附劑對P(Ⅴ)的平衡吸附量,mg·g-1;Q為進水流速,mL·min-1;t0為吸附起始時間,min;te為吸附達到平衡所需的時間,min;Cad為已被吸附的P(Ⅴ)質量濃度, mg·L-1;x為吸附劑投加量,g。
通過改變進水初始P(Ⅴ)濃度(5、10、20和30 mg·L-1)、進水流速(4.280、5.136、6.849和8.561 mL·min-1)、進水pH值(1.0、2.0、3.0、4.0、5.0、6.0、8.0、9.0和10.0)、吸附劑投加量(0.3、0.4、0.5和0.6 g)、吸附劑的粒徑(20~40目(0.841~0.4 mm)、40~60目(0.4~0.25 mm)、60~80目(0.25~0.177 mm)、80~100目(0.177~0.149 mm)和>100目(<0.149 mm))和吸附溫度(25、35和45 ℃)等條件對P(Ⅴ)動態吸附的影響因素進行研究。
1.2.3 動態吸附結果的模型 Thomas模型是一種常用的動態吸附模型, 用于預測吸附劑的吸附容量和描述吸附柱的穿透曲線[23-24]。該模型假設在吸附過程中不存在軸向擴散, 因此Thomas模型適用于預測外部和內部擴散阻力非常小的吸附過程。
(2)
式中:Ct、C0—出水、進水濃度, mg·L-1;kTh—Thomas模型常數, mL·(min·mg)-1;qe—吸附劑平衡吸附量, mg·g-1;x—吸附劑在吸附柱中的投加量, g;Q—進水流速, mL·min-1;t—吸附時間, min。
1.2.4 材料表征方法 利用SEM-EDS、FT-IR、XRD和XPS等技術手段對吸附前后的吸附劑進行固相表面元素及其形態的表征, 分析吸附前后PMC-Fe/C-B復合材料的表面元素、基團和價態的變化和分布特征, 從而為吸附過程和機制的研究提供微觀信息和佐證。
2 結果與討論
2.1 動態吸附結果
2.1.1 溶液初始濃度 當進水濃度為5、10和20 mg·L-1時, 達到穿透時(0.5 mg·L-1)的時間(處理水量)分別為96 min(352 BV)、75 min(275 BV)、21 min(77 BV), 達到衰竭時的時間(處理水量)分別為200 min(733 BV)、148 min(543 BV)、86 min(315 BV),qe分別為7.83、12.47和12.39 mg·g-1。表明隨著溶液初始濃度的增加, PMC-Fe/C-B對P(Ⅴ)的吸附效果變差(圖2)。吸附柱里面的吸附點位飽和較慢, 穿透和衰竭時間隨之增加。隨著進水濃度提高, 穿透和衰竭時間大大縮短, 出水濃度隨之升高。

圖2 溶液初始濃度對PMC-Fe/C-B吸附P(Ⅴ)的影響Fig.2 Effect of initial concentration of solution on the adsorption of P(Ⅴ) on PMC-Fe/C-B
2.1.2 進水流速 在低流速條件下吸附柱對P(Ⅴ)的吸附效果更好(圖3)。在低流速下(4.280 mL/min-1)的穿透時間比高流速(8.561 mL·min-1)從12 min(4 BV)延長到了88 min(323 BV), 衰竭時間從70 min(257 BV)延長到了188 min(689 BV)。在較低流速下的qe相對較大, 在4.280、5.136、6.849和8.561 mL·min-1下, 分別為12.92、12.47、12.00和7.95 mg·g-1, 主要是因為流速越小, P(Ⅴ)與PMC-Fe/C-B上的活性位點接觸時間更長更充分, 因此有更多的P(Ⅴ)被去除。當流速從4.280 mL·min-1增加到8.561 mL·min-1時, 總P(Ⅴ)去除率從76.43%降低至58.09%。

圖3 進水流速對PMC-Fe/C-B吸附P(Ⅴ)的影響Fig.3 Effect of inflow velocity on the adsorption of P(Ⅴ)on PMC-Fe/C-B
2.1.3 溶液初始pH 如圖4a、b所示, P(Ⅴ)的吸附受pH的影響較大, 低pH條件(2~3)下對P(Ⅴ)的吸附去除較為有效。pH為2、3時達到穿透點(0.5 mg·L-1)的時間分別為105 min(385 BV)、150 min(550 BV),qe分別為10.70 mg·g-1和12.47 mg·g-1, 去除率分別為70.63%和77.65%。而在其他的pH條件下,qe和去除率依次降低, 表明pH值對穿透曲線的影響較大。當pH從2上升到10時, 去除率從69.58%下降到43.40%。

圖4 溶液初始pH值對PMC-Fe/C-B吸附P(Ⅴ)的影響Fig.4 Effect of initial pH on the adsorption of P(Ⅴ) onPMC-Fe/C-B
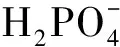
(3)

2.1.4 吸附劑投加量 吸附劑投加量(吸附劑層高)對吸附柱的穿透時間和性能存在較大的影響(圖5)。當PMC-Fe/C-B投加量分別為0.3、0.4、0.5和0.6 g, 穿透時間分別為22 min(81 BV)、25 min(92 BV)、73 min(268 BV)和115 min(422 BV),qe分別為10.28、10.29、12.47和14.38 mg·g-1, 去除率分別為60.12%、63.42%、77.65%和81.23%。在較低的PMC-Fe/C-B投加量條件下, 吸附柱穿透和衰竭都較快, 穿透曲線較陡峭。當PMC-Fe/C-B投加量(吸附劑層高)增加時, P(Ⅴ)離子有更長的時間與吸附劑接觸, 能降低出水中P(Ⅴ)的濃度, 同時可以有效地延緩吸附柱的穿透和衰竭。

圖5 吸附劑投加量對PMC-Fe/C-B吸附P(Ⅴ)的影響Fig.5 Effect of adsorbent dosage on the adsorptionof P(Ⅴ) in PMC-Fe/C-B
2.1.5 吸附劑粒徑 圖6顯示, 吸附劑粒徑越小, PMC-Fe/C-B對P(Ⅴ)的吸附效果越好。當PMC-Fe/C-B粒徑分別為60~80目、80~100目和>100目時,qe分別為7.14、10.80和12.47 mg·g-1。當吸附劑的粒徑從20~40目下降到>100目時, 吸附劑比表面積從138.17 m2·g-1增加到186.66 m2·g-1, 平均孔徑寬度從4.371 13 nm變化到3.289 67 nm, 總孔容從0.150 988 cm3·g-1增大到0.153 514 cm3·g-1, 表明隨著粒徑變小, PMC-Fe/C-B的比表面積增大, 微孔孔容增大, 可供吸附的點位增多且被緩慢結合, 穿透曲線變平坦, 穿透時間相應變長, 吸附能力也就越強。

圖6 吸附劑粒徑對PMC-Fe/C-B吸附P(Ⅴ)的影響Fig.6 Effect of particle size of adsorbent on the adsorptionof P(Ⅴ) in PMC-Fe/C-B
2.1.6 吸附溫度 如圖7所示, 溫度越高, PMC-Fe/C-B對P(Ⅴ)的吸附效果越好。當吸附溫度分別為25、35和45 ℃時, 對應的吸附容量qe分別為11.39、12.47和14.37 mg·g-1,τexp分別為112 min(411 BV)、123 min(451 BV)和143 min(524 BV)。可能是由于PMC-Fe/C-B對P(Ⅴ)的吸附屬于吸熱反應, 提高反應溫度可以促進吸熱反應向正反應方向移動, 促進PMC-Fe/C-B對水體中P(Ⅴ)的吸附, 達到更好的吸附效果。

圖7 吸附溫度對PMC-Fe/C-B吸附P(Ⅴ)的影響Fig.7 Effect of adsorption temperature on the adsorption of P(Ⅴ) in PMC-Fe/C-B
2.2 Thomas模型模擬動態吸附
Thomas模型可以擬合進水流速、溶液初始濃度、吸附劑投加量和環境溫度對PMC-Fe/C-B動態吸附水中P(Ⅴ)性能影響, 擬合參數與誤差分析結果如表1所示, 穿透曲線見圖2~7。

表1 不同條件下PMC-Fe/C-B吸附 P(Ⅴ)的Thomas參數Table 1 Thomas parameters for column adsorption of P(Ⅴ) on PMC-Fe/C-B at different conditions
當進水濃度從5 mg·L-1增加到20 mg·L-1時, Thomas常數kTh呈降低趨勢,qe, exp從7.98 mg·g-1增加到11.67 mg·g-1, 表明此階段是質量傳質主導的吸附過程, 濃度差是吸附反應發生的主要驅動力。 在較高的進水濃度下, 具有的反應驅動力相對較大, 吸附性能相應得到改善。當進水流速從4.280 mL·min-1增加到8.561 mL·min-1時,kTh從0.005 42 mL·(min·mg)-1升高到0.009 62 mL·(min·mg)-1,qe, exp從12.76 mg·g-1降低到7.46 mg·g-1。以上結果表明, 低流速、高進水濃度條件會促進PMC-Fe/C-B對P(Ⅴ)的吸附。同時, 在較低的流速下廢水在吸附柱內具有較長的停留時間, 有利于P(Ⅴ)離子的擴散。當吸附劑投加量從0.3 g增加到0.6 g時, 吸附劑層高從0.98 cm增加到1.48 cm(由吸附劑投加量換算得到[25]),kTh降低,qe, exp從9.78 mg·g-1增加到14.26 mg·g-1。 當吸附劑粒徑從60目到>100目時,kTh從0.007 24 mL·(min·mg)-1降低到0.006 33 mL·(min·mg)-1,qe, exp從6.92 mg·g-1增加到12.36 mg·g-1。當吸附劑的粒徑>100目時, 吸附劑比表面積增加, 平均孔徑寬度變小, 總孔容增大, 可供吸附的點位增多且被緩慢結合, 吸附能力增強。經測定, 吸附劑PMC-Fe/C-B的零點電位pHzpc約為3.3, 吸附劑表面帶正電荷, 易于吸附帶有負電荷的離子, 當pH=3時,qe, exp最大為12.36 mg·g-1, 吸附劑PMC-Fe/C-B對P(Ⅴ)的吸附效果最好。吸附時溫度從25 ℃到45 ℃,kTh從0.006 48 mL·(min·mg)-1降低到0.005 97 mL·(min·mg)-1,qe, exp從11.30 mg·g-1升高到14.33 mg·g-1, 表明適當提高溫度有利于PMC-Fe/C-B對P(Ⅴ)的吸附。
在給定的實驗條件下, 通過Thomas模型計算出的相關系數(R2)較高, 如進水P(Ⅴ)濃度的影響(R2=0.967 8~0.991 2), PMC-Fe/C-B投加量的影響 (R2=0.977 5~0.990 8), 流速的影響(R2=0.948 4~0.990 8), PMC-Fe/C-B粒徑的影響(R2=0.987 5~0.992 0), 溫度的影響(R2=0.979 7~0.9875), pH的影響(R2=0.936 8~0.991 5), 表明Ct/C0和t之間的相關性顯著,qe跟qe, exp存在很高的一致性, 揭示了Thomas模型能夠很好地描述PMC-Fe/C-B對P(Ⅴ)的吸附過程。
2.3 動態吸附表征
2.3.1 SEM-EDS 對初始濃度為50 mg·L-1含P(Ⅴ)溶液吸附處理后的PMC-Fe/C-B進行SEM電鏡掃描和EDS能譜分析(圖8、表2)。吸附P(Ⅴ)后的SEM-EDS結果顯示, PMC-Fe/C-B的螺紋導管上、維管束的蹄管內、纖維細胞腔的徑向壁和橫向壁上的紋孔內可見有成團的沉積物存在。同時, PMC-Fe/C-B的橫、縱截面均存在目標元素P的檢出, 且橫、縱截面的P元素占比分別為1.26%和0.94%。O元素的比例下降, Fe元素比例上升, C元素變化不大。

表2 PMC-Fe/C-B吸附P(Ⅴ)后表面原子濃度的變化

圖8 PMC-Fe/C-B吸附P(Ⅴ)前后的SEM-EDS表征結果Fig.8 SEM-EDS scan spectrogram of PMC-Fe/C-B before and after P(Ⅴ) adsorption
2.3.2 XRD 對PMC-Fe/C-B吸附P(Ⅴ)前后XRD表征結果顯示(圖9), PMC-Fe/C-B吸附P(Ⅴ)后2θ為24.50°、35.47°、49.53°、62.54°的Fe2O3特征峰消失, 2θ為33.21°、54.12°處的Fe2O3特征主峰明顯減弱, 2θ為29.98°處的Fe3O4特征峰有所加強, 揭示了PMC-Fe/C-B吸附P(Ⅴ)后氧化鐵晶型發生了改變, 可能是因為Fe2O3溶于水發生水合反應, 生成了FeOOH。

圖9 PMC-Fe/C-B吸附P(Ⅴ)前后的XRD譜圖Fig.9 XRD patterns of PMC-Fe/C-B after P(Ⅴ) adsorption
2.3.3 FT-IR PMC-Fe/C-B吸附P(Ⅴ)的FT-IR譜圖(圖10)結果顯示, 在PMC-Fe/C-B吸附P(Ⅴ)后, 在波數3 437.33 cm-1處出現較寬的吸收峰, 對應于—OH的反對稱伸縮振動和對稱伸縮振動, 說明吸附后氧化鐵表面出現—OH基團, 同時印證了PMC-Fe/C-B在吸附P(Ⅴ)過程中表面存在酸堿離解行為。

圖10 PMC-Fe/C-B吸附P(Ⅴ)前后的FT-IR譜圖Fig.10 FT-IR patterns of PMC-Fe/C-B after P(Ⅴ) adsorption

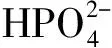

圖11 PMC-Fe/C-B吸附P(Ⅴ)后的XPS全譜掃描圖及Fe2p/C1s/O1s窄譜掃描圖Fig.11 XPS full spectrum scan and Fe2p/C1s/O1s narrow spectral scan of the PMC-Fe/C-B after P(Ⅴ) adsorption

表3 PMC-Fe/C-B吸附P(Ⅴ)后Fe、O的結合能、電荷變化及電子轉移方向
3 結 論
以鐵改性毛竹生物炭復合材料為吸附劑, 當初始濃度為5 mg·L-1, 進水流速為5.136 mL·min-1, pH為3, 吸附劑投加量為1.0 g, 粒徑>100目, 吸附溫度為35 ℃, PMC-Fe/C-B對P(Ⅴ)的最大吸附容量qe, exp為14.26 mg·g-1, 去除率為77.65%,此時PMC-Fe/C-B作為吸附劑對水體中P(Ⅴ)的吸附效果最好。

Thomas模型能較好地擬合和預測不同實驗條件下的P(Ⅴ)吸附試驗數據, 相關性系數R2>0.9。當進水流速、吸附劑投加量(吸附柱層高)和原水P(Ⅴ)濃度增大時, 達到50%穿透所需的時間會有所降低。

