有氧運(yùn)動(dòng)干預(yù)對抑郁癥大鼠HPA軸激活狀態(tài)的影響及其上游調(diào)控機(jī)制
劉威 晉倩 郝選明
摘?要:探討有氧運(yùn)動(dòng)干預(yù)對抑郁癥大鼠HPA軸激活狀態(tài)的影響及其上游調(diào)控機(jī)制。以WKY抑郁大鼠作為動(dòng)物模型,進(jìn)行8周有氧運(yùn)動(dòng)干預(yù),以下丘腦CRH分泌情況反映HPA軸激活狀態(tài),通過海馬Glu和GABA以及下丘腦中這兩種神經(jīng)遞質(zhì)受體表達(dá)探討HPA軸激活的上游調(diào)控機(jī)制。結(jié)果發(fā)現(xiàn):(1)抑郁大鼠CRH顯著升高,表明其HPA軸過度激活,其機(jī)理應(yīng)該與海馬Glu和下丘腦Glu受體高表達(dá)、海馬GABA和下丘腦GABA受體低表達(dá)直接相關(guān)。(2)運(yùn)動(dòng)干預(yù)可以顯著降低CRH的分泌從而改善HPA軸的過度激活狀態(tài),其機(jī)理在于運(yùn)動(dòng)干預(yù)可下調(diào)海馬Glu和下丘腦Glu受體的表達(dá),同時(shí)上調(diào)海馬GABA和下丘腦GABA受體的表達(dá)。(3)運(yùn)動(dòng)干預(yù)可以取得與氟西汀干預(yù)相似的改善效應(yīng),表明有氧運(yùn)動(dòng)干預(yù)可以作為藥物治療抑郁癥的良好替代手段。
關(guān)?鍵?詞:運(yùn)動(dòng)生物化學(xué);抑郁癥大鼠;HPA軸;有氧運(yùn)動(dòng)干預(yù)
中圖分類號:G804.7?文獻(xiàn)標(biāo)志碼:A?文章編號:1006-7116(2021)02-0138-07
Abstract: This study aims to explore effect of aerobic exercise intervention on the activation degree of HPA axis in depressive rats and its upstream regulation mechanism. WKY depressive rats were used as animal models and to carry out 8-week aerobic exercise, and CRH secretion in hypothalamus were used to observe the activation degree of HPA axis, and through expression of Glu and GABA in hippocampus and their receptors in hypothalamus to observe upstream regulation mechanism activated by the HPA axis. The results suggested that: (1) CRH increased significantly in depressive rats, indicating that the HPA axis was over activated, and the mechanism should be directly related to the high expression of Glu in hippocampus and its receptor in hypothalamus, and the low expression of GABA in hippocampus and its receptor in hypothalamus. (2) Exercise intervention lowered HPA axis activation obviously so that the over activation degree of HPA axis could be improved, and the mechanism should be due to down-regulate the expression of Glu in hippocampus and its receptor in hypothalamus, and up-regulate GABA in hippocampus and its receptor in hypothalamus by exercise. (3) Exercise intervention could achieve?improvement effect similar to fluoxetine intervention, which shows that aerobic exercise would be an advisable alternative means to replace the treatment of depression by drugs.
Key words: sports biochemistry;depressive rats;aerobic HPA axis;exercise intervention
抑郁癥是一種以情緒低落、悲觀厭世等為特點(diǎn)的常見的情感障礙性精神疾病,發(fā)病率高(7.8%~17.1%)、致殘率高(47%)、治療率低(不足10%)[1]。據(jù)世界衛(wèi)生組織(WHO)2017年《抑郁癥及其他常見精神障礙》報(bào)告,世界范圍內(nèi)有超過3億人飽受抑郁癥的困擾。我國的情況更不容樂觀,超過9 500萬中國人一生當(dāng)中得過抑郁癥[2]。鑒于此,探索防治抑郁癥的有效手段及其機(jī)制,不僅是一個(gè)重大的科學(xué)問題,更有著突出的實(shí)踐意義。
抑郁癥的發(fā)病機(jī)制非常復(fù)雜。近年來神經(jīng)內(nèi)分泌假說得到了越來越多的支持[3]。該學(xué)說認(rèn)為在抑郁癥發(fā)病進(jìn)程中,HPA軸(Hypothalamus -Pituitary-Adrenal Axis,下丘腦-垂體-腎上腺軸)的過度激活是抑郁癥發(fā)生發(fā)展的病理基礎(chǔ),下丘腦過度分泌CRH(促腎上腺皮質(zhì)激素釋放激素)是抑郁癥成病的關(guān)鍵。研究表明,持續(xù)的抑郁性刺激會激活HPA軸,并通過GC(糖皮質(zhì)激素)反饋性地使海馬受損,使患者出現(xiàn)各種抑郁表現(xiàn),并促進(jìn)抑郁癥的病情惡化[4]。因此HPA軸功能亢進(jìn)被公認(rèn)為是情感障礙的神經(jīng)生物學(xué)發(fā)病機(jī)理中“最后共同通路”,HPA軸功能狀態(tài)正常化對抑郁癥狀的緩解顯得至關(guān)重要[5]。
臨床治療抑郁癥多采用氟西汀等抗抑郁藥物,但其起效慢、副作用多、容易產(chǎn)生耐藥性且復(fù)發(fā)率高。前人有關(guān)運(yùn)動(dòng)對抗抑郁方面的報(bào)道多集中于運(yùn)動(dòng)能夠改善抑郁模型大鼠的行為學(xué)異常狀態(tài)[6],但對影響抑郁癥的調(diào)節(jié)機(jī)制研究不足。適度的運(yùn)動(dòng)已被證明可以影響多種神經(jīng)遞質(zhì)系統(tǒng),如5-羥色胺(5-HT)、多巴胺(DA)、去甲腎上腺素(NE)等激素的釋放[7]。也有研究表明長期參加有氧運(yùn)動(dòng)可降低下丘腦室旁核內(nèi)Glu能神經(jīng)纖維密度,增加GABA能神經(jīng)纖維密度,從而改變PVN內(nèi)交感興奮性神經(jīng)元的“興奮-抑制”平衡[8]。
鑒于此,本研究以WKY抑郁大鼠作為動(dòng)物模型,進(jìn)行8周有氧運(yùn)動(dòng)干預(yù),通過下丘腦CRH分泌的變化,觀察運(yùn)動(dòng)干預(yù)對HPA軸激活狀態(tài)的影響,并從海馬神經(jīng)遞質(zhì)Glu和GABA以及下丘腦中這兩種神經(jīng)遞質(zhì)受體表達(dá)的變化,探討運(yùn)動(dòng)干預(yù)影響HPA軸激活狀態(tài)的上游調(diào)控機(jī)制。此外應(yīng)用氟西汀單獨(dú)干預(yù)以及與運(yùn)動(dòng)結(jié)合的聯(lián)合干預(yù),比較不同干預(yù)手段之間的效果差異及相互影響。
1?實(shí)驗(yàn)材料與方法
1.1?實(shí)驗(yàn)動(dòng)物模型與分組
本實(shí)驗(yàn)研究抑郁癥動(dòng)物模型采用WKY(Wistar Kyoto)大鼠。WKY大鼠具有抑郁化的生理學(xué)行為特征,是一種公認(rèn)的非誘導(dǎo)抑郁動(dòng)物模型。抑郁狀態(tài)穩(wěn)定且對藥物反應(yīng)良好,是理想的內(nèi)源性抑郁癥模型[9]。
8周齡SPF級雄性WKY大鼠40只,Wistar大鼠10只,均購于北京維通利華實(shí)驗(yàn)動(dòng)物技術(shù)有限公司,動(dòng)物合格證編號:SCXK(京)2012-0001。所用飼料為國家標(biāo)準(zhǔn)顆粒型固體大鼠飼料,合格證號:0009161,購于廣東中醫(yī)藥大學(xué)動(dòng)物實(shí)驗(yàn)中心。動(dòng)物飼養(yǎng)環(huán)境在華南師范大學(xué)體育科學(xué)學(xué)院動(dòng)物房,溫度(22±2)℃,濕度40%~50%。動(dòng)物分籠飼養(yǎng),每籠4~5只,自由飲水、飲食,12 h晝夜循環(huán)。飲用水采用雙蒸水。為保持飼養(yǎng)環(huán)境墊料隔2天更換1次,并定期進(jìn)行紫外燈消毒。
實(shí)驗(yàn)大鼠適應(yīng)性喂養(yǎng)一周后分為5組:正常對照組(C,n=10只)、抑郁對照組(DC,n=10只)、運(yùn)動(dòng)干預(yù)組(DE,n=10只)、氟西汀干預(yù)組(DF,n=10只)、運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)組(DEF,n=10只)。
1.2?運(yùn)動(dòng)方案
運(yùn)動(dòng)干預(yù)組和運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)組采用跑臺運(yùn)動(dòng),跑臺坡度均為0°。適應(yīng)性訓(xùn)練1周后正式進(jìn)行有氧運(yùn)動(dòng)干預(yù),跑速15 m/min,30 min/d、3 d/周(周一、三、五),共持續(xù)8周。
1.3?氟西汀灌胃
氟西汀干預(yù)組、運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)組適應(yīng)性喂養(yǎng)1周后,每日早晨給予氟西汀灌胃,灌胃量為1.8 mg/kg/d,1次/d,連續(xù)8周。其余組大鼠按體質(zhì)量灌以相應(yīng)體積的生理鹽水。
1.4?取材
第8周最后一次運(yùn)動(dòng)后24 h,各組取材。具體過程:腹腔注射體積分?jǐn)?shù)10%水合氯醛(0.35~0.40) mL/kg進(jìn)行麻醉,打開胸腔,將灌注針頭經(jīng)左心室插至升主動(dòng)脈,剪開右心耳,進(jìn)行灌注,待大鼠全身僵直后無菌斷頭,剝離完整大腦,分離出海馬及下丘腦,一側(cè)海馬用錫紙包裹,做好標(biāo)記,迅速置于液氮中,隨后轉(zhuǎn)入-80℃超低溫冰箱保存待測。另一側(cè)海馬及下丘腦放入固定液中保存待測。
1.5?主要實(shí)驗(yàn)試劑與設(shè)備
兔抗CRH、NR1、NR2B、GABAAα2多克隆抗體(Thermo);即用型免疫組化試劑盒(福州邁新生物技術(shù)有限公司);Glu、GABA Elisa試劑盒(江蘇酶免生物科技);酶標(biāo)儀及洗板機(jī)(Bio-Rad);熒光顯微鏡(Olympus);切片機(jī)、組織脫水機(jī)、包埋機(jī)(德國Leica);超純水機(jī)(美國ELGA);動(dòng)物跑臺(廣州飛迪生物科技有限公司)。
1.6?測試指標(biāo)與方法
1)海馬組織Glu與GABA測定。
采用酶聯(lián)免疫吸附法(ELISA)進(jìn)行測定。海馬組織冰上解凍,冰上研磨制成勻漿,3 000 r離心20 min,取上清液保存待測。50 μL不同濃度標(biāo)準(zhǔn)品滴入相應(yīng)孔中。待測樣本50 μL滴入樣本孔中。標(biāo)準(zhǔn)品孔和樣本孔中滴入辣根過氧化物酶(HRP)標(biāo)記的被檢測抗體100 μL,封板膜密封溫育60 min(37°C),洗板5次。底物A、B各50 μL滴入每個(gè)孔,避光(37°C)孵育15 min。每孔加入終止液各50 μL,用酶標(biāo)儀在450 nm波長下測定光密度值D(λ),通過標(biāo)準(zhǔn)曲線計(jì)算樣品中所含Glu的質(zhì)量濃度和GABA的濃度。
2)下丘腦室旁核(pvn)Glu受體(NR1、NR2B亞基)、GABA受體(GABAAα2亞基)以及CRH測定。
采用SP法進(jìn)行下丘腦免疫組化染色,DAB顯色。常規(guī)脫水、透明、封固。40×10光鏡視野下,每個(gè)切片選取3~5個(gè)視野,采用ImagePro plus軟件進(jìn)行陽性面積定量分析,得出IOD(積分光密度)和Area(陽性面積),由Density=IOD/Area計(jì)算平均光密度(OD·μm-2)。
1.7?數(shù)據(jù)分析及處理
本實(shí)驗(yàn)的數(shù)據(jù)均采用SPSS21.0統(tǒng)計(jì)軟件進(jìn)行處理,采用平均數(shù)±標(biāo)準(zhǔn)差()表示,組間比較采用單因素方差分析,兩組間比較采用成對樣本T檢驗(yàn),以P<0.05作為差異顯著性水平。
2?實(shí)驗(yàn)結(jié)果與分析
2.1?各組大鼠海馬Glu、GABA的表達(dá)
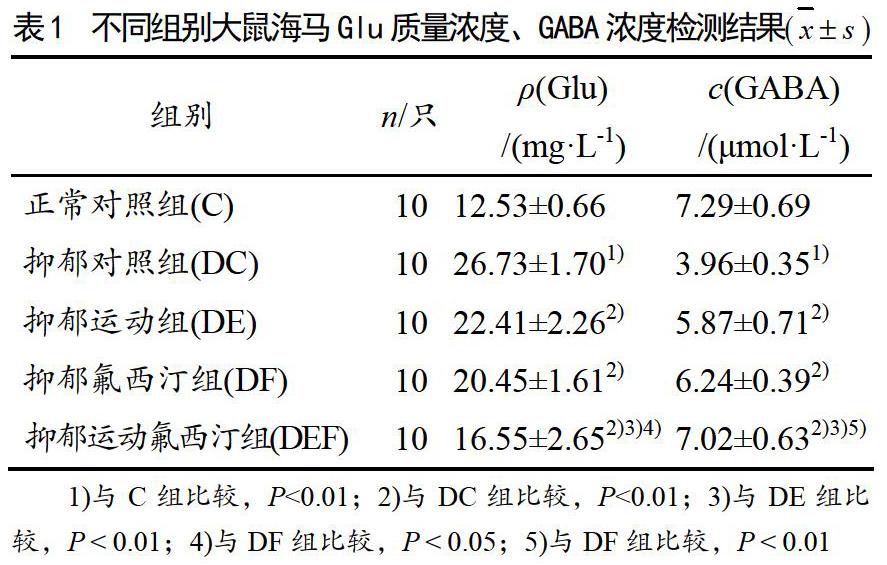
各組大鼠海馬中Glu和GABA的表達(dá)情況參見表1。
與正常對照組相比,抑郁組對照組Glu水平提升非常顯著(P<0.01),而GABA則出現(xiàn)非常顯著降低 (P<0.01),提示抑郁大鼠海馬興奮性氨基酸遞質(zhì)Glu表達(dá)顯著升高,而抑制性氨基酸遞質(zhì)GABA的表達(dá)則明顯受到抑制,興奮性氨基酸遞質(zhì)與抑制性氨基酸遞質(zhì)處于明顯的失衡狀態(tài)。
與抑郁對照組相比,運(yùn)動(dòng)干預(yù)組海馬中Glu的表達(dá)非常顯著降低(P<0.01);而海馬中GABA的表達(dá)則非常顯著性升高(P<0.01),提示有氧運(yùn)動(dòng)干預(yù)在顯著降低海馬Glu表達(dá)的同時(shí)明顯地提升海馬GABA表達(dá)水平,以此改善海馬神經(jīng)遞質(zhì)表達(dá)的平衡狀態(tài)。
氟西汀干預(yù)組的干預(yù)效果與運(yùn)動(dòng)干預(yù)組相類似,其Glu表達(dá)相對抑郁組出現(xiàn)非常顯著降低(P<0.01),而GABA表達(dá)則提升顯著(P<0.01),提示氟西汀干預(yù)也能夠顯著下調(diào)海馬Glu的表達(dá)并顯著上調(diào)GABA的表達(dá)。
運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)組的干預(yù)效果最為顯著,與單一干預(yù)手段相比,其海馬Glu表達(dá)呈現(xiàn)顯著性下降(P<0.05),而海馬GABA的表達(dá)則出現(xiàn)顯著性升高(P<0.01),提示聯(lián)合干預(yù)效果優(yōu)于運(yùn)動(dòng)干預(yù)或藥物干預(yù)單一干預(yù)手段,更有助于改善海馬神經(jīng)遞質(zhì)表達(dá)的平衡狀態(tài)。
2.2?各組大鼠下丘腦室旁核Glu受體(NR1亞基,NR2B亞基)的表達(dá)
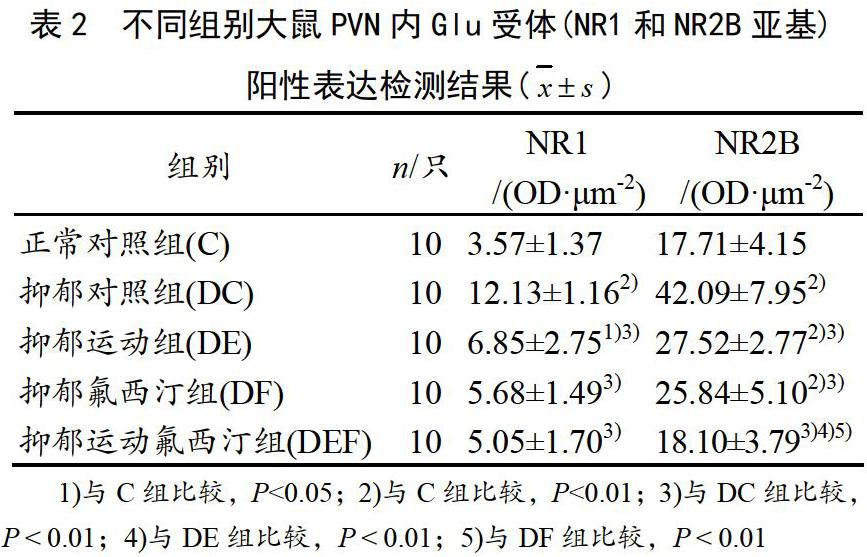
各組大鼠下丘腦PVN內(nèi)NR1和NR2B兩種受體表達(dá)情況見表2。
與正常對照組相比,抑郁對照組兩種受體表達(dá)均非常顯著性升高(P<0.01),提示抑郁對照組大鼠下丘腦PVN內(nèi)Glu的兩種受體亞型的表達(dá)均非常顯著性升高。
與抑郁對照組相比,運(yùn)動(dòng)干預(yù)組下丘腦PVN內(nèi)兩降種Glu受體亞型NR1和NR2B呈現(xiàn)非常顯著性降低(P<0.01),提示有氧運(yùn)動(dòng)干預(yù)能夠顯著下調(diào)興奮性神經(jīng)遞質(zhì)Glu受體的過度表達(dá)。
氟西汀干預(yù)組兩種Glu受體亞型變化趨勢與運(yùn)動(dòng)組類似,提示氟西汀也能夠有效下調(diào)Glu受體的過度激活。
運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)組下調(diào)兩種Glu受體亞型NR1和NR2B效果最佳,甚至可將因抑郁升高的受體表達(dá)水平下調(diào)至基本接近對照組水平,差異沒有統(tǒng)計(jì)學(xué)意義(P>0.05),提示運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)其效果優(yōu)于單一干預(yù)手段,具有一定的疊加效應(yīng)。
2.3?各組大鼠下丘腦室旁核GABA受體(GABAAα2)的表達(dá)
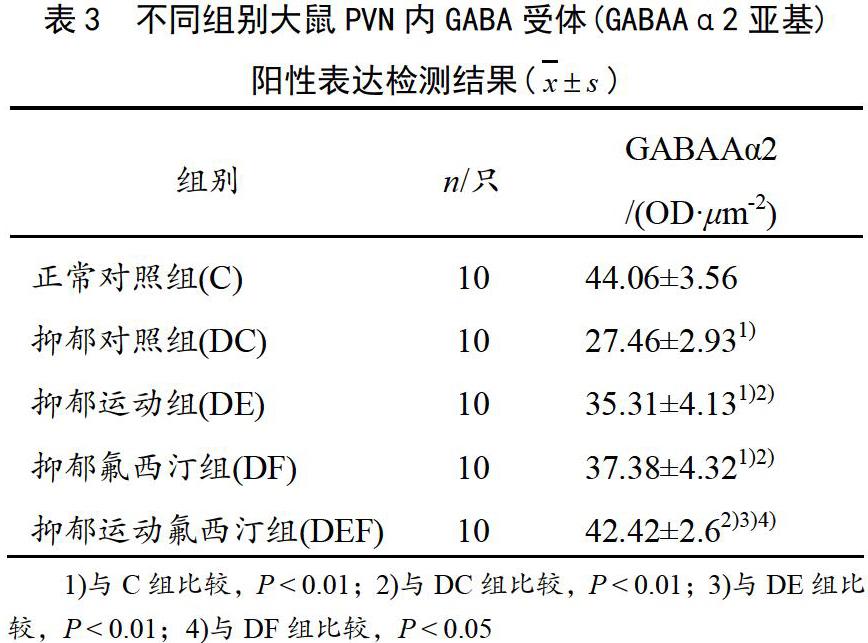
各組大鼠在下丘腦PVN內(nèi)GABA受體GABAAα2的表達(dá)情況見表3。
與正常對照組相比,抑郁對照組抑制性氨基酸GABA受體GABAAα2的表達(dá)呈現(xiàn)非常顯著性降低(P<0.01),提示抑郁對照組大鼠下丘腦PVN內(nèi)GABA受體的表達(dá)受到明顯抑制。
與抑郁對照組相比,運(yùn)動(dòng)干預(yù)組下丘腦PVN內(nèi)GABA受體亞型GABAAα2呈現(xiàn)非常顯著性升高(P<0.01),提示有氧運(yùn)動(dòng)干預(yù)能夠顯著上調(diào)抑制性神經(jīng)遞質(zhì)GABA受體的表達(dá)。
氟西汀干預(yù)組GABA受體亞型變化趨勢與運(yùn)動(dòng)組類似,GABAAα2相對于抑郁對照組出現(xiàn)非常顯著升高(P<0.01),提示氟西汀也能夠有效上調(diào)GABA受體的表達(dá)。
運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)組上調(diào)GABA受體亞型GABAAα2的效果最佳,其值與正常對照組相比未出現(xiàn)顯著性差異(P>0.05),提示運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)效果優(yōu)于單一干預(yù)手段,具有一定的疊加效應(yīng)。
2.4?各組大鼠下丘腦室旁核(PVN)CRH的表達(dá)
各組大鼠下丘腦PVN內(nèi)CRH的表達(dá)情況見表4。
與正常對照組相比,抑郁對照組大鼠下丘腦PVN內(nèi)CRH表達(dá)出現(xiàn)非常顯著性升高(P<0.01),提示抑郁大鼠HPA軸被強(qiáng)烈激活。
與抑郁對照組相比,運(yùn)動(dòng)干預(yù)組CRH表達(dá)水平出現(xiàn)非常顯著性下降(P<0.01),提示運(yùn)動(dòng)干預(yù)可明顯抑制抑郁大鼠HPA軸的過度激活。
氟西汀干預(yù)組CRH表達(dá)變化趨勢與運(yùn)動(dòng)干預(yù)組類似,CRH表達(dá)水平與抑郁對照組之間差異具有非常顯著統(tǒng)計(jì)學(xué)意義(P<0.01),提示氟西汀干預(yù)可明顯抑制HPA軸的激活程度。
運(yùn)動(dòng)聯(lián)合氟西汀干預(yù)組對CRH表達(dá)水平的下調(diào)作用優(yōu)于單一干預(yù)手段,并具有一定的疊加效應(yīng)。
3?討論
3.1?抑郁大鼠HPA軸的功能狀態(tài)及其調(diào)控機(jī)理
HPA軸(下丘腦-垂體-腎上腺軸)持續(xù)性的過度激活是抑郁癥形成和發(fā)展的重要病因?qū)W基礎(chǔ)。HPA軸是機(jī)體重要的神經(jīng)內(nèi)分泌免疫調(diào)控通路,是神經(jīng)內(nèi)分泌免疫網(wǎng)絡(luò)的樞紐[10]。HPA軸最上位的下丘腦充當(dāng)著神經(jīng)系統(tǒng)和內(nèi)分泌系統(tǒng)的“聯(lián)絡(luò)員”,即神經(jīng)-體液調(diào)節(jié)的“連接器”,當(dāng)機(jī)體感受到體內(nèi)外各種刺激時(shí),會通過向下丘腦釋放神經(jīng)遞質(zhì),并與相應(yīng)受體結(jié)合后,促使下丘腦釋放CRH,從而激活HPA軸[11]。下丘腦所釋放的CRH,會在HPA軸產(chǎn)生瀑布式的級聯(lián)放大效應(yīng),形成一個(gè)效能極高的生物放大系統(tǒng)。0.1 μg CRH可以使腺垂體釋放1 μg ACTH (促腎上腺皮質(zhì)激素),后者再進(jìn)一步引起腎上腺皮質(zhì)分泌40 μg GC[12]。
本實(shí)驗(yàn)研究發(fā)現(xiàn),與正常對照組相比,抑郁對照組大鼠下丘腦PVN內(nèi)CRH表達(dá)出現(xiàn)非常顯著性升高,其值高達(dá)正常值的2.87倍(參見圖1a),表明抑郁大鼠HPA軸處于高度激活狀態(tài)。
CRH的分泌活動(dòng)(HPA軸的激活程度)受控于海馬興奮性氨基酸遞質(zhì)Glu(以及在下丘腦PVN內(nèi)相應(yīng)受體的表達(dá))和抑制性氨基酸遞質(zhì)GABA(以及在下丘腦PVN內(nèi)相應(yīng)受體的表達(dá))的綜合作用,前者促進(jìn)CRH的分泌從而激活HPA軸,后者則對HPA軸的激活起著抑制作用[13]。
神經(jīng)遞質(zhì)通過與各自的特異性受體結(jié)合來對細(xì)胞的行為及生理活動(dòng)進(jìn)行調(diào)節(jié)。Glu是哺乳動(dòng)物腦內(nèi)最重要且含量最高的興奮性神經(jīng)遞質(zhì),對中樞神經(jīng)系統(tǒng)中幾乎所有的神經(jīng)元都有興奮作用。Glu的受體分為離子型受體(iGluR)和代謝型受體(mGluR),其中離子型受體中的NMDA受體多存在于海馬和皮質(zhì)中,并與應(yīng)激導(dǎo)致的興奮性神經(jīng)毒性、突觸可塑性、神經(jīng)退行性變等功能密切相關(guān)[14]。NR1和NR2B作為NMDA受體中的功能亞基和調(diào)節(jié)亞基,對于保持受體功能的完整性具有不可或缺的作用[15]。而GABA則是哺乳類動(dòng)物中樞神經(jīng)系統(tǒng)最重要的抑制性神經(jīng)遞質(zhì),幾乎對所有的神經(jīng)元都有抑制作用。GABAAα2則作為GABA受體亞單位逐漸成為研究情感障礙疾病的焦點(diǎn)因子[16]。
本實(shí)驗(yàn)研究發(fā)現(xiàn),與正常對照組大鼠相比,抑郁大鼠海馬興奮性氨基酸遞質(zhì)Glu水平升高達(dá)2.13倍,同時(shí),下丘腦PVN內(nèi)Glu受體亞型NR1和NR2B表達(dá)也分別提升了3.39倍和2.38倍(參見圖1b)。海馬Glu的高表達(dá)以及下丘腦相應(yīng)受體的高表達(dá)勢必會顯著加強(qiáng)對下丘腦CRH陽性神經(jīng)元的刺激,促使CRH表達(dá)顯著增多,HPA軸被過度激活。本實(shí)驗(yàn)研究還發(fā)現(xiàn),作為與興奮性氨基酸Glu起拮抗作用的抑制性氨基酸遞質(zhì),GABA在抑郁大鼠海馬的表達(dá)只占到正常對照組大鼠的54.3%,同時(shí),下丘腦PVN內(nèi)GABA受體GABAAα2的表達(dá)只占到正常對照組大鼠的62.3%(參見圖1c),海馬GABA的低表達(dá)以及下丘腦相應(yīng)受體的低表達(dá)勢必會顯著減弱對CRH分泌的抑制作用,使HPA軸更易于被過度激活。
綜上所述,抑郁會造成海馬興奮性、抑制性氨基酸神經(jīng)遞質(zhì)及其受體表達(dá)失衡,促使CRH分泌增多,過度激活HPA軸;通過應(yīng)激軸的級聯(lián)放大效應(yīng)會導(dǎo)致腎上腺皮質(zhì)分泌更多的GC。這些GC通過血液循環(huán),與海馬神經(jīng)元富含的GR(糖皮質(zhì)激素受體)結(jié)合,導(dǎo)致海馬神經(jīng)元出現(xiàn)萎縮、凋亡及神經(jīng)再生障礙等一系列的可塑性損傷,使抑郁現(xiàn)象進(jìn)行性加重。海馬神經(jīng)元受損,并進(jìn)一步上調(diào)興奮性氨基酸遞質(zhì)Glu在海馬的表達(dá)(以及下丘腦Glu受體的表達(dá)),同時(shí)下調(diào)抑制性氨基酸遞質(zhì)GABA的表達(dá)(以及下丘腦GABA受體的表達(dá)),促使下丘腦釋放更多的CRH,由此造成HPA軸被進(jìn)一步激活,從而形成一個(gè)惡性循環(huán),促使抑郁癥發(fā)生和發(fā)展。
3.2?運(yùn)動(dòng)干預(yù)對抑郁大鼠HPA軸功能狀態(tài)的影響及調(diào)控機(jī)制
HPA軸持續(xù)性過度激活是抑郁癥神經(jīng)內(nèi)分泌的主要變化之一。本實(shí)驗(yàn)研究發(fā)現(xiàn),有氧運(yùn)動(dòng)干預(yù)可以顯著降低CRH的分泌,從而有效糾正HPA軸的過度激活狀態(tài)。從圖2a可見,與正常對照組大鼠相比,抑郁大鼠下丘腦CRH表達(dá)水平顯著升高,表明抑郁大鼠HPA軸處于明顯的過度激活狀態(tài),而運(yùn)動(dòng)大鼠下丘腦CRH的表達(dá)水平較之抑郁大鼠呈現(xiàn)非常顯著性降低,降低幅度高達(dá)49.5%,表明長期有氧運(yùn)動(dòng)可以非常有效地改善抑郁癥所形成的HPA軸過度激活狀態(tài)。
如前所述,抑郁大鼠CRH分泌增多,HPA軸過度激活的主要原因在于興奮性氨基酸遞質(zhì)及其受體的高表達(dá)、抑制性氨基酸遞質(zhì)及其受體的低表達(dá)共同作用的結(jié)果。本實(shí)驗(yàn)研究表明,運(yùn)動(dòng)干預(yù)對HPA軸的影響也是通過這一機(jī)制。與抑郁組大鼠相比,運(yùn)動(dòng)干預(yù)組大鼠海馬Glu水平降幅達(dá)16.1%,下丘腦內(nèi)Glu受體亞型NR1和NR2B表達(dá)分別降至抑郁組的56.4%和65.4%(參見圖2b)。可見運(yùn)動(dòng)干預(yù)會通過下調(diào)海馬Glu的表達(dá),尤其是通過顯著下調(diào)下丘腦相應(yīng)受體NR1和NR2B的表達(dá),會顯著減弱對下丘腦CRH陽性神經(jīng)元的興奮作用。而在功能上與興奮性氨基酸相對抗的抑制性氨基酸遞質(zhì),則出現(xiàn)明顯的上調(diào)現(xiàn)象。由圖2c可見,與抑郁大鼠GABA的低表達(dá)比較,運(yùn)動(dòng)組大鼠的表達(dá)水平則明顯增高,升幅高達(dá)48.2%。同時(shí),下丘腦內(nèi)GABA的受體GABAAα2表達(dá)也升高了28.6%。可見運(yùn)動(dòng)干預(yù)主要通過顯著上調(diào)海馬GABA的表達(dá),其次上調(diào)下丘腦GABA受體GABAAα2的表達(dá)來顯著加強(qiáng)對下丘腦CRH陽性神經(jīng)元的抑制作用。
綜上所述,運(yùn)動(dòng)干預(yù)主要通過興奮性氨基酸和抑制性氨基酸的相互作用來調(diào)控CRH的分泌和HPA軸的激活狀態(tài)。一方面,通過下調(diào)興奮性氨基酸遞質(zhì)及其受體表達(dá)水平減弱對下丘腦CRH陽性神經(jīng)元的興奮作用;另一方面,通過上調(diào)抑制性氨基酸遞質(zhì)及其受體表達(dá)水平加強(qiáng)對下丘腦CRH的抑制作用。兩者共同作用的結(jié)果,下丘腦CRH表達(dá)水平顯著降低,HPA軸過度激活狀態(tài)顯著改善,GC分泌減少,GC減少后與海馬神經(jīng)元GR結(jié)合量降低;一方面改善抑郁癥造成的海馬神經(jīng)元萎縮、凋亡及神經(jīng)再生障礙等,使抑郁現(xiàn)象減輕,另一方面則會進(jìn)一步下調(diào)興奮性氨基酸遞質(zhì)Glu在海馬的表達(dá)(以及下丘腦Glu受體的表達(dá)),同時(shí)上調(diào)抑制性氨基酸遞質(zhì)GABA的表達(dá)(以及下丘腦GABA受體的表達(dá));兩者共同作用的結(jié)果使下丘腦釋放的CRH進(jìn)一步減少,HPA軸過度激活狀態(tài)進(jìn)一步改善,從而形成良性循環(huán),促使抑郁癥狀不斷改善。
3.3?氟西汀干預(yù)與聯(lián)合干預(yù)對抑郁大鼠HPA軸功能狀態(tài)的影響及調(diào)控機(jī)制
目前抑郁癥的主要治療方法是藥物治療,氟西汀是常用藥物[17]。本實(shí)驗(yàn)研究在觀察運(yùn)動(dòng)干預(yù)對抑郁大鼠HPA軸功能狀態(tài)影響的同時(shí),還觀察了氟西汀對HPA軸的影響。由圖3a可見,與抑郁對照組大鼠相比,氟西汀組大鼠下丘腦CRH水平顯著降低,降低幅度高達(dá)53.5%,甚至稍優(yōu)于運(yùn)動(dòng)組干預(yù)效果,表明氟西汀干預(yù)也可以有效地改善抑郁癥所形成的HPA軸持續(xù)性過度激活狀態(tài)。
本實(shí)驗(yàn)研究發(fā)現(xiàn),氟西汀干預(yù)組大鼠較之抑郁對照組大鼠,興奮性氨基酸遞質(zhì)Glu在海馬的表達(dá)降低了23.5%,下丘腦Glu受體NR1和NR2的表達(dá)水平也出現(xiàn)明顯降低,降幅分別達(dá)到53.2%和38.6%(見圖3b),表明氟西汀可以顯著下調(diào)興奮性氨基酸及其受體的高表達(dá)。與抑郁大鼠相比,海馬抑制性氨基酸遞質(zhì)GABA表達(dá)極顯著升高,升幅高達(dá)57.6%,下丘腦中相應(yīng)受體GABAAα2也提升了36.1%(見圖3c),表明氟西汀可以有效上調(diào)抑制性氨基酸的表達(dá)。兩種對抗性神經(jīng)遞質(zhì)及其受體表達(dá)變化綜合作用的結(jié)果,會明顯抑制CRH陽性神經(jīng)元的興奮程度,減少CRH的分泌,從而改善抑郁大鼠HPA軸的過度激活狀態(tài)。
比較運(yùn)動(dòng)干預(yù)和藥物干預(yù)實(shí)驗(yàn)結(jié)果可以看出,藥物干預(yù)對HPA軸過度激活的改善效果及其機(jī)理與運(yùn)動(dòng)干預(yù)相類似,那么氟西汀干預(yù)是否可以替代運(yùn)動(dòng)干預(yù)?分析認(rèn)為,藥物雖可控制抑郁病情,但并未從根本上改變抑郁癥發(fā)病機(jī)制,因此長期服藥效果會越來越差,且一旦停藥后,對HPA軸的抑制效應(yīng)就會解除,HPA軸又會重新陷入CRH升高—HPA軸過度激活—GC升高—同海馬GR過度結(jié)合—海馬萎縮—神經(jīng)可塑性降低—抑郁病情加重—CRH升高……這樣惡性循環(huán),導(dǎo)致抑郁癥復(fù)發(fā)甚至惡化。而長期的有氧運(yùn)動(dòng)干預(yù)則不同,它可從根本上改善海馬和下丘腦的形態(tài)、結(jié)構(gòu)和功能,從內(nèi)在機(jī)制上改善HPA軸的過度激活狀態(tài),進(jìn)入良性循環(huán),以延緩抑郁癥的發(fā)生和發(fā)展。因此,從調(diào)控HPA軸過度激活、改善抑郁癥狀這個(gè)意義上而言,藥物不能代替運(yùn)動(dòng),相反,長期有氧運(yùn)動(dòng)干預(yù)可以作為藥物治療抑郁癥的良好替代手段。
本實(shí)驗(yàn)研究還設(shè)置了聯(lián)合干預(yù)組,即氟西汀干預(yù)+運(yùn)動(dòng)干預(yù),以觀察運(yùn)動(dòng)結(jié)合藥物干預(yù)對HPA軸激活狀態(tài)的影響,結(jié)果見圖4。
由圖4可見,與抑郁對照組大鼠相比,聯(lián)合干預(yù)組大鼠CRH下降59.3%(見圖4a),Glu以及受體NR1、NR2表達(dá)分別下降38.1%、58.4%和57%(見圖4b);而GABA和受體GABAAα2的表達(dá)則分別提升77.3%和54.5%(見圖4c)。實(shí)驗(yàn)發(fā)現(xiàn),與運(yùn)動(dòng)或藥物單一干預(yù)手段相比,聯(lián)合干預(yù)時(shí)CRH、Glu、NR1、NR2的降幅更大,而GABA和GABAAα2的升幅也更明顯。可見,從改善HPA軸過度激活的角度而言,運(yùn)動(dòng)和藥物聯(lián)合干預(yù)時(shí),兩種干預(yù)手段之間沒有出現(xiàn)拮抗效應(yīng),反而具有一定程度的疊加效應(yīng)。
4?結(jié)論
1)抑郁大鼠CRH表達(dá)水平顯著升高,表明HPA軸處于過度激活狀態(tài)。其機(jī)理在于抑郁會造成海馬興奮性、抑制性氨基酸神經(jīng)遞質(zhì)及其受體表達(dá)失衡,即海馬興奮性氨基酸遞質(zhì)Glu以及相應(yīng)受體NR1、NR2在下丘腦的高表達(dá),會加強(qiáng)CRH陽性神經(jīng)元的興奮作用,而海馬抑制性氨基酸GABA以及相應(yīng)受體GABAAα2在下丘腦的低表達(dá),則減弱對CRH分泌的抑制作用。
2)運(yùn)動(dòng)大鼠CRH表達(dá)水平顯著降低,表明HPA軸過度激活狀態(tài)得到明顯改善。其機(jī)理在于運(yùn)動(dòng)干預(yù)一方面通過下調(diào)興奮性氨基酸遞質(zhì)及其受體表達(dá)水平減弱對下丘腦CRH陽性神經(jīng)元的興奮作用;另一方面則上調(diào)抑制性氨基酸遞質(zhì)及其受體表達(dá)水平加強(qiáng)對下丘腦CRH的抑制作用。
3)氟西汀干預(yù)可對HPA軸產(chǎn)生與運(yùn)動(dòng)干預(yù)相似的改善效應(yīng),表明有氧運(yùn)動(dòng)干預(yù)可以作為藥物治療抑郁癥的良好替代手段。運(yùn)動(dòng)聯(lián)合藥物干預(yù)未出現(xiàn)相互拮抗現(xiàn)象,甚至具有一定疊加效應(yīng),提示兩者可以并用。
參考文獻(xiàn):
[1] NARROW W E,RAE D S. Revised prevalence estimates of mental disorders in the United States: using a clinical significance criterion to reconcile 2 surveys' estimates[J]. Arch Gen Psychiatry,2002,59(2):115-123.
[2] HUANG Y,WANG Y,WANG H,et al. Prevalence of mental disorders in China:A cross-sectional epidemiological study[J]. Lancet Psychiatry,2019,6(3):211-224.
[3] MAKRIS AP,KARIANAKI M,TSAMIS K I,et al. The role of the gut-brain axis in depression:endocrine,neural,and immune pathways[J]. Hormones (Athens),2020,10.1007/s42000-020-00236-4.
[4] WILEY J W,HIGGINS G A,ATHEY B D. Stress and glucocorticoid receptor transcriptional programming in time and space: Implications for the brain-gut axis[J]. Neurogastroenterol Motil,2016,28(1):12-25.
[5] COWEN P J. Not fade away: the HPA axis and depression[J]. Psychol Med,2010,40(1):1-4.
[6] 魏宏文,矯瑋,張有志,等. 運(yùn)動(dòng)對慢性應(yīng)激抑郁模型大鼠行為學(xué)及體重的影響[J]. 體育學(xué)刊,2010,17(11):100-105.
[7] ZEMBERI N,ISMAIL M M,ABDULLAH M. Exercise interventions as the primary treatment for depression: Evidence from a narrative review[J]. Malays J Med Sci,2020,27(5):5-23.
[8] 王松濤,曾云貴,王安利. 有氧運(yùn)動(dòng)對大鼠心血管自主神經(jīng)中樞Glu能神經(jīng)和GABA能神經(jīng)的影響[J]. 體育科學(xué),2007,27(4):64-71.
[9] SOLBERG L C,AHMADIYEH N,BAUM A E,et al. Depressive-like behavior and stress reactivity are independent traits in a Wistar Kyoto x Fisher 344 cross[J]. Mol Psychiatry,2003,8(4):423-33.
[10] FUTCH H S,MCFARLAND K N,MOORE B D,et al. An anti-CRF antibody suppresses the HPA axis and reverses stress-induced phenotypes[J]. J Exp Med,2019,216(11):2479-2491.
[11] KLAMPFL S M,BRUNTON P J,BAYERL D S,et al. CRF-R1 activation in the anterior-dorsal BNST induces maternal neglect in lactating rats via an HPA axis-independent central mechanism[J]. Psychoneuro Endocrinology,2016,64:89-98.
[12] CASSARINO M F. Proopiomelanocortin,glucocorticoid,and CRH receptor expression in human ACTH-secreting pituitary adenomas[J]. Endocrine,2017,55(3):853-860.
[13] MAGUIRE J. Stress-induced plasticity of GABAergic inhibition[J]. Front Cell Neuro Sci, 2014(8):157.
[14] LIU Y,ZHANG J. Recent development in NMDA receptors[J]. Chin Med J,2000,113(10):948-956.
[15] BORZA I,BOIO E,BARAT-SIALAI B,et al. Selective NR1/2B N-methyl-D-aspartate receptor antagonists among indole-2-carboxamides and benzimidazole-2- carboxamides[J]. J Med Chem,2007,50(5):901-914.
[16] VOLLENWEIDER I,SMITH K S,KEIST R. Antidepressant- like properties of alpha2-containing GABA(A) receptors[J]. Behav Brain Res,2011,217(1):77-80.
[17] PANWAR R,SIVAKUMAR M. Changes in the levels of comet parameters before and after fluoxetine therapy in major depression patients[J]. Anatomy Cell Biology,2020,53(2):194-200.

