MiR-146a介導依那西普對強直性脊柱炎活動期患者炎癥因子和骨代謝的影響
直彥亮,林思薪,賀 憲,張 震
(1.廣州市番禺區中醫院,廣東廣州 511400;2.深圳市中西醫結合醫院,廣東深圳 518104)
強直性脊柱炎(ankylosing spondylitis,AS) 是發病率較高的一類自身免疫性疾病,主要導致脊柱和關節化強直[1],是AS 患者殘疾的主要病理因素。目前臨床上對AS常采用非甾體抗炎藥和生物制劑進行治療[2]。依那西普(Etanercept)是一類腫瘤壞死因子拮抗劑,通過拮抗TNF-α 表達,抑制炎癥,起到治療AS 的作用[3]。研究表明微小RNA(MicroRNA,miRNA)在成骨細胞和破骨細胞發生發展中發揮重要作用,調控骨形成、骨吸收和骨重塑等過程[4]。Wnt/β-catenin經典信號通路在成骨過程中發揮重要作用,可促進成骨細胞生成的主要通路。OPG/ RANKL/ RANK信號通路是細胞調節骨代謝平衡的關鍵系統[5]。RANKL 與RANK 結合后,激活RANK 和NF-κB,進而引發破骨細胞基因轉錄,促進破骨細胞形成分化成熟。而OPG 在破骨細胞外與RANKL 競爭性結合,使RANK 失活,抑制破骨細胞分化和破骨細胞活性,阻礙骨吸收[6]。OPG、RANKL、RANK 三者相互作用,共同構成了調節骨代謝平衡的OPG/RANKL/RANK 系統。miR-146a 可以抑制炎癥發生,并且可能成為AS的一種診斷生物學標志[7]。而依那西普是否與miR-146a存在關系,以及miR-146a對骨代謝以及Wnt/βcatenin、OPG/RANKL/RANK 信號通路是否有影響,均未有相關研究報道。本研究擬通過研究依那西普對強直性脊柱炎小鼠miR-146a 表達的影響,以及依那西普和miR-146a對炎癥因子、骨代謝的影響,為深入了解依那西普生物學機制及治療靶點提供支持。
1 研究對象及材料
1.1 研究對象
以56 例AS 活動期患者與45 只鼠齡4~5 周的雄性健康BALB/c 小鼠(北京維通利華實驗動物技術有限公司)作為研究對象。
AS 活動期患者選自2017 年1 月-2018 年12 月期間在廣州市番禺區中醫院住院診治的病例,其中男30例,女26例,年齡21~67歲,平均41.24±10.4歲;病程0.3~30 年,平均14.27±7.72 年。采用隨機數字表法將56 例AS 患者分為依那西普組和柳氮磺吡啶(sulfasalazine,SASP) 組,各28 例,2 組患者在年齡、病程等方面差異均無明顯區別,具有可比性。
納入標準:①強直性脊柱炎評估組織(Assessment of in Ankylosing Spondylitis,ASAS)發布的中軸型脊柱關節炎(axial spondyloarthritis,SpA) 分類標準[8];②入組前接受化學藥物或生物藥物治療。排除標準:①妊娠、哺乳期和近期計劃受孕患者;②嚴重關節畸形疾病;③有嚴重肝腎功能障礙者。所有研究對象簽署知情同意書并經醫院倫理委員會批準后執行。
1.2 主要試劑及儀器
酶聯免疫吸附(ELISA)試劑盒、總RNA提取試劑(Invitrogen 公司);蛋白提取試劑盒、BCA 蛋白定量試劑盒、兔抗鼠酶標二抗(碧云天生物);鼠抗人單克隆抗體Wnt、β-catenin、RANKL、RANK、OPG(CST 公司);lipofectamine 2000試劑盒(Invitrogen 公司);反轉錄試劑盒和TaqMan@MicroRNA Assays Realtime PCR 試劑盒(大連寶生物公司);miR-146a、U6 引物(上海生工生物)。Applied Biosystems 7500儀器、Bio-Rad凝膠成像分析儀(美國伯樂);全自動血液分析儀(邁瑞醫療)。
1.3 研究方法
1.3.1 對患者的治療方法以及相關檢測
治療方法:依那西普組給予依那西普(輝瑞制藥有限公司,批號:506005,規格:25 mg)皮下注射,25 mg/次,每周2 次,治療3 月;SASP 組服用SASP(上海三維制藥有限公司,國藥準字H31020450,批號:20140420,規格:0.25 g/片),4片/次,2次/d,治療3月。
RT-qPCR 檢測:Trizol 法提取血清RNA。用Taq-Man@MicroRNA Reverse Transcription kit 進行反轉錄,反應總體系為10 μL。用TaqMan@MicroRNA Assays Realtime PCR 試劑盒檢測miR-146a 表達,以U6作為內標,miR-146a 上游引物5′-CAGCTGCATTGGATTTACAA-3′;下游引物5′-GCCTGAGACTCTGCCTTCTG -3′;U6 上游引物:5′-CTCGCTTCGGCAGCACA-3′,70bp;下游引物5′-AACGCTTCACGAATTTGCGT-3′,94bp。SYBR Premix Ex TaqTMⅡ試劑盒檢測FOXO1 mRNA 表達,每組設3 個重復,根據△△CT 法對結果進行相對定量分析,根據各樣本的平均CT 值,以2-ΔΔCt 表示mRNA 相對表達水平,所有反應均在ABI7500實時定量PCR儀完成。
1.3.2 動物造模、處理及分組
45 只4~5 周的雄性健康BALB/c 小鼠,適應性喂養1周后,進行造模(蛋白聚糖+弗氏佐劑造模),造模成功表現為四肢足趾部紅腫[9]。將造模后的小鼠分為5組:①模型對照組;②依那西普組,劑量0.5 mg/kg[10],每天1 次;③miR-146a 抑制劑組,劑量80 mg/kg,每天1次(參考瑞博動物實驗用量說明);④依那西普+miR-146a 抑制劑組,同時給予依那西普0.5 mg/kg,miR-146a 抑制劑80 mg/kg,每天1 次;⑤Negtive Con組(miR-146a 抑制劑陰性對照組),給予無序miRNA80 mg/kg,每天1 次。每組9只,均為尾靜脈注射。治療4周后處死,獲得血液和脊柱組織。
1.3.3 對小鼠相關指標的檢測
檢測指標:全自動血液分析儀檢測小鼠CRP,雙抗體夾心酶聯免疫吸附(ABC-ELISA)法檢測TNFα、IL-6、PTH、OPG、BALP、OC。
Western blot:參照王簕等[11]對骨組織總蛋白的提取方法,將小鼠脊柱剪碎后,用錘擊加研磨法處理脊柱組織后,根據蛋白提取試劑盒說明提取小鼠脊柱組織總蛋白。BCA 試劑盒說明檢測總蛋白量。根據目的蛋白分子量用合適濃度的SDS-PAGE 凝膠電泳分離,繼而轉膜和封閉,孵育一抗和二抗后,化學發光后進行采集圖像。
1.3.4 統計分析
2 結果
2.1 兩組患者miR-146a表達水平
通過熒光定量PCR 檢測2 組患者血清miR-146a表達水平,結果顯示,依那西普與SASP 治療后2組患者血清miR-146a 表達水平明顯下調,但依那西普治療后更明顯,差異具有顯著性意義(P<0.05),見圖1。
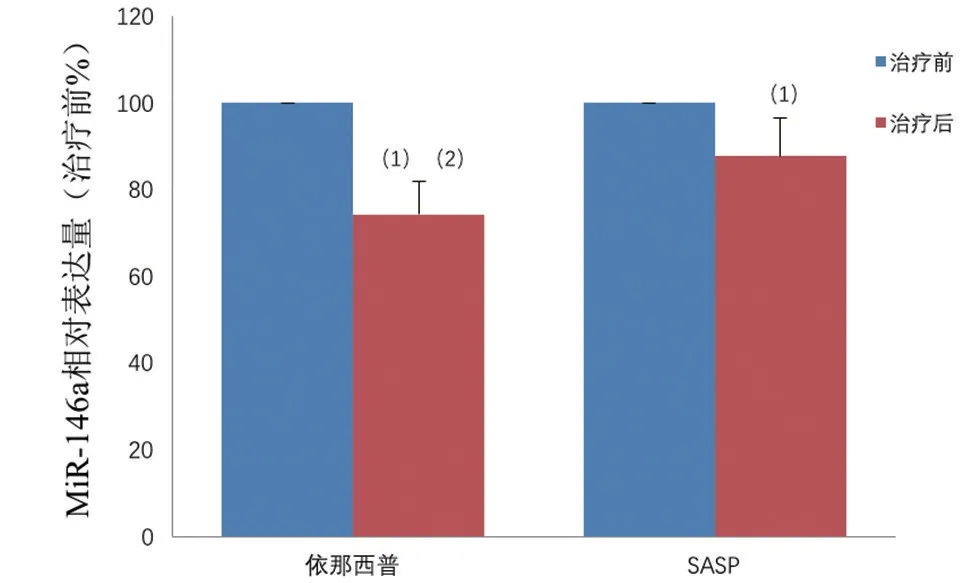
圖1 依那西普與SASP治療后對患者血清miR-146a表達水平的影響
2.2 miR-146a 轉染對模型炎癥因子及骨代謝生化指標影響
將miR-146a抑制劑注射至小鼠模型。觀察炎癥因子和骨代謝生化指標變化,結果顯示,與模型對照組及Negative Con 組相比,依那西普、miR-146a 抑制劑顯著降低炎癥因子TNF-α,IL-6,CRP 和骨代謝指標BALP 血清水平,提高骨代謝生化指標OPG、OC、PTH 血清水平,且miR-146a 抑制劑+依那西普改善更為顯著,與miR-146a 抑制劑組、依那西普組存在統計學差異(P<0.05),見表1。
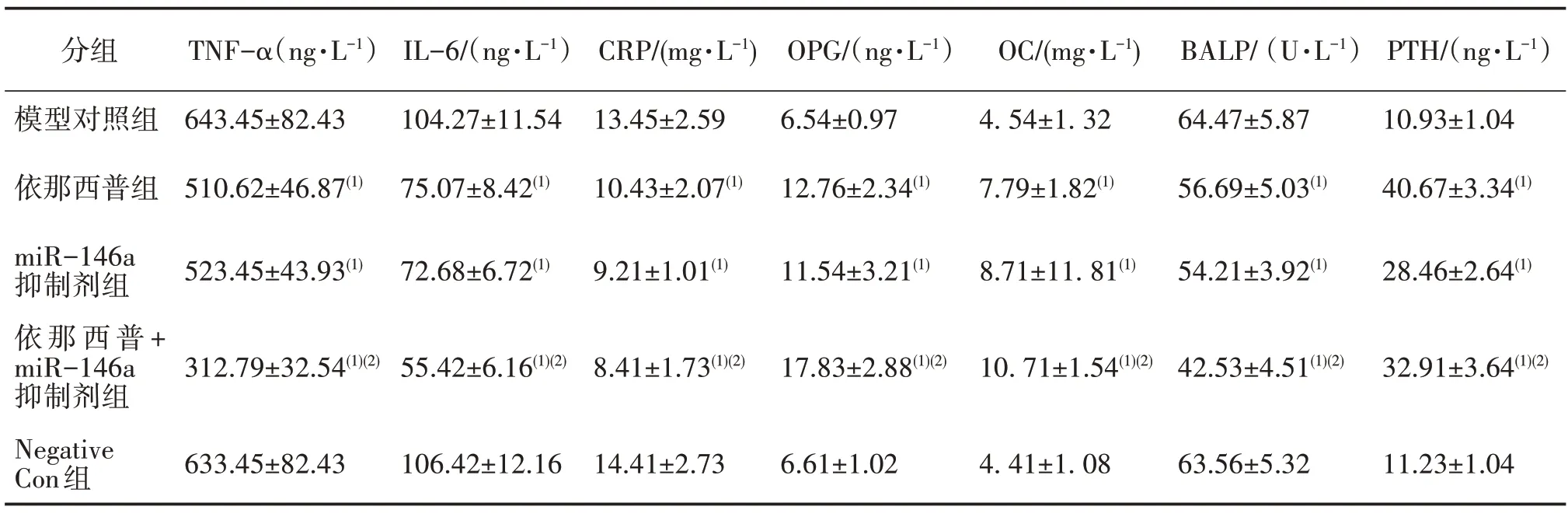
表1 炎癥因子和骨代謝生化指標
2.3 miR-146a轉染對成骨通路和破骨通路蛋白影響
與Negative Con 組比,依那西普、miR-146a 抑制劑以及miR-146a 抑制劑+依那西普組均顯著下調RANKL、RANK 蛋白表達,上調OPG、Wnt、β-catenin蛋白表達。見圖2。
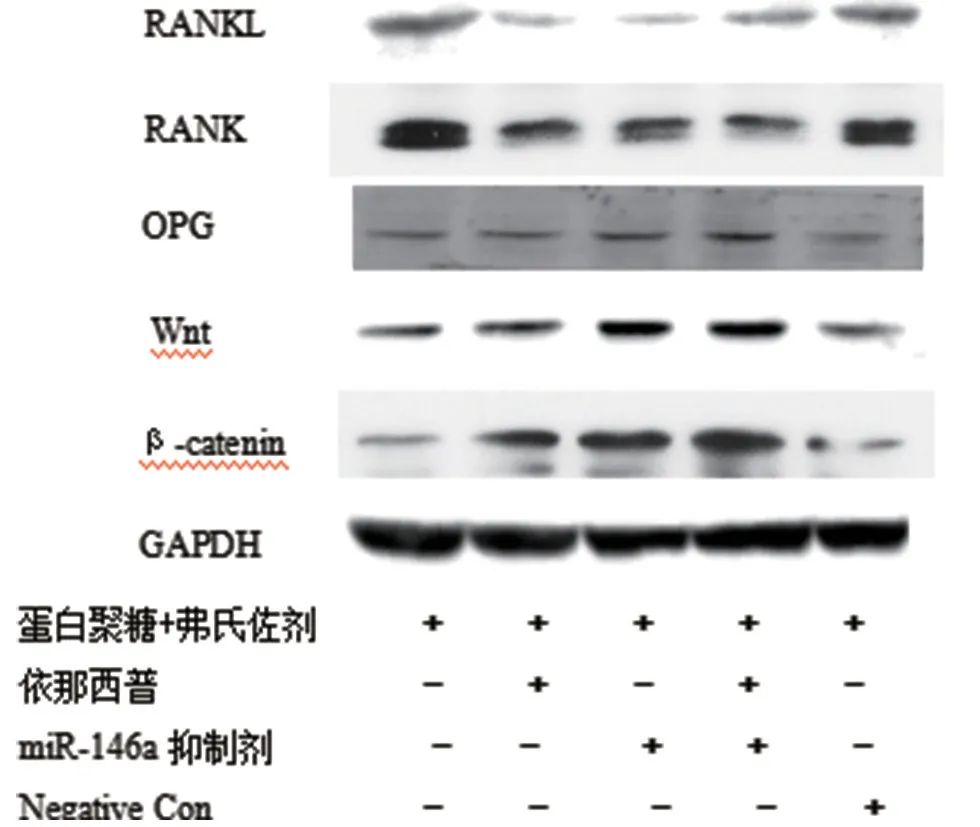
圖2 蛋白表達變化
3 討論
SA、SP 是治療AS 的傳統藥物,通過其代謝產物水楊酸起到抗炎作用。近年來,依那西普廣泛用于強直性脊柱炎治療,因其能抑制炎癥進程,緩解局部疼痛癥狀從而改善患者生活質量。在強直性脊柱炎患者中多種miRNA 分子異常表達,其機制之一是參與成骨、破骨及炎癥過程[12]。
本研究首先發現依那西普組治療后能顯著降低miR-146a 表達水平,與對照組在明顯差異(P<0.05)。進一步研究發現依那西普和miR-146a抑制劑可以顯著降低小鼠血清炎癥因子TNF-α,IL-6,CRP 和骨代謝指標BALP 血清水平,提高骨代謝生化指標OPG、OC、PTH 血清水平,兩者聯合效果更為顯著,推測依那西普可能是通過抑制miR-146a 表達,使得治療效果疊加從而改善小鼠病情。后續的研究證明依那西普和miR-146a 抑制劑治療后可促進成骨生成的Wnt、β-catenin 蛋白表達上調、抑制破骨細胞生成的OPG 蛋白上調,而促進破骨細胞生成的RANKL、RANK 破骨通路下調,差異具有顯著性意義。上述結果表明伊那西普改善活動期AS患者的炎癥反應和骨代謝的機制是通過miR-146a介導。依那西普可下調miR-146a 表達,這種調節作用可能通過促進成骨和抑制破骨,從而改善患者炎癥因子和骨代謝。本研究為全面了解依那西普的治療作用以及針對miR 分子開發潛在治療手段提供支持。
綜上所述,依那西普通過抑制強直性脊柱炎患者miR-146a 表達,進而通過促進調節成骨作用并抑制破骨等過程,從而改善患者炎癥因子及骨代謝。在AS患者中有諸多miRNA 分子異常表達,本研究只研究了一種,不清楚依那西普對其它miRNA 的調節作用,在后續的研究中需要深入了解依那西普對其它miRNA的表達調控。

