ECMO治療重癥急性呼吸衰竭患者預后影響因素及OCT10、OCI、APACHEⅣ評分對其預測價值
李建成 王東 羅凇元 夏瑞 王喜梅 李小霞 單艷華 王存真
體外膜氧合(extraeorporeal membrane oxygenation,ECMO)是臨床維持重癥急性呼吸衰竭(acute respiratory failure,ARF)的通氣,改善預后的常用方法,但重癥ARF患者死亡率仍居高不小[1]。探索重癥ARF預后影響因素,并予以針對性預防,有利于改善進行ECMO治療患者的預后。急性生理和慢性健康狀況(APACHEⅣ)評分量表,是國際上用來評估重癥患者病情程度的常用評分系統,具有預測效果較好[2]。既往報道顯示OCT10、OCI在評估重癥患者的預后方面有較高價值[3],且操作簡單、快速。基于此,筆者對重癥ARF患者的預后影響因素進行分析,并采用受試者工作特征(receiver operating characteristic,ROC)曲線分析OCT10、OCI及APACHEⅣ評分對重癥ARF患者預后的預測價值,旨在為減少ARF死亡率提供參考,研究結果如下。
資料與方法
一、一般資料
前瞻性選取2018年1月至2019年12月在駐馬店市中心醫院和河南省人民醫院重癥科進行治療的重癥ARF患者126例作為研究對象,并根據其30d預后情況分為生存組(68例)和死亡組(58例)。納入標準:(1)符合《呼吸急危重癥診療概要》[4]中重癥ARF診斷標準;(2)均接受ECMO治療;(3)重度ARDS急救措施及其他挽救性治療措施失敗;(4)其他病因導致急性重度低氧癥;(5)嚴重肺栓塞伴血流動力學障礙,但不適用溶栓等手術治療者;(6)治療后平臺壓超過35cmH2O,并伴有嚴重呼吸酸中毒的重癥哮喘者。排除標準:(1)已行ECMO治療者;(2)循環衰竭者者;(3)肺癌等其他肺部疾病者;(4)治療依從性低者;(5)前胸皮膚損傷致無法行經皮氧分壓監測者者。
二、方法
1 ECMO治療
采用Medtronic公司(美國) ECMO系統及套包進行ECMO治療。經皮穿刺建立血管通道,頸內靜脈為動脈端,動脈導管為15~17 F,股靜脈為靜脈端,靜脈倒換為19~23 F。其次進行ECMO參數設定,初始血流量為2~4 L/min,調節血、氧參數脈搏血氧飽和度≥92%。采用肝素抗凝,維持活化凝血時間在160~200 s范圍內。機械通氣參數維持FiO2不足50%,潮氣量為 4~6 mL/kg,呼吸頻率為7~12次/min,呼氣末正壓為8~10 cmH2O,平臺壓低于30 cmH2O。ECMO撤除要求為疾病控制顯著,血流量減到1.5~2 L/min,自主呼吸功能逐漸恢復。撤除ECMO,暫停氣流量供應,FiO2≤60%,觀察患者生命體征及血氣分析6小時,波動不明顯,考慮撤機。
采用PeriFlux 6000(PERIMED)經皮檢測儀,記錄氧分壓穩定時PtO2和動脈氧分壓(PaO2),及吸入純氧10 min后PtO2和PaO2值。計算OCT 10、OCI水平,OCT10=吸入純氧10 min后PtO2與基礎PtO2的差值,OCI=OCT 10/(吸入純氧10 min后PaO2與基礎PaO2的差值)。
三、觀察指標
(1)收集患者性別、年齡、體質量指數(BMI)、ARF病因、免疫抑制、心率、平均動脈壓、白細胞、血紅蛋白、白蛋白、肌酐、ECMO治療時間、Murray肺損傷評分、序貫器官功能衰竭(SOFA)評分、機械通氣時間等資料,以及呼吸機參數(機械通氣時間、潮氣量、呼氣末正壓、平臺壓)和6 h血氣分析參數(pH值、氧合指數、碳酸氫根、血乳酸)。(2)記錄6 h OCT 10、6 h OTI及經ECMO治療患者急性生理和慢性健康狀況(APACHEⅣ)評分。
四、統計學處理
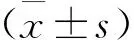
結 果
一、重癥ARF患者的基本資料及影響因素分析
兩組患者性別、年齡、BMI、ARF病因、免疫抑制、心率、平均動脈壓、白細胞、血紅蛋白、白蛋白、肌酐、ECMO治療時間、潮氣量、呼氣末正壓、平臺壓、pH值、氧合指數、碳酸氫根、血乳酸比較,差異無統計學意義(P>0.05);而死亡組Murray肺損傷評分、SOFA評分、機械通氣時間、APACHEⅣ評分高于生存組,OCT10、OCI水平低于生存組,差異有統計學意義(P<0.05)(見表1)。

表1 重癥ARF患者的基本資料及影響因素分析
二、影響ARF患者預后的多因素分析
以ECMO治療ARF患者預后為因變量(預后死亡賦值“1”,預后死亡賦值“0”),以單因素分析有統計學差異的因素作為自變量;多因素Logistic 回歸顯示,OCT 10、OCI是ARF患者預后死亡的保護因素(OR<1,P<0.05),APACHEⅣ評分是ARF患者預后死亡的獨立危險因素(OR>1,P<0.05)(見表2)。

表2 影響ARF患者預后的多因素分析
三、OCT10、OCI及APACHEⅣ評分對ARF患者預后死亡的預測價值分析
ROC曲線分析顯示,OCT10、OCI、APACHEⅣ評分預測ARF患者預后死亡的AUC分別為0.880、0.879、0.765,當OCT10低于68.12 mmHg時,其敏感度為80.9%,特異度為88.2%;當OCI低于0.71 時,其敏感度為75.0%,特異度為88.2%;當APACHEⅣ評分高于38分時,其敏感度為98.5%,特異度為50.0%(見圖1,表3)。

圖1 OCT10、OCI及APACHEⅣ評分對ARF患者預后死亡預測價值的ROC曲線分析

表3 OCT10、OCI及APACHEⅣ評分對ARF患者預后死亡的預測價值分析
討 論
ARF是由各種原因引起的換氣功能障礙,可造成機體氧氣供需失衡,損害機體,多種器官損傷,嚴重危害患者生命[5]。ECMO是治療重癥ARF的常用手段,可較好維持患者生命,然而臨床死亡率仍然較高[6]。明確導致重癥ARF死亡的危險因素,對患者預后進行有效評估,于重癥ARF的治療而言有重要意義。本研究中兩組患者的呼吸機參數和血氣分析指標比較差異無統計學意義。分析可能為呼吸衰竭早期,器官仍存在一定代償性,加上統一的ECMO和呼吸機治療可能會對指標造成一定影響,導致差異不顯著[7]。
本研究多因素回歸分析顯示,Murray肺損傷評分、SOFA評分、機械通氣時間,不是導致ARF患者預后死亡的獨立危險因素,但OCT10、OCI是ARF患者預后死亡的保護因素,APACHEⅣ評分是ARF患者預后死亡的獨立危險因素。Murray肺損傷評分是臨床用于評估肺部損傷程度的常用量表[8],其不是影響預后的獨立危險因素可能是重癥ARF的肺部損傷都較為嚴重,治療時患者的呼吸功能主要靠ECMO和呼吸機支持。機械通氣時間為患者采用呼吸機進行呼吸治療的時間,以往呼吸支持是治療ARF的主要方法,但近年來研究顯示一半以上的并不需要呼吸支持[9],因此本研究中死亡組患者機械通氣時間雖然較高,但卻不是ARF患者預后死亡的獨立危險因素。目前,臨床用來評估重癥患者預后的評分系統較多,各有側重點和優缺點,其中 SOFA評分和APACHE評分是較為常用的評分系統[10-11]。但由于本研究中患者均為重癥ARF患者,此時只有個別患者存在循環和腎臟功能異常,而其他多數臟器功能仍表現正常或在代償期內,故死亡組患者SOFA評分高于生存組,但卻不是ARF患者預后死亡的獨立危險因素。APACHⅣ為相對而言應用于預后評估準確度最高的一種評分系統[2]。重癥ARF治療的本質是改善機體組織的缺氧狀態,因此表明組織氧代謝的治療可作為影響和評估預后的關鍵因素[12]。OCT10、OCI是由經皮氧分壓的氧負荷試驗檢測出的指標,能夠對肺和組織缺氧狀態進行評估[13]。正常情況下,吸入純氧10 min后,PtO2、PaO2均隨之上升,但組織缺氧時,缺氧組織會掠取部分負氧離子,導致PtO2增幅降低,從而導致OCT10、OCI降低,因此本研究中顯示OCT10、OCI是ARF患者預后死亡的保護因素,與文獻報道結果一致[14]。此外筆者采用ROC曲線分,對OCT10、OCI及APACHEⅣ評分進行預測價值分析,結果顯示OCT10、OCI、APACHEⅣ評分預測ARF患者預后死亡的AUC分別為0.880、0.879、0.765,說明三者預測價值均較高,且OCT10、OCI對ARF預后的預測價值高于APACHEⅣ評分。
綜上所述,OCT10、OCI是ARF患者預后死亡的保護因素,APACHEⅣ評分是ARF患者預后死亡的獨立危險因素;OCT10、OCI及APACHEⅣ評分,均對ARF預后死亡有預測價值,且OCT10、OCI的預測價值高于APACHEⅣ評分。

