甲狀旁腺切除術對尿毒癥透析繼發甲狀旁腺功能亢進癥患者肌肉功能的影響
羅華榮徐艷松趙杰劉永謝磊王建國趙帥
中國貴航集團三○二醫院腎內科,貴州 安順 561000
肌少癥(sarcopenia)亦稱骨骼肌減少癥或增齡性骨骼肌減少癥,是以骨骼肌質量、力量及功能降低為主要臨床特征的退行性綜合征[1-2]。與普通人群相比,肌少癥在尿毒癥患者中的發生率明顯升高[3],尤其是尿毒癥患者合并繼發性甲狀旁腺功能亢進癥(secondary hyperthyroidism,SHPT)后,很多患者會出現腰部肌肉力量明顯下降,嚴重者坐位站起困難或不能站起,部分患者走路呈現蹣跚步態,增加了骨折發生的風險,甚至完全不能行走,嚴重影響患者的生活質量,極大增加了患者死亡率[4]。有研究[5]顯示成功實施甲狀旁腺切除術(parathyroidectomy,PTX)的尿毒癥患者生活質量會明顯改善。但這些患者生活質量的改善是否與肌肉質量及功能改善有關,國內外尚缺乏相關的具體研究。因此,本研究擬選擇尿毒癥合并嚴重SHPT患者作為研究對象,觀察甲狀旁腺切除術對SHPT患者肌肉功能的影響。
1 材料和方法
1.1 研究對象
所有患者均來自中國貴航集團三○二醫院腎內科行PTX手術的規律血液透析患者,診斷為SHPT,且符合《中國慢性腎臟病礦物質和骨異常診治指南》對PTX的手術標準[6]。納入標準:①患有嚴重的SHPT (iPTH > 800 pg/mL),伴有高磷血癥或高鈣血癥;②用活性維生素D (4~6 μg /周)沖擊治療3個月以上無效者;或者沖擊治療過程中因嚴重的高鈣或高磷血癥而無法使用活性維生素D者;③超聲檢查證實有一個以上的甲狀旁腺增大,其中至少一個直徑大于l cm 或體積大于0.5 cm3;④年齡18~70歲。排除標準:患有惡性腫瘤、原發性甲狀旁腺疾病、精神方面疾病等以及存在肢體殘缺等。所有入選受試者均簽署知情同意書。
1.2 方法
1.2.1一般資料:收集受試者的一般臨床資料,包括性別、年齡、身高、體重、透析齡等一般人口學資料。所有受試者均于手術前、術后1周進行血清鈣、磷、全段甲狀旁腺素(iPTH)、堿性磷酸酶(ALP)的檢測。
1.2.2上臂圍、皮褶厚度及上臂肌圍測量和計算:采用軟尺分別測量受試者術前、術后6個月、12個月的上臂圍(MAC),通過皮質厚度計(精凱達JK6113皮脂厚度計)測量術前、術后6個月、12個月的肱三頭肌部皮褶厚度(TSF),并計算上臂肌圍水平(AMC),公式:AMC(mm)=MAC(mm) - 3.14 × TSF(mm)[7]。
1.2.3骨骼肌力量測量:采用香山EH101電子握力計,對研究對象進行術前、術后第6個月及術后第12個月的握力測試。測量方法:受試者站立位,雙臂自然下垂,掌心向內,單手持握力計,顯示屏向外,勿與身體和衣物接觸。一次性用力握緊握力計,讀數并記錄,休息后重復測量,左、右手分別測3次,取均值并記錄優勢手握力。
1.2.4骨骼肌功能測量:在術前、術后第6個月、術后第12個月,通過日常步速法對受試者進行評估,評價其骨骼肌功能狀況。參照亞洲肌少癥工作組(AWGS)發布的《2019肌少癥診斷及治療專家共識》中對骨骼肌功能測定的方法[8],本研究中采用6 m步行速度,即從移動開始以正常步速行走6 m所需的時間,中途不加速不減速,并至少測量兩次,記錄平均速度。
1.3 統計學方法

2 結果
行甲狀旁腺切除術的患者共35例,研究期間1例患者行腎移植術脫離透析,1例患者腦出血死亡,4例患者轉至其他醫院血透室未完成觀察,最終有29例患者完成了研究。其中男性患者19例,平均年齡為(39.63±10.82)歲,女性患者10例,平均年齡為(48.10±9.77)歲,所有患者平均血液透析齡為(7.64±3.40)年。29例患者中有24例原發病為慢性腎小球腎炎,另外多囊腎、痛風性腎病各1例,還有3例原發病不詳。
2.1 治療前后受試者iPTH、ALP、Ca、P比較
術后一周患者iPTH水平明顯降低,其中27例患者iPTH水平<120 pg/mL,達到了手術成功的標準;2例患者術后iPTH水平仍>120 pg/mL,并且在以后的檢測中iPTH水平持續>120 pg/mL,為術后持續性甲狀旁腺功能亢進;術后患者血磷下降明顯(P<0.000);所有患者均口服或靜脈補鈣,術后血清Ca下降不明顯(P=0.528);術后一周堿性磷酸酶無明顯變化(P=0.437)。見表1。

表1 手術治療前后受試者iPTH、ALP、Ca、P變化情況比較
2.2 治療前后受試者上臂圍、肱三頭肌皮褶厚度變化比較
術后6個月受試者上臂圍及肱三頭肌部皮褶厚度較術前有改善趨勢,然而,男女患者與術前比較均無明顯差異(P>0.05);而術后1年受試者的上臂圍男性、女性均有增加趨勢,而統計學顯示無明顯差異(P>0.05);術后1年受試者的肱三頭肌部皮褶厚度有增加趨勢,但比較差異無統計學意義(P>0.05)。見表2。
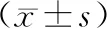
表2 手術治療前后受試者上臂圍、肱三頭肌皮褶厚度變化情況比較
2.3 治療前后受試者上臂肌圍變化比較
術后6個月、12個月受試者上臂肌圍較術前有改善趨勢,然而,無論男性還是女性與術前比較均無明顯差異(P>0.05);而術后6個月男性、女性受試者的上臂肌圍都有明顯增加(P<0.05)。術后1年女性受試者的上臂肌圍增加明顯(P<0.05),而男性增加更加明顯,與術前比較差異更加顯著(P<0.01)。見表3。

表3 手術治療前后患者上臂肌圍、體質指數調整的上臂肌圍變化情況比較
2.4 治療前后受試者握力、步速變化情況比較
術后6個月受試者握力較術前比較均有明顯提高,但統計學方面無明顯差異(P>0.05);術后12個月受試者的握力提高更明顯,在統計學方面差異顯著(P<0.05)。術后6個月、12月受試者的步速較術前均有明顯改善(P<0.05)。見表4。
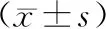
表4 手術治療前后受試者握力、步速變化情況比較
3 討 論
慢性腎臟病(chronic kidney disease,CKD)患者往往由于食欲減退、蛋白攝入減少、慢性炎癥、尿毒素蓄積、蛋白質-能量消耗以及運動減少等原因,蛋白質穩態處于負平衡狀態,即蛋白質的分解代謝增加而合成減少,進而出現肌肉力量降低、結構改變及肌肉萎縮,出現肌肉減少癥。當存在繼發性甲狀旁腺功能亢進癥時,PTH水平會顯著升高,患者會有皮膚瘙癢、骨痛、乏力,甚至喪失活動能力,增加患者的死亡風險。研究[9-10]顯示,慢性腎臟疾病患者肌少癥的發生率高達30 %~67 %,肌少癥會導致透析患者死亡率增加2倍,因此尿毒癥引起的肌肉減少癥越來越引起學者們的關注。
本研究結果表明,PTX術后受試者肌肉功能得到明顯改善,握力和步速明顯提高,可能是SHPT患者行PTX術后生活質量改善的重要原因之一。目前,關于甲狀旁腺切除術對SHPT患者肌肉功能影響的研究較少,PTX手術通過何種途徑改善了肌肉功能并不明確。筆者分析,首先,PTX手術改善患者肌肉功能可能與iPTH水平降低有關,來自美國的研究[11]顯示,原發性甲狀旁腺功能亢進癥患者肌少癥發生率明顯增高,并且在“無癥狀”的原發性甲狀旁腺功能亢進癥患者中肌肉減少癥的發生率也顯著增加,說明肌肉減少癥的發生可能是PTH水平升高所導致的[12]。來自美國全國健康和營養調查數據庫(National Health and Nutrition Examination Surveys,NHANES)的資料分析研究[13]顯示,高iPTH水平是肌肉減少癥發生的重要原因, iPTH大于4.0 pmol/L組較iPTH小于3.0 pmol/L組的肌少癥發生率會增加1.35倍。也有小樣本的臨床研究[14]發現,成功的PTX手術可以改善輕中度原發性甲狀旁腺功能亢進女性患者的四肢肌肉力量。同理,SHPT患者成功的PTX手術可以使iPTH水平從高水平降至正常甚至低于正常值下限[15],iPTH水平的降低可能會對肌肉的合成和分解平衡有積極的影響,進而改善肌肉的質量和功能;其次,由于PTX術前SHPT患者往往都存在高磷血癥,患者需要嚴格控制含磷食物的攝入,會導致蛋白營養物質的攝入不足。同時患者口服西那卡塞、碳酸鑭等SHPT治療藥物,也會導致胃腸道的不適,影響患者的飲食,這些原因都可以引起肌肉合成與分解的平衡狀態打破,導致肌肉減少癥的發生。而成功行PTX術后,SHPT患者鈣磷水平會明顯降低,出現“骨饑餓”,此時患者需要放開飲食,大量補充含鈣、含磷高的食物,營養狀況會明顯改善,進而促進肌肉的合成,增加肌肉含量,改善肌肉功能;另外,SHPT患者往往合并骨痛,活動減少或受限也可以導致肌少癥的加重或發生。成功行PTX術后,患者骨痛會“神奇”的消失,破骨指標會顯著下降[16],患者運動功能會立刻改善,運動的增加可改善肌肉的質量和功能。
本研究結果也提示,PTX術后患者的上臂圍、肱三頭肌皮褶厚度有增加趨勢,然而并沒有統計學意義,這可能與本研究納入患者樣本量較小有關系,擴大樣本量或許會得出有意義的陽性結果,這也是本研究的局限之一。盡管本研究納入的樣本量較小,但握力及步速的改善明顯,研究結果也能夠反映PTX手術對患者肌肉功能的影響;另外,在其他一些指南中,把雙能X線檢測及生物阻抗法作為肌少癥診斷的金標準,然而本研究未進行雙能X線及生物阻抗的肌肉質量的測定,也是局限之一。在實際研究開始前,本研究組考慮采用生物阻抗的方法去評估肌肉質量,但是維持性血液透析患者由于無尿,透析間期體重增加各不相同,可能對結果判斷會有較大的影響,而且患者最好是透析間期來院測定,會給嚴重的繼發性甲旁亢患者帶來很大的困難,出于倫理考慮,沒有測定患者的肌肉質量指標,但上臂肌圍、肱三頭肌皮褶厚度的結果也間接反應了肌肉質量的改善。今后的研究應該增加樣本量,并探索生物阻抗法評估透析患者肌肉質量的方法,以提高臨床研究的質量;最后,本研究沒有設立對照組,主要是考慮到手術的選擇應該尊重患者的意愿,不能違背醫學倫理,單純為了研究而研究。
總之,本研究的結果提示,PTX術可以改善繼發性甲旁亢患者的肌肉功能,是維持性血液透析患者合并SHPT的理想選擇。今后的研究應該擴大樣本量或進行多中心研究,也應該開展肌肉質量相關的觀察研究,并展開深入的機制探討,為臨床決策提供更多的證據支持。

