慢性萎縮性胃炎中醫藥相關臨床試驗注冊現狀分析
獨思靜,國嵩,方霜霜,楊洋,魏瑋 中國中醫科學院望京醫院,北京 100102
慢性萎縮性胃炎(chronic atrophic gastritis,CAG)是以胃黏膜固有腺體萎縮、數目減少,或伴腸腺化生和假幽門腺化生,或有異型增生(或上皮內瘤變)為特征的慢性消化系統疾病,作為胃癌前病變,日益受到關注[1-2]。中醫藥對CAG病因病機和治療的認識較為成熟[3],并結合現代醫學知識及檢查手段,臨床療效較好。
目前,中醫藥治療CAG主要處于臨床觀察階段, 尚缺乏高質量循證醫學證據[2,4]。隨著循證醫學的發展,臨床試驗的規范注冊和研究逐漸受到重視,對提高臨床試驗質量具有重要意義。2006年5月,世界衛生組織(WHO)正式啟動國際臨床試驗注冊平臺(International Clinical Trials Registry Platform,ICTRP),中國臨床試驗注冊中心(Chinese Clinical Trial Registry,ChiCTR)于2007年成為ICTRP認證的一級注冊機構,接受中國及世界范圍內的臨床試驗注冊[5]。本文基于ChiCTR,對其登記的CAG中醫藥相關臨床試驗注冊情況進行總結與分析,探討如何更好地實現CAG中醫藥臨床試驗的規范化并提高相關循證醫學證據質量。
1 資料與方法
1.1 數據來源
登錄ChiCTR(http://www.chictr.org.cn),進入檢索入口,以“慢性萎縮性胃炎”“胃癌前病變”為關鍵詞,檢索ChiCTR建庫至2020年10月31日注冊的臨床試驗。
1.2 文獻篩選標準
納入標準:CAG中醫藥臨床試驗,無論采用何種試驗設計或是否已完成。
排除標準:注冊信息有誤、重復注冊或提示已經撤銷注冊的研究。
1.3 文獻篩選、資料提取與統計
由2名研究者獨立篩選文獻、提取資料并交叉核對。若遇分歧則通過討論或與第三方協商解決。文獻篩選時首先閱讀文題,排除明顯不相關文獻后,進一步查看內容以確定是否納入。納入文獻提取三方面內容。①注冊研究的基本信息:注冊號、研究題目、注冊時間;②研究的設計信息:研究設計類型、研究疾病、干預措施、樣本量、隨機方法、盲法實施、研究負責單位;③其他:注冊狀態、倫理審查等。采用Excel2016錄入數據,并進行整理統計。
2 結果
2.1 篩選流程及結果
初檢共獲得43項注冊研究,剔除重復試驗2項、非中醫藥研究9項、信息不全研究1項,最終納入CAG中醫藥相關臨床試驗31項。
2.2 注冊時間分布
自ChiCTR建庫,CAG中醫藥相關臨床試驗注冊數目整體偏少。2008年注冊首個相關試驗,2009、2010、2011、2014、2015年均無注冊項目,2016年起注冊情況較為穩定并逐步上升,至2019年注冊數量最多(11項),詳見圖1。注冊項目中補注冊7項、預注冊24項,完成研究7項(均為補注冊項目),正在進行或尚未開始24項,通過倫理委員會審查26項。
2.3 研究地區及機構分布
納入的31項臨床試驗覆蓋全國6個省、3個直轄市,其中上海市、北京市分布最多,共注冊16項,占注冊臨床試驗總數的51.61%,詳見表1。其中,注冊臨床試驗≥3項的4家機構分別為浙江大學醫學院附屬邵逸夫醫院、廣州中醫藥大學第一附屬醫院、上海市中醫醫院、上海中醫藥大學附屬岳陽中西醫結合醫院。
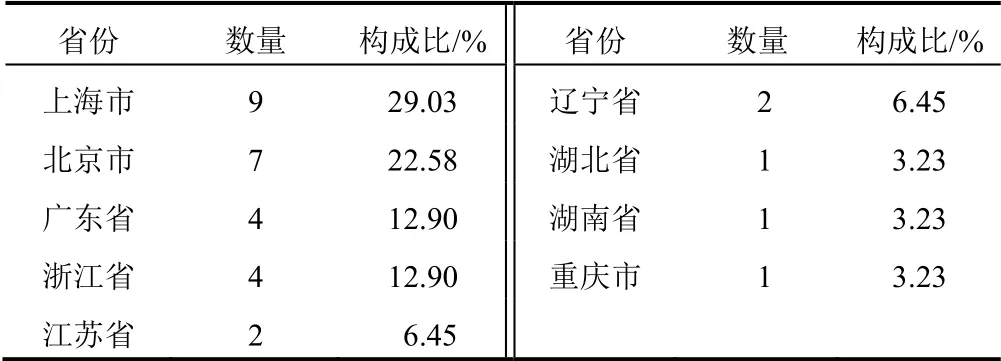
表1 31項ChiCTR注冊CAG中醫藥相關臨床試驗地區分布
2.4 研究設計類型
納入研究包括干預性研究25項(80.65%)、觀察性研究4項(12.90%)、病因學/相關因素研究2項(6.45%)。研究設計以隨機平行對照試驗最多,共25項(80.65%),均描述了隨機方法,僅5項注明盲法;另有非隨機平行對照試驗3項(9.68%),病例對照研究、連續病例、單臂研究各1項(3.23%)。
2.5 研究樣本量
納入研究預計招募樣本總量11 378例,例數≤100有8項,100<例數≤500有19項,500<例數≤1 000有3項,1 000<例數≤5 000有1項。其中,干預性研究樣本量最大,總樣本量為5 449例,樣本量區間為20~800例,各型研究具體樣本量及樣本量區間詳見表2。其中,廣州中醫藥大學第一附屬醫院開展的“基于真實世界的健脾清熱活血法治療慢性萎縮性胃炎的臨床觀察研究”樣本量達5 000例。
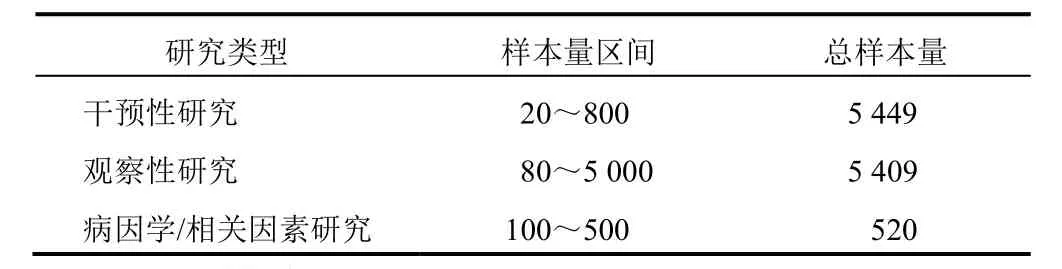
表2 31項ChiCTR注冊CAG中醫藥相關臨床試驗樣本量情況
2.6 干預措施
納入的25項干預性研究中干預措施分別為中藥制劑內服和針灸、穴位敷貼外治2種干預途徑。其中單純中藥制劑內服研究19項,主要包括經方和協定方的探索性研究/預實驗、中成藥臨床試驗和上市后藥物研究等;單純外治法研究3項,聯合中藥制劑內服和外治3項,主要為治療新技術臨床試驗。對照組使用最多的干預措施分別為葉酸、胃復春和安慰劑。
2.7 測量指標
納入研究的測量指標以療效指標為主,部分包括安全性指標。療效指標主要包括癥狀評分、中醫證候評分、胃鏡和病理及胃蛋白酶原、胃泌素等改善情況,其中僅1項研究涉及病理診斷質量控制,寫明“兩位病理醫師同時評估并形成一致診斷”;安全性指標主要包括血常規、尿常規、便常規、肝功能、腎功能及心電圖等。
3 討論
臨床試驗透明化包括臨床試驗注冊、清楚準確報告結果、共享臨床試驗結果及原始數據,是21世紀醫學研究領域最重要的革命性理念[6],具有倫理和科學的雙重意義。2004年9月,國際醫學雜志編輯委員會宣布,自2005年7月1日起,其成員雜志只發表經注冊的臨床試驗[7],這在臨床試驗研究領域具有里程碑意義。2018年,《中國腫瘤》也提出了“凡臨床試驗都應在中國臨床試驗注冊中心注冊”的聲明[8]。臨床試驗注冊是臨床試驗規范化建設關鍵環節。
3.1 時間與地域分布欠理想
2017年全球胃癌發病超過122萬,其中近一半發生在中國[9],我國胃癌的發生率和病死率在國內各類惡性腫瘤中位居前列[10]。因此,對胃癌前病變的有效干預是降低我國胃癌發生率和病死率的關鍵手段。回顧ChiCTR整體注冊量,已從最初的每年僅注冊數十項試驗發展到2019年的8 109項試驗。然而,本研究發現,CAG中醫藥相關臨床試驗數量整體偏少,且增長趨勢較緩。分析其原因,可能有以下兩方面[6]:①大部分研究者對臨床試驗注冊意識較弱,對已有注冊平臺了解較少;②即使對于臨床試驗注冊有所了解,也常存在誤解,如認為臨床試驗注冊僅為發表論文。因此,研究者應加強規范研究的觀念,認識到臨床試驗注冊是臨床試驗透明化的重要環節,通過注冊可提升臨床試驗規范性,還可通過后續數據共享減少不必要的重復試驗。同時,ChiCTR于2007年成為WHO ICTRP認證的一級注冊機構,被國際醫學期刊編輯委員會承認,相關文章可在國際醫學期刊發表。
胃癌在我國地區分布廣泛,以西北地區和東南沿海較為集中[11]。本研究顯示,CAG中醫藥研究以經濟發達地區最多,如上海市、北京市和廣東省等。建議政府向胃癌高發地區的胃癌前病變研究做適度政策導向和經費支持,相關地區科研水平參差不齊,應鼓勵單位間聯合研究,以提高胃癌高發地區科研水平,有效探索并實現降低胃癌發病率的有效途徑。
3.2 研究設計欠規范
隨機對照試驗(RCT)是檢驗臨床干預措施安全性和有效性的理想方法,其結論對指導臨床實踐和制定藥物政策有重要意義。本研究發現,RCT占總注冊量的80.65%,且均描述了隨機方法,但僅5項寫明盲法。可見,研究者隨機設計意識較強而對盲法未予充分重視,但也可能與注冊時具體設計未完善有關。
樣本量對臨床試驗結果的可靠性有重要意義,需考慮檢驗效力、差異顯著水平、效應量等綜合因素[12]。本研究發現,多數注冊研究的樣本量設計較為合理,尤其在基于真實世界的觀察性研究中樣本量充足。在此基礎上,若研究者可嚴格按照納排標準選擇病例,并在實際研究中密切跟進以提高依從性,則可在較大程度上保證結果的可靠性。
關于干預措施,試驗組采用中藥制劑內服和針灸、穴位敷貼等均可發揮中醫特色。對照組除使用安慰劑外最常用葉酸和胃復春口服,然而兩者是否可作為陽性藥物暫缺乏充分依據。動物研究表明,葉酸可通過防止DNA甲基化和抑制炎癥降低胃癌發生[13-14];然而一項納入了16個葉酸和胃癌風險研究的Meta分析顯示,葉酸攝入與胃癌風險無顯著關聯[15];《中國慢性胃炎共識意見(2017年,上海)》指出,對于部分體內低葉酸水平者,適量補充葉酸可改善CAG組織學改變[16]。因此,暫無充分證據支持葉酸在CAG患者中的普遍療效。胃復春由紅參、香茶菜、麩炒枳殼組成,具有健脾益氣、活血解毒之功。研究表明,胃復春可較好地改善CAG患者中醫癥狀和病理表現等[17-20]。然而相關研究多為與西藥聯用,且樣本量少,臨床設計欠嚴謹,其治療CAG的有效性暫缺乏充分依據。因此,在滿足倫理審查要求的前提下,CAG臨床試驗中使用安慰劑對照更為嚴謹,陽性藥物對照仍需臨床大樣本進一步證實。
本研究中多數試驗將胃鏡和病理改善情況作為主要療效指標,可較大程度保證研究質量,顯著提高證據級別[21]。因活檢組織病理學是診斷CAG的金標準,是公認的療效評定標準。然而我國各地區CAG胃鏡與病理診斷一致性并不理想,符合率僅60%~80%[22-26],故臨床試驗中需多位病理醫師參與并形成一致診斷。因此,我們推薦至少2名病理醫師進行盲法診斷以提高CAG臨床試驗的病理質控水平。
4 結語
綜上所述,提高中醫藥干預CAG的循證醫學證據質量是推廣臨床應用、制定行業標準、促進成果轉化及獲得國際認可的關鍵環節。臨床試驗注冊作為規范研究的初始環節,對于提高臨床試驗質量具有重要意義。然而,目前CAG中醫藥相關臨床試驗注冊存在時間與地域分布欠理想和研究設計欠規范的問題,研究者應針對其中薄弱環節,規范臨床試驗設計,加強臨床試驗注冊理念,有效提升臨床研究質量。

