關(guān)節(jié)止痛膏控制菌微生物限度檢查方法的建立
李亞東,張紅霞
1.聯(lián)勤保障部隊第九四〇醫(yī)院臨夏診療區(qū),甘肅 臨夏 731100;2.解放軍西寧聯(lián)勤保障中心藥品儀器監(jiān)督檢驗站,甘肅 蘭州 730050
關(guān)節(jié)止痛膏處方來源于1991 年《中藥成方制劑標(biāo)準(zhǔn)》,作為一種局部外用橡膠膏,是目前治療相關(guān)病癥的常用藥物[1-7]。其主要成分包括辣椒流浸膏、顛煎流浸膏、薄荷素油、水楊酸甲酯、樟腦以及鹽酸苯海拉明[8],所用基質(zhì)包括橡膠、氧化鋅、松香、凡士林、羊毛脂等[9-10]。關(guān)節(jié)止痛膏具有活血散瘀,溫經(jīng)鎮(zhèn)痛的功效,在臨床上主要用于寒濕瘀阻經(jīng)絡(luò)所致的風(fēng)濕關(guān)節(jié)痛及關(guān)節(jié)扭傷[11-12]。
《中國藥典》2015 年版四部非無菌產(chǎn)品微生物限度檢查法[13],對計數(shù)培養(yǎng)基、微生物限度用培養(yǎng)基、培養(yǎng)溫度、培養(yǎng)時間、方法適用性檢查等各方面都進行了調(diào)整,《中國藥典》2010 年版控制菌檢查中使用的增菌培養(yǎng)基營養(yǎng)肉湯、膽鹽乳糖培養(yǎng)基均被胰酪大豆胨瓊脂培養(yǎng)基替代,為了確認(rèn)所采用的新培養(yǎng)基適合于關(guān)節(jié)止痛膏的控制菌的檢查,本研究對其檢查方法進行了方法適用性試驗[14]。作為傳統(tǒng)中藥制劑,關(guān)節(jié)止痛膏目前在國內(nèi)共有48個批準(zhǔn)文號[15],涉及的生產(chǎn)企業(yè)多達(dá)30 多家,本研究收集了6 家生產(chǎn)企業(yè)共17 個批號的樣品進行試驗,以期對其控制菌的檢查方法進行統(tǒng)一,確認(rèn)此方法適合關(guān)節(jié)止痛膏中控制菌的測定,并確保該方法的有效性和試驗結(jié)果的科學(xué)性[16]。
按照《中國藥典》2015 年版四部通則1106 的規(guī)定,關(guān)節(jié)止痛膏每10 cm2不得檢出金黃色葡萄球菌和銅綠假單胞菌。
1 儀器與材料
1.1 儀器
ME4002E/02 電子分析天平[梅特勒-托利多(上海)有限公司];LDZX-60KBS 立式壓力蒸汽滅菌器(上海申安醫(yī)療器械廠);UPS 醫(yī)療純水機(成都優(yōu)普凈化科技有限公司);JJNYI 霉菌培養(yǎng)箱(上海虹浦儀器廠);HW-B-2 培養(yǎng)干燥箱(廈門醫(yī)療儀器廠);PYX-DH 電熱恒溫培養(yǎng)箱(國光醫(yī)療器械廠);H.H.S 電熱恒溫水浴鍋(江蘇醫(yī)療器械廠)。
1.2 培養(yǎng)基和稀釋劑
pH 7.0 無菌氯化鈉-蛋白胨緩沖液(批號:20160426)、甘露醇氯化鈉瓊脂培養(yǎng)基(批號:20160113)、溴化十六烷基三甲銨瓊脂培養(yǎng)基(批號:20170619)、沙氏葡萄糖瓊脂培養(yǎng)基(批號:20160328)、沙氏葡萄糖液體培養(yǎng)基(批號:20160204)、胰酪大豆胨瓊脂培養(yǎng)基(批號:20160505)、胰酪大豆胨液體培養(yǎng)基(批號:20160407)均購自青島高科園海博生物技術(shù)有限公司。
1.3 菌種
試驗菌種包括金黃色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]、銅綠假單胞菌(Pseudomonas aeruginosa)[CMCC(B)10104],上述兩種菌種均為第3 代,均由甘肅省食品藥品檢定研究院提供。
1.4 樣品
本試驗所用的樣品信息見表1。
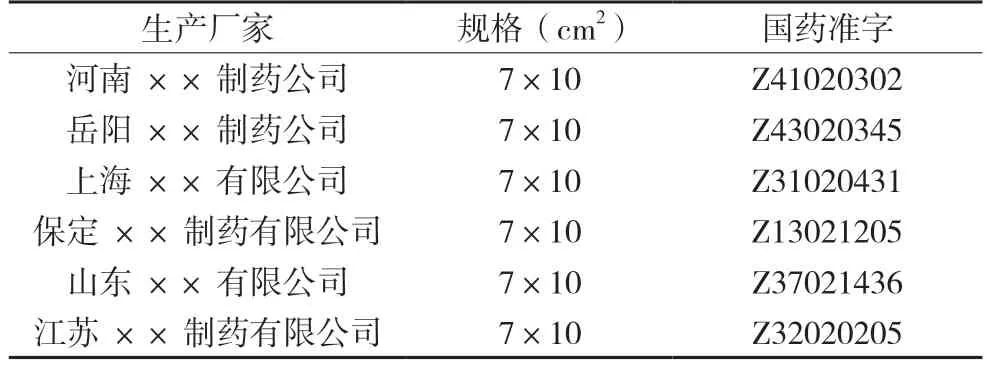
表1 關(guān)節(jié)止痛膏來源信息
2 試驗方法與結(jié)果
2.1 菌液制備
將銅綠假單胞菌、金黃色葡萄球菌接種至胰酪大豆胨液體培養(yǎng)基中,33 ℃培養(yǎng)24 h,取上述兩種菌的培養(yǎng)物,用pH 7.0 無菌氯化鈉-蛋白胨緩沖液制成每1 mL 含菌數(shù)小于100 cfu 的菌懸液。
2.2 控制菌檢查用培養(yǎng)基適用性檢查
2.2.1 溴化十六烷基三甲銨瓊脂培養(yǎng)基檢查用涂布法分別接種不大于100 cfu 的銅綠假單胞菌于被檢培養(yǎng)基和對照培養(yǎng)基中,35 ℃培養(yǎng)24 h。結(jié)果顯示,被檢培養(yǎng)基與對照培養(yǎng)基上生長的菌落大小、形態(tài)特征一致,說明被檢培養(yǎng)基的促生長能力符合規(guī)定;涂布不少于100 cfu 的大腸埃希菌于被檢培養(yǎng)基和對照培養(yǎng)基中,35 ℃培養(yǎng)72 h,結(jié)果顯示,兩種培養(yǎng)基上均未有菌生長,說明被檢培養(yǎng)基的抑制能力符合規(guī)定。
2.2.2 甘露醇氯化鈉瓊脂培養(yǎng)基檢查用涂布法分別接種不大于100 cfu 的金黃色葡萄球菌于被檢培養(yǎng)基和對照培養(yǎng)基中,35 ℃培養(yǎng)24 h,結(jié)果顯示,被檢培養(yǎng)基與對照培養(yǎng)基上生長的菌落大小、形態(tài)特征一致,說明被檢培養(yǎng)基的促生長能力和指示特性符合規(guī)定;涂布不少于100 cfu 的大腸埃希菌于被檢培養(yǎng)基和對照培養(yǎng)基中,35 ℃培養(yǎng)72 h,結(jié)果顯示,兩種培養(yǎng)基上均未有菌生長,說明被檢培養(yǎng)基的抑制能力符合規(guī)定。
2.3 供試液的制備
取供試品2 貼,去掉貼膏劑的保護層,放置在無菌操作臺上,粘貼面朝上,用無菌紗布覆蓋粘貼面,剪碎,將碎片置于含10%聚山梨酯80 的pH 7.0無菌氯化鈉-蛋白胨緩沖液140 mL 中,于水浴加熱45 ℃振搖30 min,混勻,作為1∶10 供試液。
2.4 銅綠假單胞菌檢查方法適用性試驗
試驗組:取1∶10 供試液10 mL 和1 mL(含菌數(shù)<100 cfu)的銅綠假單胞菌菌懸液接種至100 mL胰酪大豆胨液體培養(yǎng)基中,混勻。
供試品對照組:取1∶10 供試液10 mL,稀釋液代替菌液,同試驗組操作。
陽性對照組:取不含聚山梨酯80 的稀釋液(pH 7.0 無菌氯化鈉-蛋白胨緩沖液)取代供試液,同試驗組操作。
陰性對照組:取2 瓶100 mL 胰酪大豆胨液體培養(yǎng)基,其中一瓶作為陰性對照1;另一瓶加入稀釋劑(含10%聚山梨酯80 的pH 7.0 無菌氯化鈉-蛋白胨緩沖液)作為陰性對照2。
上述各組在35 ℃培養(yǎng)24 h 后,取培養(yǎng)物分別劃線接種于溴化十六烷基三甲銨瓊脂培養(yǎng)基的平板上,在35 ℃培養(yǎng),試驗組與陽性對照組24 h 后有菌落生長,供試品組與陰性對照組繼續(xù)培養(yǎng)72 h。若溴化十六烷基三甲銨瓊脂培養(yǎng)基平板上有菌落生長,應(yīng)進行分離、純化及適宜的鑒定試驗,確證是否為銅綠假單胞菌;若溴化十六烷基三甲銨瓊脂培養(yǎng)基平板上無菌落生長,或雖有菌落生長但鑒定結(jié)果為陰性,判未檢出銅綠假單胞菌。結(jié)果見表2。
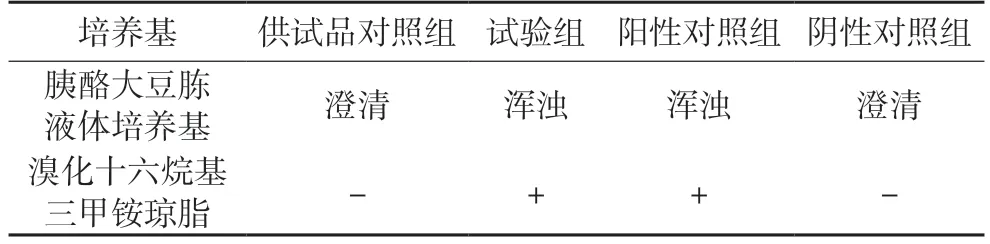
表2 銅綠假單胞菌檢查方法適用性試驗結(jié)果
2.5 金黃色葡萄球菌檢查方法適用性試驗
試驗組:取1∶10 供試液10 mL 和金黃色葡萄球菌菌懸液1 mL(含菌數(shù)<100 cfu)接種至100 mL胰酪大豆胨液體培養(yǎng)基中,混勻。
供試品對照組:取1∶10 供試液10 mL,稀釋液代替菌液,同試驗組操作。
陽性對照組:取不含聚山梨酯80 的稀釋液(pH7.0 無菌氯化鈉-蛋白胨緩沖液)取代供試液,同試驗組操作。
陰性對照組取2 瓶100 mL 胰酪大豆胨液體培養(yǎng)基,其中一瓶作為陰性對照1;另一瓶加入稀釋劑(含10%聚山梨酯80 的pH 7.0 無菌氯化鈉-蛋白胨緩沖液)作為陰性對照2。
上述各組在35 ℃培養(yǎng)24 h 后,取培養(yǎng)物分別劃線接種于甘露醇氯化鈉瓊脂培養(yǎng)基的平板上,在35 ℃培養(yǎng),試驗組與陽性對照組24 h后有菌落生長,供試品組與陰性對照組繼續(xù)培養(yǎng)72 h。若甘露醇氯化鈉瓊脂培養(yǎng)基平板上有菌落生長,應(yīng)進行分離、純化及適宜的鑒定試驗,確證是否為金黃色葡萄球菌;若甘露醇氯化鈉瓊脂培養(yǎng)基平板上無菌落生長,或雖有菌落生長但鑒定結(jié)果為陰性,判未檢出金黃色葡萄球菌。結(jié)果見表3。
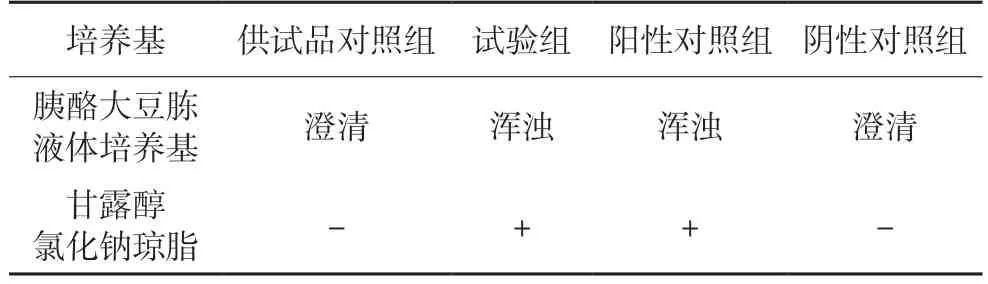
表3 金黃色葡萄球菌檢查方法的驗證結(jié)果
表2 及表3 結(jié)果顯示,按照《中國藥典》2015年版的規(guī)定進行控制菌方法適用性檢查時,陽性對照試驗組和試驗組的試驗菌都生長良好,陰性對照組均無菌生長,表明17 批樣品在該條件下對金黃色葡萄球菌和銅綠假單胞菌無抑菌作用或其抑菌作用可以忽略不計,說明采用該法進行金黃色葡萄球菌和銅綠假單胞菌檢查可行。
3 討論
根據(jù)《中國藥典》2015 年版四部非無菌產(chǎn)品微生物限度檢查法中貼膏劑供試品的制備通則“取供試品,去掉防黏層,將粘貼面朝上放置在無菌玻璃器皿上,在粘貼面上覆蓋一層無菌紗布,避免貼膏劑粘貼在一起。將處理后的貼膏劑放入盛有適宜體積并含有表面活性劑(如聚山梨酯80 或卵磷脂)稀釋液的容器中,振蕩至少30 min。必要時,用同一稀釋液將供試液進一步10 倍系列稀釋”[13],為了簡化試驗步驟,本試驗最初按照藥典規(guī)定,采取“取樣品100 cm2,加入含30%無菌十四烷酸異丙酯的pH 7.0 無菌氯化鈉-蛋白胨緩沖液100 mL,45℃保溫振搖30 min”的方法,除了發(fā)現(xiàn)有些樣品存在供試品溶解不完全的情況外,部分樣品還出現(xiàn)了油水分層不明顯的狀況,需要增加萃取的步驟。經(jīng)過反復(fù)試驗,若將最后把加入的表面活性劑“無菌十四烷酸異丙酯”改為“聚山梨酯80”濃度確定為10%,即稀釋液采用“含10%聚山梨酯80 的pH7.0無菌氯化鈉-蛋白胨緩沖液”,在此稀釋液中,供試品溶解較為完全,油水分層明顯,可以取水層作為1∶10 供試液,同時為了使供試品充分溶解,供試液制備方法中還加入了“將樣品剪碎”的步驟。
綜上所述,最后確定的供試液制備方法為“取供試品2 貼,去掉貼膏劑的保護層,放置在無菌操作臺上,粘貼面朝上,用無菌紗布覆蓋粘貼面,剪碎,將碎片置于含10%聚山梨酯80 的pH 7.0 無菌氯化鈉-蛋白胨緩沖液140 mL 中,于水浴加熱45 ℃振搖30 min,混勻,作為1∶10 供試液”。
本實驗采用《中國藥典》2015 年版四部通則1106 進行關(guān)節(jié)止痛膏控制菌微生物限度檢查方法的分析,該試驗方法操作步驟簡便、準(zhǔn)確度高,且具有儀器簡單、快速、方便快捷的優(yōu)點。

