長效GnRH-a降調節方案有利于改善子宮內膜異位癥患者IVF/ICSI-ET的妊娠及新生兒結局
魏小萌,孔慧娟,李靜,胡琳莉,牛文彬,王芳,郭藝紅
(鄭州大學第一附屬醫院生殖醫學中心 河南省生殖與遺傳重點實驗室,鄭州 450052)
子宮內膜異位癥(Endometriosis,EMS)是女性不孕常見原因之一,不孕女性中約有10%~15%患有EMS,EMS患者約有30~50%合并不孕癥[1]。EMS相關性的不孕癥是多因素作用的結果:EMS引起的性交痛導致同房頻率減少[2];內膜異位處病灶的纖維化和攣縮造成輸卵管拾卵和運送配子能力異常[3];盆腔處于炎癥狀態,增加了炎癥相關產物的水平,影響卵泡微環境,干擾精子功能,改變精卵之間的相互作用[4];影響在位子宮內膜容受性,不利于胚胎著床[5-6]。采用輔助生殖技術(ART)助孕可以避開部分影響因素,且在臨床診療中發現,部分EMS患者選擇手術去除異位病灶,以期提高自然受孕率,但是這會進一步損傷卵巢,從而導致卵巢儲備功能降低,EMS生育指數(EFI)較低[7]。目前更多的EMS患者通過ART獲得妊娠[8],多采用GnRH-a降調節后促排卵的方案,但不同降調節方式對妊娠結局的影響尚存爭議,且沒有關于新生兒結局的研究。本研究中,我們同時比較長/短效GnRH-a降調節方案對EMS患者不同移植周期的妊娠結局和新生兒結局的影響,以期為臨床實踐提供更多參考。
資料與方法
一、研究對象
回顧性分析2009年1月至2019年12月于我院生殖中心行長/短效GnRH-a降調節促排卵后首次移植的EMS患者的臨床資料。
納入標準:(1)經腹腔鏡或者開腹手術確診為EMS患者;(2)于我院行長/短效GnRH-a降調節促排卵方案且有可移植胚胎形成;(3)只包括刺激周期后的首次胚胎移植,即新鮮促排卵周期移植或者全胚冷凍后凍融胚胎移植(FET)。
排除標準:(1)合并多囊卵巢綜合征、苗勒管異常、子宮內膜結核、輸卵管積水的患者;(2)采用供卵周期的患者;(3)采用胚胎植入前遺傳學診斷或篩查(PGD/PGS)的患者;(4)存在糖尿病、甲狀腺功能異常等內分泌異常者;(5)合并嚴重的心、腦、肺、肝臟等疾病不宜妊娠者。
所有研究對象均進行電話隨訪,評估記錄了妊娠結局(流產、胎齡和新生兒體重等)數據。
共納入符合標準的1 805個周期,根據降調節方案分為長效組(采用長效GnRH-a降調節促排卵方案,n=1 499)和短效組(采用短效GnRH-a降調節促排卵方案,n=306);再根據移植周期的不同,分為A組(長效方案所獲胚胎新鮮移植周期,n=1 394)、B組(長效方案所獲胚胎FET周期,n=105)、C組(短效方案所獲胚胎新鮮移植周期,n=274),D組(短效方案所獲胚胎FET周期,n=32)。
二、研究方法
1.促排卵/胚胎移植:新鮮促排卵移植方案包括超長方案、卵泡期長效長方案以及黃體期短效長方案;FET內膜準備方案包括自然周期和非降調節人工周期。具體詳細方案參考本中心已發表文章[10-12]。
2.結局指標:主要結局指標為活產率,次要結局指標包括妊娠率、流產率和新生兒結局。
臨床妊娠:移植后35 d超聲檢查可見妊娠囊,包括宮內妊娠、宮外妊娠以及宮內外同時妊娠;流產:孕周不滿28周且胎兒體重不足1 000 g的妊娠終止;活產:孕周滿28周的至少1個新生兒活產;小于胎齡兒(SGA):出生體重低于同胎齡平均體重的第10百分位數的新生兒;大于胎齡兒(LGA):出生體重在相同胎齡平均體重的第90百分位以上的新生兒[9]。
結局指標計算方法:臨床妊娠率=臨床妊娠周期數/總移植周期數×100%;流產率=流產周期數/總妊娠周期數×100%;活產率=活產周期數/總移植周期數×100%;SGA發生率=小于胎齡兒數/總活產兒數×100%;LGA發生率=大于胎齡兒數/總活產兒數×100%;早產率=分娩孕周<37周的活產兒數/總活產數×100%;低出生體重(LBW)率=出生體重<2 500 g的活產兒數/總活產數×100%。
三、統計學分析
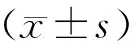
結 果
一、患者一般臨床資料比較
共納入符合標準的1 805個周期,長、短效GnRH-a降調節方案組分別為1 499周期和306周期。兩組間體質量指數、不孕類型無統計學差異(P>0.05),而長效組的年齡、不孕年限、基礎FSH值顯著低于短效組(P<0.05)(表1)。
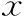
表1 不同降調節方案組一般臨床資料比較[(-±s),n(%)]
二、控制性促排卵資料比較
長效組的Gn啟動劑量顯著低于短效組(P<0.05),而Gn總劑量、Gn天數以及獲卵數、正常受精數、形成可移植胚胎數則顯著高于短效組(P<0.05)(表2)。
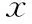
表2 不同降調節方案組促排卵情況比較(-±s)
三、不同移植周期亞組妊娠結局和單胎活產新生兒結局比較
1.長效降調節方案移植亞組:鮮胚移植周期(A組)1 394周期、FET周期(B組)105周期。A組與B組相比,活產率低、分娩孕周短、出生體重低、巨大兒發生率低、早產率高(P<0.05)(表3)。
2.短效降調方案移植亞組:鮮胚移植周期(C組)274周期,FET周期(D組)32周期。C組臨床妊娠率、活產率、LGA發生率顯著低于D組(P<0.05)(表3)。
3.跨方案比較:鮮胚移植周期中,A組的臨床妊娠率、活產率顯著高于C組,單胎活產的巨大兒發生率顯著低于C組(P<0.05)。FET周期中,B組的LGA發生率顯著低于D組(P<0.05)。無論是鮮胚移植還是FET,分娩孕周、出生體重、LBW率、早產率、SGA發生率在不同的降調節方案間均無顯著差異(P>0.05)(表3)。
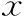
表3 不同降調節方案移植周期亞組妊娠結局和單胎活產新生兒結局比較[(-±s),%]
三、各組妊娠和新生兒結局指標的多因素Logistic回歸分析
單因素Logistics回歸分析表明,移植方案、降調節方案、年齡、不孕年限、移植日內膜厚度、可移植胚胎數顯著影響臨床妊娠率、活產率(P<0.05);移植方案、降調節方案以及體質量指數顯著影響到活產兒的LGA發生率(P<0.05);移植方案、降調節方案、體質量指數、基礎FSH水平以及分娩孕周顯著影響到巨大兒發生率(P<0.05)。我們對上述結局變量進行多因素Logistic回歸分析,校正混雜因素后發現:與短效組相比,長效組臨床妊娠率高、活產率高、LGA發生風險低、巨大兒發生風險低(P<0.05)(表4);與FET周期相比,新鮮周期的LGA發生風險低、巨大兒發生風險低(P<0.05),而臨床妊娠率和活產率無顯著差異(P>0.05)(表5)。

表4 降調節方案對妊娠結局和新生兒結局的多因素Logistic回歸分析

表5 移植周期對妊娠結局和新生兒結局的多因素Logistic回歸分析
討 論
EMS可以通過排卵、受精、著床等多個環節影響妊娠甚至胎兒活產結局。為了得到一個理想的助孕結局,必須采用合適的促排卵方案,在改善胚胎質量的同時最大程度的提高子宮內膜容受性。ART中,垂體降調節是EMS患者接受IVF-ET的一個重要環節,目前推薦EMS患者使用3~6個月的GnRH-a預處理以期獲得較好的治療效果[13-14]。臨床上也采用多種GnRH-a降調節方案,其主要優勢是:(1)GnRH-a通過下調下丘腦-垂體-性腺軸(HPG軸)抑制FSH和LH分泌,防止卵泡過早黃素化,提高卵母細胞質量,同時卵巢分泌的雌激素下降,異位子宮內膜萎縮[15-17];(2)提高外周血中自然殺傷細胞活性,抑制自身抗體生成,改善盆腔微環境和免疫狀態,幫助胚胎著床[18-19];(3)提高子宮內膜細胞的自然凋亡活性,增加子宮內膜與著床相關整合素的表達,增強子宮內膜腺體的血流,從而改善子宮內膜容受性,有助于提高妊娠率[20]。
GnRH-a在降調節中的使用劑量一直是臨床研究的熱點,其參與的多種降調節方案對EMS患者的妊娠結局影響仍有爭議,我們的研究結果顯示,長效GnRH-a降調節方案在改善胚胎質量的同時更多的作用于子宮內膜,通過提高子宮內膜的容受性,從而提高新鮮移植周期的活產率。有學者認為,黃體期長方案在減少Gn時間和Gn劑量的同時,可獲得與超長方案類似的促排卵效果和妊娠結局[21]。但在研究中、重度EMS患者的降調節促排卵方案時,有學者發現,超長方案比黃體期長方案更有利于改善妊娠結局[22]。徐嘉寧等[23]比較了卵泡期長效長方案、超長方案與黃體期長方案應用于EMS患者的妊娠結局,發現無論是新鮮周期還是FET周期,著床率和妊娠率在各組間均無顯著差異,但是該研究沒有分析活產率的差異。這些研究大部分是對不同程度的EMS應用其中兩個或三個降調節方案的妊娠結局的分析,并未對GnRH-a參與的降調節方案有一個定性的分析,我們將應用全量長效GnRH-a的降調節方案均歸為一組,與短效GnRH-a降調節方案在不同的移植周期做比較分析。研究結果顯示,長效GnRH-a降調節組的Gn用量和Gn時間均高于短效GnRH-a降調節組,差異有統計學意義(P<0.05),這可能是由于GnRH-a長時間的作用會對卵巢功能產生較深的抑制作用,使得體外受精/卵胞漿內單精子注射(IVF/ICSI)超促排卵過程中增加Gn用量。其次,新鮮移植周期中的長效GnRH-a降調節組的妊娠率和活產率均高于短效GnRH-a降調節組,而長效GnRH-a組的Gn啟動劑量低于短效組,我們推測日促排卵劑量低且增加緩慢時,不會對子宮內膜產生不良影響,這與最近一項研究結果[24]一致。
最近一項Meta分析表明,與短效GnRH-a方案相比,超長GnRH-a方案增加了EMS不孕癥患者的臨床妊娠率[25],我們的結果與其一致。有學者認為這可能是不同劑量GnRH-a的垂體抑制作用影響了脂質過氧化和子宮內膜間的關系,從氧化應激角度解釋了短效長方案的內膜容受性降低以致于著床率低的原因[26]。我們同時比較了全胚冷凍后首次FET周期的妊娠結局,并且只納入了非降調節人工周期和自然周期兩種內膜準備方案,完全避免了GnRH-a對子宮內膜及盆腔環境的影響,結果顯示兩種降調節方案得到的胚胎在首次FET后妊娠率和活產率均無顯著差異。這進一步表明長效GnRH-a有利于改善EMS患者的內膜容受性從而提高了新鮮移植周期的臨床妊娠率和活產率。
從單胎活產的新生兒結局來看,長效新鮮周期組的巨大兒發生率低于短效新鮮周期組,長效凍融周期組的LGA發生率低于短效凍融周期組,短效新鮮周期組的LGA發生率低于短效凍融周期組,差異均有統計學意義(P均<0.05)。眾所周知,所有可能導致卵母細胞和子宮內膜改變的因素都會導致早期胚胎發育和植入的表觀遺傳學改變,并可能改變妊娠和圍產兒結局[27]。為此,我們進行了多因素Logistic回歸分析,結果表明相比于短效GnRH-a降調節組,長效GnRH-a降調節組的臨床妊娠率高,活產率高,發生LGA、巨大兒的風險低,差異均有統計學意義(P均<0.05)。新鮮周期組發生LGA、巨大兒的風險低于FET周期組,臨床妊娠率和活產率在兩種移植周期組無顯著差別。既往研究認為,與拮抗劑方案促排卵相比,短效GnRH-a降調節方案通常使子宮內膜脫落更為完整,因為在刺激開始之前,雌激素水平低下的情況會持續數天[28]。我們推測,長效GnRH-a降調節使得子宮內膜低雌激素狀態持續更長時間,這種接近于自然周期的內膜狀態更有利于胚胎植入以及后續胚胎發育。既往研究也表明子宮內膜對胎兒生長的影響可能比胚胎的影響更大[29]。我們的研究結果支持長效GnRH-a降調節在改善胚胎質量的同時通過提高子宮內膜容受性增加活產率,降低新生兒圍產期風險。
本研究分析了EMS患者應用長/短效GnRH-a降調節方案對新鮮移植周期和FET周期的妊娠結局和新生兒結局的影響。但是該研究也存在一定的局限性,研究設計為單中心回顧性分析,存在其固有的局限性,且個別分組的樣本量較少,未來需要進行更大樣本的前瞻性研究。其次,本研究采用基礎FSH來評估卵巢儲備,各組都偏向于卵巢功能正常,所以研究結果可能不適用于EMS合并卵巢儲備功能減退的病人。
綜上所述,為了使EMS患者獲得理想的活產率,應該采取更合適的促排卵方案和移植方案,我們認為采用長效GnRH-a降調節方案可以改善EMS患者在新鮮移植周期的妊娠率和新生兒結局。

