上調NDRG1基因對人卵巢癌OVCAR3細胞周期和凋亡的影響
王蓓 代聰偉 李娜 楊艷艷 秦英
(河北省人民醫院婦科,河北 石家莊 050051)
NDRG1基因,也稱為Drg-1,Cap43,RTP,Rit42 and PROXY-1,屬于NDRG基因家族。這個家族由四個基因組成:NDRG1,NDRG2,NDRG3,NDRG4。其余三個基因與NDRG1是同源性基因,有57%~65%相似性〔1〕。NDRG1,是43 kD蛋白,由394個氨基酸組成,廣泛存在于多細胞生物的正常細胞和腫瘤細胞的細胞質中〔2〕。NDRG1表達與腫瘤發生、發展及轉移關系的相關研究表明:NDRG1在抑制腫瘤轉移的過程中發揮著重要的作用〔3,4〕。但有關該方面的研究報道目前仍不多,而且也存在較大爭議。NDRG1表達與腫瘤尤其在卵巢腫瘤轉移的相關性如何,目前國內外尚未發現關于NDRG1與卵巢癌細胞OVCAR3的研究報道。本研究采用分子生物學方法,改變卵巢癌細胞OVCAR3中NDRG1的表達,分析其對卵巢癌細胞周期和凋亡的影響。
1 材料與方法
1.1細胞株 人卵巢癌OVCAR3細胞株中國醫學科學院腫瘤醫院提供。
1.2試劑及儀器 細胞培養基RPMI1640、胎牛血清購自Sigma公司,Trizol試劑及LipofectamineTM 2000、RNA提取試劑購自Invitrogen 公司,Transwell小室購自Costar公司,RT-PCR試劑盒及引物購自Takara公司。質粒pcDNA3.1(+)/NDRG1和pcDNA3.1(+)為Clontech合成。
1.3細胞培養 OVCAR3細胞培養于37℃含5%CO2細胞培養箱內,培養液為含10%胎牛血清的RPMI1640,0.25%胰蛋白酶消化傳代,倒置顯微鏡下觀察細胞生長狀態。
1.4實驗方法
1.4.1細胞轉染 細胞在RPMI1640培養液于37℃、5%CO2飽和濕度的培養箱中培養生長。轉染前1 d,胰酶消化細胞并計數,4×105/孔細胞接種于6孔板,當細胞融合度為80%時即可轉染。轉染時,按照Lipofectamine 2000(Invitrogen公司)說明書進行轉染,實驗分3組:未轉染組(control組),陰性對照組〔pcDNA3.1(+)組〕,實驗組〔pcDNA3.1(+)/NDRG1組〕。
1.4.2熒光定量PCR檢測NDRG1在OVCAR3細胞中的表達 按 Trizol試劑盒說明書分別提取轉染后48 h未轉染組(control組),陰性對照組〔pcDNA3.1(+)組〕,實驗組〔pcDNA3.1(+)/NDRG1組〕細胞的總RNA。逆轉錄-聚合酶鏈反應(RT-PCR)按照Takara 反轉錄PCR試劑盒說明書進行操作,反轉錄合成 cDNA 的第一條鏈,利用Primer5.0設計NDRG1的鑒定引物:上游引物5′-ACACCTACCGCCAGCACA-3′,下游引物:5′-GCCACAGTCCGCCATCTT-3′,擴增片段長度245 bp。PCR擴增條件為:95℃預變性10 min,95℃ 15 s,退火58℃ 20 s,延伸72℃ 27 s,40個循環。以β-actin作為內參照。上游引物:5′-ACTTAGTTGCGTTACACCCTT-3′,下游引物:5′-GTCACCTTCACCGTTCCA-3′,擴增片段長度為156 bp。以上兩對PCR引物均由Takara公司合成。PCR結束后得出Ct值,分析各組之間NDRG1基因的mRNA表達水平差異。
1.4.3Western印跡檢測 將收集的細胞用含非離子去垢劑的緩沖液充分裂解,進行蛋白定量,取50 μg處理好的蛋白樣品進行十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳分析;100 V恒壓轉膜2 h;5 %脫脂奶粉室溫封閉1 h;將膜與抗 NDRG1抗體室溫孵育1 h,4℃過夜;TBST緩沖液洗膜3次,每次15 min,加入二抗室溫孵育1 h,再用TBST洗膜3次;化學法發光,膠片顯色,用Fluorochem E分析結果。以β-actin作為內參照。
1.4.4RT-PCR檢測各組細胞p21及p53基因的mRNA表達 取各組細胞,同上述抽提總RNA,進行逆轉錄及PCR。PCR引物如下:p21上游引物為:5′-TACTCCCCTGCCCTCAACAAGA-3′;下游引物為:5′-CGCTATCTGAGCAGCGCTCAT-3′;產物243 bp。p53上游5′GCGCACAGAGGAAGAGAATC-3′,下游5′-GGCCAACTTGTTCAGTGGAG-3′,產物501 bp。內參為β-actin同1.4.2。每一樣本的最后結果為3次獨立電泳實驗的平均值。
1.4.5Western印跡法檢測各組細胞p21及p53及基因的蛋白表達 取各組細胞,具體過程同上述。一抗為鼠抗人p21單克隆抗體(1∶200)及鼠抗人p53單克隆抗體(1∶200),二抗為辣根過氧化物酶標記的山羊抗鼠二抗(1∶5 000)。每一樣本的最后結果為3次獨立電泳實驗的平均值。以β-actin作為內參照。
1.4.6流式細胞術檢測細胞周期 將轉染后的各組細胞用不含EDTA的胰酶消化成單細胞懸液;具體操作步驟嚴格按試劑盒說明書進行,加入碘化丙啶(PI,濃度為 100 mg/L)溶液染色20~30 min 后,在流式細胞儀上進行檢測分析。
1.4.7流式細胞術檢測細胞凋亡 將轉染后的各組細胞用不含EDTA的胰酶消化成單細胞懸液;具體操作步驟嚴格按試劑盒說明書進行,使用流式細胞儀檢測細胞凋亡情況,每組細胞重復檢測4次。
1.5統計學分析 采用SPSS17.0軟件進行t檢驗、方差分析法、LSD-t法。
2 結 果
2.1PCR檢測NDRG1 mRNA表達 pcDNA3.1(+)/NDRG1組中NDRG1 mRNA相對表達量(1.00±0.03)明顯高于control組(0.57±0.04)和pcDNA3.1(+)組(0.59±0.02,P<0.05)。
2.2Western印跡檢測轉染NDRG1過表達載體后細胞中蛋白表達的變化 在使用NDRG1過表達載體pcDNA3.1(+)/NDRG1和空載體pcDNA3.1(+)分別轉染OVCAR3細胞,并使用RT PCR和Western印跡方法鑒定轉染效果,結果表明:control組和轉染pcDNA3.1(+)空載體的OVCAR3細胞中NDRG1表達量與轉染過表達載體pcDNA3.1(+)/NDRG1組相比顯著降低(0.46±0.02、0.49±0.03、1.85±0.05,P<0.05),見圖1。
2.3NDRG1作用后卵巢癌細胞OVCAR3中p21及p53基因的mRNA表達 control組、pcDNA3.1(+)組 NDRG1、p21及p53 mRNA表達均明顯低于pcDNA3.1(+)/NDRG1組(P<0.05),見表1。
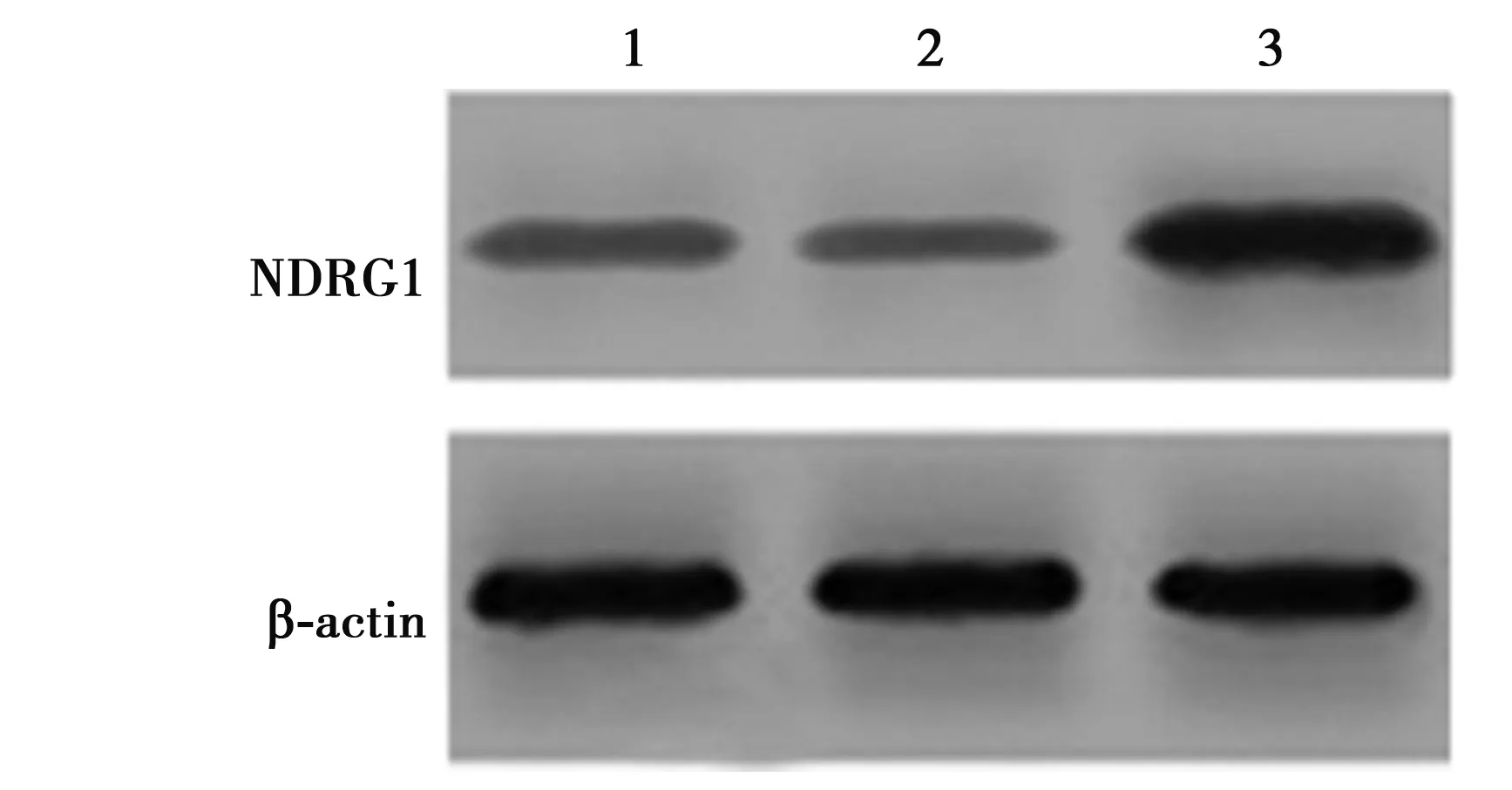
1~3:control組,pcDNA3.1(+)組,pcDNA3.1(+)/NDRG1組,下圖同圖1 各組OVCAR3細胞NDRG1表達水平比較
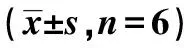
表1 各組卵巢癌細胞OVCAR3中p21及 p53基因的mRNA表達
2.4NDRG1作用后卵巢癌細胞OVCAR3中p21及p53基因的蛋白表達 control組及pcDNA3.1(+)組NDRG1、p21及p53的表達均明顯低于pcDNA3.1(+)/NDRG1組(P<0.05),見表2,圖2。
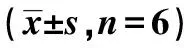
表2 各組OVCAR3細胞NDRG1蛋白表達水平比較
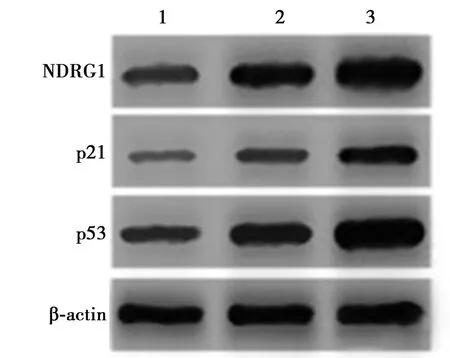
圖2 各組OVCAR3細胞NDRG1、p21及 p53基因表達水平比較
2.5流式細胞儀檢測細胞周期 pcDNA3.1(+)/NDRG1組細胞與control組、pcDNA3.1(+)組相比,G0/G1期細胞數明顯增多,而S期細胞數減少,差異均有統計學意義(均P<0.05),G2/M期細胞數無明顯變化(P<0.05)。見表3。
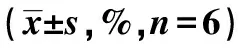
表3 流式細胞儀檢測各組OVCAR3細胞 周期
2.6流式細胞儀檢測卵巢癌細胞OVCAR3細胞凋亡的影響 與control組、pcDNA3.1(+)組比較,pcDNA3.1(+)/NDRG1組細胞凋亡率明顯增加(P<0.05),而control組pcDNA3.1(+)組之間細胞凋亡率無明顯變化(P>0.05),見表4。
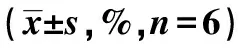
表4 流式細胞儀檢測各組OVCAR3 細胞凋亡
3 討 論
本研究說明人卵巢細胞癌OVCAR3細胞受到質粒pcDNA3.1(+)/NDRG1轉染的影響,出現細胞周期阻滯。細胞凋亡數據表明,發現上調NDRG1基因后OVCAR3細胞凋亡率顯著提高;本研究結果說明過表達NDRG1可以顯著增加OVCAR3細胞凋亡,使細胞周期發生改變,誘導細胞凋亡,證明了NDRG1在卵巢癌細胞中可能作為抑癌基因發揮著腫瘤抑制作用。
很多文獻表明,NDRG1作為一種腫瘤抑制基因,在轉移瘤中NDRG1基因的低表達,由N-myc下調實現,并且也可由過表達HIF-1、p53等多種轉錄因子實現〔5〕。細胞中DNA損傷后,NDRG1表達是通過p53介導途徑來實現的,此過程對p53介導的凋亡是非常必要的條件之一〔6〕。在胰腺癌的相關研究中證實,NDRG1基因表達較低的細胞株比表達高的細胞株侵襲遷移能力明顯增強〔7〕。人肝細胞肝癌中NDRG1的過表達與腫瘤的侵襲性和預后差關系密切,提示NDRG1在肝癌中具有加速腫瘤生長的作用;低表達肝癌細胞株中NDRG1可使細胞的增殖和侵襲作用顯著受到抑制,并可以誘導細胞凋亡,表明NDRG1基因具有抗凋亡作用〔8〕。然而,很多研究證明,腫瘤組織中NDRG1的表達與正常細胞差異不大或稍有下降〔9〕。NDRG1基因的下調與結直腸癌、乳腺癌、前列腺癌、胰腺癌、肝癌等患者愈后不良關系密切〔10~16〕。
p21基因是一種抑癌基因,作為細胞周期蛋白依賴激酶抑制劑(CKIs)家族中的一員,是目前已知的具有最廣泛激酶抑制活性的CKIs,不僅在子宮內膜癌、肺癌、胃癌等惡性腫瘤組織中不表達或表達減少,而且與腫瘤分化程度、侵襲轉移能力關系密切〔17〕。MDM2主要與p53蛋白相結合,參與調節細胞增殖及凋亡的多種信號通路。很多惡性腫瘤組織中MDM2表達異常,MDM2的過度表達與腫瘤發生發展及預后較差關系密切,MDM2今后也可能成為腫瘤治療的另一個新靶點〔18〕。Kovacevic等〔19〕學者認為,利用脂質體介導的方法將NDRG1基因導入人前列腺癌PC3MM細胞株中,結果證實細胞凋亡加速而增殖明顯下降,分子機制可能與NDRG1通過非p53依賴信號通路來調節p21的表達密切相關。在非轉移瘤中p53的改變可調節NDRGl的表達,而在轉移瘤細胞中通過細胞內鈣離子釋放來調節其表達,這個過程不依賴p53的表達〔20〕。另外,NDRG1的低表達可消除p53基因介導的細胞凋亡作用,表明 NDRG1基因與細胞的多種傳導通路關系密切。
NDRG1基因不僅存在于多種正常細胞和組織中,在其生長發育過程中發揮著較為重要的作用,并且在腫瘤細胞和組織的發生發展中也起著至關重要的作用〔21〕。人類很多腫瘤組織中,如肺癌、胃癌、前列腺癌、乳腺癌等,NDRG1 基因都呈現低表達〔22~25〕;但是,NDRG1轉染到腫瘤細胞中,可使腫瘤細胞的生長呈現顯著抑制。也有研究證實,通過流式細胞儀研究正常細胞中NDRG1的表達出現周期性變化,在G1期和G2/M期達到較高水平,而在S期則呈現較低表達〔26〕;然而,在腫瘤細胞中并沒有發現NDRG1表達呈現周期性表達,在細胞周期表達中出現均一性,這表明NDRG1被轉染到人腫瘤細胞株中可使細胞周期受到阻滯,同時可以誘導細胞出現凋亡的改變。

