血清脂蛋白相關磷脂酶A2、脂質代謝與兒童阻塞性睡眠呼吸暫停低通氣綜合征嚴重程度的相關性分析
郭宇,彭韶
(鄭州大學第一附屬醫院 兒科,河南 鄭州 450000)
兒童阻塞性睡眠呼吸暫停低通氣綜合征(obstructive sleep apnea-hypopnea syndrome,OSAHS)是兒童于睡眠期間出現的異常呼吸節律現象,其特征為上呼吸道長時間部分阻塞或間歇性完全阻塞,影響睡眠期間的正常通氣和睡眠模式[1]。近年來,OSAHS在兒童中的發病率升高明顯,如不及時治療、糾正睡眠模式,則會影響患兒正常能量代謝、生長發育、精神狀態及學習生活,導致患兒出現腺樣體面容、生長發育遲緩、易激惹、學習成績下降。脂蛋白相關的磷脂酶A2(lipoprotein-associated phospholipase A2,Lp-PLA2)是由巨噬細胞、肥大細胞等分泌的新型炎癥標志物[2],外周血Lp-PLA2升高在成人OSAHS患者中常提示存在血管炎性反應,并發動脈粥樣硬化的風險增加[3],高Lp-PLA2和血脂水平可預測心腦血管風險及不良預后[4]。但研究Lp-PLA2對兒童OSAHS疾病的發生進展的影響較為少見。通過研究OSAHS患兒外周血中Lp-PLA2的水平及脂質代謝的情況,分析Lp-PLA2、血脂代謝情況與兒童OSAHS疾病嚴重程度的關系。
1 資料與方法
1.1 研究對象選取2018年1月至2020年10月在鄭州大學第一附屬醫院住院治療的OSAHS患兒151例,年齡3~13歲,平均(7.24±2.60)歲,其中男87例,女64例。
1.2 分組利用PSG記錄AHI,根據美國麻醉醫師協會[5]對兒童OSAHS疾病嚴重程度分級標準,將收集的OSAHS患兒分為輕度組(5次·h-1≥AHI>1次·h-1)46例,年齡3~13歲,平均(8.07±1.51)歲,其中男27例,女19例;中度組(10次·h-1≥AHI>5次·h-1)51例,年齡3~13歲,平均(8.50±1.76)歲,其中男31例,女20例;重度組(AHI>10次·h-1)54例,年齡3~13歲,平均(7.89±2.02)歲,其中男29例,女25例。選擇50例同期于鄭州大學第一附屬醫院體檢的健康兒童,作為對照組,年齡3~13歲,平均(7.63±2.51)歲,其中男26例,女24例。4組間一般資料比較,差異無統計學意義(P>0.05)。本研究由鄭州大學第一附屬醫院醫學倫理委員會審核通過,并提前告知兒童及家屬檢查目的取得對方同意,兒童家屬已簽知情同意書。
1.3 選取標準
1.3.1OSAHS患兒 (1)納入標準:①年齡3~13歲;② 8 h多導睡眠監測儀(polysomnography,PSG)記錄呼吸暫停低通氣指數(apnea hypopnea index,AHI)>1次;③伴有呼吸暫停、張口呼吸、打鼾、日間貪睡等癥狀。(2)排除標準:①患有嚴重心肺疾病;②其他嚴重睡眠障礙;③中樞性睡眠呼吸暫停低通氣綜合征;④喪失自我控制能力的精神病;⑤服用阿片類藥物;⑥神經肌肉疾病;⑦先天性顏面部畸形及外傷;⑧先天性呼吸系統發育不良;⑨遺傳代謝異常;⑩既往行上呼吸道手術等。
1.3.2對照組 (1)納入標準:①年齡3~13歲;②既往體健,無先天性、遺傳性、傳染性疾病,無使用激素等藥物史,無外傷、手術、輸血史;③生長發育與同齡兒相符,隨社會計劃免疫接種,無不良反應;④精神智力正常,具有自我意識可正常交流。(2)排除標準:①鼻塞、流涕、咽腔不適、咳嗽、咳痰、喘息等呼吸道疾病癥狀;②張口呼吸、呼吸暫停、打鼾、日間嗜睡等睡眠障礙癥狀;③家族鼾癥史。
1.4 觀察指標
1.4.1一般資料采集 基礎信息:性別、年齡、體質量指數(body mass index,BMI)、血壓。臨床病史:主要癥狀、伴隨癥狀、既往史、生長發育史、家族史。
1.4.2PSG監測 采用PSG(美國 Alice4及Sandman Elite)對OSAHS患兒進行連續8 h的睡眠呼吸監測,由同一監測人員進行操作及記錄,記錄AHI值。
1.4.3生化指標 所有患兒入院完成PSG后采集晨起7:30至8:00空腹狀態下靜脈血標本3 mL,3 500 r·min-1離心10 min后,由全自動酶聯免疫分析儀檢測血清Lp-PLA2、 低密度脂蛋白(low-density lipoprotein,LDL)、高密度脂蛋白(high-density lipoprotein,HDL)、甘油三酯(triglyceride,TG)、總膽固醇(total cholesterol,TC)水平,檢驗試劑盒分別來自于美國Rapidbio公司、天津康爾克生物科技有限公司。
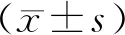
2 結果
2.1 一般資料4組性別、年齡、BMI、收縮壓、舒張壓差異無統計學意義(P>0.05)。見表1。

表1 4組一般資料比較
2.2 生化指標輕度組、中度組、重度組外周血Lp-PLA2、LDL、TG、TC高于對照組(P<0.05);輕度組、中度組、重度組外周血HDL低于對照組(P<0.05);重度組外周血Lp-PLA2、LDL、TG、TC高于輕度組、中度組(P<0.05);重度組外周血HDL低于輕度組、中度組(P<0.05);中度組外周血Lp-PLA2、LDL、TG高于輕度組(P<0.05);中度組外周血HDL、TC較輕度組差異無統計學意義(P>0.05)。見表2。
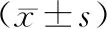
表2 4組Lp-PLA2、LDL、HDL、TG、TC水平比較
2.3 OSAHS患兒生化指標與AHI的相關性分析OSAHS患兒血清Lp-PLA2、LDL、TG與AHI呈正相關(P<0.05),HDL與AHI呈負相關(P<0.001)。見表3。

表3 OSAHS患兒血清生化指標與AHI的相關性
3 討論
OSAHS為慢性呼吸系統疾病,其發生發展主要是由狹窄或可折疊等上呼吸道的解剖學異常導致,同時伴有非解剖學因素,包括呼吸興奮閾值降低,呼吸驅動減退等[6]。OSAHS在學齡前兒童多表現為呼吸暫停、頻發覺醒、遺尿、虛汗;學齡期兒童則多表現為張口呼吸、間斷打鼾、異常的胸腹呼吸運動[7]。OSAHS患兒常因早期癥狀不明顯、特異性較低未能引起患兒家屬重視或出現誤診,后因長期睡眠呼吸紊亂影響正常能量代謝、免疫調節,出現腺樣體面容、生長發育遲緩、異常體質量增長、胸悶等癥狀后才入院治療。
OSAHS是心血管病、腦卒中發病率及死亡率的獨立危險因素,Quan等[8]發現OSAHS患兒長期氣道擴張受限或氣道提前關閉會導致夜間呼吸受限而出現慢性間歇性低氧(chronic intermittent hypoxia,CIH),CIH導致交感-迷走平衡紊亂使心率變異性增加,同時可導致鉀離子水平升高,去除高血糖、高血壓等疾病的影響,OSAHS嚴重程度的增加可使心血管病發病率及死亡率進一步提高。M?ller-Levet等[9]發現睡眠限制可改變外周血細胞基因表達,包括PRDX2、PRDX5等免疫細胞活化通路和SLC2A3、SGHLC25、ABCA1等脂質代謝通路上調,當睡眠受限加重可出現累積效應,循環系統的慢性炎癥導致機體出現心血管疾病、代謝性疾病等病理狀態。
Lp-PLA2是由人PLA2G7基因編碼的一種鈣依賴性脂肪酶,主要由成熟的單核巨噬細胞、肥大細胞產生[10]。Northern印跡分析表明,當組織或器官(如扁桃體、腺樣體、胸腺、胎盤)內有大量巨噬細胞時能表達高水平的Lp-PLA2mRNA,該水平在單核細胞分化過程中可持續存在[11]。在低氧狀態下,氧化應激反應產生的氧自由基可激活Lp-PLA2活性[12],激活后的Lp-PLA2在外周血循環過程中可與LDL和HDL生成炎癥復合物,形成炎癥級聯反應[13]。Bonnefont-Rousselot等[14]發現,Lp-PLA2在動脈粥樣硬化斑塊的壞死中心表達明顯升高,可將Lp-PLA2作為心血管疾病的獨立風險指標,并且用作臨床風險預測的輔助手段。Bekci等[15]發現,男性OSAHS患者睡眠期間覺醒次數增加可出現Lp-PLA2、TG、TC升高(P<0.05),Lp-PLA2水平與覺醒獨立相關(P=0.002),夜間覺醒作為OSAHS直觀表現方式,OSAHS患者夜間覺醒增多,導致交感神經興奮性增加,心率加快、血管損傷加重,為OSAHS患者繼發心血管疾病提供血流動力學障礙依據。Moise等[16]發現,OSAS患者Lp-PLA2水平升高(P<0.05),在患有代謝綜合征的OSAHS患者表現明顯,Lp-PLA2水平可與AHI呈正相關(P=0.015),表明OSAHS患者Lp-PLA2等炎癥標志物的增加可與內皮損傷和動脈粥樣硬化的發展相關。OSAHS患兒體內Lp-PLA2水平較對照組明顯升高,且隨AHI升高而升高,符合目前研究現狀,由于兒童仍處于生長發育階段,免疫調節機制尚不完善,對于OSAHS應激反應較明顯,Lp-PLA2水平升高,且長期OSAHS可使機體出現持續性損傷加重,出現免疫組織和器官代償性增生,使Lp-PLA2水平依賴性升高,心血管疾病風險升高。
OSAHS患者由于夜間呼吸睡眠不穩定出現食欲升高、運動量降低,其肥胖風險及速度與健康人群相比日益提升。Karkinski等[17]發現同等BMI水平的OSAHS患者TG、TC、LDL水平明顯升高,HDL明顯降低(P<0.05),表明OSAHS可通過胰島素敏感度降低、胰島素抵抗等在非肥胖患者的脂質代謝障礙中起重要作用。Nadeem等[18]對OSAHS患者的一項薈萃分析中發現,OSAHS患者TG水平升高,HDL降低,且與AHI密切相關(P=0.001),表明OSAHS患者HDL、TG水平的改變與CIH導致機體全身炎癥水平升高、白介素-1等促血管內皮LDL、TG代謝的細胞因子生成增多有關,同時OSAHS嚴重程度增加,氧化物生成增多,脂肪細胞脂解,脂質過氧化也可促進OSAHS體內血脂異常代謝加重與累積。OSAHS患兒與對照組比較,結果顯示LDL、TG、TC水平明顯升高,且隨疾病嚴重程度升高而升高,HDL水平降低,隨疾病嚴重程度升高而降低,符合目前研究現狀,兒童由于神經及內分泌系統尚未完善,基礎代謝率較高,當出現睡眠障礙時,神經-內分泌系統紊亂,且由于嗜睡、精神狀態低下,代謝減慢,出現惡性循環,出現代謝綜合征的風險升高。
血清Lp-PLA2、脂質代謝與OSAHS患兒疾病嚴重程度的相關性研究表明,OSAHS患兒存在慢性炎癥反應及異常能量代謝,且隨著嚴重程度升高而加重。傳統OSAHS診斷存在耗時較長、操作復雜、舒適度低等缺點,患兒不易配合,可通過檢測外周血Lp-PLA2、血脂水平了解OSAHS患兒疾病進展、心血管疾病及代謝性疾病的風險情況,為OSAHS患兒早期預防、病情診療、生活管理提供了方向。

