空心釘結合錨釘與空心釘單獨固定治療脛骨后交叉韌帶止點撕脫骨折對比研究
吳馮勝,徐執揚,李 晗,吳飛華,蘇新杰,梁喜斌,陳 蕾
北京市垂楊柳醫院骨科,北京 100022
后交叉韌帶(posterior cruciate ligament,PCL)是維持機體膝關節穩定的重要結構,承載膝關節90%的后移力量,一旦斷裂將直接導致膝關節后直向及旋轉不穩定,進一步導致半月板損傷、膝關節發生退行性改變[1]。脛骨PCL止點撕脫骨折是引起PCL損傷的特殊類型之一,屬于PCL韌帶體部和股骨附著部結構完整,而脛骨附著部結構出現不同程度損傷的骨折[2]。近年來,隨著運動損傷的增多以及交通事故的頻繁發生,高能量損傷所致的脛骨PCL止點撕脫骨折發病率呈逐年上升趨勢,若治療不及時會引起機體PCL松弛,嚴重影響膝關節穩定及患者身體健康[3]。臨床治療止點撕脫骨折較為常用的方法是切開復位內固定術,固定方式有克氏針、空心釘、鋼板、鋼絲、錨釘等[4],目前有關空心釘結合錨釘治療脛骨PCL止點撕脫骨折的報道較少。本研究回顧性分析2016年1月—2020年1月筆者醫院骨科收治的28例脛骨PCL止點撕脫骨折患者的臨床資料,探討膝關節后內側入路空心釘結合錨釘固定治療脛骨PCL止點撕脫骨折的臨床療效。
臨床資料
1 一般資料
納入標準:(1)年齡20~65歲;(2)根據臨床癥狀、體征、X線片檢查等確診為單純性脛骨PCL止點撕脫骨折[5],且影像學提示脛骨PCL附著點骨折移位≥3mm;(3)最大骨折塊>15mm且伴周邊小碎骨;(4)不伴血管、神經損傷的閉合性骨折;(5)既往無膝關節損傷病史。排除標準:(1)陳舊性骨折;(2)PCL斷裂;(3)嚴重心、肝、腎功能不全。
本組患者28例,根據手術方法分為觀察組和對照組,各14例。觀察組行膝關節后內側入路空心釘結合錨釘固定治療,男性7例,女性7例;年齡20~65歲,平均33.8歲;骨折Meyers-McKeever分型:Ⅱ型7例,Ⅲ型7例;運動損傷4例,道路交通傷10例。對照組行膝關節后內側入路空心釘治療,男性8例,女性6例;年齡20~65歲,平均34.7歲;骨折Meyers-McKeever分型:Ⅱ型8例,Ⅲ型6例;運動損傷3例,道路交通傷11例。兩組患者一般資料比較差異均無統計學意義(P>0.05),具有可比性。本研究經筆者醫院醫學倫理委員會批準,患者均簽署知情同意書。
2 手術方法
觀察組:行膝關節后內側入路空心釘(天津市威曼生物材料有限公司)結合錨釘固定治療。患者腰硬聯合麻醉或氣管插管全身麻醉后,取俯臥位并在氣囊止血帶下進行手術。常規消毒鋪巾,患側小腿前方墊軟枕。屈膝約20°后,在膝關節后內側取一長5~6cm斜形小切口,充分分離各層組織后,在半膜肌與腓腸肌內側頭之間暴露關節囊。將肌肉、血管、神經鞘牽向外側,切開顯露后關節囊,暴露PCL脛骨附著點,清理骨折斷端間凝血塊及嵌入的軟組織,屈膝45°,在PCL脛骨附著點的后下方將直徑5.5mm鈦質帶線施樂輝錨釘擰入1枚后,將其自帶的其中1~2根不可吸收線縫線應用導引器部分穿過或自前方繞過后叉韌帶及小的撕脫骨塊,并拉攏固定。解剖復位后分別在骨塊上2枚導針,透視確認斷端位置可,導針位置好,置入直徑4.5mm帶墊圈鈦質空心釘。其中3例較大骨塊應用2枚空心螺釘(對照組1例,觀察組2例,兩組空心螺釘使用數量差異無統計學意義),其余均為1枚螺釘固定。將錨釘上另外1根不可吸收線應用導引器部分穿過PCL,兩根線分別打結、形成雙交叉荷包固定骨折塊并加固。再次透視確認斷端位置、內固定位置可,檢查后抽屜試驗呈陰性后,逐層縫合。
對照組:行膝關節后內側入路空心釘治療。術中麻醉、體位、復位固定均同觀察組,但術中未使用施樂輝錨釘復位固定。
3 術后處理及康復
術后常規抗炎、止痛3d。觀察組術后第2天即開始進行膝關節被動屈曲功能鍛煉,每天1~2次,每次10~15min,每隔1d增加10°~15°,骨折愈合前練習至120°,并在支具保護下行直腿抬高、踝泵等下肢肌肉力量功能訓練,術后6~8周膝關節支具保護下逐步負重,每隔1d增加10°~15°。對照組術后術側膝關節石膏托固定或支具固定至5°~10°屈曲位3周。術后6周將支具調整屈曲30°進行膝關節被動功能鍛煉,每天1~2次,每次10~15min,并在支具保護下行直腿抬高、踝泵等下肢肌肉力量功能訓練,術后6~8周逐步負重。
4 觀察指標
觀察并記錄兩組患者骨折愈合時間(骨折愈合標準:局部無壓痛、縱向叩擊痛以及異常活動;X線片顯示骨折線模糊,有連續性骨痂通過骨折線)、術中出血量以及手術時間。采用美國膝關節協會(AKS)評分系統[6]評估兩組患者術前以及術后9個月膝關節整體功能和形態,總分0~200分,得分越高,表明患者膝關節整體功能和形態越好。采用Lysholm評分[7]評估兩組患者的膝關節日常功能及運動功能,得分0~100分,得分越高,表明患者膝關節日常功能及運動功能越好。觀察并記錄兩組患者術后并發癥發生情況,包括關節滲液、積血、感染;下肢靜脈血栓;螺釘與錨釘松動、斷裂。計算各組并發癥發生率。
5 統計學分析

結 果
兩組骨折愈合時間、術中出血量以及手術時間比較差異無統計學意義(P>0.05),見表1。術前,兩組AKS評分及Lysholm評分比較差異無統計學意義(P>0.05);術后9個月,兩組AKS評分及Lysholm評分均明顯高于術前,且觀察組明顯高于對照組(P<0.05),見表2。觀察組未出現關節滲液、下肢靜脈血栓、螺釘與錨釘松動等并發癥,并發癥發生率為0;對照組發生關節滲液、下肢靜脈血栓并發癥各1例,并發癥發生率為14.29%,觀察組并發癥發生率顯著低于對照組(Fisher=10.083,P<0.05)。典型病例見圖1。
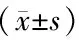
表1 兩組患者手術指標比較

圖1 患者女性,45歲,運動時摔傷。左脛骨后交叉韌帶止點撕脫骨折,全麻下行膝關節后內側入路空心釘結合錨釘固定治療。a、b.術前CT三維、二維重建示左膝后交叉韌帶脛骨止點撕脫骨折;c、d.術前正位、側位X線片示左脛骨后交叉韌帶止點撕脫骨折;e、f.術前MRI示左脛骨后交叉韌帶止點撕脫骨折;g、h.行膝關節后內側入路空心釘結合錨釘固定治療后,術后側位、正位X線片示左脛骨后交叉韌帶止點撕脫骨折空心釘及錨釘固定位置良好
討 論
脛骨PCL止點撕脫骨折又稱PCL脛骨附著區骨折,多因膝關節過屈時股骨遭遇向下暴力或膝關節過伸損傷、脛骨屈曲時脛骨前方遭受暴力所致,可造成患者膝關節后方不穩定[8]。研究表明,若不能實現PCL的解剖復位,則可能導致患者骨不連、創傷性關節炎等發生,嚴重影響患者生活質量[9]。目前臨床上對于移位的脛骨PCL止點撕脫骨折一般主張進行切開復位內固定手術,固定材料包括克氏針、空心螺釘、錨釘、鋼絲等[10]。但傳統的克氏針因具有固定不穩定及退針等缺點,影響患者治療效果,已基本放棄使用[11]。鋼纜、鋼絲固定撕脫骨折塊需人工建立合適的骨隧道,增加了手術操作難度,延長手術時間,影響患者術后康復。因此,本研究采用膝關節后內側入路空心釘結合錨釘固定治療脛骨PCL止點撕脫骨折,發現該治療方法可有效促進患者康復。
本研究結果發現,兩組患者骨折愈合時間、術中出血量以及手術時間比較差異無統計學意義,說明空心釘治療與空心釘結合錨釘固定治療,兩種術式均可有效促進患者骨折愈合,不增加患者手術創傷,且手術時間與骨折愈合時間相當。空心釘結合錨釘固定治療雖然在術中增加了使用錨釘固定時間,但有利于骨碎塊的復位與固定,減少空心釘固定時間,因此和單獨使用空心釘治療整體手術時間相當。脛骨近端血供豐富,且為松質骨,兩組均使用空心螺釘固定,骨折固定效果較好,因此兩組骨折愈合時間并無明顯區別。本研究中兩組均采用膝后內側弧形切口,從腓腸肌內側頭和半膜肌肌間隙進入膝關節囊,可在骨折處清晰顯露神經、血管束,從而在安全有效暴露PCL脛骨止點的基礎上有效保護血管神經束,無需解剖血管神經,避免深靜脈血栓及神經損傷[12]。此外,兩組手術過程中不切斷腓腸肌內側頭,避免后期小腿肌力減退,較傳統的S形切口,明顯減少手術創傷,并促進骨折愈合[13]。
本研究發現,術后9個月觀察組AKS評分及Lysholm評分均明顯高于術前和對照組。提示與單獨采用空心釘治療相比,采用空心釘結合錨釘固定治療的術式更有利于促進脛骨PCL止點撕脫骨折患者術后膝關節功能恢復,降低并發癥發生率。施樂輝錨釘為鈦合金材質,具有良好的組織相容性,埋入脛骨平臺內無需二次取出,能夠免除患者二期手術造成的再次損傷,有利于患者術后膝關節功能恢復。另外,帶線錨釘所帶縫線可耐受50磅的拉伸力,是同樣直徑普通縫線的2.5倍,可以最大限度復位并固定撕脫骨折塊,增強空心釘的固定強度,有效避免術中內固定骨折塊時發生骨折塊破碎、移位的風險,達到良好PCL止點重建效果,患者術后可盡可能早地恢復膝關節功能活動[14]。此外,采用錨釘系統結合帶墊片空心釘固定骨折塊,可使應力分散,使各固定點受力相對均勻,穩妥固定大小骨塊,從而為撕脫骨折塊的愈合提供動靜結合的修復環境,有助于患者術后盡可能早地恢復膝關節功能活動,促進患者膝關節功能恢復[15]。
本研究不足:樣本量偏少,患者隨訪時間較短;未觀察應用鉚釘縫合后是否影響脛骨PCL止點撕脫骨折交叉韌帶血供。盡管所用術式獲得了滿意的早期臨床療效,仍需要大樣本量和長期隨訪提供更加可靠的結論。
綜上所述,采用膝關節后內側入路空心釘結合錨釘固定治療的手術方式,可有效改善PCL止點撕脫骨折患者術后患肢膝關節功能,減少術后并發癥發生,且不增加手術時間及骨折愈合時間。