大腦中動脈區腦梗死伴腦皮質層狀壞死臨床報告
楊 淑,張 蕾,符 浩,朱會敏,王全玉,楊 瑩,丁 里
(云南省第一人民醫院/昆明理工大學附屬醫院 神經內科,云南 昆明 650032)
皮質層狀壞死(cortical laminar necrosis,CLN),也被稱為假層狀壞死(pseudolaminar necrosis),由Sawada 等于1990年最先報道,可發生在不同年齡,見于多種原因導致的中樞神經系統氧和(或)糖攝取障礙及腦能量代謝異常,隨時間改變可出現影像學特征性變化[1]。但目前國內許多臨床醫師和影像科醫師因對CLN 認識不足,常誤診為出血性疾病,進而影響治療決策[2]。
1 資料與方法
1.1 一般資料
回顧性分析我院2019年3月-2019年6月收治的3 例急性腦梗死患者,責任病灶均為大腦中動脈供血區,男性1 例,女性2 例,年齡分別為52 歲、61 歲和66 歲。其中2 例既往有高血壓病史,1 例有風濕性心臟瓣膜病、心房纖顫病史。1例在病程中有腦梗死區非癥狀性出血轉化。入選病例符合中國腦血管疾病分類2015 診斷標準[3],均進行了非增強型頭顱電子計算機斷層掃描(non-enhanced cranial computed tomography,NCCT),電子計算機斷層掃描血管成像(computed tomography angiography,CTA),電子計算機斷層掃描灌注成像技術(computed tomography perfusion weighted imaging,CTP),磁共振成像技術(magnetic resonance imaging,MRI) 檢查。
1.2 影像學檢查及評價方法
入院后均第一時間完成NCCT 掃描,后續完成頭頸CTA+CTP 檢查,動態監測頭顱CT 表現,出現腦皮質層狀壞死后完善頭顱MRI 檢查。由2名高年資影像醫師共同閱片,重點觀察腦梗死區域影像改變。
1.3 治療方法
3 例病例中有1 例進行靜脈溶栓,另2 例由于超過靜脈溶栓及血管內治療時間窗僅予抗血小板聚集、他汀、降低顱內壓、清除自由基及對癥治療。
2 結果
2.1 影像表現
3 例患者均為單側發病,CTP 均提示大腦中動脈區大片狀低灌注,1 例CTA 提示患側大腦中動脈重度狹窄,1 例CTA 提示患側大腦中動脈閉塞,1 例CTA 未見大腦中動脈狹窄、腦梗死部位非癥狀性出血轉化。在后續隨訪中NCCT 提示腦梗死區出現沿皮質分布的線狀高密度影,見圖1,同步MRI 檢查提示患側大腦中動脈供血區大片狀梗死,病灶呈T1 加權成像低、T2 加權成像及水抑制成像高信號、彌散加權成像和表觀擴散系數(apparent diffusion coefficient,ADC) 高信號,見圖2。CLN均表現為沿梗死區皮質表面分布的線狀或腦回樣T1WI 高信號,部分高信號病灶可深達基底節區,磁敏感成像呈等信號,見圖3。
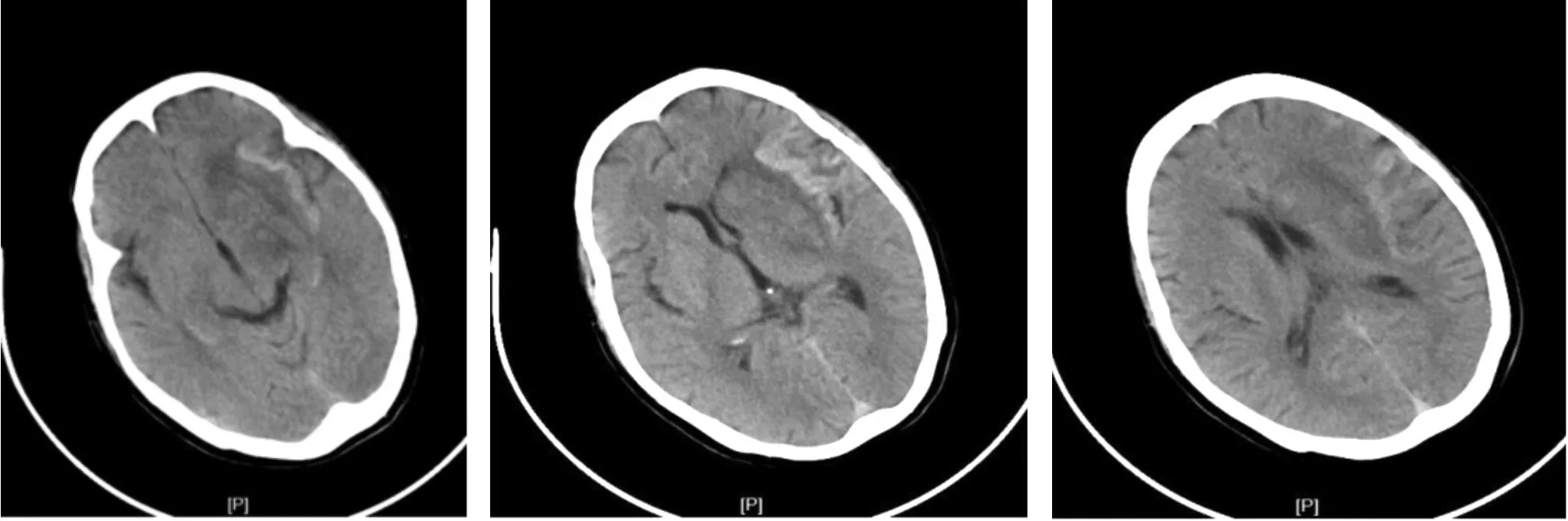
圖1 腦梗死區出現沿皮質分布的線狀高密度影

圖2a 病灶呈T1WI 低信號
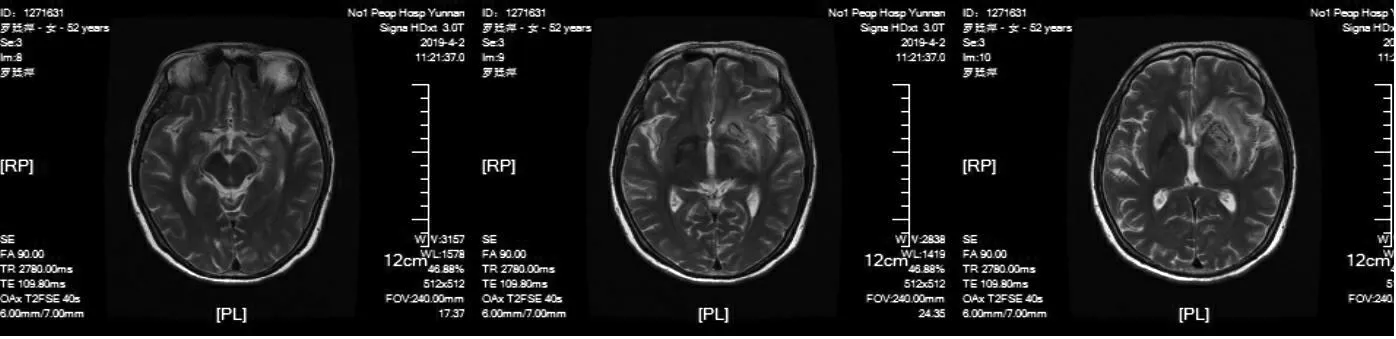
圖2b 病灶呈T2WI 高信號
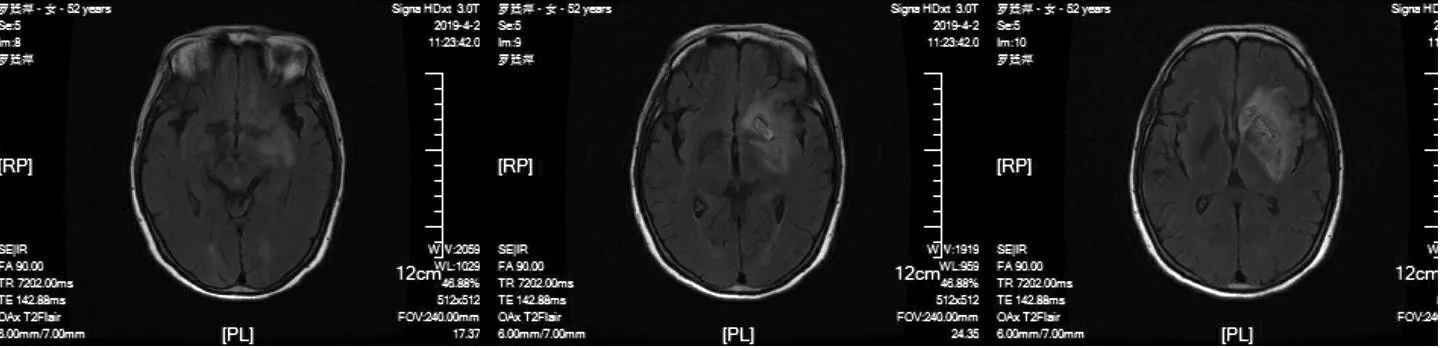
圖2c 病灶呈FLAIR 高信號

圖2d 病灶呈DWI 和ADC 高信號
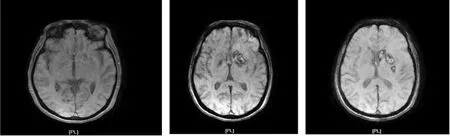
圖3 CT 顯示的皮層線樣高信號在SWI 上呈等信號
2.2 預后
3 例患者均存活,發病后3 個月改良Rankin評分(modified Rankin scale,mRS) 評分分別為4分、5 分、5 分。
3 討論
大腦中動脈為腦卒中最易受累血管,2 例病例患者有大動脈粥樣硬化的危險因素,后期CTA 檢查也證實存在大腦中動脈重度狹窄或閉塞,另1例病例CTA 檢查未見大血管狹窄、同時存在顱內出血轉化,心臟超聲證實存在風濕性心臟瓣膜病,24h 心電圖提示心房纖顫,腦梗死病因考慮為心源性。患者顱內出血轉化后并未增加美國國立衛生院卒中量表(National Institute of Health Stroke Scale,NIHSS)評分,不考慮為癥狀性顱內出血轉化。3例病例中在后期頭顱NCCT 隨訪中均提示CLN,表現為大腦中動脈供血區域出現特征性的T1WI 線狀或腦回狀高信號,后期影像學隨訪高信號未見消失。
大腦皮層六層中諸層對損害性刺激耐受性不同,以第3 層最敏感,其次為第5、6 層,而第2、4 層耐受性相對最佳。當腦皮質因梗死等發生缺血缺氧、能量供應異常時,大腦皮質第3 層最易損害發生CLN,尤以腦溝兩側及底部的皮質損害重于嵴部區域。CLN 病理上為受累區域的神經元、神經膠質及血管的彌漫性壞死,表現為神經元缺血改變、膠質增生及富脂肪巨噬細胞的層狀沉積[4]。影像學上CLN 主要應與以下疾病鑒別:腦淀粉樣血管病伴出血多累及表淺皮層動脈;蛛網膜下腔出血邊緣欠規則,周圍伴水腫等占位效應;MRI上還應與T1WI 高信號的高鐵血紅蛋白、脂肪瘤及皮樣囊腫等其他含脂質損傷、轉移性黑素瘤、不全鈣化、Fahr's 病、銅、錳異常沉積等疾病相鑒別[5]。大腦中動脈區域腦梗死伴發的CLN 重點需與出血性梗死相鑒別。綜上所述,認識大腦中動脈供血區較大面積腦梗死伴CLN 的MRI 表現特點對準確診斷具有重要意義。

