LncRNA TMPO-AS1調(diào)控miR-143-3p的表達(dá)影響肺癌細(xì)胞增殖、侵襲、遷移和凋亡
周斌鋒 彭兵鋒 王志強(qiáng) 喻國平 張小強(qiáng)
(1鷹潭市人民醫(yī)院心胸外科,江西 鷹潭 335000;2南昌大學(xué)附屬第二醫(yī)院胸外科)
肺癌是臨床常見惡性腫瘤之一,據(jù)調(diào)查研究顯示全世界范圍內(nèi)肺癌發(fā)病率持續(xù)升高,其中非小細(xì)胞肺癌是肺癌的主要病理類型,目前臨床常采用手術(shù)、化療等手段治療肺癌,但肺癌患者生存率仍未明顯升高〔1〕。近年來,免疫治療與分子靶向治療成為研究熱點(diǎn),因而深入探究肺癌發(fā)生的分子生物過程有助于尋找新的治療靶點(diǎn)以此提高患者生存率。長鏈非編碼RNA(LncRNA)TMPO-AS1可促進(jìn)非小細(xì)胞肺癌、前列腺癌等腫瘤發(fā)生及發(fā)展〔2,3〕。但TMPO-AS1在肺癌發(fā)生及發(fā)展過程中的分子機(jī)制尚未完全闡明。LncBase v.2網(wǎng)站預(yù)測顯示微小RNA-143-3p(miR-143-3p)可能是TMPO-AS1的靶基因,研究表明miR-143-3p在結(jié)腸癌、宮頸癌、喉部鱗狀細(xì)胞癌等惡性腫瘤中均呈低表達(dá),上調(diào)其表達(dá)可抑制腫瘤細(xì)胞增殖及轉(zhuǎn)移〔4~8〕。但TMPO-AS1是否可通過靶向miR-143-3p促進(jìn)肺癌發(fā)生及發(fā)展尚未可知。因此,本研究主要探討TMPO-AS1與miR-143-3p在肺癌細(xì)胞中的相互作用關(guān)系,初步分析其對肺癌細(xì)胞增殖、遷移、侵襲及凋亡的影響,為肺癌靶向治療提供潛在靶點(diǎn)。
1 材料與方法
1.1材料與試劑 BEAS-2B、肺癌細(xì)胞A549、SPC-A-1、H446、PC-9均購自美國ATCC細(xì)胞庫。DMEM培養(yǎng)基、胎牛血清、胰蛋白酶均購自美國Gibco公司;二甲基亞砜(DMSO)購自美國Sigma公司;Lipofectamine2000購自美國Invitrogen公司;Matrigel基質(zhì)膠購自美國BD公司;TMPO-AS1小干擾RNA(si-TMPO-AS1)、si-con、miR-143-3p mimics、miR-con、miR-143-3p抑制劑(anti-miR-143-3p)、anti-miR-con均購自上海吉瑪制藥技術(shù)有限公司;pcDNA3.1購自北京合生基因科技有限公司;Transwell小室購自美國Corning公司;MTT細(xì)胞增殖試劑盒購自美國Sigma公司;Annexin V-FITC/PI雙染法細(xì)胞凋亡檢測試劑盒購自北京寶賽生物技術(shù)有限公司;雙熒光素酶報(bào)告基因檢測試劑盒購自北京全式金生物技術(shù)有限公司;Trizol、反轉(zhuǎn)錄及qRT-PCR試劑盒均購自大連寶生物工程有限公司;兔抗人PCNA、基質(zhì)金屬蛋白酶(MMP)-2多克隆抗體均購自美國Santa Cruz公司;兔抗人酶切含半胱氨酸的天冬氨酸蛋白水解酶(caspase)-3抗體購自美國Abcam公司;辣根過氧化物酶(HRP)標(biāo)記的山羊抗兔IgG二抗購自武漢博士德生物工程有限公司。
1.2方法
1.2.1細(xì)胞轉(zhuǎn)染及分組 BEAS-2B細(xì)胞與肺癌細(xì)胞A549、SPC-A-1、H446、PC-9均培養(yǎng)于含有10%胎牛血清及青霉素-鏈霉素混合溶液的DMEM培養(yǎng)基,置于37℃、5%CO2培養(yǎng)箱內(nèi)培養(yǎng),待細(xì)胞生長至80%左右時(shí)進(jìn)行傳代培養(yǎng),取對數(shù)生長期肺癌SPC-A-1、H446細(xì)胞,0.25%胰蛋白酶消化細(xì)胞,制備細(xì)胞懸液,接種于6孔板,置于37℃、5%CO2培養(yǎng)箱內(nèi)繼續(xù)培養(yǎng),待細(xì)胞生長融合至50%時(shí),參照Lipofectamine2000試劑說明書進(jìn)行轉(zhuǎn)染,轉(zhuǎn)染前更換為Opti-MEM減血清培養(yǎng)基,實(shí)驗(yàn)將肺癌SPC-A-1、H446細(xì)胞隨機(jī)分為si-con組(si-con分別轉(zhuǎn)染入SPC-A-1、H446細(xì)胞)、si-TMPO-AS1組(si-TMPO-AS1分別轉(zhuǎn)染入SPC-A-1、H446細(xì)胞)、miR-con組(miR-con分別轉(zhuǎn)染入SPC-A-1、H446細(xì)胞)、miR-143-3p組(miR-143-3p mimics分別轉(zhuǎn)染入SPC-A-1、H446細(xì)胞)、si-TMPO-AS1 +anti-miR-con組(si-TMPO-AS1與anti-miR-con分別共轉(zhuǎn)染入SPC-A-1、H446細(xì)胞)、si-TMPO-AS1 +anti-miR-143-3p組(si-TMPO-AS1 與anti-miR-143-3p分別共轉(zhuǎn)染入SPC-A-1、H446細(xì)胞),各組細(xì)胞轉(zhuǎn)染6 h后更換為含有10%胎牛血清及青霉素-鏈霉素混合溶液的DMEM培養(yǎng)基繼續(xù)培養(yǎng)48 h,收集對數(shù)生長期細(xì)胞進(jìn)行后續(xù)功能驗(yàn)證。
1.2.2qRT-PCR檢測細(xì)胞中TMPO-AS1、miR-143-3p表達(dá)水平 采用Trizol法提取細(xì)胞總RNA,應(yīng)用NanoDrop2000分光光度計(jì)檢測RNA濃度,取2μg RNA參照反轉(zhuǎn)錄試劑盒說明書將其反轉(zhuǎn)錄為cDNA,qRT-PCR檢測TMPO-AS1、miR-143-3p的表達(dá)水平,反應(yīng)體系:2×SuperReal PreMix Plus 10 μl,上下游引物各1 μl,cDNA模板2 μl,ddH2O補(bǔ)足體系至20 μl;反應(yīng)條件:95℃ 2 min(循環(huán)1次),95℃ 30 s,60℃30 s,72℃ 30 s(循環(huán)40次),檢測miR-143-3p表達(dá)時(shí)以U6為內(nèi)參,TMPO-AS1以β-actin為內(nèi)參,采用2-ΔΔCt法計(jì)算TMPO-AS1、miR-143-3p相對表達(dá)量。
1.2.3噻唑藍(lán)(MTT)檢測細(xì)胞增殖 轉(zhuǎn)染后各組肺癌SPC-A-1、H446細(xì)胞按照每孔5 ×103個(gè)細(xì)胞的密度接種于96孔板,同時(shí)設(shè)置空白孔(培養(yǎng)液、無細(xì)胞),每孔加入20 μl MTT溶液(5 mg/ml),繼續(xù)培養(yǎng)4 h,棄培養(yǎng)液,每孔加入150 μl DMSO,低速振蕩,充分混勻,應(yīng)用酶標(biāo)儀檢測波長為490 nm處各孔吸光度值(OD),計(jì)算細(xì)胞存活率,細(xì)胞存活率(%)=〔(實(shí)驗(yàn)組OD值-空白對照組OD值)/(正常培養(yǎng)組OD值-空白對照OD值)〕×100%。
1.2.4克隆形成實(shí)驗(yàn) 收集各組肺癌SPC-A-1、H446細(xì)胞,用胰蛋白酶消化細(xì)胞,4℃,1 000 r/min轉(zhuǎn)速離心3 min(離心半徑12 cm),棄上清,加入無菌磷酸鹽緩沖液(PBS)5 ml,洗滌細(xì)胞沉淀,相同條件下再次離心,反復(fù)洗滌3次,加入培養(yǎng)基,制備單細(xì)胞懸液,調(diào)整細(xì)胞濃度為1×103個(gè)/ml,單細(xì)胞懸液接種于6孔板進(jìn)行克隆形成培養(yǎng),每3 d更換一次培養(yǎng),繼續(xù)培養(yǎng)14 d后觀察細(xì)胞克隆形成情況,實(shí)驗(yàn)設(shè)置3次重復(fù)。
1.2.5流式細(xì)胞術(shù)檢測細(xì)胞凋亡 分別收集各組肺癌SPC-A-1、H446細(xì)胞,胰蛋白酶消化細(xì)胞,4℃,1 000 r/min轉(zhuǎn)速離心5 min,棄上清,加入預(yù)冷PBS洗滌2次,每次5 min,棄上清,渦旋振蕩30 s,制備細(xì)胞懸浮液,加入200 μl結(jié)合緩沖液,再加入10 μl Annexin V-FITC。振蕩混勻,冰上避光孵育30 min,加入5 μl PI,渦旋振蕩混勻,冰上孵育5 min,加入400 μl結(jié)合緩沖液,渦旋振蕩混勻,使用300目尼龍網(wǎng)過濾,于1 h內(nèi)應(yīng)用流式細(xì)胞儀檢測各組細(xì)胞凋亡情況。
1.2.6Transwell實(shí)驗(yàn)檢測細(xì)胞遷移及侵襲 細(xì)胞侵襲實(shí)驗(yàn):肺癌SPC-A-1、H446細(xì)胞培養(yǎng)于含有0.1%胎牛血清的DMEM培養(yǎng)基,培養(yǎng)24 h后,用不含胎牛血清的DMEM培養(yǎng)基重懸細(xì)胞,取2×105個(gè)細(xì)胞接種于含有基質(zhì)膠的Transwell小室上室中(直徑6.5 μm,孔徑8 μm),取500 μl含有10%胎牛血清的DMEM培養(yǎng)基置于Transwell小室的下腔中,置于37℃、體積分?jǐn)?shù)5%CO2培養(yǎng)箱機(jī)修培養(yǎng)24 h,去除上膜表面上的細(xì)胞,用多聚甲醛固定20 min,0.5%結(jié)晶紫染色液染色10 min,無菌水清洗后置于倒置顯微鏡下隨機(jī)選取10個(gè)視野計(jì)數(shù)。細(xì)胞遷移實(shí)驗(yàn):用不含胎牛血清的DMEM培養(yǎng)基重懸細(xì)胞,取2×105個(gè)細(xì)胞接種于Transwell小室上室中,其余實(shí)驗(yàn)步驟同細(xì)胞侵襲實(shí)驗(yàn),實(shí)驗(yàn)均設(shè)置3次生物學(xué)重復(fù)。
1.2.7雙熒光素酶報(bào)告基因檢測 構(gòu)建TMPO-AS1攜帶的3′UTR的熒光素酶報(bào)告因子,每個(gè)基因的結(jié)合位點(diǎn)與miR-143-3p結(jié)合位點(diǎn)相對應(yīng),熒光素酶測定顯示TMPO-AS1與miR-143-3p存在結(jié)合位點(diǎn),將結(jié)合位點(diǎn)與突變位點(diǎn)分別載入熒光素酶報(bào)告基因載體,分別為野生型WT-TMPO-AS1、突變型MUT-TMPO-AS1,WT-TMPO-AS1、MUT-TMPO-AS1分別與miR-143-3p mimics、miR-con分別共轉(zhuǎn)染入肺癌SPC-A-1、H446細(xì)胞,繼續(xù)培養(yǎng)24 h,應(yīng)用雙熒光素酶報(bào)告基因測定系統(tǒng)檢測熒光素酶活性,實(shí)驗(yàn)重復(fù)3次。
1.2.8Western印跡檢測PCNA、MMP-2、酶切caspase-3蛋白表達(dá) 分別取各組肺癌SPC-A-1、H446細(xì)胞,加入蛋白裂解液,冰上裂解30 min,12 000 r/min轉(zhuǎn)速離心10 min(離心半徑6 cm)提取細(xì)胞總蛋白,采用BCA法測定蛋白濃度,蛋白煮沸變性,取變性完成蛋白樣品30 μg/孔加入十二烷基硫酸鈉-聚丙烯酰胺凝膠電泳(SDS-PAGE)的加樣孔內(nèi),經(jīng)SDS-PAGE分離蛋白,轉(zhuǎn)移至聚偏氟乙烯(PVDF)膜,5%脫脂奶粉封閉1 h,加入一抗(1∶1 000),4℃輕搖24 h,TBST洗膜3次,每次5 min,加入二抗(1∶3 000),室溫孵育2 h,TBST洗膜3次,每次10 min,避光加入ECL顯色液,曝光,顯影,凝膠分析系統(tǒng)及ImageJ軟件分析條帶灰度值。
1.3統(tǒng)計(jì)學(xué)方法 應(yīng)用SPSS21.0軟件進(jìn)行t檢驗(yàn)、單因素方差分析。
2 結(jié) 果
2.1TMPO-AS1和 miR-143-3p在肺癌細(xì)胞中的表達(dá) 與BEAS-2B相比,肺癌細(xì)胞A549、SPC-A-1、H446、PC-9中TMPO-AS1的表達(dá)水平均顯著升高(P<0.05),而肺癌細(xì)胞A549、SPC-A-1、H446、PC-9中 miR-143-3p的表達(dá)水平均顯著降低(P<0.05),見表1。其中肺癌SPC-A-1、H446細(xì)胞中TMPO-AS1的表達(dá)水平相比于其他肺癌細(xì)胞系明顯升高(均P<0.05),因而本研究選取肺癌SPC-A-1、H446細(xì)胞進(jìn)行后續(xù)實(shí)驗(yàn)。
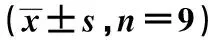
表1 檢測肺癌細(xì)胞中TMPO-AS1和 miR-143-3p表達(dá)
2.2沉默TMPO-AS1或過表達(dá) miR-143-3p對肺癌細(xì)胞增殖的影響 與si-con組相比,si-TMPO-AS1組肺癌SPC-A-1、H446細(xì)胞存活率及克隆形成率顯著降低(P<0.05),PCNA蛋白的表達(dá)水平顯著降低(P<0.05);相較于miR-con組,miR-143-3p組肺癌SPC-A-1、H446細(xì)胞存活率、克隆形成率與PCNA蛋白的表達(dá)水平均顯著下降(P<0.05),見圖1、表2。

圖1 檢測肺癌細(xì)胞中PCNA蛋白表達(dá)

2.3沉默TMPO-AS1或過表達(dá) miR-143-3p對肺癌細(xì)胞凋亡的影響 流式細(xì)胞術(shù)檢測結(jié)果顯示,si-TMPO-AS1組肺癌SPC-A-1、H446細(xì)胞凋亡率均顯著高于si-con組(均P<0.05),酶切caspase-3表達(dá)水平均顯著升高(均P<0.05);相較于miR-con組,miR-143-3p組肺癌SPC-A-1、H446細(xì)胞凋亡數(shù)顯著增多(均P<0.05),酶切caspase-3的表達(dá)均上調(diào)(均P<0.05),見圖2、表3。

圖2 流式細(xì)胞術(shù)檢測細(xì)胞凋亡和Western印跡檢測肺癌細(xì)胞中酶切caspase-3蛋白表達(dá)

2.4沉默TMPO-AS1或過表達(dá) miR-143-3p對肺癌細(xì)胞遷移和侵襲的影響 肺癌SPC-A-1、H446細(xì)胞中沉默TMPO-AS1或 miR-143-3p過表達(dá)后,與si-con組比較,si-TMPO-AS1組細(xì)胞遷移及侵襲均數(shù)顯著減少(均P<0.05),MMP-2蛋白的表達(dá)水平顯著降低(P<0.05);與miR-con組比較,miR-143-3p組細(xì)胞遷移及侵襲數(shù)顯著減少(P<0.05),MMP-2蛋白的表達(dá)水平顯著降低(P<0.05),見圖3、圖4、表4。

圖3 Transwell檢測肺癌細(xì)胞遷移和侵襲(結(jié)晶紫染色,×200)

圖4 Western印跡檢測各組MMP-2表達(dá)

2.5TMPO-AS1靶向調(diào)控 miR-143-3p的表達(dá) LncBase v.2網(wǎng)站預(yù)測顯示TMPO-AS1與 miR-143-3p存在互補(bǔ)靶向序列,見圖5。雙熒光素酶報(bào)告實(shí)驗(yàn)結(jié)果顯示,肺癌SPC-A-1、H446細(xì)胞中轉(zhuǎn)染克隆有TMPO-AS1-3′UTR突變型載體質(zhì)粒實(shí)驗(yàn)中,miR-143-3p組與miR-con組比較,熒光素酶活性差異無顯著性;轉(zhuǎn)染克隆有TMPO-AS1-3′UTR載體質(zhì)粒實(shí)驗(yàn)中,miR-143-3p組熒光素酶活性明顯受到抑制,與miR-con組比較,熒光素酶活性差異具有顯著性(P<0.05),見表5。

圖5 TMPO-AS1與 miR-143-3p存在互補(bǔ)靶向序列
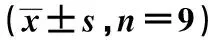
表5 雙熒光素酶報(bào)告實(shí)驗(yàn)
qRT-PCR檢測結(jié)果顯示,si-TMPO-AS1組肺癌SPC-A-1、H446細(xì)胞中miR-143-3p的表達(dá)水平顯著高于si-con組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),pcDNA-TMPO-AS1組肺癌SPC-A-1、H446細(xì)胞中miR-143-3p的表達(dá)水平顯著低于pcDNA組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見表6。
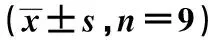
表6 LncRNA TMPO-AS1調(diào)控 miR-143-3p的表達(dá)
2.6干擾 miR-143-3p表達(dá)逆轉(zhuǎn)沉默TMPO-AS1對肺癌細(xì)胞的抑制作用 相較于si-TMPO-AS1+anti-miR-con組,si-TMPO-AS1+anti-miR-143-3p組肺癌SPC-A-1、H446細(xì)胞存活率與克隆形成率均顯著升高,差異有統(tǒng)計(jì)學(xué)意義(均P<0.05),遷移細(xì)胞數(shù)與侵襲細(xì)胞數(shù)均顯著增加,差異有統(tǒng)計(jì)學(xué)意義(均P<0.05),細(xì)胞凋亡率顯著降低,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),PCNA、MMP-2蛋白的表達(dá)水平均顯著升高,差異有統(tǒng)計(jì)學(xué)意義(均P<0.05),而酶切caspase-3蛋白的表達(dá)水平顯著降低,差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見圖6、表7、表8。

1~4:si-con組、si-TMPO-AS1組、si-TMPOAS1+anti-miR-con組、si-TMPOAS1+anti-miR-143-3p組圖6 Western印跡檢測肺癌細(xì)胞中酶切caspase-3、PCNA和MMP-2蛋白表達(dá)


3 討 論
大部分肺癌患者確診時(shí)已處于中晚期,經(jīng)臨床治療后患者預(yù)后較差〔9〕。因而急需尋找早期診斷及監(jiān)測肺癌的新方法。研究表明LncRNA可能通過調(diào)控miRNA而參與肺癌發(fā)生及發(fā)展過程〔10,11〕。但仍有部分LncRNA-miRNA在肺癌發(fā)生過程中的作用機(jī)制尚未完全闡明。本研究深入分析TMPO-AS1與miR-143-3p在肺癌發(fā)生發(fā)展過程中的可能作用機(jī)制。
TMPO-AS1在肺腺癌患者血清中呈高表達(dá),其高表達(dá)量與患者預(yù)后不良密切相關(guān),研究表明TMPO-AS1還可能競爭性吸附miRNA而參與肺腺癌發(fā)生發(fā)展過程〔12,13〕。本研究結(jié)果提示TMPO-AS1表達(dá)水平升高可能促進(jìn)肺癌的發(fā)生,沉默TMPO-AS1表達(dá)可顯著降低肺癌細(xì)胞增殖、遷移及侵襲能力,誘導(dǎo)細(xì)胞凋亡。研究表明PCNA可反映腫瘤細(xì)胞增殖,其表達(dá)水平升高預(yù)示細(xì)胞增殖能力增強(qiáng),MMP-2過表達(dá)可增強(qiáng)腫瘤細(xì)胞遷移及侵襲能力,酶切caspase-3蛋白是細(xì)胞凋亡發(fā)生過程中的關(guān)鍵因子,其表達(dá)量升高預(yù)示凋亡細(xì)胞數(shù)增加〔14~16〕。本研究結(jié)果提示沉默TMPO-AS1表達(dá)可通過上調(diào)Cleaved caspase-3蛋白表達(dá)及下調(diào)PCNA、MMP-2蛋白表達(dá)而促進(jìn)肺癌細(xì)胞凋亡,抑制細(xì)胞增殖、遷移及侵襲。
miR-143-3p在乳腺癌細(xì)胞中呈低表達(dá),miR-143-3p過表達(dá)可通過靶向LIM結(jié)構(gòu)域激酶1的表達(dá)而抑制乳腺癌發(fā)生及發(fā)展〔17〕。研究表明miR-142-3p通過靶向CDC25C,TGFβR1,GNAQ,WASL、RAC1抑制黑色素瘤惡性進(jìn)展〔18〕。與上述研究結(jié)果相似,本研究結(jié)果表明miR-143-3p在肺癌細(xì)胞中的表達(dá)水平顯著降低,miR-143-3p過表達(dá)與沉默TMPO-AS1后對肺癌細(xì)胞增殖、遷移、侵襲及凋亡的作用效果相同,同時(shí)本研究通過雙熒光素酶報(bào)告實(shí)驗(yàn)及qRT-PCR實(shí)驗(yàn)證明TMPO-AS1可靶向負(fù)性調(diào)控miR-143-3p的表達(dá),提示TMPO-AS1可能靶向抑制miR-143-3p表達(dá)而促進(jìn)肺癌細(xì)胞增殖、遷移、侵襲,抑制細(xì)胞凋亡。本研究結(jié)果提示沉默TMPO-AS1表達(dá)可通過上調(diào)miR-143-3p表達(dá)而減弱肺癌細(xì)胞增殖、遷移、侵襲能力,促進(jìn)細(xì)胞凋亡。
綜上,TMPO-AS1可調(diào)控miR-143-3p的表達(dá)影響肺癌細(xì)胞增殖、遷移、侵襲及凋亡,為揭示肺癌發(fā)生的分子機(jī)制奠定理論基礎(chǔ),可為肺癌的靶向治療提供新的靶點(diǎn)。

