IL-10及相關促炎因子與冠心病伴代謝綜合征患者冠狀動脈病變程度的關系
楊鳴宇, 李康榮, 何航宇
化州市人民醫院心血管內科(廣東茂名 525100)
代謝綜合征(metabolic syndrome,MetS)是一組心臟代謝風險因素,有助于加速動脈粥樣硬化的發展,導致冠心病(coronary heart disease,CHD)[1]。目前,動脈粥樣硬化的過程被認為是一種慢性炎癥性疾病,其中具體機制包括由發炎的內皮表達黏附分子和白細胞向內膜的遷移,同時吸附膽固醇、修飾的脂蛋白顆粒及負載脂質的巨噬細胞以形成動脈粥樣硬化[2]。白細胞介素(IL)-10是主要由巨噬細胞和Th2淋巴細胞產生的抗炎細胞因子。近年來,有證據[3]表明IL-10在多方面發揮其抗炎作用,包括抑制泡沫細胞活性改變等細胞的脂質代謝,以及降低金屬蛋白酶基質、親炎性細胞因子和環氧合酶-2的表達。它還在動脈粥樣硬化的不同階段的斑塊發展期間發揮抗動脈粥樣硬化作用,一旦動脈粥樣化形成通過將單核細胞募集到內膜中,隨后是將募集的單核細胞分化為巨噬細胞進行炎癥激活。內膜層中的巨噬細胞被摻入ox-LDL微粒,從而促進膽固醇轉運和斑塊核心中泡沫細胞的形成[4]。最近的證據[5]表明,即使存在炎癥狀態,IL-10的增加也是抗心血管疾病的重要保護因素。然而,關于CHD伴MetS患者中IL-10的表達水平以及其與嚴重缺血性心臟病發生的關系仍未明確。由于高水平的IL-10可以轉化抗炎作用,因此IL-10的表達水平可能與CHD患者獲得更好的預后相關,但仍需要進一步通過臨床數據驗證。因此,本研究旨在分析患者的血清IL-10以及其他促炎細胞因子,如TNF-α、IL-6、IL-18、IL-12和IL-1β的表達水平,探討IL-10與其他相關促炎細胞因子與CAD伴MetS患者病情嚴重程度的關系。
1 資料與方法
1.1 一般資料 選擇2018年1月至2019年4月因CHD于我院住院的患者共90例。
納入標準:(1)符合CHD的診斷標準,具體診斷標準參考《穩定性冠心病診斷與治療指南》[6];(2)合并或不合并MetS,具體MetS的診斷標準參考合《中華醫學會糖尿病學分會關于代謝綜合征的建議》[7]:至少具備以下4項的3項即可診斷為MetS:①超重和(或)肥胖[體質指數(BMI)≥25 kg/m2];②合并高血壓或既往已確診為高血壓并正在接受治療;③高血糖(空腹血糖≥6.1 mmol/L,餐后2 h血糖≥7.8 mmol/L或既往已確診為糖尿病且接受治療);④血脂紊亂:血三酰甘油≥1.7 mmol/L,和(或)HDL-C<0.9 mmol/L(男性)或<1.0 mmol/L(女性);(3)行冠狀動脈造影;(4)預計生存時間>3個月;(5)年齡45~80歲;(6)男女不限;(7)簽署知情同意書。
排除標準:(1)合并免疫系統相關疾病,獲得性免疫缺陷綜合征;(2)合并甲狀腺功能減退、痛風、敗血癥;(3)嚴重肝腎功能不全;(4)合并惡性腫瘤;(5)類風濕性關節炎或其他免疫系統疾病。
90例CHD患者合并MetS的共52例(MetS組),未合并MetS的共38例(非MetS組),另外選擇40例健康體檢者作為對照組。
1.2 檢測指標
1.2.1 樣本收集 所有參與者清晨抽取靜脈血5 mL,通過4℃條件下3 000 r/min離心后,取上清存于-80℃備測。
1.2.2 炎性指標及生化指標檢測 采用微量樣本多重蛋白定量技術測定相關的炎性指標,通過Cytometric Bead Array Kit-CBA(BD Biosciences)試劑盒測量,通過流式細胞儀(FACSCanto Ⅱ)分析血清IL-10、IL-6、IL-8、IL-1β、IL-18、腫瘤壞死因子-α(TNF-α)和IL-12的表達水平,具體操作嚴格按照說明書進行。同時采用全自動生化分析儀(貝克曼庫爾特AU480)檢測血清膽固醇、三酰甘油和葡萄糖水平。以上檢測由本院檢驗科人員完成。
1.2.3 冠狀動脈造影及評定方法 按照judkin法標準操作進行冠狀動脈造影,冠狀動脈前降支、回旋支、右冠狀動脈中至少有一支狹窄≥50%診斷為CHD。具體造影的結果至少由兩名具有經驗的醫生進行評定,采用冠脈Gensini評分評定冠狀動脈的嚴重程度,根據美國心臟病協會(AHA)標準將冠狀動脈分為15個分段,通過評估不同分段的冠脈Gensini評分×評分系數得到各段Gensini積分之和為最后心臟病情嚴重程度的得分。

2 結果
2.1 納入對象的一般資料對比 3組納入研究患者的性別比例和年齡對比差異無統計學意義(P>0.05),其中MetS組的BMI水平顯著高于非MetS組和對照組,而非MetS組顯著高于對照組,差異有統計學意義(P<0.05)。MetS組糖尿病和高血壓的比例顯著高于非MetS組,差異有統計學意義(P<0.05)。見表1。
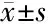
表1 3組患者一般資料對比
2.2 3組的生化指標及心臟Gensini評分對比 MetS組的膽固醇、三酰甘油、LDL-C和血糖水平均顯著高于非MetS組和對照組(P<0.05),HDL-C水平顯著低于非MetS組和對照組,差異有統計學意義(P<0.05)。其中MetS組的Gensini評分顯著高于非MetS組,差異有統計學意義(P<0.01)。見表2。
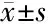
表2 3組的生化指標及心臟Gensini評分對比
2.3 3組血清相關炎癥因子水平對比 3組患者的IL-10、IL-6、IL-8、IL-1β、IL-18、TNF-α和IL-12水平對比差異均有統計學意義(P<0.05),其中MetS組和非MetS組的IL-10、IL-6、IL-8、IL-1β、IL-18、TNF-α和IL-12水平均顯著高于對照組(P<0.05),MetS組的IL-10水平顯著低于非MetS組,MetS組的TNF-α和IL-12水平顯著高于非MetS組,差異有統計學意義(P<0.05)。見表3。

表3 3組的血清相關炎癥因子比較
2.4 相關炎癥因子水平與Gensini評分的相關性分析 90例CHD患者、MetS組和非MetS組患者IL-10水平與Gensini評分呈顯著負相關(P<0.05),且MetS組的相關系數最高(r=-0.574,P<0.001),血清IL-6、IL-8、IL-1β、IL-18、TNF-α和IL-12水平與CHD患者、MetS組和非MetS組患者的Gensini評分均沒有顯著相關性(P>0.05),見表4。

表4 3組的血清相關炎癥因子與Gensini評分的相關性
3 討論
MetS是一種多因素疾病,可引發肥胖并導致與慢性低度炎癥相關的全身氧化應激。這種情況導致內皮功能障礙,脂質代謝改變并影響胰島素敏感性[8]。MetS產生的炎癥和肥胖及代謝異常同時也影響了心臟代謝風險因子的發展和進展。動脈粥樣硬化的病理過程不僅來自脂質的積累,還來自內皮功能障礙和炎癥系統的激活[8]。由于炎癥和血栓形成是動脈粥樣硬化發展的重要病因,因此炎癥標志物的檢測是評估CHD疾病風險和預后的重要標記物。但對于相關炎癥因子與CHD合并MetS患者病情的關系仍缺乏評估。本研究首次通過檢測CHD患者血清促炎因子IL-8、IL-12、TNF-α、IL-6、IL-1β、IL-18和抗炎因子IL-10的表達水平,并分析其與冠心病患者病情的關系。本研究結果表明,IL-10在CHD合并MetS患者中與心臟病情嚴重程度呈顯著的負相關,表明CHD合并MetS患者IL-10的表達水平病情進展具有保護作用。
近年來心血管疾病的研究均表明IL-10是重要的抗炎細胞因子,本研究則進一步明確了IL-10可能在CHD合并MetS患者的病理生理學中起著重要的保護作用。IL-10具有多種抗動脈粥樣硬化特性,其具體發揮作用的機制包括抑制巨噬細胞/單核細胞的內皮浸潤,抑制核因子-κB(NF-κB)活化[9],同時IL-10能抑制許多促炎分子信號的表達,導致基質金屬蛋白酶的產生減少。其也能抑制組織因子和環氧合酶-2的表達,最后抑制細胞死亡和凋亡[10]。在本研究中,CHD合并MetS的患者中較低的IL-10水平與較高的冠狀動脈狹窄程度相關,同時根據其他促炎因子也在CHD患者中高表達,表明即使存在較高水平的促炎細胞因子,IL-10也具有抗炎活性。既往研究[11]報告表明低水平的IL-10與未來心血管事件的風險增加有關,而本研究則明確了IL-10在CHD合并MetS中的保護作用。
本研究也同時檢測血清促炎因子IL-8、IL-12、TNF-α、IL-6、IL-1β、IL-18在CHD患者中的表達水平。有證據[12]表明,升高的血漿IL-8與健康個體發生CHD風險有關。IL-8在單核細胞遷移到內皮下空間中起著關鍵作用,這是動脈粥樣硬化初期階段的關鍵過程[13]。在這項研究中,對照組相比,CHD合并或不合并MetS患者的IL-8均顯著增加,但其在這群病例中與冠狀動脈狹窄程度并沒有顯著的相關性。本研究也發現CHD合并MetS的患者組其IL-12和TNF-α水平顯著高于非MetS患者,由于IL-12是一種能夠在T細胞和NK細胞中誘導γ干擾素(IFN-γ)合成的細胞因子,IL-12和TNF-α之間存在強烈的相關性[14]。IFN-γ是活化巨噬細胞釋放TNF-α的關鍵介質,研究表明,在肥胖患者中,當存在高脂肪飲食時,存在促炎性TH1細胞和巨噬細胞的活化,隨后產生IFN-γ、TNF-α和IL-12[15]。TNF-α是一種有效的細胞因子,在肥胖個體中主要誘導IL-6的產生,TNF-α水平升高與急性心肌梗死風險增加有關[16]。雖然許多白細胞介素如IL-4、IL-5、IL-12、IL-13在合并MetS時表達增加,但IL-6、IL-12和TNF-α與CHD合并MetS患者的心臟冠脈狹窄程度沒有顯著的相關性。Nod樣受體(Nod-like receptor,NLR)家族的先天免疫細胞傳感器,如NLRP3炎性體是導致caspase-1活化和隨后的IL-1β和IL-18分泌的重要因素[17]。IL-1β是心肌梗死中炎癥反應早期的重要介質。我們的結果顯示血清IL-1β和IL-18水平在CHD合并MetS或非MetS組之間沒有顯著差異,證明NLRP3炎性體可能不參與MetS患者的心血管病變。
本研究存在一定的局限性,包括每組受試者納入數量有限。此外,盡管各組之間的基礎疾病存在差異,因此在藥物服用方面可能存在差異,因此仍需要進一步加大樣本量和增加隨訪時間以評估。綜合上述,本研究的數據表明CHD合并MetS患者的IL-10水平升高與病情嚴重程度呈負相關,即使存在較高水平的促炎細胞因子,也表明其具有抗炎活性的保護作用。

