可注射硫酸鈣與聚甲基丙烯酸甲酯混合的骨水泥在骨質疏松性椎體壓縮性骨折經皮椎體成形術中的應用*
陳志光, 孫素和, 顏光宇, 曾坤青, 劉悅, 關開枝, 林淮, 王剛
廣州市天河區人民醫院 1外二科, 2中醫科(廣東廣州 510660)
隨著我國步入老齡化階段,骨質疏松患者逐漸增多,預估到2050年,我國骨質疏松患者將達到5.33億[1]。骨質疏松所致的骨折最常見的部位是脊柱,其中胸腰段椎體骨折發生率最高,約達50%[2]。骨質疏松性椎體壓縮性骨折(steoporotic vertebral compression fractures, OVCF)常引起急性或慢性胸腰背部疼痛,活動明顯受限,嚴重者可導致脊髓神經損傷,甚至截癱[3]。近年來,椎體強化術包含經皮椎體成形術(percutaneous vertebroplasty, PVP)和經皮后凸椎體成形術(percutaneous kyphoplasty, PKP)被廣泛應用于臨床來治療 OVCFs,因其微創、快速、有效緩解疼痛的優點已成為治療OVCFs的經典手術方法[4]。椎體強化術傳統常用的椎體填充物有聚甲基丙烯酸甲酯 (polymethylmethacrylate,PMMA) 骨水泥、硫酸鈣、磷酸鈣等、其中PMMA臨床應用最早且最廣泛,臨床療效確切、但是骨水泥滲漏是PMMA應用最常見的并發癥,有文獻報道其發生率為:PVP 41%、PKP 9%,嚴重的滲漏可能導致肺栓塞、神經損傷等災難性并發癥[5]。磷酸鈣及硫酸鈣屬于新型椎體填充物具有骨誘導、可吸收等優點,常被用于骨缺損等治療,但是因其體內吸收過程不可控、可注射性差、機械剛度差等因素限制了其在椎體壓縮性骨折中的應用[6]。所以目前這兩類椎體填充物均不能完美達到臨床應用的最理想的要求。因此,在施行椎體成形術治療OVCFs的過程中,如何在保證臨床療效的同時又能有效減少骨水泥滲漏已成為臨床醫生關注和探索的焦點。2019年1月至2020年6月間我科采用新型生物材料可注射性硫酸鈣與PMMA制備成混合骨水泥結合PVP治療骨質疏松性胸腰椎椎體壓縮性骨折,并與傳統單用PMMA的PVP進行比較,探索硫酸鈣與PMMA制備的混合骨水泥的療效與可靠性。
1 資料與方法
1.1 一般資料 選擇于2019年1月至2020年6月在廣州市天河區人民醫院外二科住院治療的骨質疏松性胸腰椎壓縮性骨折患者,依據納入及排除標準納入患者65 例,觀察組34例,其中男9例,女25例,平均年齡(69.35±10.55)歲;對照組31例,其中男7例,女24例,年齡(68.54±11.34)歲。兩組一般資料差異無統計學意義(P>0.05)。均為單一椎體骨折,術前均無脊髓和神經根受損癥狀,影像學檢查示椎體壓縮骨折,后凸畸形,骨小梁稀疏,椎體后壁無破壞,骨密度檢查均提示骨質疏松。術前排除患者均無凝血機制障礙及出血體質,無碘過敏史等手術禁忌證。所有患者均簽署知情同意書,手術由同一組醫師完成。
納入標準:(1)OVCF的患者,體格檢查陽性表現、臨床表現與影像學提示一致;(2)骨折到手術時間間隔≤2周;(3)X線片提示只存在單一椎體壓縮, MRI 提示為新鮮的單一椎體骨折。
排除標準:(1)繼發性骨質疏松癥患者;(2)影像學檢查提示存在骨折塊突入椎管壓迫脊髓或者患者本身有神經癥狀;(3)腫瘤等導致的病理性椎體骨折;(4)既往接受過椎體強化術及其他脊柱手術;(5)多節段連續或不連續的骨折;(6)凝血功能異常、心肺功能較差不能耐受手術和麻醉者;(7)其他原因無法接受手術者。
1.2 手術方法 為減少誤差,所有手術均由同一名高年資副主任醫師完成。整個手術過程需在局麻及C型臂X線機透視下進行。患者取俯臥位,局麻后,墊高胸部及髂部,對骨折椎體行體位復位,均選擇PVP術式,透視定位傷椎椎弓根體表投影并選取穿刺點(常規穿刺方法:穿刺點位于正位透視椎弓根投影外上緣)。選取適當角度經椎弓根穿刺,適當調整角度直至X線透視見:正位像針尖至中線位置,側位像針尖達椎體前1/3。調制骨水泥,待骨水泥凝固到抽絲期,在透視監測下少量多次注入適量體積的骨水泥并做好記錄,對照組選擇PMMA作為椎體填充物,觀察組選擇可注射硫酸鈣與PMMA按1∶3體積比制備的混合骨水泥作為椎體填充物。骨水泥注入完成后,留置通道數分鐘待骨水泥凝固再拔除通道(圖1)。術后要求患者平臥3 h,觀察如無特殊不適,術后第1天佩戴腰圍下地活動,出院時囑患者門診接受正規抗骨質疏松治療,定期門診隨診。此外,所有患者出院前均復查X線片。
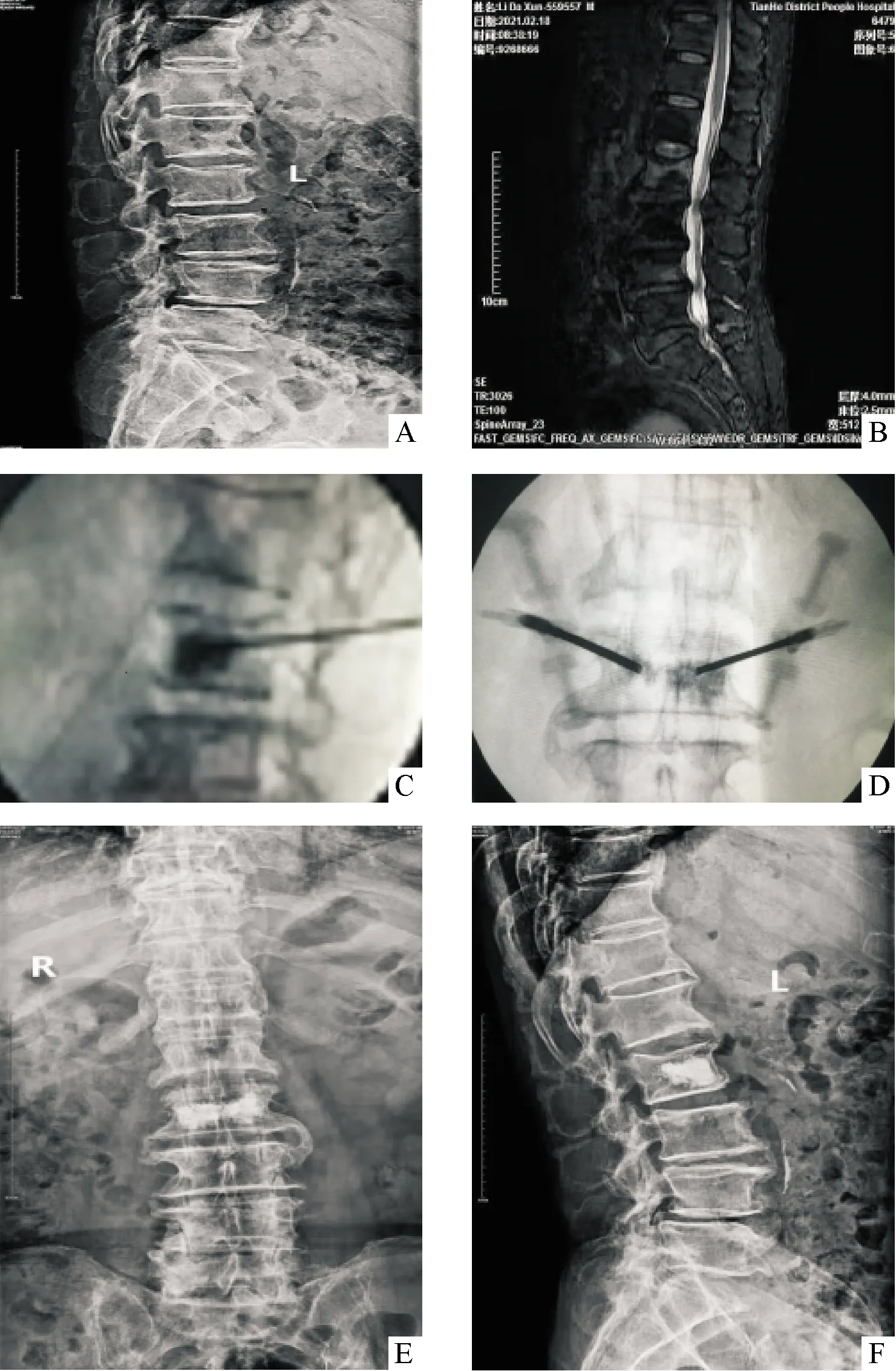
注:A、B:術前影像,提示L2椎體新鮮壓縮性骨折;C、D:術中用硫酸鈣與PMMA混合后經椎體穿刺針注入至L2椎體內,見骨水泥均勻分布在椎體內,無滲漏;E、F:術后復查的正側位X線圖1 硫酸鈣與PMMA混合的骨水泥在PVP術式中的應用相關影像
1.3 評價指標 記錄患者性別、年齡。行X線片、MRI或CT檢查。記錄骨折椎體節段、手術時間、注入骨水泥量、椎體填充物凝固時間、術前及術后1 d及3、6、12個月的VAS評分。閱讀術后1 d及3、6、12個月的X線片,與術前片進行比較,觀察術后椎體高度改善情況及骨水泥滲漏率。椎體高度改善情況,采用椎體前緣壓縮百分比作為評價指標,即測量患者病椎前緣及后緣高度,并將二者相減,所得值即為椎體前緣壓縮高度,再將椎體前緣壓縮高度除以椎體后緣高度即得椎體前緣壓縮百分比。
1.4 統計學方法 應用SPSS 22.0統計軟件,計數資料采用頻數表示,行2檢驗,計量資料以表示,行獨立樣本t檢驗;以P<0.05為差異有統計學意義。
2 結果
2.1 兩組患者術中指標比較 所有患者均較順利完成手術,術后均未出現血管栓塞、神經損傷、腹脹等不良反應。兩組在手術時間、術中出血量、骨水泥注入量差異無統計學意義(P>0.05),而觀察組混合骨水泥凝固時間較對照組PMMA凝固時間顯著縮短(P<0.05),術后骨水泥滲漏率也比對照組顯著減少(P<0.05)。見表1。
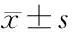
表1 兩組患者術中臨床資料對比
2.2 兩組患者術前及術后疼痛情況比較 與術前相比,兩組患者術后1 d及3、6、12個月的VAS評分均明顯降低,組間差異無統計學意義(P>0.05)。見表2。
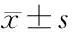
表2 兩組患者術后各時間段的VAS評分對比
2.3 兩組術前與術后椎體前緣恢復高度對比 通過術后第1天及3、6、12個月的時間點復查的X線影像資料測得椎體前緣壓縮程度百分比,顯示與術前比較,兩組患者術后椎體前緣壓縮程度百分比均顯著降低(P<0.05);組間差異無統計學意義(P>0.05);所有回訪病例均未發現椎體再骨折。見表3。
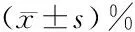
表3 兩組患者術前與術后椎體前緣壓縮程度比較
3 討論
由骨質疏松導致的OVCF在老年患者中是一種常見病及多發病,具有較高的致殘率及致死率[7]。部分OVCF患者的疼痛可以在接受保守治療后得到緩解,但是保守治療有較多并發癥,如骨量、肌力下降、壓瘡、深靜脈血栓形成等,椎體強化術(PVP/PKP)因其微創且能快速緩解疼痛等特點已被廣泛用于OVCF的治療,研究報道這兩種手術的疼痛緩解率可達到95%[8]。隨著這兩種手術方式的推廣和應用,其手術相關并發癥逐漸被報道,其中最主要的并發癥是骨水泥滲漏,嚴重的骨水泥滲漏可導致肺栓塞、神經刺激、甚至癱瘓等災難性并發癥[9]。常見的滲漏部位有椎管內滲漏、椎間孔滲漏、椎間盤滲漏、椎旁軟組織滲漏、椎旁靜脈滲漏、穿刺針道滲漏、上下終板滲漏等,其中最嚴重的并發癥是椎管內滲漏[10]。Lee等[11]對經皮椎體后凸成形和經皮椎體成形的并發癥進行分析得出經皮椎體成形術的無癥狀骨水泥滲漏率竟高達75%。本研究65例患者經椎體成形術后臨床癥狀均明顯改善,術后1 d均能逐漸下地行走,共有9例(13.8%)發生了骨水泥滲漏,觀察組2例均為椎體前滲漏,而對照組7例,7例中有3例發生了上下終板滲漏、3例發生了椎旁軟組織內滲漏、1例發生了針道滲漏,均未造成明顯神經及血管壓迫或栓塞、根性疼痛等癥狀。我們所獲得的骨水泥滲漏率較文獻報道的稍低,可能與樣本量的多少有關;同時我們在注射骨水泥的過程中會調整穿刺深度,采用多次、少量注射的方式,讓骨水泥盡量分布均勻,如C臂透視發現骨水泥有滲漏跡象,則調整注射方向或停止注射,從而在手術操作上可盡量防止骨水泥滲漏。
為了更好地解決椎體強化術的高骨水泥滲漏率這一問題,廣大國內外學者做了許多的研究和探索。Ren等[12]認為骨水泥滲漏與手術方式、注入骨水泥量、椎體壓縮高度、傷椎終板、后壁完整性等因素有關。然而,國內有學者認為手術方式并不是發生滲漏的危險因素,可能是納入的各項研究在患者選擇時有一定偏差,導致得出不同的結論,仍需要更大樣本的隨機對照試驗進一步驗證[13]。毫無疑問,傷椎注入骨水泥量越多,骨水泥滲漏發生率越高,而骨水泥注入的量與臨床緩解效果并不呈正相關。因此,許多學者建議不必刻意追求骨水泥的注入量,而應當以安全為主[14-15]。如果術前影像發現傷椎的終板及后壁不完整,手術醫生則在術中需要特別注意穿刺位置和骨水泥注射速度,有學者建議采用分階段注射方法,待之前注入的骨水泥稍凝固,方可再次注入,需在C臂機透視下正側位反復確認,以防止骨水泥滲漏的發生[16]。目前椎體成形術的手術方式較為成熟且固定,本研究所有手術操作均由同一名高年資副主任醫師完成,雖然每一例都注意了術前傷椎的情況、放緩骨水泥注射速度、也沒有刻意追求骨水泥注入量,但仍不能避免骨水泥滲漏的發生,考慮其原因主要與椎體填充物有關。
經過長時間大量的臨床應用證明,PMMA并不是最理想的椎體填充物。PMMA雖然有制備方便、不透射線性及良好的生物力學性能等特點,然而因其黏度低、流動性強等特點,容易發生骨水泥滲漏[17]。近年來,一些新型的椎體填充物逐漸應用于臨床,如硫酸鈣骨水泥、磷酸鈣骨水泥、復合骨水泥等,經研究報道,這些新型椎體填充物無發熱反應、無毒副作用、有可吸收性及骨誘導等作用,然而,也有體內吸收過快、機械支撐力不足、可注射性及顯影差等缺點[18],這些缺點也限制了這些新型椎體填充物在臨床中的應用。因此,不管是傳統用的PMMA、還是新型的硫酸鈣、磷酸鈣等,均未達到臨床最理想的椎體填充物要求。許多學者嘗試將硫酸鈣、磷酸鈣、PMMA等按不同種類、不同比例進行組合制備成椎體填充物應用于椎體成形術。吉萊骨粉 (GeneX) 是磷酸鈣和硫酸鈣骨水泥混合形成的新型骨水泥,亦具有良好的生物相容性、可吸收性和介導成骨作用[19]。有研究對86例OVCF患者進行隨訪,發現GeneX骨水泥在術后疼痛緩解方面與PMMA相似; 但在術后3個月、6個月和1年后注射PMMA組在維持椎體高度方面明顯優于GeneX組[20]。朱建華等[21]將硫酸鈣一脫鈣骨基質顆粒粉末和PMMA按40∶60混合具有合適凝固時間、聚合溫度、力強度及合適的空隙結構,具備良好的生物相容性、骨傳導性及可降解性等優點。這種混合的骨水泥被制備后其理化性質會隨著混合比例的不同而發生變化,如凝固時間、發熱性、黏稠度、流動性等,Yang等[22]通過將磷酸鈣與PMMA 按不同比例混合,隨著PMMA含量的增加,其抗壓強度和抗拉強度也相應增強,凝固時間則逐漸縮短,當PMMA體積占75%、67%、50%時,生物相容性較好,適于骨細胞的生長,因此他認為復合骨水泥在骨組織工程中具有很大的應用前景。但關于這種混合骨水泥在降低骨水泥滲漏方面的相關報道較少。
在本研究開展過程中,參考之前學者的配比比例,將硫酸鈣與PMMA按1∶3的體積比進行混合后,在體外與單純PMMA進行比較發現混合骨水泥凝固時間為6 min左右,而單純PMMA的凝固時間在10 min左右,此外混合骨水泥的黏度增加、流動性也明顯降低、有明顯的發熱反應,待二者凝固后通過用手擠壓及用錘子敲擊的方式發現二者的機械剛度相當。常規椎體成形術在C臂透視下骨水泥注射時間常規為4~6 min,所以在術者手術操作熟練的情況下,骨水泥凝固時間縮短并不影響手術操作。觀察組與對照組術后疼痛均明顯緩解,但是觀察組較對照組骨水泥滲漏率明顯降低,我們考慮按照這種比例將二者進行混合后,其機械剛度并不降低,所以其臨床療效并不受影響,而因為其凝固時間縮短、黏稠度增加、在傷椎內的流動性降低,從而能有效減少骨水泥滲漏的發生。
綜上所述,將硫酸鈣與PMMA按一定體積比混合制備成的混合骨水泥作為椎體填充物用于OVCF的治療,不僅可以獲得較好的臨床效果、而且可以顯著降低椎體成型術的骨水泥滲漏率。因此,這種混合的椎體填充物在臨床中有一定的推廣應用價值。

