補腎化瘀生新方對缺血缺氧微環境下骨髓間充質干細胞生存率及凋亡率的影響?
王詩琦, 惠小珊, 張金生, 袁書章, 薛 珂
(1.河南中醫藥大學, 鄭州 450046;2.中國中醫科學院廣安門醫院, 北京 100053;3.河南中醫藥大學第三附屬醫院, 鄭州 450008)
BMSCs是一種具有多向分化潛能的成體干細胞,在臨床腦梗死、急性心肌梗死等心腦血管疾病臨床移植治療中取得了一定的療效。但梗死區微環境缺血缺氧對BMSCs的存活、分化等造成了不利的影響[1]。課題組針對微環境與干細胞的研究已經取得一定進展,進一步探索缺血缺氧微環境對BMSCs的影響,通過中藥干預缺血缺氧微環境,提高BMSCs的生存率、分化率,可能對缺血缺氧性心腦血管疾病的治療有一定的價值和意義。本研究以BMSCs為研究對象,建立缺血缺氧微環境細胞模型,動態觀察不同時間點缺血缺氧微環境下BMSCs的狀態,探究BMSCs在惡劣微環境下的漸變過程,再給予補腎化瘀生新方含藥血清干預,對比缺血缺氧微環境下中藥干預后BMSCs發生的變化,為中藥復方調控缺血缺氧微環境,提高干細胞生存率,降低ROS損害和凋亡率提供實驗依據。本研究經河南中醫藥大學倫理文員會批準,倫理編號DWLL2018030051。
1 材料
1.1 動物
SPF級SD雄性大鼠30只,體質量(180±10)g,實驗動物合格證號SCXK(豫)2015-0005,由鄭州大學醫學院實驗動物中心提供。在河南中醫藥大學第三附屬醫院實驗動物中心飼養,飼養室內氨濃度<20ppm,通風清潔,明暗周期各12 h,自由攝食和飲水,定期更換墊料。
1.2 藥品
補腎化瘀生新方組成:熟地黃12 g,當歸12 g,巴戟天10 g,石斛10 g,川芎 15 g,肉桂3 g,甘草3 g,上述藥物購于深圳市三九中醫藥健康產品有限公司。
1.3 主要試劑與儀器
High Glucose DMEM (廣州賽業公司,批號RASMX-90011);1XPBS(北京索萊寶公司,批號P1020);Cell Counting Kit-8(日本同仁公司,批號JAPAN(CCK-8));Annexin V-FITC/PI Apoptosis Detection Kit(康為世紀,批號CW2574 S);活性氧(ROS)化學熒光法測試盒(Elabscience公司,批號E-BC-K138-F);H35低氧工作站(英國Don Whitley 公司);LHS-300SC 型二氧化碳培養箱(上海精密儀器儀表有限公司);U-RFLT50型熒光裝置,CKX41 型倒置顯微鏡(日本奧林巴斯公司);BD FACSAria TM Ⅲ型流式細胞分選儀(美國BD公司)。
1.4 含藥血清制備
SPF級SD雄性大鼠20只,結合前期課題組研究基礎[2],給藥劑量按照成人每日給藥量的18倍計算,即為12.29 g/mL/100 g。連續7 d灌胃給藥,早晚各1次,于第8天末次給藥90 min后麻醉,腹主動脈采血至離心管,室溫靜置30 min,4 ℃離心機3500 r/min離心15 min,取血清于56 ℃恒溫水浴鍋滅活30 min,-80 ℃冰箱保存備用。
2 方法
2.1 BMSCs 的提取、培養及分離純化
SPF級SD雄性大鼠10只,采用全骨髓貼壁法脫頸處死。于體積分數為75%乙醇中浸泡5 min,無菌條件剝離兩側股骨及脛骨,在4 ℃的DMEM/F12培養液中除去骨周圍肌肉組織,剪去兩側骺端暴露髓腔,5 mL注射器適量吸取DMEM/F12培養液(含有10%FBS)緩慢反復沖洗骨髓腔,至髓腔變白反復吹打細胞懸液,使細胞均勻懸浮,15 ml注射器抽取適量完全培養基沖洗骨髓腔,200目滅菌鋼篩過濾骨髓液至離心管,1280 r/min離心5 min,取3 ml細胞懸液接種于25 cm2培養瓶,于37 ℃、5% CO2飽和濕度恒溫培養箱內培養。48 h后首次半量換液,后每72 h換液1次,細胞接近90%融合時取足夠數量單細胞懸液,1280 r/min離心5 min。加入FITC標記工作濃度為1∶50的抗CD105+抗體,輕緩振搖后,于37 ℃、5% CO2飽和濕度恒溫培養箱避光孵育30 min。流式分選制成細胞懸液,以1×1010接種于T25培養瓶,置于37 ℃常溫培養箱中培養。24 h后換液除去懸浮細胞,加入含10%FBS完全培養基,每48 h更換培養基。細胞傳代培養至P3~P5用于實驗。
2.2 缺血缺氧細胞模型制備
結合前期研究[2]及參考文獻[8-12],采用DMEM培養基及94% N2、1% O2、5%CO2、37 ℃ H35低氧工作站培養細胞。時間設立為6 h、12 h、24 h、36 h、40 h、44 h、48 h、60 h 8個時間點,建立缺血缺氧細胞模型。
2.3 BMSCs分組與培養
BMSCs分為正常培養組(Control Group)、缺氧組(Hypoxia Group)、缺血缺氧組(hypoxia ischemia group, HI Group)、補腎化瘀生新方組(BSHYSX Group, BSHY Group)。正常組使用完全培養基(含10%FBS),于37 ℃ 5%CO2恒溫培養箱內培養;缺氧組使用完全培養基,缺血缺氧組使用DMEM培養基,補腎化瘀生新方組(BSHYSX Group, BSHY Group)使用補腎化瘀生新方含藥血清,于H35低氧工作站中培養細胞。
2.4 各時間點BMSCs生存率和凋亡率檢測
2.4.1 CCK-8法細胞生存率檢測 接種P3代BMSCs細胞1×105個/孔于96孔板中,分為正常培養組、缺氧組、缺血缺氧組,分別在缺血缺氧條件及正常培養條件下培養6 h、12 h、24 h、36 h、40 h、44 h、48 h、60 h后,每孔加入10 μlCCK-8溶液,于37 ℃常溫培養箱孵育2 h,酶聯免疫檢測儀480 nm處測吸光度(A)值,同時設置空白對照孔。細胞生存率(%)=(A實驗組-A空白對照)/(A對照組-A空白對照)×100%,實驗重復3次。
2.4.2 Annexin V-FITC/PI凋亡檢測 接種P3代BMSCs細胞2×105個/孔于6孔板中,分組及培養條件同上。在各時間點取出細胞,PBS洗滌后0.125%胰酶(不含EDTA)消化1 min,終止消化 1000 r/min 離心5 min收集細胞。加入Annexin V-FITC和PI溶液,輕柔混勻,室溫避光孵育15 min,加入400 μl PBS輕輕混勻,流式細胞儀迅速檢測,實驗重復3次。
2.5 ROS活性氧檢測
2.5.1 ROS流式檢測 接種P3代BMSCs細胞2×105個/孔于6孔板中,分組及培養條件同上。在各時間點取出細胞,PBS洗滌后0.125%胰酶(不含EDTA)消化1 min,終止消化 1000 r/min 離心5 min,收集細胞、調整細胞濃度1×105個/mL,加入0.5 mlPBS重懸細胞后,加入1 ml DCFH-DA熒光探針,置37 ℃常溫培養箱孵育40 min后緩沖液洗滌3次,以充分去除未進入細胞內的熒光探針。加入400 μl緩沖液重懸,于流式細胞儀迅速檢測,每個實驗重復3次。
2.5.2 ROS熒光檢測 接種P3代BMSCs以2×105個/孔的密度接種于6孔板中,與CCK-8相同的分組方法,在各時間點取出細胞,按照說明書操作,加入1 ml DCFH-DA熒光探針,放入正常培養箱孵育40 min后取出,緩沖液輕柔沖洗,以充分去除未進入細胞內的DCFH-DA,加入400 μl緩沖液,在共聚焦熒光顯微鏡下觀察細胞形態,每個實驗重復3次。
BMSCs細胞正常培養,待細胞分化良好且貼壁80%~85%時,更換5 ml高糖DMEM培養基,于1%O2、94%N2、5%CO2的低氧條件下繼續培養。
2.6 補腎化瘀生新方對缺血缺氧模型生存率、凋亡率及ROS的影響
在確立的缺血缺氧模型建立最佳時間點基礎上,以補腎化瘀生新方含藥血清干預細胞,CCK-8法測定細胞生存率,流式細胞儀檢測凋亡率和平均熒光強度,倒置熒光顯微鏡觀察細胞內ROS的表達,實驗步驟同前。
2.7 統計學方法

3 結果
3.1 各時間點BMSCs生存率和凋亡率檢測
3.1.1 BMSCs生存率變化 表1圖1示,經統計學檢驗,各時間點缺血缺氧組與正常組、缺氧組比較差異有統計學意義(P<0.05)。40 h缺血缺氧組細胞生存率最低(24.86%),后續細胞開始大量死亡。

表1 各組BMSCs生存率變化比較

圖1 各時間點BMSCs生存率比較
3.1.2 BMSCs凋亡率變化 表2圖2示,缺血缺氧組各時間點與正常組、缺氧組比較差異有統計學意義(P<0.05)。40 h缺血缺氧組BMSCs凋亡率最高(92.77%),后續細胞逐漸出現大量死亡。

圖2 各組BMSCs凋亡變化比較

表2 各組BMSCs凋亡變化比較
3.2 各時間點BMSCs熒光強度檢測
表3圖3示,各時間點缺血缺氧組與正常組比較差異有統計學意義(P<0.05);各時間點缺血缺氧組與缺氧組比較(60 h除外)差異有統計學意義(P<0.05)。熒光顯微鏡下觀察,40 h細胞內ROS熒光強度較高、細胞量較前增多明顯。提示缺氧微環境與缺血缺氧微環境下,明顯提升了細胞內的活性氧積累。對多種不同的細胞進行分析可以得出結論,活性氧可能誘導細胞凋亡[3,4]。

圖3 各組BMSCSs活性氧水平變化比較
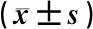
表3 各組BMSCs活性氧平均熒光強度變化比較
3.3 BMSCs缺血缺氧模型建立
根據本實驗細胞生存率、凋亡率、ROS含量等平行實驗結果互相驗證,結合課題組前期研究基礎及缺血缺氧細胞模型建立的相關參考文獻[8-12],認為40 h為BMSCSs缺血缺氧模型建立的成功最佳時間點。
3.4 補腎化瘀生新方對缺血缺氧微環境下BMSCs生存率和凋亡率的影響
3.4.1 補腎化瘀生新方對缺血缺氧微環境下BMSCs生存率影響 表4、圖a示,補腎化瘀含藥血清干預后,明顯提升了BMSCs在缺血缺氧微環境下的生存率,各時間點差異有統計學意義(P<0.05)。
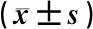
表4 補腎化瘀生新方對缺血缺氧微環境中BMSCs生存率影響比較
3.4.2 補腎化瘀生新方對缺血缺氧微環境下BMSCs凋亡率影響
表5圖b示,各時間點提示,補腎化瘀組凋亡率較缺血缺氧組明顯下降,各組比較差異有統計學意義(P<0.05)。
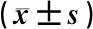
表5 補腎化瘀生新方對缺血缺氧微環境中BMSCs凋亡率影響比較
3.5 補腎化瘀生新方對缺血缺氧微環境下BMSCs活性氧的影響
表6圖c示,與缺血缺氧組比較,補腎化瘀組干預效果明顯,差異有統計學意義(P<0.05)。熒光顯微鏡下觀察,補腎化瘀生新方干預后細胞熒光強度明顯減弱。
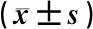
表6 補腎化瘀生新方對缺血缺氧微環境中BMSCs活性氧的影響
4 討論
微環境是干細胞分化領域的重要學說之一,在局部微環境的調控下,干細胞通過旁分泌、自分泌、內分泌等方式,干預或增強某些介導分化的關鍵基因表達,使干細胞保持持續更新的潛能。但大量研究表明,梗死區微環境缺血缺氧,短時間內釋放大量氧自由基,形成局部氧化應激反應,破壞線粒體膜完整性,無法正常供應細胞活動所需ATP,最終造成細胞凋亡或死亡;壞死細胞聚集產生局部炎癥反應、壞死局部為保持內環境穩定產生免疫應答等特異性免疫效應等,亦不利于移植后干細胞的存活和分化,無法達到預期目標[5-7]。因此,改善局部缺血缺氧微環境,提高干細胞存活率是未來干細胞研究的新方向。
缺血缺氧條件下的體內外實驗研究多各自設立單一時間點或時間段,未能形成模型建立的統一標準。YONG-SEOK HAN等[8,9]研究單個時間點,通過JAK2/STAT3通道調節hMSCs增殖情況,在低氧預處理12 h后對其進行檢測;之后這些研究者又設立多個時間點,通過c-met激活BMSCs與細胞朊蛋白PrPC相結合作用挽救缺血性損傷,實驗設置在低氧下培養0 h、6h、12 h、24 h和48 h這5個時間點進行檢測;張妮等[10]模擬炎癥誘導缺血缺氧微環境BMSCs模型,時間點設置為6 h、12 h、24 h;一些研究從動物實驗著手,時間設置以天或周為單位[11,12]。本實驗基于缺血缺氧實驗條件,設置6 h、12 h、24 h、36 h、40 h、44 h、48 h、60 h 8個時間節點,采用3種檢測方法平行驗證以觀察BMSCs在缺血缺氧微環境下的動態漸變過程。研究結果發現,6 h、12 h時缺氧組、缺血缺氧組細胞活力與對照組相比不減反升,可能與BMSCs處于短暫、非致死性的低氧條件下可激活細胞自噬,形成內源性的保護蛋白、激活胞外信號調節激酶 (extracellular signal regulated kinase,Erk)等有關,從而提高細胞的再生能力,減少細胞凋亡[13,14]。24 h開始,缺氧組、缺血缺氧組細胞活力與對照組比較明顯降低。細胞凋亡的測定,36 h開始缺氧組與缺血缺氧組細胞凋亡率明顯升高,但36 h與48 h缺血缺氧組2個時間點無顯著差異,這可能與BMSCs逐漸適應該缺血缺氧環境有關,遂加入40 h和44 h 2個時間點以作動態觀察。與正常組各時間點比較,缺血缺氧組40 h時細胞活力最低,凋亡率最高,ROS形成的細胞損傷最明顯。結合各項結果,課題組前期研究及相關細胞模型建立標準,認為40 h時BMSCs缺血缺氧模型建立成功。

圖4 CCK-8檢測中藥干預后BMSCs生存率變化比較

圖5 Annexin V-FITC/PI流式檢測中藥干預后骨髓間充質干細胞凋亡水平變化比較

圖6 ROS檢測中藥干預后骨髓間充質干細胞活性氧水平變化比較
補腎化瘀生新方以熟地黃、巴戟天共為君藥,起到滋腎陰、壯腎陽的功效;川芎活血行氣,當歸補血化瘀共為臣藥;肉桂、石斛共為佐藥,起到溫腎陽、滋陰斂陽之功;甘草調和諸藥,全方不僅可以調控機體整體的大環境,還可保證腎精充足,脈道通利[15]。課題組前期采用液相色譜-串聯質譜(LC-MS/MS)研究補腎化瘀生新方含藥血清體內吸收入血成分,共分析鑒定其藥物活性成分為主要吸收入血成分。本實驗研究得出,補腎化瘀生新方含藥血清干預缺血缺氧微環境下BMSCs的表達,可提升BMSCs在缺血缺氧微環境下的生存率。與缺血缺氧組對比,40 h時補腎化瘀生新組BMSCs凋亡率水平明顯降低。這一結果可能與補腎促進“腎精”的生長發育,激活損傷組織中干細胞損傷修復能力有關[16]。與缺血缺氧組比較,補腎化瘀生新組明顯降低細胞內氧化應激水平(圖c);48 h顯示(圖c),中藥干預組熒光強度降低,細胞成大面積、小聚落分布,提示細胞內ROS水平降低,可能有利于細胞的增殖[17]。
本研究發現,補腎化瘀生新方可提高BMSCs在缺血缺氧環境中生存率,降低凋亡率,對抗ROS對細胞的損傷,推測通過改良缺血缺氧微環境可作為提高BMSCs移植后存活率的又一新途徑,這一作用的具體機制仍有待進一步研究。

