4種結核分枝桿菌潛伏感染檢測方法的比較
鐘明浩,黃裕春,關海艦,謝文聰,梁漢成,麥偉珍,葉小華,鐘新光
(1.東莞市第六人民醫院,廣東東莞 523000;2.東莞市中心血站,廣東東莞 523000;3.廣東藥科大學公共衛生學院,廣東廣州 510310)
結核病是一種嚴重危害人群健康的呼吸道傳染病,在人群中流行和傳播可能產生新的結核病患者,同時也可能會產生新的結核桿菌潛伏感染者,潛伏感染者可在一定條件下發病成為結核病患者。據估計,全世界有四分之一至三分之一的人口可能感染結核分枝桿菌[1],因此對潛伏感染群體的篩查有重要意義。最新數據表明[2],廣東省流動人口達到五千萬。據報道[3],在肺結核整體發病率下降的同時,流動人口的發病率出現了上升趨勢。流動人口活動范圍大,接觸人群廣,是肺結核的高危人群。傳統結核桿菌潛伏感染的檢測依賴結核菌素皮膚試驗,該方法實際應用具有一定的局限性,而國外的γ-干擾素釋放試驗相關試劑價格昂貴,限制了在人群中的大規模應用。近年來,國內研發多種結核潛伏感染檢測試劑,如蛋白芯片以及γ-干擾素檢測試劑,但這些試劑缺乏在不同人群中的大規模評估。本研究選取華大IgG抗體檢測試劑盒、普瑞康IgG抗體檢測試劑盒、希格T細胞檢測試劑盒、迪澳T細胞檢測試劑盒共4種國產試劑,分別與世界衛生組織推薦的QuantiFERON-TB(QFT)試驗檢測試劑進行比較分析。
1 對象與方法
1.1 一般資料
研究對象為未被診斷為活動性肺結核的人群,選取符合納入標準的研究對象共1 200人,研究對象均知情同意。其中男性738人,女性462人;年齡中位數35歲,四分位距12歲,最小年齡18歲,最大年齡62歲;20歲以下35人,20~40歲766人,40歲及以上399人。進行結核分枝桿菌IgG抗體檢測的適用樣本為血清,標本采集時不加抗凝劑,自然凝血,要求標本清亮、無溶血。進行γ-干擾素釋放試驗檢測的標本為肝素抗凝血標本,不得使用EDTA抗凝,室溫15~25℃運輸和保存,不得冷藏或冷凍。
1.2 主要儀器和試劑
TS-1000恒溫振蕩器(常州金壇精達儀器制造有限公司)、AE-1000生物芯片閱讀儀(北京華大吉比愛生物技術有限公司);結核分枝桿菌IgG抗體譜檢測試劑盒(微陣列酶聯免疫法,北京華大吉比愛生物技術有限公司);結核分枝桿菌IgG抗體檢測試劑盒(化學發光蛋白芯片法,深圳市普瑞康生物技術有限公司);結核感染T細胞釋放γ-干擾素檢測試劑盒(酶聯免疫斑點法,廣東希格生物科技有限公司);SPOTest檢測試劑盒(廣州迪澳生物科技有限公司)。
1.3 方法
對采集的樣本分別使用4種方法進行檢測,與QFT檢測結果進行比較分析。
1.3.1 華大IgG抗體譜檢測試劑盒4種重組抗原16 kDa、38 kDa、Ag85B和MPT64以特定微陣列的形式排布在微孔板內,板孔中加入待測血清樣本溫育反應、洗滌最后加入發光液。若樣本中含有一種或多種針對上述幾種抗原的抗體,其特異性相對應的抗原點會產生發光信號。陽性對照發光信號值應>500,陰性對照發光信號值應<150。
1.3.2 普瑞康IgG抗體檢測試劑盒 基于化學發光蛋白芯片技術檢測血清中的TB-IgG。將16 kD、38 kD和LAM等5種抗原固定在醛基化玻片片基上制備成蛋白芯片,用來捕捉被測血清樣本中上述結核抗原的IgG抗體,利用抗人IgG的酶標抗體來測定樣本中的TB-IgG。
1.3.3 希格γ-干擾素檢測試劑盒 經適當分離、處理的外周血單個核細胞(PBMCs)與結核分枝桿菌特異性抗原一起加入到預包被抗γ-干擾素抗體的PVDF膜微孔中,培養一段時間。分泌出的γ-干擾素會被PVDF薄膜上特異抗體捕獲,通過顯色底物使其在反應部位形成不溶性斑點。每一個斑點代表1個γ-干擾素分泌結核特異效應T細胞。記數斑點數量可以獲得外周血中結核特異的效應T細胞數量。
1.3.4 迪澳SPOTest檢測試劑盒 在檢測時,將人外周血T淋巴細胞與致病性結核外周血結核桿菌刺激物在預包被了抗人IFN-γ的細胞培養板上共培養,經過酶聯免疫顯色,通過目測或使用放大鏡等計數斑點。每個斑點代表一個分泌細胞因子的效應T細胞,計數斑點數量可以獲得外周血中結核特異性T細胞的數量,進而判斷機體是否存在結核分枝桿菌特異性的免疫反應。
1.4 統計學分析
所有數據均采用SPSS23.0軟件進行統計學分析,一般資料以中位數和四分位距表示,不同檢測方法間進行一致性檢驗,率的比較采用χ2檢驗,P<0.05為差異有統計學意義。采用診斷試驗評價4種國產試劑的靈敏度、特異度、陽性預測值和陰性預測值、陽性似然比和陰性似然比、約登指數。
2 結果
2.1 檢測試劑盒檢測陽性率
選取1 200例研究對象標本檢測,其中華大IgG抗體檢測試劑盒、普瑞康IgG抗體檢測試劑盒、希格T細胞檢測試劑盒檢測結果陽性率分別為0.92%、13.5%、12.42%,均低于QFT檢測法(P<0.01)。迪澳T細胞檢測試劑盒陽性率32.42%,高于QFT檢測法(P<0.01),見表1。
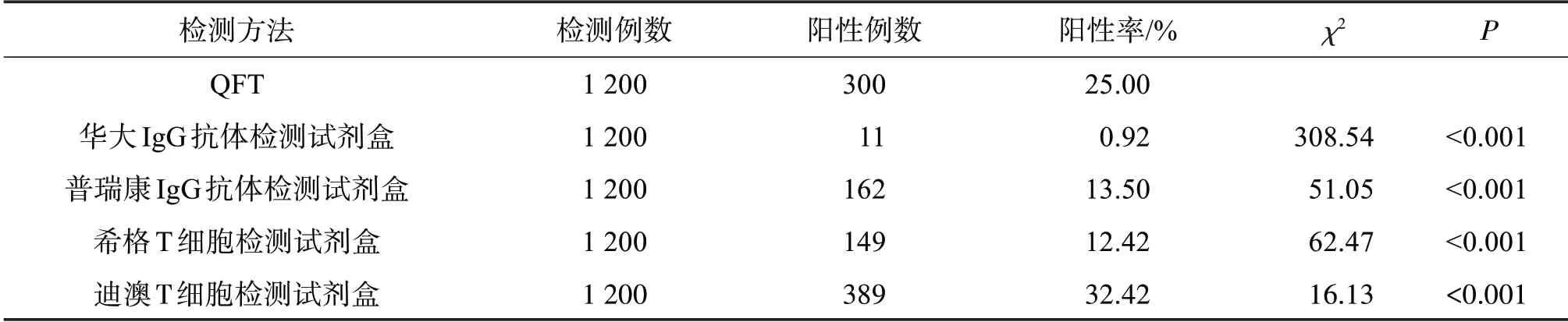
表1 4種國產檢測試劑盒與QFT檢測結果比較Table 1 Comparison of four domestic test kits and QFT test results
2.2 一致性檢驗
結果顯示,華大IgG抗體檢測試劑盒與QFT的Kappa值為0.034,差異有統計學意義(P<0.01),提示兩種方法檢測結果具有一致性。普瑞康IgG抗體檢測試劑盒與QFT的Kappa值為0.013,差異無統計學意義(P>0.05),提示兩種方法檢測結果不一致。希格T細胞檢測試劑盒與QFT的Kappa值為0.511,且具有統計學意義(P<0.01),提示2種方法檢測結果具有一致性。迪澳T細胞檢測試劑盒與QFT的Kappa值為0.699(一致性最高),且具有統計學意義(P<0.01),提示2種方法檢測結果具有一致性,見表2。
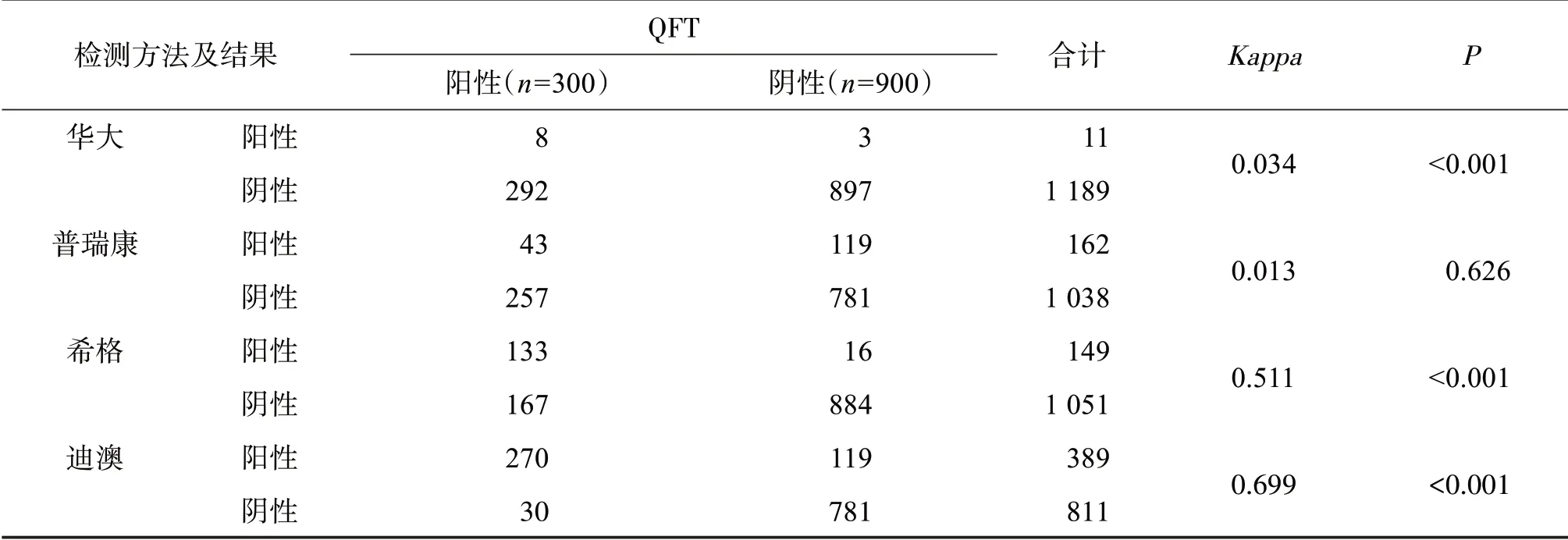
表2 4種檢測方法的一致性檢驗Table 2 Consistency test of four testing methods
2.3 靈敏度和特異度檢驗
以QFT檢測方法為標準,對4種國產檢測方法進行靈敏度和特異度的檢驗,結果顯示,華大IgG抗體試劑盒靈敏度和特異度分別為2.67%、99.67%,普瑞康IgG抗體試劑盒靈敏度和特異度分別為14.33%、86.78%,希格T細胞檢測試劑盒靈敏度和特異度分別為44.33%、98.22%,迪澳T細胞檢測試劑盒靈敏度和特異度分別為90.00%、86.78%,其他評價指標見表3。
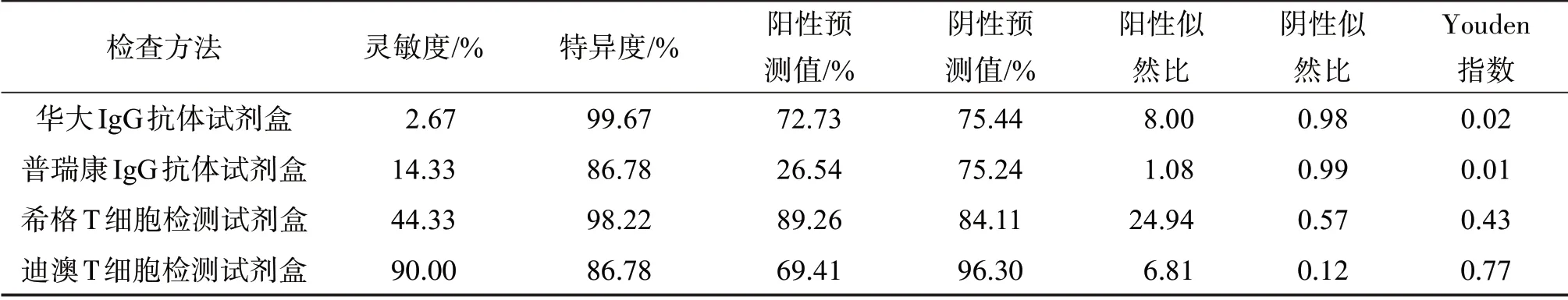
表3 4種檢測方法的診斷試驗分析結果Table 3 Analysis of the diagnostic value of four detection methods
3 討論
結核病是由結核分枝桿菌感染導致的慢性傳染性疾病,2020年全球結核報告顯示[4],2019年全球新發結核病患者約996萬,死亡約121萬。全球結核潛伏感染人群接近20億,大約5%~10%會發展為結核病患者。結核潛伏感染(LTBI)病例被定義為對結核分枝桿菌持續免疫反應的狀態,沒有臨床上證明的活動性結核病證據。美國境內發生的結核病傳播也表明[5],超過85%的結核病病例來自潛在結核病感染的重新激活。識別結核潛伏感染者是結核病控制的一個重要組成部分[6]。因此,為了實現2035年終止結核,就必須解決結核潛伏感染問題。
由于沒有診斷LTBI的黃金標準測試,因此評估LTBI的真實流行率和診斷測試的準確性具有挑戰性。準確識別和治療LTBI對于結核病的控制和消除至關重要。缺乏診斷LTBI的黃金標準意味著該疾病的真正流行率未知,并且對診斷測試的敏感性和特異性的估計帶來偏差[7]。在一項對QFT和TST(tuberculin skin test,結核菌素皮膚試驗)檢驗效能的測試中,發現QFT比TST有更高的特異性,甚至在免疫功能低下的受試者中,都有著高度可比的結果。與TST相比,QFT陽性與結核病感染風險一致[8],而且在QFT值為負的受試者中結核病發展的風險也非常低[9]。但QFT檢測成本高,且實驗室密集型QFT測試仍然有限或不可用[10-11]。因此,為探索能大規模應用于日常檢測的測試方法,本次研究選取了4種檢測試劑盒,通過與QFT進行比較分析,得到成本低、特異性高、診斷陽性率高的檢測技術。
華大IgG抗體檢測試劑盒(微陣列酶聯免疫法)是集成酶聯免疫吸附試驗(ELISA)技術和微陣列(Array)技術形成的新一代檢測技術體系。在保持了ELISA方法學的成熟、方便、敏感性及特異性都較為良好的基礎上,又具有微陣列技術的高通量、低成本、高平行、微型化等特點[12]。本次研究結果顯示,與國際推薦的QFT檢測結果25.00%相比,華大IgG抗體檢測試劑盒檢驗陽性率只有0.92%,差異有統計學意義(P<0.01),這與另外一項研究[10]的陽性率結果相近(1.25%)。
普瑞康IgG抗體蛋白芯片是一種能夠簡便快速診斷肺結核的方法,通過測定人血清中特異性的結核分枝桿菌抗體來診斷肺結核,通過多種抗原對應抗體互補,彌補了其他方法檢測漏檢的不足。一項研究發現[13],在組合蛋白抗原與血清的作用中,陽性率(12.7%)高于單獨抗原蛋白的陽性率(7.6%)。本研究結果表明,普瑞康IgG抗體檢測試劑盒陽性率13.50%,與國際推薦的QFT檢測結果25.00%相比,差異具有統計學意義(P<0.01)。陽性率較低可能與此檢測方法本身性質有關,對于所選人群中免疫低下的研究對象,可能降低了其陽性率。
希格T細胞檢測試劑盒所用方法屬酶聯免疫斑點法,與傳統的結核菌素皮試試驗相比,該方法不受卡介苗(BCG)接種的影響,特異性檢測結核分枝桿菌復合群(人型、牛型、非洲型)引起的結核感染。另外,檢測結果一次就能獲得,患者無須返回觀察,實驗室質量控制更為容易。有研究標明[14],在健康人群中,酶聯免疫斑點干擾素釋放試驗的陽性率為16.7%。本研究結果顯示,希格T細胞檢測試劑盒陽性率12.42%,低于國際推薦的QFT檢測結果25.00%,差異具有統計學意義(P<0.01)。由于受試者身體狀況的原因(如HIV感染、糖尿病、使用免疫抑制劑治療等)造成免疫功能下降甚至喪失,可能出現假陰性結果。
迪澳T細胞檢測試劑盒所用方法屬酶聯免疫斑點法,于體外定性檢測外周靜脈抗凝血中結核分枝桿菌特異性的T細胞免疫反應。酶聯免疫斑點法在淋巴結核和肺結核等檢測中,均具有較高的陽性率,能更敏感的檢測出早期或者既往感染的患者,是作為診斷肺結核的重要輔助依據[15]。有報道表明[16],酶聯免疫斑點檢測法在潛伏組的檢測中,陽性率為31.0%,本研究結果顯示,希格T細胞檢測試劑盒陽性率32.42%,高于國際推薦的QFT檢測結果25.00%,差異具有統計學意義(P<0.01)。
通過分析4組檢測方法的一致性,均以世界衛生組織推薦的QFT檢測結果為評價標準,其中迪澳T細胞檢測試劑盒檢測方法Kappa值>0.6,一致性較好,希格T細胞檢測試劑盒檢測方法Kappa值<0.4,一致性中等,其他Kappa值均>0.4,一致性較差。通過對4種檢測方法的靈敏度和特異度檢驗,迪澳T細胞檢測試劑盒具有最高的靈敏度和特異度,能更準確地檢測到陽性對象,減少漏診的情況,但本次研究對象的陽性預測值略低,可能受到人群差異和實驗室操作等因素的影響,應加大篩查人群,進一步探究其檢驗效能。本次研究迪澳T細胞檢測試劑盒陽性率檢出在4種檢測方法中最高,與其他相關研究結果[17]相近。
目前對于LTBI,仍缺乏大規模篩查檢測技術,雖然世界衛生組織推薦QFT,但仍存在許多不足之處,比如,價格昂貴[18],不同人群檢驗效能的差異。有研究表明[19],對于接種了卡介苗的個體來說,QFT具有更高的特異性和靈敏性。但在未接種卡介苗人群中診斷LBTI的QFT效能可能不如TST。此外本次選取的4種檢測方法,結果仍受到多方面的因素影響,包括免疫功能低下可能為陰性,只能用于血清樣本的檢測而不能用于檢測其他體液樣本等,這些都會制約大規模開展篩查來發現LTBI。因此,應綜合考慮實際情況,選擇具有更好預測價值的篩選方法或開展更大規模的科學實驗進行驗證。

