綠原酸眼用溫敏型凝膠的制備及兔眼房水內藥動學研究
李新南 景年水
濟南市第二人民醫院藥劑科 250001
綠原酸是中藥金銀花中的主要成分,是由咖啡酸與奎尼酸生成的縮酚酸,又稱為咖啡鞣酸,屬于苯丙素類化合物[1]。其具有抗氧化、抗病毒、抗菌、抗腫瘤、降血脂、降血糖和免疫調節等多方面的藥理作用,在食品、醫藥和化工等領域具有廣泛的應用[2-5]。金銀花因其清熱解毒,可治療風火目赤,常用于治療暴發火眼、目赤腫痛、瘡癰腫毒等,臨床上廣泛用于治療單皰病毒角膜炎、沙眼、結膜炎等[6]。
傳統的滴眼液由于淚液分泌、眨眼反射、鼻淚管排出等造成藥物作用時間短,一般滴眼液具有超過70%的藥液損失,生物利用度低[7]。另外,大量的藥物可以經鼻淚管進入鼻腔或者消化道從而被全身吸收,勢必大大增加誘發各種不良反應的風險。開發以泊洛沙姆等高分子材料為基質的新型眼用溫敏凝膠,以液態形式滴入眼部,在結膜囊內形成凝膠呈半固體狀態,不僅可以解決普通滴眼液眼內滯留時間短、生物利用度低的問題,還可以克服普通眼用凝膠缺乏良好的鋪展性及計量不易控制等諸多問題,具有良好的應用和發展前景[8]。本實驗于2020年1月至10月以泊洛沙姆為溫敏材料制備綠原酸溫敏凝膠,給藥后采用高效液相色譜法(HPLC)以及微透析技術測定不同時間綠原酸在眼房水中含量,比較綠原酸滴眼液與綠原酸溫敏凝膠在家兔眼內的藥動學特征。
1 材料與儀器
1.1 儀器 微滲析系統(微量泵控制器和MD-1001型微量注射泵,美國BAS 公司);LM-10微滲析探針(美國BAS公司);裂隙燈顯微鏡(日本尼德科公司);Agilent1260 高效液相色譜儀(DAD 檢測器);SYC-15 超級恒溫水浴(南京桑力電子設備廠);BS110S 電子分析天平(德國塞多利斯公司);KQ-5200E型醫用超聲波清洗器(功江蘇昆山市超聲儀器有限公司)。
1.2 試藥 綠原酸對照品(上海源葉生物科技有限公司,批號B20782);綠原酸,山東中醫藥大學藥學院提供,純度97%;泊洛沙姆188(Pluronic F68,BASF 德國);泊洛沙姆407(Pluronic F127,BASF 德國);甲醇(色譜純,天津四友);乙腈(色譜純,天津四友);純凈水(哇哈哈,市售);其余試劑均為分析純。
1.3 實驗動物 新西蘭大耳白家兔[濟寧魯抗公司,動物飼養合格證SCXK(魯)20130001],雌雄各2 只,體質量2.2~2.5 kg,裂隙燈顯微鏡下檢查雙眼無疾病,單籠飼養。
2 方法與結果
2.1 綠原酸眼用溫敏凝膠的制備 精密稱取綠原酸適量,溶于注射用水中,配成4%(mg/ml)溶液,加入20%的泊洛沙姆407 和1%的泊洛沙姆188,室溫攪拌后置于4 ℃冷藏,完全溶解后,加入5% 的苯扎溴銨使其濃度為1/10 000,制得綠原酸眼用溫敏凝膠,混勻,濾過滅菌,分裝,即得。測定其pH 為7.01,相變溫度為26.9 ℃,人工淚液稀釋后膠凝溫度為33.8 ℃,所得凝膠為淡黃色、均勻,在儲存期為液態,滴入眼內形成凝膠呈半固體狀態。
2.2 眼部藥代動力學
2.2.1 房水藥物濃度HPLC分析方法的建立
2.2.1.1 色譜條件的選擇 Diamond C18色譜柱,柱溫25 ℃,檢測波長318 nm,流速1.0 ml/min,流動相:乙腈-0.1%磷酸梯度洗脫,洗脫程序見表1。

表1 梯度洗脫時間程序(%)
2.2.1.2 方法專屬性考察 在上述色譜條件下,制備空白滲析液樣品,進樣,得滲析液樣品色譜圖,結果見圖1。由結果可以看出,在上述色譜條件下,空白滲析液對綠原酸測定無干擾。
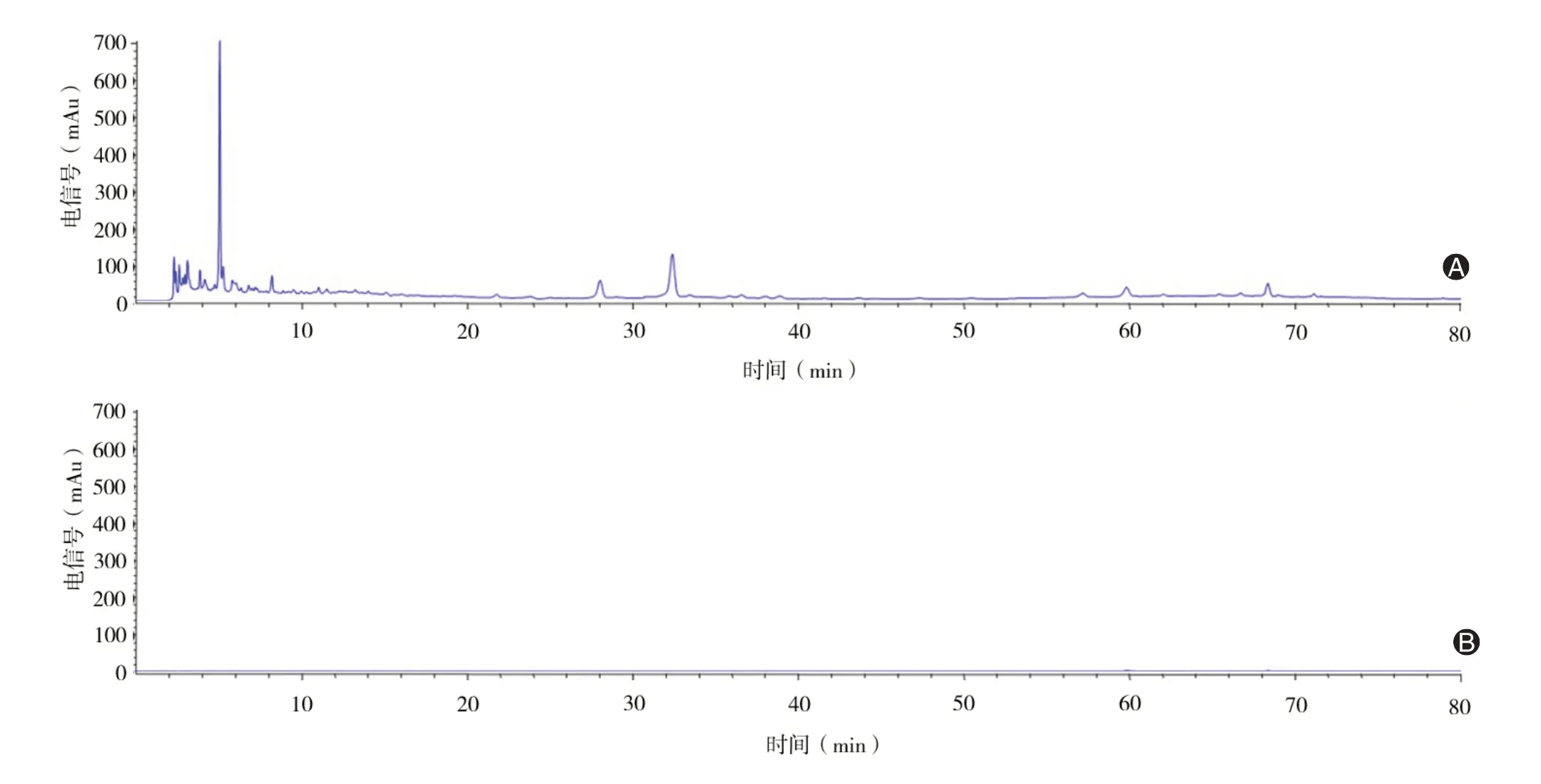
圖1 空白滲析液與給藥后透析液樣品(A為綠原酸透析液,B為空白透析液)
2.2.1.3 標準曲線的制備 精密稱取綠原酸適量,精密加入流動相稀釋,制成每毫升溶液含綠原酸38.16μg,搖勻,即得綠原酸對照品溶液。分別進樣3、6、9、12、15μl,以峰面積為縱坐標,進樣量為橫坐標,做標準曲線,結果見圖2。
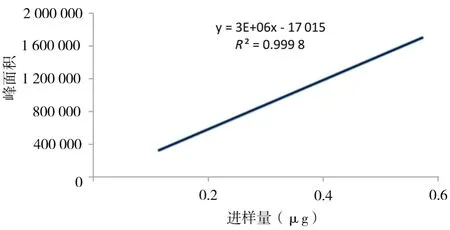
圖2 綠原酸標準曲線
2.2.1.4 方法學考察 精密度、重復性及穩定性方法學考察符合規定。
2.2.2 植入探針與給藥 術前30 min 以及手術后4 h,于家兔耳緣靜脈注射100 U/kg 肝素鈉。家兔眼結膜下注射2%利多卡因表面麻醉,開瞼器撐開眼瞼,用5#針頭于角膜結膜緣前1 mm 處斜刺入眼前房室內,LM-10微滲析探針沿針孔導入眼前房內,棄去針頭,調整滲透窗使其全部置于房水中,探針的兩端分別固定于鼻顳側和外眼角。窗口處給予一定抗生素滴眼液預防感染,恢復至傷口完全愈合后,微注射泵以1.0 μl/min 流速向探針內灌裝0.9%氯化鈉注射液,平衡一定時間后開始給藥。食指與拇指分開家兔上下眼瞼,分別將50μl 綠原酸滴眼液、綠原酸溫敏凝膠滴在靠外側眼角白眼珠下方的結膜囊內,將上眼瞼稍稍提起,讓藥液盡可能保留在結膜囊內,然后輕輕閉合眼瞼片刻,以增加藥水與眼球接觸時間,防止藥物溢出,開始收集滲析液。
2.2.3 濃差法探針體外回收率 分別配制3 個1.0、2.0、3.0 mg/ml 不同濃度的綠原酸樣品溶液,調整微滲析滲透窗的位置,保證其全部置于3 個不同濃度的樣品生理鹽水溶液中,分別調整微注射泵的流速為1、2、3μl/min,以氯化鈉注射液為灌注液,每次平衡0.5 h,收集滲析液,HPLC法測定滲析液中綠原酸的含量。計算回收率,結果見表2。回收率(R)=Cd/Cin×100%,Cd 為滲析液藥物濃度,Cin 為已知藥物濃度。
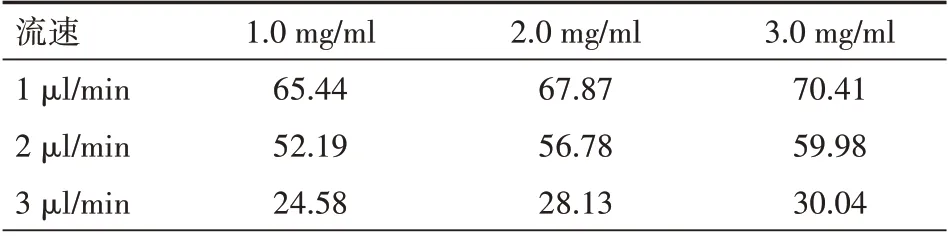
表2 不同綠原酸濃度在不同微注射泵流速下的體外回收率(n=3,%)
由實驗結果可知,綠原酸體外回收率均隨著灌注液的流速的增大而呈明顯的降低趨勢,分析原因可能是在低流速下,探針滲析膜內外藥物有充足的時間進行擴散,從而使更多的組織藥物進入滲析液內,從而使相對回收率較高,并且實驗中發現,低流速的灌注液組得到的滲析液中藥物的濃度較高。灌注液高流速組由于缺少足夠的時間進行平衡交換而造成回收率下降。但是,如果灌注速度太小,也會導致采集樣品的體積較小,造成采集時間延長。因此,綜合考慮,選擇2.0μl/min作為灌注液流速。
2.2.4 反向滲析法測定在體探針回收率 家兔眼表面丁卡因麻醉后,植入探針至前房內,經過一定恢復期后,觀察傷口完全愈合。分別配制0.1、0.5、1.0、1.5、2.0、2.5 mg/ml濃度的樣品溶液。灌注液流速設定為2.0μl/min,以不同濃度樣品生理鹽水溶液進行灌注。每次更換灌注液后沖洗30 min,每一樣品采集15 min,平行測定3次,結果見表3、圖3。相對回收率(R)=Cd-Cp/Cm-Cp,其中Cd為滲析液中藥物濃度,Cm為組織液中藥物濃度,Cp為灌注液中的藥物濃度,以Cd-Cp 對Cp 作圖。由實驗結果可知,以(Cd-Cp)對Cp 分別作圖,得到線性方程Cd-Cp=-0.436 2 Cp+0.006 6,計算的回收率為(43.62±2.55)%。由實驗結果可知,綠原酸在體回收率均低于體外回收率,可能與滲透膜表面的少量纖維化以及房水中大分子蛋白質等物質吸附、沉聚于膜表面從而阻礙藥物擴散造成。
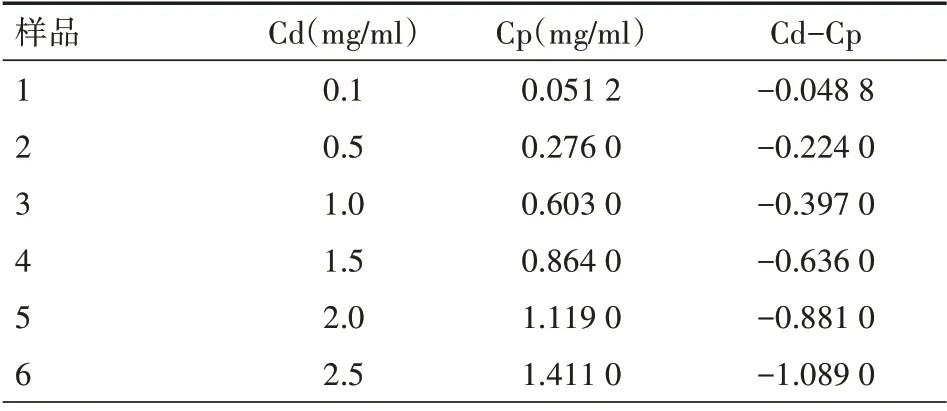
表3 反向滲析法測定綠原酸濃度
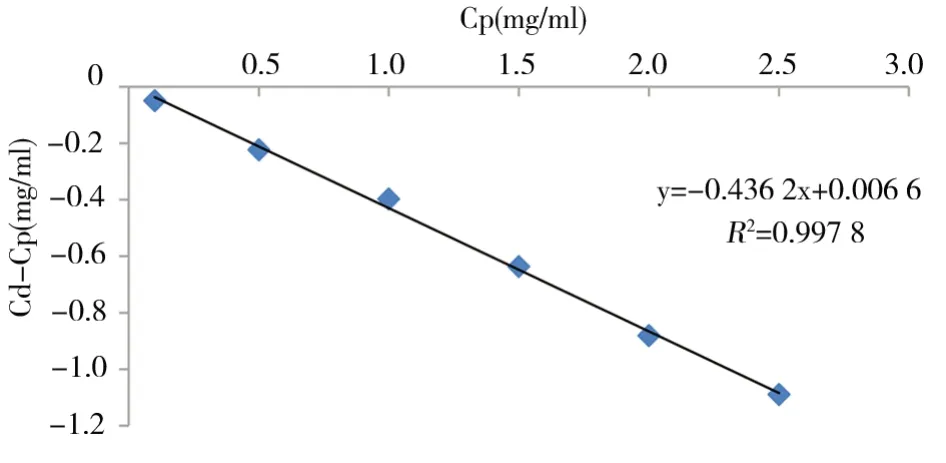
圖3 反向滲析法測定綠原酸在體探針回收率
2.2.5 綠原酸制劑眼內藥動學測定 設定流速2.0μl/min的生理氯化鈉為灌注液,沖洗30 min 后,分別將50μl 綠原酸滴眼液、眼用綠原酸溫敏凝膠滴在靠外側眼角白眼珠下方的結膜囊內,將上眼瞼稍稍提起,讓藥液盡可能保留在結膜囊內,然后輕輕閉合眼瞼片刻,以增加藥水與眼球接觸時間,防止藥物溢出,開始收集滲析液,在最開始的1 h 內,每隔15 min 取樣1 次,然后30 min 取樣1 次,共測定6 h。HPLC法測定滲析液中綠原酸的含量,結果見表4、圖4。

表4 不用藥物家兔局部給藥后的房水藥動學參數(n=4)
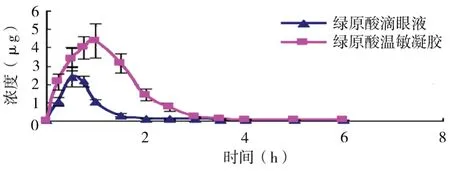
圖4 家兔眼部房水中綠原酸濃度-時間曲線(n=4)
由實驗結果可知,當綠原酸滴眼液作用于家兔眼部表明時,綠原酸立即透過角膜,作用較為迅速,但是由于藥液的迅速流失,作用時間短,生物利用度低,并且眼睛具有流淚和眨眼反射等非常有效的保護機制,一般滴眼液具有超過70%的藥液損失。滴眼液中綠原酸的藥物濃度在0.5 h達峰,峰濃度為(2.390±0.427)μg/ml,然后逐漸降低,藥時曲線下面積分別為(2.257±0.516)μg/(h·ml),當眼用綠原酸溫敏凝膠作用于家兔眼部表面時,綠原酸的藥物-時間AUC顯著增大,綠原酸的Cmax 為(4.370±0.942)μg/ml,生物利用度為綠原酸滴眼液中的3.175倍,顯著提高了綠原酸制劑中有效成分的生物利用度,并且Tmax 均有所延長。間接說明凝膠基質中對藥物的釋放具有阻滯作用,從而使藥物可以持續釋放并透過角膜進入房水,延緩了房水中藥物濃度的降低。
3 討 論
目前常用的眼內組織液的取樣方法為穿刺取樣法,通常為給藥后在不同時間點處死動物,對房水或玻璃體進行一次取樣,動物個體差異性較大,并且單次取樣所得的樣品集合是非連續性的。微透析技術能夠在同一組織內連續不間斷的取樣,并且可以進行藥物的動態監不但可以減少動物數量,還能減少誤差,對組織損傷較小,可以排除麻醉劑和蛋白結合對藥物測定的干擾,為眼部藥物動力學的研究提供了新的手段[9-10]。本部分首先建立了HPLC 測定綠原酸含量的方法,利用濃差法測定探針體外回收率,反向滲析法測定在體探針回收率,建立了眼局部給藥后在體測定藥動學參數模型,降低了實驗成本,實現了在體連續取樣。實驗中發現,在體回收率明顯低于體外回收率,分析原因可能是由于探針植入后,造成局部的輕微損傷,從而在滲析窗表面形成纖維,從而使回收率降低。并且微透析技術也有不足之處,如樣品采集量較小,有時候對分析結果有較大影響,植入眼部過程中稍有不慎便會造成眼部較為明顯損傷,從而導致滲出明顯等問題。
通過本實驗結果發現,眼部分別滴入綠原酸滴眼液和眼用綠原酸溫敏凝膠滴眼液后,兩者的藥動學參數有較大差異。綠原酸凝膠組的綠原酸的AUC 為綠原酸滴眼液的3.0 倍,且Cmax 和Tmax 均有明顯增大,分析可能是溫敏凝膠采用泊洛沙姆作為凝膠基質,提高了制劑的凝膠粘度和強度,增大了滴眼劑的黏滯度,可使藥物在眼內停留時間延長,增加藥物與角膜的接觸時間,有效減少藥物角膜前流失。
利益沖突:作者已申明文章無相關利益沖突。

