T2-FLAIR血管高信號征及其對急性缺血性腦卒中功能預后影響:基于病因研究
趙玉嬋,袁濤,班然然,高珍,全冠民
急性缺血性腦卒中(acute ischemic stroke,AIS)是人類致死和致殘的重要疾病,嚴重影響國人健康和壽命,早期評估AIS預后有助于降低致殘率及死亡率[1]。AIS功能預后與多種因素有關,其中良好的側支循環可改善AIS功能預后[2]。目前評價側支循環金標準為數字減影血管造影(digital subtraction angiography,DSA),但因其操作復雜、具有侵入性,應用受限[3]。近期研究[4,5]發現T2-液體衰減反轉恢復(fluid-attenuated inversion recovery,FLAIR)序列上血管高信號(FLAIR vascular hyperintensity,FVH)可在一定程度上反映軟腦膜側支循環狀態,但其預后價值尚存在爭議,這可能與研究納入人群、治療方式、研究終點及FVH評估方法不同有關,但較少研究考慮AIS病因類型的影響。據急性卒中治療Org10172試驗[6](Trial of Org10172 in Acute Stroke Treatment,TOAST),AIS分為大動脈粥樣硬化(large artery atherosclerosis,LAA)型、心源性栓塞(cardioembolism,CE)型、小動脈閉塞型、其他原因型和原因不明型,亞洲人群以LAA型(50%)及CE型(20%~25%)最常見[7],因此分析這兩種類型AIS的預后差異及其影響因素具有重要臨床意義。LAA型AIS的側支循環狀態優于CE型[8],而LAA型、CE型AIS間FVH是否存在差異尚不明確。筆者推測LAA型與CE型AIS的血栓產生機制、血管栓塞位置不同[9],可能影響FVH的陽性率且相應影響其對于兩種類型AIS的預后評估。因此,本研究旨在探討LAA型、CE型AIS的FVH出現率差異并進一步分析其預后評估作用是否不同。
材料與方法
1.一般資料
回顧性搜集2019年10月-2020年10月AIS病例資料。納入標準:①發病至MR檢查時間<72 h;②前循環大血管中重度狹窄或閉塞所致單側大腦中動脈(middle cerebral artery,MCA)供血區AIS;③按TOAST分型診斷[6];④臨床與影像檢查資料齊全。排除標準:①伴后循環或對側前循環腦梗死;②影像或臨床資料不足;③圖像偽影明顯。搜集以下資料:性別,年齡,腦血管病危險因素[2](高血壓、糖尿病、高脂血癥、冠心病、嗜煙史),TOAST分型,發病-影像檢查時間,入院NIHSS評分,90 d改良Rankin量表(modified Rankin scale,mRS)評分。治療原則包括抗凝藥物、抗血小板藥物和口服他汀類藥物治療。
2.影像檢查
MR檢查采用Philips Achieva 3.0T MR設備,8通道頭部線圈。主要掃描序列及參數:T2-FLAIR:TR 9000 ms,TE 140 ms,TI 2600 ms,翻轉角120°,層厚及層間距分別為6.5 mm、1.3 mm,矩陣232×181,FOV 22 cm,掃描時間26.5 s。擴散加權成像(diffusion weighted imaging,DWI):單次激發SE-EPI序列,b=1000 s/mm2,TR 2208 ms,TE 96 ms,矩陣168×105,FOV 22 cm,層厚6.5 mm,層間距1.3 mm。磁共振血管成像(magnetic resonance angiography,MRA),TOF法:TR 20 ms,TE 35 ms,翻轉角20°,FOV 20 cm,矩陣284×182,層厚1.2 mm,層間距0.6 mm。
3.圖像處理與分析
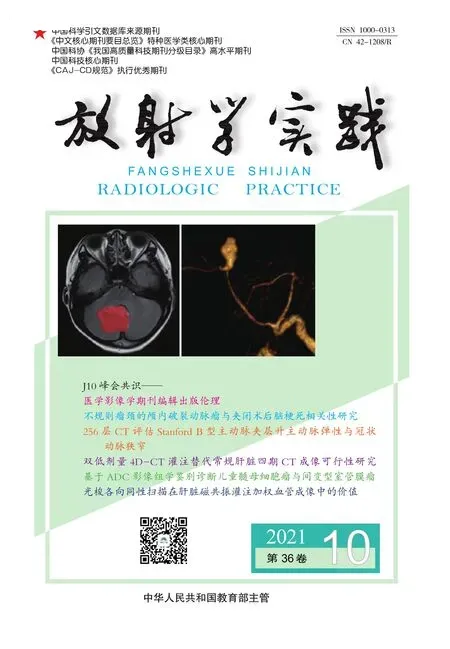
采用Philips Extended MR WorkSpace 2.6.3.4工作站行MRI圖像后處理。FVH定義[4]為T2-FLAIR序列上沿腦皮質溝、裂分布的相對于腦脊液呈局灶點狀或管條狀高信號(圖1)。以改良ASPECTS區域評價FVH評分,島葉皮層、MCA皮層前區、島葉外側皮層區、MCA皮層后區及其上方皮層區(M1~M6)任一區域發現FVH陽性為1分,最高7分,以上區域均無FVH則為0分[10]。責任血管病變部位:包括頸內動脈(internal carotid artery,ICA)和MCA,進一步以M1中點為界將MCA分為近段及遠段[9]。梗死體積測量:在軸面DWI圖像上手動勾畫每層AIS病灶得到每層面積,逐層累計面積,然后乘以圖像層厚與層間距之和,獲得AIS病變體積[11]。腦白質病變Fazekas評分[12]在FLAIR圖像上評定,包括腦室旁和深部白質病變,兩處分數相加為Fazekas總分,共6分。由兩位具有13年和18年經驗的影像醫生雙盲分析患者影像資料,意見有分歧時協商后達成一致。
圖1 FVH征陽性。左側基底節AIS,T2-FLAIR示左側額顳葉腦溝處多發線狀高信號(箭)。
4.AIS病因及預后評價
據 TOAST分型[6]責任血管狹窄>50%或閉塞且排除CE型者診斷為LAA型AIS,具有高危或中危心源性栓子來源者則為CE型AIS。采用頸動脈超聲、CTA或MRA判斷責任血管狹窄程度及閉塞[13];經胸超聲心動圖(包括右左分流檢測)、經食道超聲心動圖及24 h動態心電圖等檢查確定高危或中危心源性栓子。發病后90 d mRS≤2為預后良好、mRS>2為預后不良[14]。
5.統計學分析
結 果
研究期間共144例AIS,由于以下原因排除24例:合并后循環梗死12例、圖像質量不佳6例、臨床或影像資料不全6例;另外,非LAA型及非CE型AIS 僅4例(不明原因型4例、其他原因型及小血管閉塞型0例),因病例過少,也未包括在內;最終排除28例、納入116例。116例年齡(60.97±12.47)歲,男性80例。116例中FVH陽性94例(81.0%)、陰性組22例。LAA型AIS 84例中FVH陽性64例(76.2%)、陰性20例(23.8%)(圖2);CE型AIS 32例中FVH陽性30例(93.8%)、陰性2例(6.3%)(圖3),說明兩型AIS的FVH征陽性率差異明顯(P=0.031),CE型者更高。與FVH陰性組相比,FVH陽性組高脂血癥發生率較低(8.5%與27.3%,P=0.026)、入院NIHSS評分較高(6分與2.50分,P=0.004)、梗死體積較大(18.85mL 與6.26mL,P=0.019)、預后不良發生率高(48.9%與22.7%,P=0.004),而責任血管病變部位無明顯差異(P=0.108,表1、2),提示FVH陽性與預后不良有關。兩種類型AIS預后比較:LAA型84例的mRS評分為2.06±1.62,CE型32例mRS評分為2.72±1.80,無顯著統計學差異(P=0.06),但仍提示CE型AIS遠期預后較差。兩種類型AIS預后不良(mRS>2)比較:LAA型84例預后不良34例,CE型32例中不良預后者17例,無顯著統計學差異(P=0.22)。
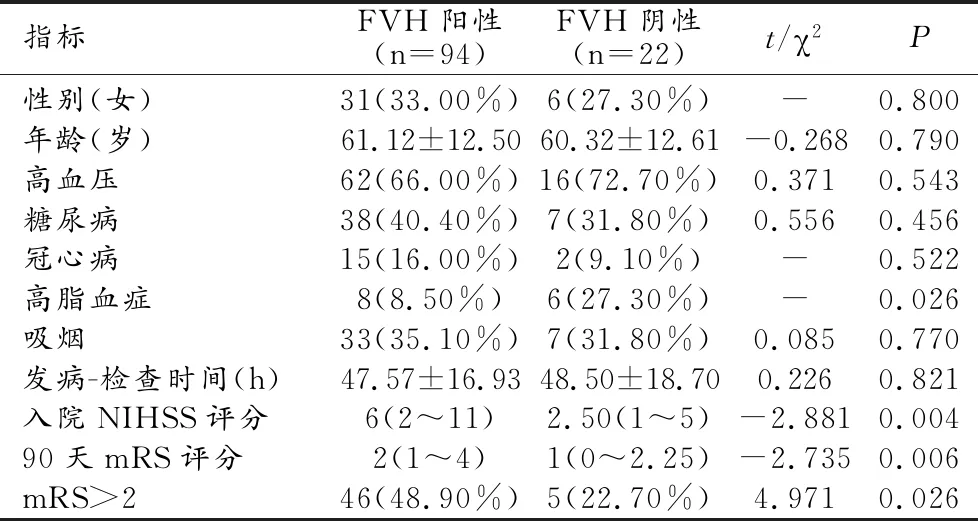
表1 116例AIS FVH征陽性與FVH征陰性的臨床特征
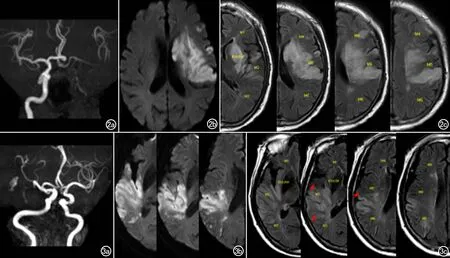
圖2 LAA型AIS患者,入院NIHSS評分33分,90d mRS評分5分。a)MRA示左側頸內動脈閉塞;b)DWI示左側大腦半球急性腦梗死,梗死體積38.54mL;c)MCA供血區(M1-M6和島葉)均未見FVH征,FVH評分0分。 圖3 CE型AIS患者,入院NIHSS評分7分,90d mRS評分3分。a)MRA示右側大腦中動脈M2段閉塞;b)DWI示右側額、頂、顳、島葉急性腦梗死,梗死體積44.70mL;c)MCA供血區(M2、M3、M5)見FVH征(箭),FVH評分3分。
FVH征陽性的多因素logistic回歸分析顯示入院NIHSS評分較高(OR=1.265,95%CI:1.049~1.525,P=0.014)和病因為CE型(CE型比LAA型,OR=5.983,95%CI:1.186~30.179,P=0.030)是FVH陽性的獨立影響因素,病因是CE型時FVH陽性概率是LAA型5.983倍,提示AIS病因類型對是否出現FVH有重要影響。
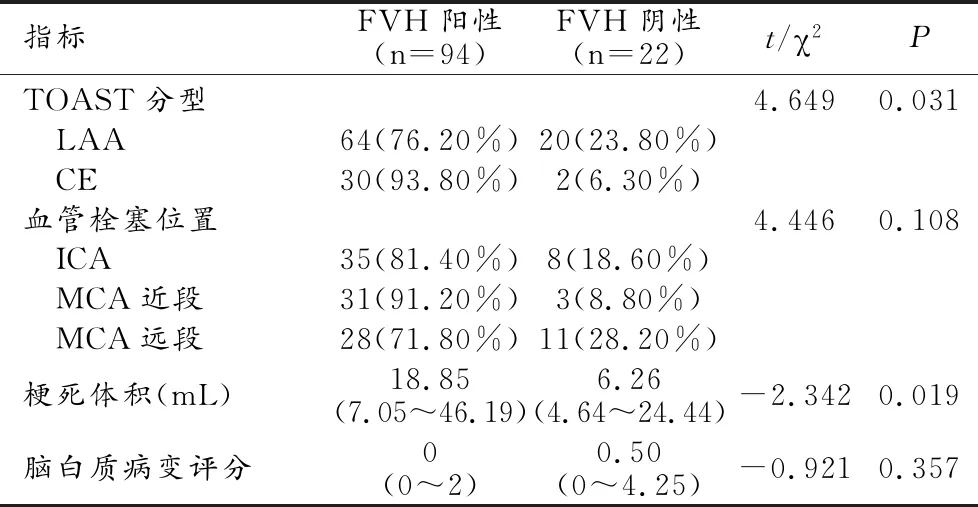
表2 116例AIS FVH征陽性與FVH征陰性的影像特征
全部AIS病例(圖4a)FVH評分與90d mRS評分正相關(r=0.260,P=0.005);LAA型者(圖4b)FVH與90d mRS評分正相關(r=0.296,P=0.006);CE型者(圖4c)FVH評分與90d mRS評分無相關性(r=0.064,P=0.728),說明FVH與AIS遠期預后有一定關聯,但應區分AIS病因類型評估這種相關關系。
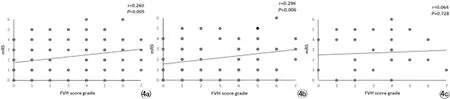
圖4 a,b,c分別為全部AIS病例、LAA型、CE型AIS FVH評分與mRS評分相關性。
AIS不良預后的多因素logistic回歸分析:①全部AIS病例,年齡較大(OR=1.052,95%CI:1.006~1.099,P=0.014)、入院NIHSS評分較高(OR=1.305,95%CI:1.153~1.478,P<0.001)、FVH評分較高(OR=1.278,95%CI:1.015~1.609,P=0.037)與AIS不良預后獨立相關;②LAA型者,入院NIHSS評分較高(OR=1.360,95%CI:1.157~1.600,P<0.001)、FVH評分較高(OR=1.405,95%CI:1.066~1.851,P=0.016)與AIS不良預后獨立相關;③CE型者,FVH評分(OR=0.834,95%CI:0.487~1.429,P=0.509)與AIS不良預后未見明確相關(表3)。上述結果提示在眾多臨床、影像學因素中FVH也具有預測特定病因AIS遠期的價值,但前提是應首先考慮AIS病因分類。
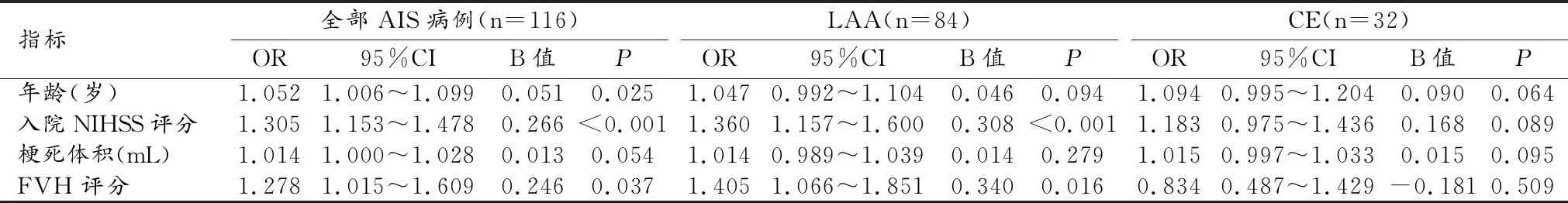
表3 全部AIS病例和LAA型、CE型AIS中FVH評分與不良預后的關系
一致性檢驗。兩位影像醫師間FVH評分Kappa值0.848(95%CI:0.775~0.915,P<0.001),腦白質病變Fazekas評分Kappa值0.837(95%CI:0.753~0.916,P<0.001),入院NIHSS評分Kappa值0.804(95%CI:0.716~0.870,P<0.001),90d mRS評分Kappa值0.927(95%CI:0.873~0.979,P<0.001),說明不同影像學醫師之間對FVH這一征象評估的一致性較好,這對于臨床推廣AIS同質化評估具有重要意義。
討 論
本研究顯示AIS病因分型是FVH征的獨立影響因子,與LAA型AIS相比CE型者FVH陽性率更高;FVH評分對AIS的預后價值與AIS病因類型有關。FVH評分較高是LAA型預后不良的獨立危險因素,但與CE型者預后無關。上述結果提示評價FVH及其預后價值時應對AIS病因類型進行區分。
不同病因類型AIS的FVH出現率有差異。本組資料顯示CE型者FVH更常見,這與Zhou等[16]結論一致,具體機制尚不清楚,推測可能與LAA型、CE型血栓形成機制及血管栓塞位置有關。LAA型者血栓多由原位血栓或不穩定斑塊脫落形成,體積較大且富含紅細胞,常致ICA和MCA近段血管狹窄或閉塞,血管栓塞位置更靠近近心端[9,17];而CE型AIS栓子大多由房顫、感染性心內膜炎及先天性心臟病等引起,栓子較小、質地較韌,血管栓塞位置更易到達遠心端[9,17]。本研究約26/84的LAA型AIS為遠心端狹窄或閉塞,而在CE型中這一比例上升至13/32,與文獻基本相符。Demchuk等[18]報道為維持梗死側血流量,血管近心端閉塞時對側大腦半球血流速度增加70%,同側后循環血流速度增加88.4%;而血管遠心端閉塞時對側大腦半球血流速度增加62.5%,同側后循環血流速度僅增加46.2%。這表明血管近心端閉塞者(LAA型)梗死側大腦半球血流量易經wills環得以補充[19],血流速度降低程度相對較輕,可能難以達到FVH產生的速度閾值(5.72 cm/s)[20],因此FVH出現率較低。而血管遠心端閉塞者(CE型)梗死側大腦半球血流量經wills環補充量有限[21],血流速度較為緩慢,FVH出現率較高。此外,據Kashiwazaki等[22]提出的微栓子理論,廣泛的MCA遠端閉塞容易導致大范圍低灌注區內血流動力學受損,血管“流空效應”消失,因此CE型FVH易于出現、評分較高。
本研究提示FVH對于不同病因類型AIS預后評估的價值不同,LAA型者FVH評分較高與AIS不良預后相關,而CE型者則無關,其原因可能是不同類型AIS的FVH形成機制有差異。早期研究表明FVH代表動脈管腔內的斑塊或血栓(氧合血紅蛋白)[23];近期則普遍認為其顯示與血管內緩慢血流有關包括順行血流動力學下降、軟腦膜側支血流緩慢逆流或兩者組合[24]。筆者推測區分二者的方法應為穿刺法血管造影,通過多支血管選擇性造影可逐一觀察病變局部的血流方向;動態增強MRA通過多期相掃描也能顯示類似的血流信息。由于相對無創性,動態增強MRA可能是更適合臨床實際的研究方法[25]。此外,Kashiwazaki等[22]首次發現MCA遠端微小栓子參與FVH形成。Wang等[24]認為當FVH位于DWI病變外時FVH形成機制傾向于血流動力學障礙,而當FVH位于DWI病變內時更傾向于血管內微小栓塞所致。本研究LAA型AIS中FVH評分與90d mRS呈正相關,FVH位于DWI病變外者約占FVH陽性者的45/65,表明LAA型者FVH產生機制以持續性血流動力學受損為主,評分較高者血流動力學異常范圍廣、梗死體積較大,因此預后較差。這與Jiang等[10]的結果一致,其FVH評分與AIS患者90d mRS評分相關系數r=0.376(P=0.034),表明FVH評分較高者預后不良。但筆者未發現CE型者FVH評分與90d mRS評分的相關性(P=0.728),并且僅有16/30的病例FVH位于DWI病變之外,這在一定程度上表明CE型者FVH的形成機制可能更為復雜,包括緩慢血流、血管內斑塊及MCA遠端微小栓子等,同時不同個體及不同部位腦組織對缺血的耐受性存在異質性,因此FVH單一因素不足以決定AIS預后[24,26]。此外,本研究中CE型AIS例數較少(32例),尚不能確定FVH評分與AIS預后之間的關系,有待于進一步大樣本研究確定。
本研究局限性:①由于其他病因類型AIS例數過少(4例),本組未包括其他原因和不明原因型病AIS病例,這些類型AIS的FVH出現率及其預后影響尚有待于進一步研究;②CE型AIS樣本量較小,FVH出現率、FVH等評分與AIS預后的相關性尚需進一步大樣本研究證實;③缺乏對不同AIS病因類型中血液動力學參數的直接測量,對于FVH與血流速度的關系闡述僅屬于推論;④有學者認為MR斑塊成像及灌注成像等有助于判斷FVH的形成機制[22,27],不同AIS病因類型中FVH的形成機制需在MR斑塊成像及灌注成像中進一步驗證。
綜上所述,前循環AIS中CE型AIS FVH陽性率高于LAA型,但FVH評分對AIS的預后價值因病因不同而異,僅LAA型者FVH較高評分是不良預后的獨立預測因子,而CE型者FVH評分與不良預后無關,推測與栓子大小及形成機制有關。本研究結果提示評價FVH及其預后價值時應首先區分是否為LAA型與CE型,再綜合考慮其他多種相關臨床及影像因素的影響。