肺亞實性結節CT定量分析對肺腺癌病理侵襲性診斷價值
蔣宇,賈曉民,趙杰
隨著胸部低劑量 CT 篩查的逐步推廣和普及,肺亞實性結節(subsolid nodules,SSNs)的檢出率越來越高,尤其是在年輕、女性、非吸煙者中[1,2]。SSNs也稱為磨玻璃結節(ground-glass nodules,GGNs),在肺窗上表現為“云霧狀”密度增高結節灶,通過這些密度增加的區域,正常的肺實質結構包括支氣管和血管仍可顯示。而在縱隔窗圖像上不能顯示或僅能顯示病灶的實性成分[3]。據其影像學上是否含有實性成分分為兩種亞型:純磨玻璃結節(pure ground-glass nodules,pGGNs)和部分實性結節(part solid nodules,PSNs)[4]。SSNs可在各種良性疾病中檢出,包括炎性疾病、局灶性出血、纖維化以及非典型腺瘤樣增生。而高分辨CT上顯示SSNs還提示惡性腫瘤的可能性,如早期肺腺癌[5]。許多研究報告指出亞實性結節可能比實性結節具有更高的惡性潛能[6]。
據世界衛生組織肺腺癌病理分類[7],肺腺癌分為浸潤前病變[非典型腺瘤樣增生(atypical adenomatous hyperplasia,AAH),原位腺癌(adenocarcinoma in situ,AIS)],微浸潤性腺癌(minimally invasive adenocarcinoma,MIA)和浸潤性腺癌(invasive adenocarcinoma,IAC)。2019年美國國立綜合癌癥網絡關于肺癌篩查的指南指出pGGNs或實性成分<5 mm的PSNs應該密切隨訪。對于表現為SSNs的AIS或MIA患者,基于其100%的5年生存率,每年CT掃描隨訪是合理可靠的。而IAC的5年無病生存率只有74.6%[4,8]。此外,研究表明病理上疑為AIS或MIA的pGGNs可考慮行密切隨訪或局限切除(節段或楔形切除),而肺葉切除仍然被認為是IAC的標準外科治療方法[9]。因此,評價存在SSNs患者的IAC發生率,對于確定最佳治療方案和評估預后具有重要意義。
以往研究已經通過定性或定量測量揭示SSNs的病理學類型或侵襲性與CT表現之間的相關性。目前研究表明[10,11]只有很少的研究探討了組織學類型與SSN質量或CT差值之間的關系。事實上質量測量可同時反映SSN體積和密度,其精確度可能優于體積、直徑或CT值[12]。此外,尚未見基于肺結節分析軟件結合胸部HRCT對表現為SSNs的CT值與肺組織差值的報道。本研究我們使用肺結節分析軟件,自動準確測量SSNs的體積、CT值,結合HRCT測得正常肺組織CT值,由此計算出結節的質量和CT差值。此外,還考慮了其他定量影像學特征。我們目的是探討這些影像學特征在鑒別IAC與MIA及浸潤前病變的有效性。
材料與方法
1.研究對象
回顧性搜集2017年4月-2020年8月獲得明確病理診斷101例患者107個切除的SSNs的臨床與影像資料。納入標準:①HRCT檢出至少1個直徑≤3 cm的SSNs;②pGGNs或實性成分最大直徑≤5 mm的PSNs;③術前1個月內行HRCT檢查者;④有完整的臨床和病理資料。排除標準:①病理診斷證實的良性病變如纖維化或慢性炎癥者;②彌漫性GGNs,間質性肺病、毛細支氣管炎、肺部嚴重感染、外傷或合并腫瘤、轉移瘤等肺基礎疾病而影響診斷者;③術前1個月內未行HRCT檢查;④CT 圖像有金屬或呼吸偽影而影響圖像質量者。
最后,共搜集101例患者107個SSNs,其中60個SSNs為pGGNs,47個為實性成分≤5 mm的PSNs。這項回顧性研究已獲得本院倫理委員會批準,所有患者均放棄知情同意的要求。
2.影像學檢查
采用GE Revolution CT掃描儀,常規取仰臥位,所有患者均在吸氣末屏氣后進行掃描。掃描參數:管電壓120 kV,管電流自動調整,螺距為1.0,層厚5 mm,標準算法及肺算法進行重組圖像,重組層厚0.625 mm,層間距1.25 mm,并做冠狀面、矢狀面重組。肺亞實性結節的觀察采用中華放射學會胸部學組推薦的窗寬及窗位即肺窗窗寬1500 HU,窗位-600~650 HU;縱隔窗寬350 HU,窗位40 HU。
3.圖像采集與分析
由2名高年資放射科醫師對所有肺結節進行后處理分析,雙方達成一致意見。將所有薄層圖像傳到PACS后處理工作站,使用深睿肺結節分析軟件,軟件可對肺部行自動分割和可疑結節位置自動檢測,系統將自動統計結節的定量參數分析:平均直徑、最大/最小CT值、平均CT值、體積、最大橫截面積。SSNs質量由以下公式計算:質量=體積·(平均CT值+1000);單位:mg。再以結節為中心,于肺窗結節最大薄層橫斷面上,勾畫與該病灶大小相似的周圍正常肺組織的感興趣區,測得周圍肺組織CT值,CT差值由以下公式計算:CT差值=平均CT值-肺組織CT值。每位醫師測量3次并取平均值,綜合兩位醫師數據為最終結果。
4.病理診斷
所有病理標本由一名具有豐富肺部腫瘤診斷經驗的高年資病理科醫師進行審核。組織學診斷遵循2015年世界衛生組織對肺腺癌的分類,分為AAH、AIS、MIA和IAC。這項研究我們將浸潤前病變(包括AAH、AIS)和MIA歸為預后相似且較好的A組,將IAC分為B組。
5.統計分析
結 果
101名患者共檢出107個SSNs,其中女64例,男43例(平均年齡61.20±13.39歲,年齡30~86歲);31例有吸煙史;93例為無癥狀篩查者,14例有咳嗽、咳痰、咯血、胸痛等癥狀。
其中pGGNs60例,實性成分≤5 mm的PSNs47例。根據病理檢查結果,將107個SSNs分為兩組:A組,包括AAH、AIS和MIA(n=52);B組,包括IAC(n=55)(圖1~3)。兩組患者的臨床資料比較性別、吸煙史、癥狀經χ2檢驗結果顯示差異均無統計學意義(P>0.05)。兩組患者年齡經獨立樣本t檢驗結果顯示差異亦無統計學意義(P>0.05,表1)。
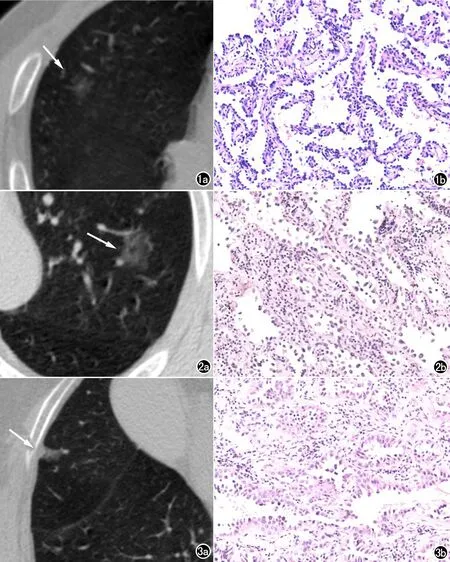
圖1 男,63歲,AIS。a)結節分析軟件自動檢測右肺上葉1枚pGGN(箭),大小9mm×9mm,平均直徑9mm,體積328.4mm3,平均CT值-619HU,HRCT肺窗上計算CT差值157HU;b)病理圖像(HE×50)示以貼壁生長為主的腺癌,傾向原位腺癌,切緣未見病變累及。 圖2 男,41歲,MIA。a)結節分析軟件自動檢測左肺上葉1枚PSN(箭),大小19mm×15mm,平均直徑17mm,體積2529.5mm3,平均CT值-629HU,HRCT肺窗上計算CT差值213HU;b)病理圖像(HE×50)示以貼壁為主的腺癌,局部傾向微浸潤。 圖3 女63歲,IAC。a)結節分析軟件自動檢測右肺中葉1枚pGGN(箭),大小9mm×6mm,平均直徑7.5mm,體積182.7mm3,平均CT值-429HU,HRCT肺窗上計算CT差值366HU;b)病理圖像(HE×50)示浸潤性腺癌,未見明確脈管內癌栓及神經侵襲。

表1 患者臨床資料
影像學定量參數與不同病理類型的關系(表2),經Mann-WhitneyU檢驗兩組患者最大CT值、最小CT值、最大橫截面積在A、B組差異均無統計學意義(P>0.05)。B組患者平均直徑、平均CT值、CT差值、體積、質量均明顯高于A組,差異均有統計學意義(P<0.05)。
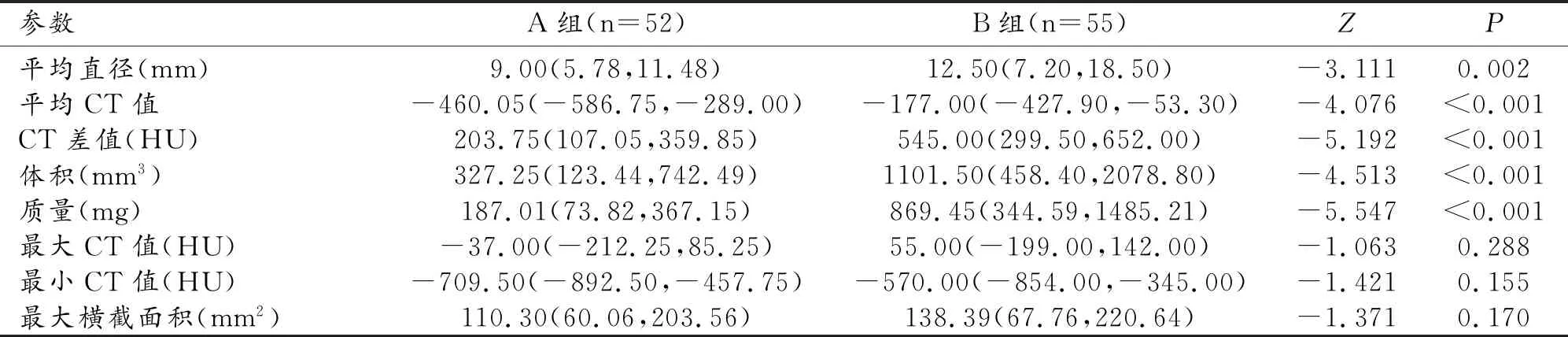
表2 兩組患者定量參數比較 [M(Q25,Q75)]
影響患者發生IAC的多因素logistic回歸結果見表3。以患者是否發生IAC為因變量,以平均直徑、平均CT值、CT差值、體積、質量為自變量,采用進入法建立二元logistic回歸模型。結果顯示CT差值、質量在模型中均有統計學意義(P<0.05)且均為影響患者發生IAC的獨立危險因素即CT差值每增加一個單位,患者發生IAC的風險是原來的1.006倍;質量每增加一個單位,患者發生IAC的風險是原來的1.004倍。
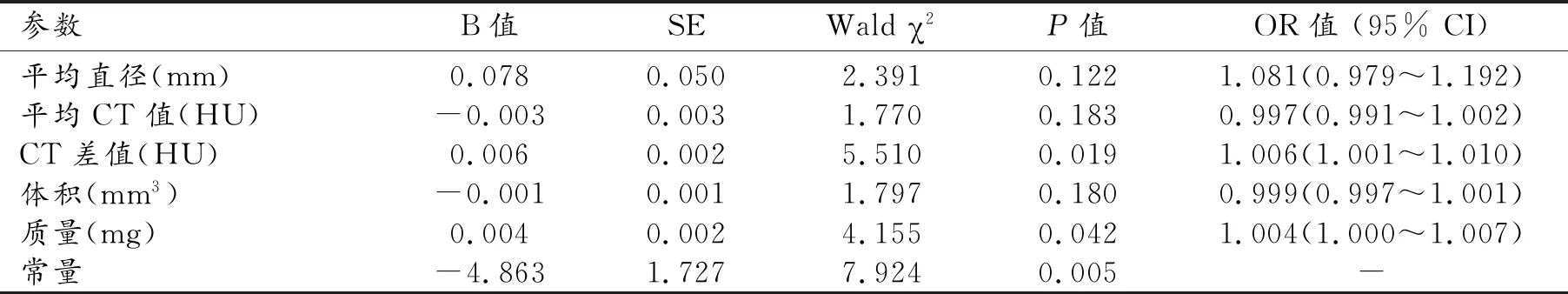
表3 影響患者發生IAC的多因素logistic回歸
CT差值及質量鑒別IAC與MIA和浸潤前病變的ROC曲線(圖4)可知CT差值、質量以及二者聯合鑒別IAC的曲線下面積分別為0.791、0.811、0.842,對應P<0.05,說明兩指標對鑒別IAC與MIA和浸潤前病變均有統計學意義。CT差值鑒別IAC的臨界值為342.55 HU,對應的敏感度72.7%,特異度73.1%;質量鑒別患者發生IAC的臨界值376.54 mg,對應的敏感度72.7%,特異度80.8%;二者聯合鑒別IAC與MIA和浸潤前病變對應的敏感度81.8%,特異度75.0%。
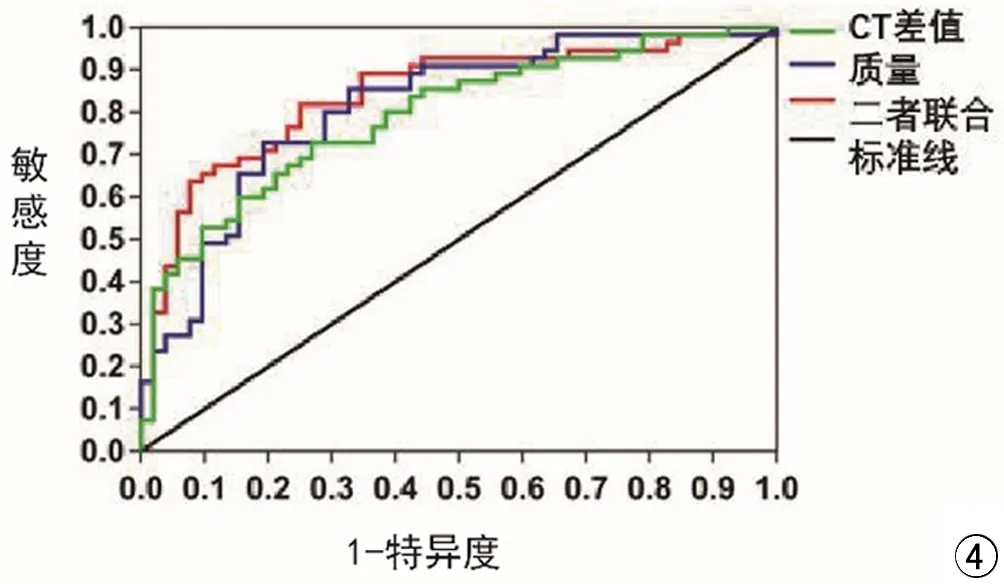
圖4 CT差值及質量鑒別發生IAC的ROC曲線
討 論
以往的研究AIS和MIA通常被視為葉下切除的指標,若進行完全切除且切緣為陰性,其術后5年無病生存率幾乎為100%[13]。因此,使用CT評價SSNs的侵襲性可能會影響肺結節管理方法的選擇。本研究結果提示SSNs的CT定量指標對鑒別IAC與MIA及浸潤前病變有重要意義且發現SSNs的CT差值和質量是發生IAC的獨立危險因素,其最佳臨界值分別為342.55 HU(敏感度72.7%,特異度73.1%)和376.54 mg(敏感度72.7%,特異度80.8%)。
本研究我們采用了不同于其他相關研究的分組方法來分析肺結節的定量影像學特征是否能區分IAC和MIA及侵襲前病變。通常來說AAH不接受手術切除[13];然而,無論是從CT上表現的磨玻璃外觀還是其他形態學特征來看AAH都不容易與AIS及MIA區分[14]。Ding等嘗試將AIS與MIA作為同一組,研究該組與IAC組的侵襲性[15]。他們認為對于pGGNs其最大直徑>12 mm是IAC的可靠預測因子,而PSNs其最大直徑>15.4 mm更傾向IAC,但并未將AAH考慮在內。本研究11個AAH被納入MIA及浸潤前病變組(A組),作為對Ding等研究的補充,這可能導致兩項研究結果的差異。因此,這兩項研究的結果仍有待進一步驗證。
值得一提地是我們只納入直徑≤3 cm的pGGNs和實性成分≤5 mm、總直徑≤3 cm的PSNs。入選標準的主要原因有3個:首先,取肺結節的直徑臨界值為3 cm。與直徑>3 cm的SSNs相比對于直徑≤3 cm的SSNs的管理存在很大爭議。其次,0.6~3 cm的pGGNs臨床T分期被分為cTis;pGGNs>3 cm被認為是鱗狀為主型腺癌。總直徑≤3 cm且實性成分≤5 mm的PSNs認為是cT1mi;如果PSNs的實性成分>5 mm,則T分期由實性成分[16]的大小決定。第三,臨床實踐中我們發現pGGNs和實性成分≤5 mm的PSNs有相同的生物學行為,因此把他們放在一起。
質量可以同時反映肺結節的體積和密度,從而更準確地反映結節特征[12]。因此,質量有助于鑒別SSNs中IAC的發生,其精確度可能優于直徑、密度或體積。本研究單變量分析顯示兩組患者平均直徑、體積、質量等方面存在顯著差異,而在二元logistic回歸分析中質量的診斷效能更高,其最佳臨界值是376.54 mg。Lim等[17]報道鑒別IAC和AIS/MIA的質量最佳臨界值是0.472 g,Liu等[10]報告指出區分IAC和AAH/AIS/MIA的質量最佳臨界值為386 mg。這種差異可能是由于納入SSNs的類型和大小不同造成的。本研究我們納入直徑≤3 cm的pGGNs和總直徑≤3 cm且實性成分≤5 mm的PSNs,而Lim等[17]僅納入直徑≥1 cm的pGGNs且未納入AAH;Liu等[10]報告鑒別IAC和AAH/AIS/MIA的質量臨界值為386 mg,僅適用于pGGNs。此外,Son等[18]報告IAC與MIA或AIS之間的質量在單變量分析上存在顯著差異;但是,在多變量分析中沒有顯著差異。
以往對SSNs的定量影像學特征分析多集中在最大/最小CT值和平均CT值等[19-21]。但平均 CT 值即使避開血管等部位仍易受患者年齡、病灶的部位、患者不同的呼吸程度、是否合并肺部基礎疾病、是否注射對比劑等因素的影響。本研究采用結節與肺組織的CT差值作為定量指標,用來減少各種因素對于研究的影響,具有較可靠的診斷效能。經ROC曲線分析CT差值是鑒別IAC發生的獨立危險因素。當 CT 差值>342.55 HU,鑒別SSNs發生IAC的敏感度72.7%,特異度73.1%,AUC 0.791。謝超等報道CT差值作為IAC的預測因素,當閾值為226 HU,敏感度和特異度分別為81.94%和85.71%,AUC為0.87。這種差異可能是由于謝超等僅納入pGGNs且病理類型未包含AAH造成的。
本研究利用ROC分析危險因素對鑒別IAC和MIA及浸潤前病變的診斷價值,經ROC分析,質量和CT差值二者結合起來,AUC值為0.842,這表明與這些因素的單獨使用相比聯合使用有助于更準確地鑒別IAC的發生。
本研究還存在一些局限性。本研究為回顧性研究,病例數較少,所選擇的SSNs僅包含外科手術后的SSNs,排除了有長期隨訪但沒有手術干預的SSNs,樣本存在選擇偏倚;第二,測量方法存在誤差,盡管是計算機自動計算,但人為勾畫肺組織的感興趣區不能避開所有的血管、支氣管等,這些都存在誤差,影響結果的重復性。
綜上所述,我們認為CT差值和質量的最佳臨界值分別為342.55 HU和376.54 mg,可作為鑒別IAC與MIA和浸潤前病變的可靠指標。聯合這兩個指標鑒別IAC與MIA和浸潤前病變的效能大于單獨指標。