光梭各向同性掃描在肝臟磁共振灌注加權血管成像中的價值
趙延潔,王紹芳,孟曉巖,鄒乾,李華玲,吳思思,李震,彭成東
磁共振灌注加權成像(perfusion-weighted imaging,PWI)是利用快速掃描序列獲得組織的血流灌注信息提供血流動力學參數的功能成像技術,在肝臟疾病診斷中具有不可替代優勢[1,2]。基于壓縮感知技術的多動脈期磁共振增強屬于灌注加權成像范疇,目前已成為肝臟病變影像學診斷的主要方法[3-5],但該技術一次采集只能獲取單個方位的圖像信息,且由于空間分辨率局限性,使其難以實現對微小病灶尤其是1~2 mm病灶的檢測和診斷[6,7]。光梭各向同性掃描是利用光梭技術快速、各向同性三維掃描方式。它以傅里葉技術、并行成像和新一代壓縮感知技術3種技術為依托[8],以智能化迭代算法重建圖像,采集薄層且等體素的三維T1加權相。本研究擬將光梭各向同性掃描應用于肝臟磁共振灌注加權成像中,通過它與常規動脈期多時相掃描方法作對比,探討光梭各向同性掃描技術的特點與優勢,為臨床提供更多參考價值。
材料與方法
1.病例資料
該研究回顧性分析本院2020年9月-2021年2月患者30例,所有患者均實施肝臟磁共振灌注加權成像。其中15例患者利用光梭各向同性掃描技術行灌注成像(ISO組);15例患者利用多動脈期相灌注成像技術行灌注成像(常規組)。排除標準:MRI檢查禁忌癥者;屏氣不配合者;圖像質量不達標,無法滿足診斷要求者。常規組男8例,女7例,平均年齡50.1±16.4歲。ISO組男9例,女6例,平均年齡47.7±12.7歲(表1)。

表1 病例資料
2.檢查方法
采用聯影3.0T uMR 790磁共振掃描儀,聯合使用12通道腹部相陣線圈和脊柱矩陣線圈。掃描前對患者進行嚴格的呼吸訓練,保證患者配合并順利完成檢查。患者檢查前禁食禁水6 h,采用仰臥位足先進。利用高壓注射器按0.2 mL/kg的劑量單位注射軋噴酸葡胺對比劑(Gd-DTPA)。兩組掃描參數如下。
常規組:TR 3.77 ms,TE 1.3 ms,翻轉角15°,視野370 mm×280 mm,矩陣225×196,層厚5 mm,層方向插值2,層間距2 mm,體素大小1.64 mm×1.43 mm×5 mm。常規組采用T13D WFI序列對肝臟進行采集。
ISO組:TR 3.53 ms,TE 1.43 ms,翻轉角12°,視野400 mm×300 mm,矩陣240×179,層厚1.5 mm,層方向插值1.6,層間距1.5 mm,體素大小1.67 mm×1.67 mm×1.5 mm。ISO組采用T1Quick 3D UCS ISO序列對肝臟進行采集。
3.圖像分析
所有圖像均在后處理工作站上進行分析處理。由2名放射科技師同時對動脈期、門脈期的肝臟圖像的信號強度、肌肉組織的信號強度和背景的信號強度進行測量。在動脈期、門脈期均選取第一肝門水平,在肝臟的右后葉內勾畫長ROI,大小為1 mm2,注意避開血管。選取3個ROI,所測數據取平均值為組織信號強度。并計算信噪比(SNR)和對比信噪比(CNR)。
SNR=SI肝臟/SD背景
CNR=SI肝臟-SI肌肉/SD背景
4.主觀評分
2名放射科技師同時對肝臟邊緣的銳利度、血管清晰度、形變和偽影進行評分。評分標準如下。肝臟邊緣的銳利度:1分=差,2分=不好,3分=尚可,4分=好;血管清晰度:1分=差,2分=不好,3分=尚可,4分=好;形變:1分=嚴重,2分=中度,3分=稍許,4分=無;偽影:1分=嚴重,完全不能診斷;2分=中度,影響局部診斷;3分=稍許,不影響診斷;4分=無偽影。
5.統計分析
采用Graphpad Prism軟件對數據進行統計分析。ISO和常規組的圖像質量的主觀評分項目(肝臟邊緣銳利度、血管清晰度、偽影、形變)采用Wilcoxon's秩和檢驗進行差異性統計分析。兩組間圖像質量的客觀評分(SNR、CNR)采用T檢驗進行差異性統計分析。
結 果
1.常規組和ISO組的肝臟解剖細節及血供信息
入組患者30例均實施肝臟磁共振灌注加權成像,其中15例患者利用多動脈期相方法行灌注成像,為常規組;15例患者利用光梭各向同性掃描方法行灌注成像,為ISO組。脈期相,常規組的冠狀面和矢狀面圖像質量較差、與直接掃描的軸面圖像相差甚遠(圖1a~c),而ISO組的冠狀面和矢狀面圖像質量較優,與直接掃描的軸面圖像水平相當(圖1d~f)。門脈期相與動脈期相具有一致的效果(圖2)。換言之,利用光梭各向同性掃描技術,同時獲取了軸面、冠狀面和矢狀面3個方位的高分辨圖像,在動脈期、門脈期均能高分辨地顯示肝臟解剖細節和血管分支(圖3)情況。
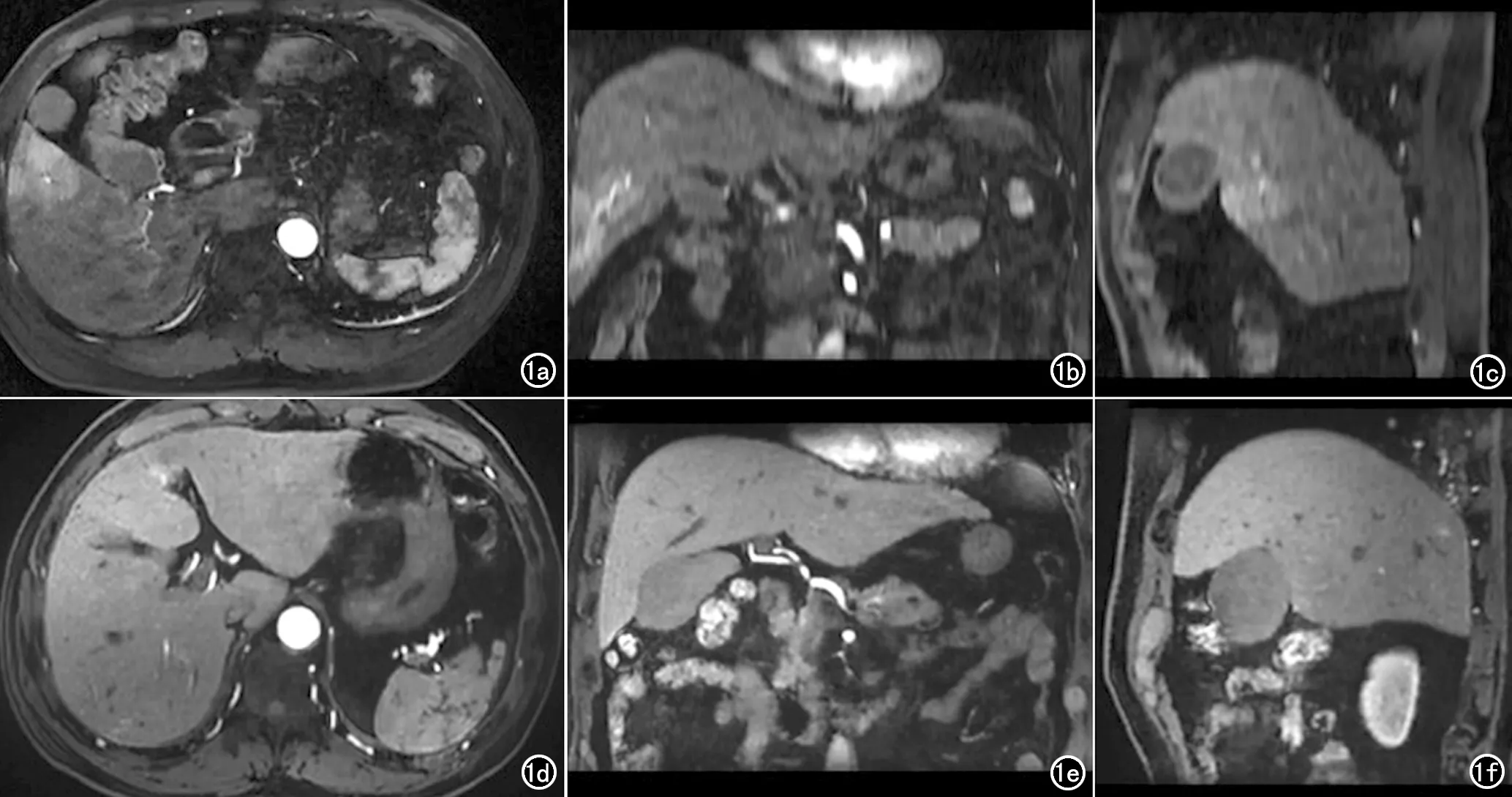
圖1 動脈期相,常規組和ISO組在不同方位肝臟解剖細節。利用常規技術獲取 a)肝臟軸面;b)冠狀面;c)矢狀面;利用光梭各向同性掃描技術獲取的 d)肝臟軸面;e)冠狀面;f)矢狀面。
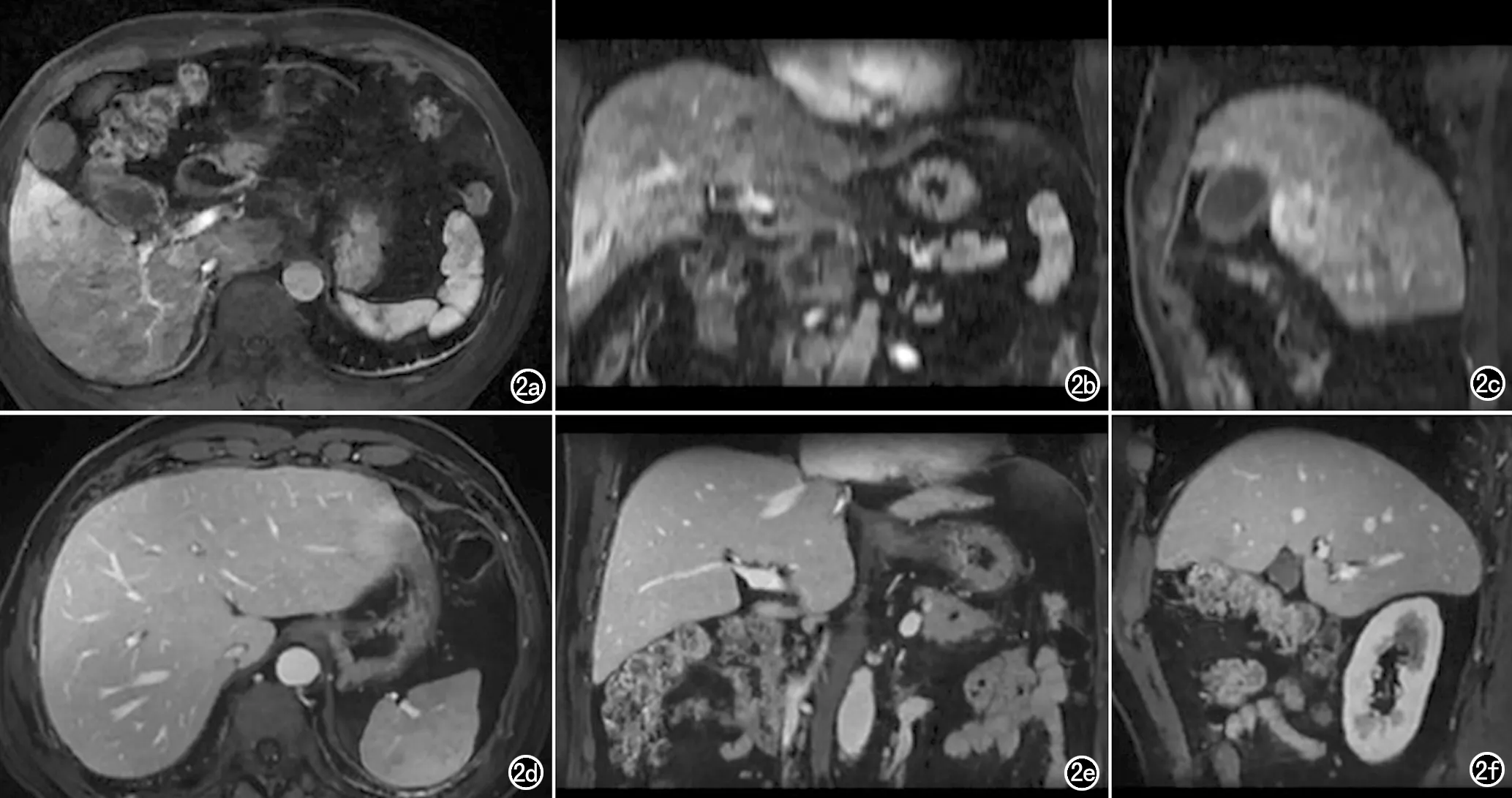
圖2 門脈期相,常規組和ISO組在不同方位的肝臟解剖細節。利用常規技術獲取的a)肝臟軸面;b)冠狀面;c)矢狀面;利用光梭各向同性掃描技術獲取的 d)肝臟軸面;e)冠狀面;f)矢狀面。
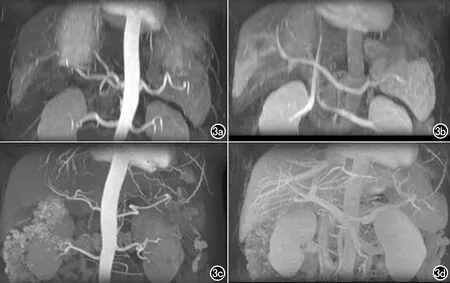
圖3 常規組和ISO組的肝臟血管分支信息。利用常規技術獲取的a)肝臟動脈;b)門脈血管;利用ISO技術獲取的 c)肝臟動脈;d)門脈血管。
2.主觀評分結果
兩名放射科技師同時對兩組圖像主觀圖像質量進行評分,評分項目包含肝臟邊緣銳利度、血管清晰度、偽影和形變。軸面圖像ISO組圖像偽影明顯<常規組,兩組具有顯著性差異,而兩組圖像在肝臟邊緣銳利度、血管清晰度和形變無顯著性差異。肝臟邊緣的銳利度、血管清晰度、偽影和形變的主觀評分對比分別為3.60±0.63 vs 3.87±0.35,P=0.1646;3.53±0.64 vs 3.47±0.51,P=0.7559;2.87±0.84 vs 3.67±0.49,P=0.0016;3.53±0.64 vs 3.93±0.26,P=0.4099(常規組 vs ISO組,表2)。
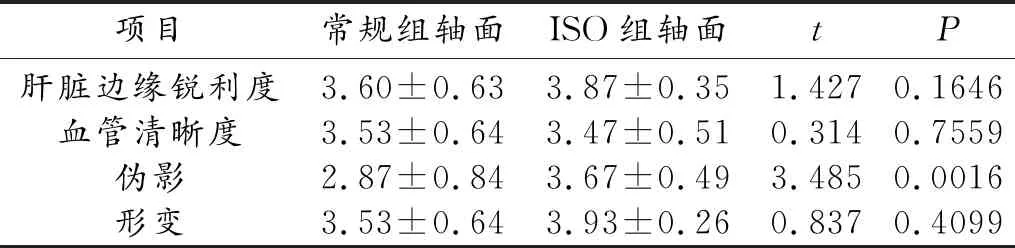
表2 常規組和ISO組軸面圖像主觀評分結果
矢狀面和冠狀面圖像(表3)兩組之間的主觀圖像質量評分均存在顯著性差異,ISO的主觀圖像質量明顯高于常規組。肝臟邊緣的銳利度、血管清晰度、偽影和形變的評分對比分別為2.20±0.68 vs 3.87±0.35,P<0.0001;2.53±0.63 vs 3.47±0.51,P<0.0001;2.33±0.62 vs 3.67±0.49,P<0.0001;2.27±0.59 vs 3.93±0.26,P<0.0001(常規組 vs ISO組)。
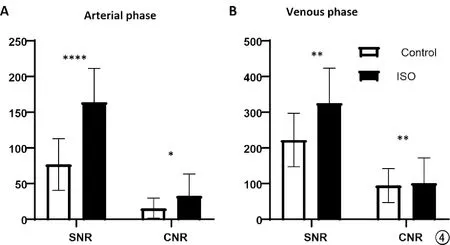
圖4 常規組和ISO組在不同期相SNR、CNR的對值。a)常規組和ISO組動脈期圖像的SNR和CNR對比值;b)常規組和ISO組門脈期圖像的SNR和CNR對比值。*P<0.05,** P<0.01,***P<0.001,****P<0.0001
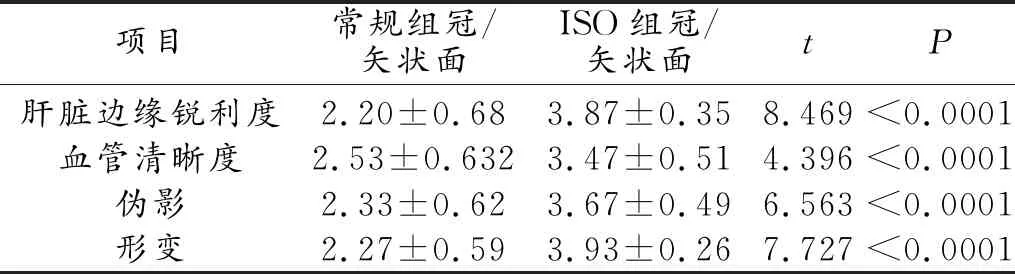
表3 常規組和ISO組冠狀面和矢狀面圖像主觀評分結果
3.客觀評分結果
客觀評分項目包括空間分辨率、SNR和CNR。ISO組層厚1.5 mm、層方向插值1.6,常規組層厚5 mm、層方向插值2,ISO組和常規組Z軸最小可分辨尺寸分別為0.94 mm和2.50 mm,因此ISO組Z軸空間分辨率達到常規組2.67倍,有效避免了微小病灶(尤其是1~2 mm)及肝臟解剖細節的遺漏。通過對動脈期、門脈期圖像信噪比和對比噪聲比進行計算,證實了兩組圖像在動脈期、門脈期SNR均存在顯著性差異,分別為76.73±36.16 vs 163.77±47.50,P<0.0001;221.73±74.80 vs 325.7±97.28,P=0.0016;兩組圖像在動脈期、門脈期CNR具有顯著性差異,分別為15.27±14.16 vs 32.69±30.58,P=0.0253;94.46±47.42 vs 101.20±70.20,P=0.0044(常規組 vs ISO組,圖4)。
討 論
各向同性掃描是通過采集薄層且等體素的數據集,使所有方位的圖像的空間分辨率完全相等。CUBE、SPACE、VISTA、ISO序列均屬于各向同性技術的范疇。該技術最早應用于大腦的結構成像,隨后在脊柱、肌肉、骨骼中廣泛應用,特別是對走行復雜的結構如膝關節、踝關節、腕關節等結構的顯示[9,10],然而在灌注增強掃描的應用中鮮有報道。本研究將光梭各向同性掃描應用于肝臟磁共振灌注加權血管成像中獲取了肝臟組織灌注后的各向同性影像學信息,可任意角度高分辨地顯示肝臟解剖細節與血供信息,為早期肝癌的診斷及肝臟外科手術的導航提供有價值的參考。
主觀評分的項目包含肝臟邊緣的銳利度、血管的清晰度、偽影和形變。本研究通過對比ISO組和常規組的主觀圖像質量發現在軸面圖像上ISO組的圖像偽影明顯<常規組,而在肝臟邊緣的銳利度、血管清晰度、形變上無顯著性差異。常規組利用壓縮感知技術實現多動脈期相掃描,一次屏氣17 s實現6個期相動脈期采集,加速倍數大,偽影相對重。而ISO組1次屏氣18 s采集1個期相,加速倍數小,偽影相對輕。相關研究曾表示加速因子超過5時圖像噪聲增加[11],本研究常規組的加速因子為14,因此可能是加速因子過高導致的采樣不足,偽影重。而ISO組加速因子小,采樣充分,因此偽影相對小。而肝臟銳利度、血管清晰度、形變的主觀評分,兩組間無顯著性差異,可能的原因是我們比較的是采集到的軸面圖像,兩組的軸面圖像均能滿足診斷要求。而在重建的矢狀面和冠狀面上,主觀評分項目均存在顯著性差異,這與理論是相符的,ISO組采用各向同性掃描技術,其重建的矢狀面和冠狀面的圖像質量與采集的軸面水平相當,而常規技術不是等體素掃描,因此其重建的冠狀面和矢狀面分辨率低,圖像質量較差。
客觀評分項目包含空間分辨率、SNR、CNR。本研究ISO組的空間分辨率(0.94 mm)達到常規組(2.50 mm)的2.67倍。常規多動脈期灌注成像1次屏氣掃描可完成多個動脈時相的連續采集,被公認為一種最準確評估肝癌檢測和表征的方法[7,11-14]。但該技術受射頻波帶寬限制,掃描所需的層厚及層間距較大。從而,對于微小病灶尤其是1~2 mm病灶的顯示受到限制[6,15]。ISO技術利用T1Quick 3D UCS ISO序列,該序列搭載新的光梭成像技術,以傅里葉技術、并行成像和新一代壓縮感知技術3種技術為依托[8]讓我們可以采集到薄層高清且等體素的三維T1加權相。薄層掃描的優勢減少了部分容積效應,更有利于肝臟解剖細節及微小病灶的顯示,有效避免了微小病灶(1~2 mm病灶)的遺漏,及早地發現微小病灶,對于肝臟疾病的早期診斷意義重大;ISO組的動脈期、門脈期的SNR均明顯高于常規組。說明ISO組的圖像T1信號值均高于常規組,而噪聲明顯低于常規組。相關研究曾表明當加速因子超過5時圖像噪聲增加,SNR和CNR明顯下降[11],這與我們的研究結果是一致的。常規組的加速因子為14,遠遠超過5,因此其SNR較低。而對于CNR而言,兩組圖像的動脈期、門脈期的CNR具有顯著性差異。可能的原因是對比劑的引入會減小T1弛豫時間,使得T1信號值增加,在動脈期和門脈期肝臟組織和肌肉組織被對比劑灌注,但灌注程度不同,在門脈期組織被對比劑灌注更加充分,導致肝臟和肌肉的T1信號值差值小。
光梭各向同性技術應用于肝臟灌注成像中具有明顯的優勢:采集的數據可進行多方位的三維重建且重建的任一平面/斜面圖像的空間分辨率水平相當。不僅可高分辨率地顯示掃描方位軸面的圖像,還可高清地顯示其它方位如冠狀面、矢狀面、任一斜面的圖像,這是常規技術所無法實現的。因為傳統技術如若采集等體素的數據需要的時間非常長,臨床上難以接受,尤其是對于灌注增強而言則難以實現。此外,該技術實現了1次打藥灌注即可對動脈期、門脈期的血管重建,同時獲取了肝動脈、門脈和靜脈系統的三維血管結構信息。最大強度投影MIP能顯示病灶的毗鄰血管和血管受累情況,同時也能顯示肝臟血管的解剖結構、病灶的供血動脈與靜脈且可任一平面、斜面地觀察血供信息。Lars Kopka等[16]研究曾表明磁共振血管成像與傳統的血管造影相比在肝動脈結構的一致性達到95%,Katsuyoshi Ito等[17]研究認為冠狀面的MIP顯示門靜脈的解剖結構最為清晰且對于肝臟的解剖分段、肝腫瘤侵犯的血供情況顯示較佳。
本研究缺點是樣本量較小,會造成測量的SNR、CNR值的選擇偏倚。另外,采用固定的時相對數據進行采集,由于患者個體差異較大,個人生理與病理因素的影響如心輸出量、血液循環,并不能完全保證所有患者被采集數據的期相是我們所預期的最佳時間,因此對于動脈期的把握不及多期相動脈期灌注的準確。
綜上所述,光梭各向同性掃描應用于肝臟磁共振灌注加權成像中,獲取了任一平面/斜面的高分辨影像學信息,可任意角度顯示肝臟的剖面及血供信息,為肝內微小病灶的準確定位及評估提供可信的信息。為肝臟外科手術的實施提供更為充分且直觀的手術導航圖像。因此該技術在肝癌的早期診斷和外科手術導航中具有不可替代的優勢,值得應用推廣。