早期腸內營養聯合腸外營養、多種微量元素 對重癥高血壓腦出血術后患者營養狀況的影響
趙冬梅,劉 洋
(新沂市人民醫院重癥監護室,江蘇徐州 221400)
腦出血是神經系統的常見急癥,高血壓是主要誘因之一,其可導致腦實質內血管破裂,引發顱內血腫,造成腦組織機械壓迫,引發頭痛、惡心嘔吐、意識障礙等臨床癥狀,且重癥高血壓腦出血是嚴重的腦出血類型,具有出血量大、病情發展迅速等特點。腸外營養是針對重癥高血壓腦出血術后患者的營養支持方式之一,營養成分經靜脈途徑進入機體,可在一定程度上補充糖、脂肪等營養物質,但未直接進入胃腸,不利于胃腸功能的早期恢復[1]。早期腸內營養支持也是臨床重癥高血壓腦出血術后的一種營養支持方式,有助于增強腸道功能,同時輔助補充多種微量元素,可促進腸黏膜免疫屏障恢復,改善營養狀態[2]。本研究探討了早期腸內營養聯合腸外營養、多種微量元素對重癥高血壓腦出血術后患者營養狀況的影響,現將研究結果作如下報道。
1 資料與方法
1.1 一般資料選取2018年12月至2020年9月新沂市人民醫院收治的重癥高血壓腦出血術后患者88例,按照隨機數字表法分為對照組與觀察組,各44例。對照組患者中男性24例,女性20例;年齡39~78歲,平均(63.46±9.25)歲;格拉斯哥昏迷指數(GCS)評分[3]5~8分,平均(6.82±0.75)分。觀察組患者中男性25例,女性19例;年齡40~79歲,平均(63.72±9.18)歲;GCS評分4~8分,平均(6.76±0.71)分。兩組患者一般資料經比較,差異無統計學意義(P>0.05),組間具有可比性。診斷標準:參照《高血壓腦出血預防與治療》[4]中的相關診斷標準。納入標準:符合上述診斷標準,且經頭顱CT或MRI檢查確診為重癥高血壓腦出血者;既往有高血壓史者;進行顱內血腫清除術者等。排除標準:合并消化系統疾病者;既往存在營養不良、癌癥、糖尿病等疾病者;對本研究藥物過敏者等。本研究經院內醫學倫理委員會批準,患者家屬均簽署知情同意書。
1.2 方法對照組患者在術后24~48 h內給予早期腸外營養聯合多種微量元素治療:靜脈輸入糖、脂肪及氨基酸等營養物質配制成的全靜脈營養混合液,同時使用多種微量元素注射液(II)(百正藥業股份有限公司,國藥準字H20057799,規格:10 mL),將10 mL藥物加入5%葡萄糖溶液500 mL中進行靜脈滴注,1次/d。觀察組患者在對照組的基礎上給予早期腸內營養治療,選用腸內營養混懸液(TPF)[紐迪西亞制藥(無錫)有限公司,國藥準字H20030011,規格:1.5 kcal/mL],經鼻胃管持續營養泵泵入腸內,第1天控制在患者所需量的25%,速度控制在20 mL/h,之后按每天25%的量遞增,直至全量,速度控制在40 mL/h,最大泵入速度不超過125 mL/h,1次/d。兩組患者均連續治療14 d。
1.3 觀察指標①營養指標。采集兩組患者治療前后空腹靜脈血5 mL,取其中3 mL,以3 000 r/min的轉速離心10 min取血清,采用全自動生化分析儀檢測兩組患者血清白蛋白(Alb)、前清蛋白(PA)、血紅蛋白(Hb)及血清總蛋白(TP)水平;采用流式細胞分析儀檢測總淋巴細胞計數(TCL)。②免疫功能。血液采集方法同①,取剩余2 mL血液,采用流式細胞儀檢測兩組患者外周血CD3+、CD4+、CD8+百分比,并計算CD4+/CD8+比值。③并發癥、死亡率。比較兩組患者并發癥發生情況,包括肺部感染、顱內感染、應激性潰瘍、腹瀉腹脹等,并統計死亡率。
1.4 統計學分析采用SPSS 21.0統計軟件分析數據,計數資料以[ 例(%)]表示,行χ2檢驗;計量資料以(±s)表示,行t檢驗。以P<0.05表示差異有統計學意義。
2 結果
2.1 營養指標治療后,兩組患者血清Alb、PA、Hb及觀察組患者TP水平均顯著升高,且觀察組顯著高于對照組,差異均有統計學意義(均P<0.05);而兩組患者治療前后和組間TCL與對照組患者治療前后TP水平經比較,差異均無統計學意義(均P>0.05),見表1。
表1 兩組患者營養指標比較(±s)

表1 兩組患者營養指標比較(±s)
注:與治療前比,*P<0.05。Alb:白蛋白;PA:前清蛋白;Hb:血紅蛋白;TP:血清總蛋白;TCL:總淋巴細胞計數。
組別 例數Alb(g/L) PA(mg/L) Hb(g/L)治療前 治療后 治療前 治療后 治療前 治療后對照組 44 27.61±4.70 29.98±5.07* 202.26±34.14 239.43±43.92*110.97±12.73 117.82±9.35*觀察組 44 27.56±4.53 32.42±5.19* 201.94±33.78 268.75±49.37*110.68±12.49 123.84±7.86*t值 0.051 2.231 0.044 2.943 0.108 3.269 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05組別 例數TP(g/L) TCL(×108/L)治療前 治療后 治療前 治療后對照組 44 63.02±7.42 62.73±7.28 10.59±1.48 10.68±1.45觀察組 44 65.11±6.19 70.19±5.58* 11.08±1.39 11.28±1.61 t值 1.435 5.395 1.601 1.837 P值 >0.05 <0.05 >0.05 >0.05
2.2 免疫功能治療后,兩組患者外周血CD3+、CD4+百分比、CD4+/CD8+比值均顯著升高,且觀察組顯著高于對照組,觀察組患者外周血CD8+百分比顯著降低,且顯著低于對照組,差異均有統計學意義(均P<0.05);而對照組患者治療前后外周血CD8+百分比經比較,差異無統計學意義(P>0.05),見表2。
表2 兩組患者免疫功能指標比較(±s)

表2 兩組患者免疫功能指標比較(±s)
注:與治療前比,*P<0.05。
組別 例數CD3+(%) CD4+(%) CD8+(%) CD4+/CD8+治療前 治療后 治療前 治療后 治療前 治療后 治療前 治療后對照組 44 51.90±8.07 63.24±4.16*26.02±4.38 36.75±3.86*24.54±6.23 23.31±4.52 1.06±0.23 1.58±0.26*觀察組 44 51.68±7.84 68.75±4.53*25.83±4.69 42.37±4.72*24.62±6.15 21.39±4.03* 1.05±0.21 1.98±0.14*t值 0.130 5.943 0.196 6.114 0.061 2.103 0.213 8.985 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.3 并發癥與死亡率治療后,兩組患者并發癥發生率與死亡率經比較,差異均無統計學意義(均P>0.05),見表3。
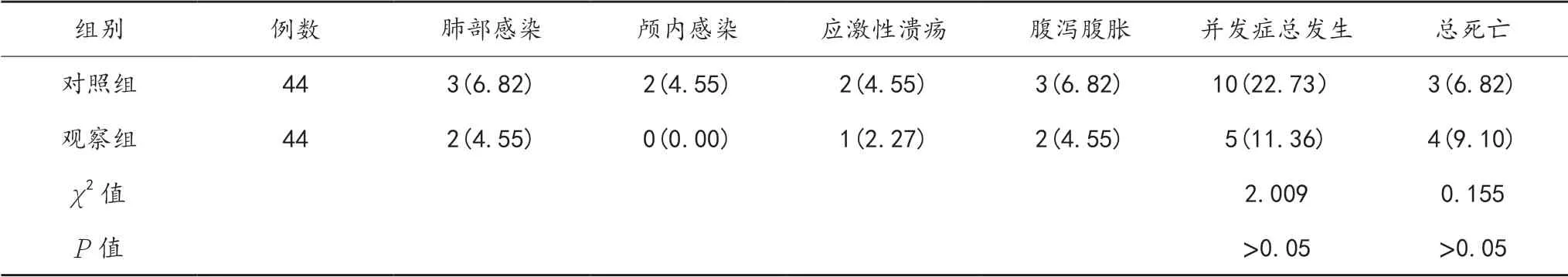
表3 兩組患者并發癥發生率與死亡率比較[ 例(%)]
3 討論
重癥高血壓腦出血極易發生多種并發癥,早期手術清除顱內血腫是釋放顱內壓、改善腦血液循環的常用治療方法,但患者機體處于高代謝與負氮平衡狀態,免疫力下降,增加了感染和其他并發癥的發生風險。腸外營養支持是以往臨床常用的營養供給方式,經靜脈途徑給藥簡單易行,減輕了機體胃腸負擔,且可降低胃腸對營養物質的不耐受性,但腸外營養只可在特定的短時間內使用,且易產生飽感綜合征,在一定程度上抑制了胃蠕動,不利于術后患者胃腸功能的恢復[5]。
經鼻飼給予早期腸內營養支持是重癥高血壓腦出血術后患者重要的營養供給方式,通過鼻飼注入營養液,可促進胃腸蠕動,加快胃腸功能的恢復,并提供機體代謝必需的營養物質,改善負氮平衡,從而促進免疫功能恢復[6]。臨床研究顯示,高代謝狀態下的危重癥患者對微量元素的需求明顯增加,尤其是機體炎癥反應較重時,對鋅、銅、錳等微量元素的消耗顯著增加[7]。T淋巴細胞亞群主要用于抵御病原體與穩定T細胞受體結構,其水平的高低可直接反映機體免疫功能高低。本研究結果顯示,治療后,觀察組患者外周血CD3+、CD4+百分比及CD4+/CD8+比值均顯著高于對照組,外周血CD8+百分比顯著低于對照組,提示早期腸內營養聯合腸外營養、多種微量元素治療重癥高血壓腦出血可增強患者免疫功能,且安全性良好。
在重癥高血壓腦出血術后患者的恢復中,因機體缺乏營養供給,營養指標隨疾病發展不斷下降,且術后患者處于高代謝狀態,加快了自身營養成分的消耗,進而影響術后恢復。血清Alb、PA、Hb、TP、TCL水平是反映機體營養狀態的重要指標,經鼻飼給予腸內營養支持,不足的部分由多種微量元素補充,可通過機體消化酶的分泌,使營養得到全面的吸收,且有助于腸黏膜結構與功能的完整性[8]。本研究結果顯示,治療后,觀察組患者血清Alb、PA、Hb、TP、TCL水平均顯著高于對照組,提示早期腸內營養聯合腸外營養、多種微量元素治療重癥高血壓腦出血可有效提升患者的營養指標,促進機體恢復。
綜上,早期腸內營養聯合腸外營養、多種微量元素可提升重癥高血壓腦出血術后患者的營養指標,增強免疫功能,且安全性良好,值得臨床推廣與應用。

