可注射型富血小板纖維蛋白聯合封閉式負壓引流技術治療慢性難愈性創面的應用研究
陳道才,謝 娟,李紅紅,朱邦中,陳增紅,婁 寅,方 穎,曹東升
慢性難愈性創面通常指因各種因素引起的經過常規治療無法在可預期的時間內按正常生物學步驟完全愈合的創面。其形成機制復雜,治療周期長,耗費大量醫療資源。封閉負壓引流(vacuum sealing drainage,VSD)技術是將封閉式敷料與創面引流技術創造性的結合,被廣泛應用于多學科的各類慢性創面,有一定療效,但在治療一些復雜慢性創面及促進創面組織再生等方面仍有局限。Choukroun et al研究表明降低自體血液濃縮制品制備過程中的離心力與離心速度,能獲得性能更為優良的新一代自體血小板濃縮物可注射型富血小板纖維蛋白(injectable platelet-rich fibrin,i-PRF),其中的血小板、生長因子、細胞因子和白細胞含量更高,擁有較強的流動性及抗細菌活性,具有促進組織再生及傷口愈合的作用。i-PRF在慢性難愈創面治療中罕見報道,該研究旨在探討i-PRF聯合封閉式負壓引流技術對比傳統單純負壓創面引流治療在慢性創面治療中的療效。
1 材料與方法
1.1 病例資料
選取2018年10月至2020年11月在安徽醫科大學第二附屬醫院整形外科收治的80例慢性難愈性創面患者,根據隨機數字表法將80例患者分成對照組和i-PRF組,每組各40例,兩組患者入院相關臨床資料比較差異均無統計學意義(P
>0.05),見表1。本研究經過醫院倫理委員會批準,患者均簽署了知情同意書。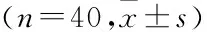
表1 兩組患者一般臨床資料比較
1.2 納入與排除標準
1
.2
.1
納入標準 ① 年齡18~65歲;② 符合慢性難愈創面診斷標準:出現創面經常規換藥清創治療4周以上無好轉跡象或加重者;③ 病情穩定無明顯手術禁忌者。1
.2
.2
排除標準 ① 有精神或者認知功能障礙患者;② 診斷有血液系統疾病,血小板計數<100×10/L,血紅蛋白<110 g/L的患者;③ 近期服用抗凝藥物或者免疫抑制劑的患者;④ 處于妊娠期、哺乳期的婦女;⑤ 創面面積大于100 cm、下肢嚴重壞疽的患者;⑥ 惡性腫瘤導致的潰瘍。1.3 方法
1
.3
.1
i-
PRF制備 根據創面大小,用50 ml無菌注射器自患者肘靜脈抽取20~50 ml靜脈血,立即注入離心機無菌離心管中,700 r/min離心3 min,血液經低速離心后分兩層,上層液體即為i-PRF。1
.3
.2
創面處理 對照組:創面行徹底清創術,修剪適當大小VSD敷料覆蓋創面,生物膜貼合包裹;i-PRF組:創面行徹底清創術,然后用2 ml無菌注射器抽取i-PRF多點分散注射于創面及創面周緣,修剪適當大小VSD敷料覆蓋創面,生物膜貼合包裹;術后:兩組患者處理一致,接中心負壓持續吸引,負壓值維持在26.66~46.66 kPa,期間予生理鹽水間斷沖洗創面;以7 d為一治療周期,兩組患者分別重復上述操作直至創面肉芽組織新鮮飽滿達修復標準后修復創面。1.4 觀察指標
1
.4
.1
炎癥指標及疼痛評分 術后第7、14天復查炎癥指標WBC、CRP、ESR,并進行NRS疼痛評分。1
.4
.2
創面細菌培養結果 術前、術后第7、14天分別取創面分泌物做細菌培養,計算創面細菌轉陰率,創面細菌轉陰率=(原有創面細菌培養陽性例數-治療后創面細菌培養陽性例數)/原有創面細菌培養陽性例數×100%。1
.4
.3
肉芽組織生長情況 術后第7、14天查看創面肉芽組織生長情況,采用無菌薄膜勾邊法計算創面新鮮紅色肉芽組織覆蓋率=新鮮紅色肉芽組織面積/原創面面積×100%;并切取少量創緣組織行HE染色組織學觀察及免疫組織化學標記血管內皮生長因子(vascular endothelial growth factor,VEGF)表達情況。1
.4
.4
創面達修復標準時間及創面愈合時間 記錄創面達修復標準準備時間(初次清創至達手術修復標準的時間)、創面愈合時間(初次清創至創面愈合的時間)。
2 結果
2.1 兩組患者治療后創面細菌培養結果比較
對照組治療后7、14 d細菌轉陰率分別為30.00%、56.67%;i-PRF組治療后7、14 d細菌轉陰率分別為56.25%、90.63%;治療后14 d兩組患者創面細菌培養結果差異有統計學意義(P
<0.05),見表2。
表2 兩組患者治療后創面細菌培養結果比較
2.2 兩組患者治療前后炎癥指標水平比較
兩組患者治療后第7、14天復查WBC、CRP、ESR水平均呈降低趨勢,i-PRF組較對照組下降趨勢更明顯,差異均有統計學意義(P
<0.05),見表3。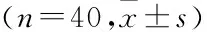
表3 兩組患者治療前后WBC、CRP、ESR水平比較
2.3 兩組患者治療前后創面疼痛程度比較
兩組患者治療后局部疼痛均較前緩解,i-PRF組患者疼痛緩解程度較對照組明顯,差異有統計學意義(P
<0.05),見表4。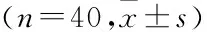
表4 兩組患者治療前后NRS疼痛評分比較
2.4 兩組患者治療后創面新鮮紅色肉芽組織覆蓋率比較
i-PRF組治療后7、14 d創面新鮮紅色肉芽組織覆蓋率均較對照組高,差異均有統計學意義(P
<0.05),見表5和圖1、2。
圖1 i-PRF組典型病例A:術前;B:術后第7天;C:術后第14天 D:植皮術后7 d

圖2 對照組典型病例A:術前;B:術后第7天;C:術后第14天;D:術后第21天;E:植皮術后7 d
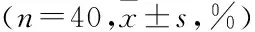
表5 兩組患者治療后創面新鮮紅色肉芽組織覆蓋率比較
2.5 創緣組織HE染色及免疫組織化學標記對比
i-PRF組術后第7、14天創緣組織新生微血管數高于對照組,見圖3;VEGF免疫組化染色呈不同程度黃棕色,i-PRF組術后第7、14天 VEGF表達較對照組顯著,見圖4。
圖3 創緣組織HE染色 ×400A:觀察組術后第7天;B:對照組術后第7天;C:觀察組術后第14天;D:對照組術后第14天
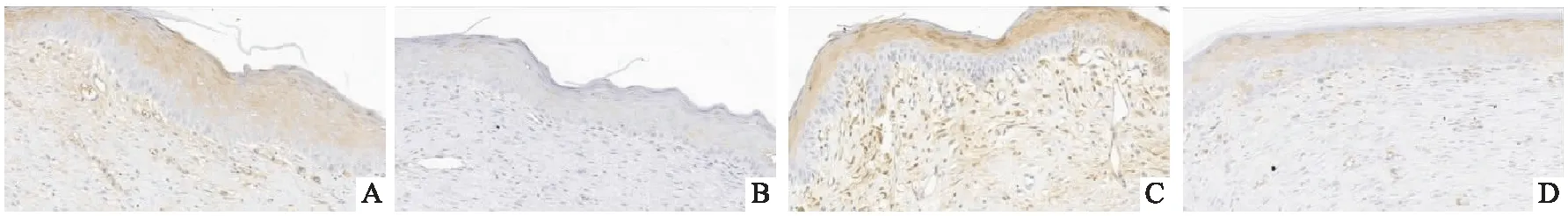
圖4 創緣組織免疫組化標記結果 ×400A:觀察組術后第7天;B:對照組術后第7天;C:觀察組術后第14天;D:對照組術后第14天
2.6 兩組患者創面達修復標準準備時間及創面愈合時間比較
i-PRF組患者創面達修復標準準備時間及創面愈合時間均較對照組縮短,差異均有統計學意義(P
<0.05),見表5。
表5 創面達修復標準準備時間及愈合時間比較[n=40,d,n(%)]
3 討論
創面愈合過程包括出血、炎癥反應、肉芽組織形成和組織重塑四個階段,是一個動態的、有序的、相互交錯的過程,但此過程可能在各種內外因素作用下被破壞,形成病理性炎癥反應,最終導致慢性難愈創面。其形成原因復雜,血糖異常、細菌生物膜形成、缺血-再灌注損傷、生長因子缺乏、相關基因表達異常等均會影響創面修復,導致創面遷延不愈。
創面換藥及清創手術等常規治療方法療效不佳,VSD技術能將局部壞死組織及分泌物持續引流,減輕局部感染及水腫,為創面創造良好的愈合條件,但創面肉芽組織生長及組織再生需要足夠濃度的生長因子、控制細胞過度凋亡、血運重建等條件,VSD技術在這些方面并無優勢。自體血液濃縮物中含有大量的血小板、生長因子、纖維蛋白和白細胞,因其能夠加速傷口愈合,促進軟硬組織再生,已經在修復和重建領域廣泛應用。i-PRF作為新一代血小板濃縮物,生物活性更高,不含任何添加劑,避免了免疫排斥及過敏反應等問題,通過一次低速離心即可獲得,制備過程相對簡單,而且具有良好的流動性,可局部注射,增強了局部應用時的可操作性。
在本研究中,觀察組患者治療后創面感染控制情況、炎癥指標下降程度、新鮮肉芽組織生長情況、局部疼痛緩解程度等方面均較對照組效果顯著,表明負壓引流技術聯合i-PRF治療慢性難愈創面治療較單純應用負壓引流技術療效更佳,分析其機制可能如下:① 細菌生物膜的形成是導致創面難愈的重要因素甚至起決定作用,其可促使細菌耐藥,逃避宿主免疫作用和抗生素殺傷,使創面長期處于炎癥反應階段。因此破壞并消滅創面表面的細菌生物膜至關重要。相關文獻報道i-PRF富含血小板、白細胞、抗菌肽、凝血酶等成分,通過相關通透蛋白、乳鐵蛋白、防御素、肝素結合蛋白、磷脂酶A2等活性分子的作用干擾細菌細胞的代謝活性,導致其進入凋亡和壞死階段,發揮較強的抗細菌生物膜和抗菌活性;② i-PRF包含多種參與炎癥調節的細胞因子:腫瘤壞死因子-α、白細胞介素(interleukin,IL)-1β、IL-6 、IL-4和VEGF能夠調節免疫應答,使促炎和抗炎細胞因子保持動態平衡,增強抗感染能力,促進血管再生,利于創面愈合。③ i-PRF中的血小板被激活,可以釋放大量的生長因子,如VEGF、表皮生長因子、成纖維細胞生長因子、轉化生長因子-β、血小板源生長因子和胰島素樣生長因子等,這些活性分子能夠刺激參與傷口愈合相關細胞的遷移、增殖與分化,包括中性粒細胞、巨噬細胞、成纖維細胞和間充質干細胞等,同時促進創面愈合各個階段的血管生成,在組織再生修復過程中發揮著極為重要的作用。④ i-PRF特殊的纖維蛋白立體網狀結構,能夠附著大量的血小板和生長因子,形成緩釋系統,可以延長活性成分在創面中的作用時間;纖維蛋白還能刺激CD11/CD18以及整合素αvβ3受體的基因表達,促使參與組織再生愈合相關細胞結合到纖維蛋白、玻連蛋白和纖連蛋白,并為這些細胞的附著、遷移與增殖分化提供場所。⑤ VSD技術能及時將創面分泌物及滲液引流,減輕水腫,建立利于創面愈合的液體平衡微環境,與i-PRF相輔相成,加速創面愈合。

